依据下列实验现象,得出的结论正确的是
| 选项 | 操作 | 实验现象 | 结论 |
| A | 向两支盛有少量溴水溶液的试管中分别加入适量苯和通入足量乙烯 | 溶液均褪色 | 溴与苯和乙烯都能发生反应 |
| B | 测定等浓度的 溶液和 溶液和 溶液的pH 溶液的pH | 前者的pH比后者的大 | 元素的非金属性:S>C |
| C | 向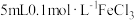 溶液中加入5滴同浓度的KI溶液,再加入几滴KSCN溶液 溶液中加入5滴同浓度的KI溶液,再加入几滴KSCN溶液 | 溶液显血红色 |  与KI的反应是可逆反应 与KI的反应是可逆反应 |
| D | 向 的 的 溶液中滴加几滴同浓度的NaCl溶液后,滴加KI溶液 溶液中滴加几滴同浓度的NaCl溶液后,滴加KI溶液 | 先产生白色沉淀,后出现黄色沉淀 | 证明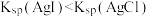 |
| A.A | B.B | C.C | D.D |
更新时间:2021-12-23 09:22:15
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】由下列实验操作及现象得出的相应结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向含有酚酞的 溶液中加入少量 溶液中加入少量 固体 固体 | 出现白色沉淀且溶液红色变浅 |  溶液中存在水解平衡 溶液中存在水解平衡 |
| B | 向乙醇中加入绿豆大小的钠块 | 有气泡产生 | 乙醇中含有水 |
| C | 用锌与稀硫酸反应制氢气时,滴入几滴硫酸铜溶液 | 反应速率加快 |  具有催化作用 具有催化作用 |
| D | 向 溶液中滴加过量氨水 溶液中滴加过量氨水 | 得到澄清溶液 |  与 与 能大量共存 能大量共存 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知草酸H2C2O4是二元弱酸,常温下电离平衡常数:Ka1=5.60×10-2,Ka2=5.42×10-5。下列叙述错误 的是
| A.H2C2O4溶液的电离程度随温度升高而增大 |
| B.常温下,NaHC2O4溶液呈碱性 |
C.0.001mol·L-1 Na2C2O4溶液中:c(Na+)=2×[c(C2O )+c(HC2O )+c(HC2O )+c(H2C2O4)] )+c(H2C2O4)] |
| D.常温下将pH=3的H2C2O4溶液与pH=11的NaOH溶液等体积混合,所得溶液呈酸性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】短周期主族元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是次外层电子数的3倍,Z可与X形成淡黄色化合物Z2X2,X、W的最外层电子数相同。下列说法正确的是
| A.简单离子的半径:Z>Y | B.单质的氧化性:X<W |
| C.气态氢化物的稳定性:Y>X | D.Z2X2属于共价化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】物质M可用于处理废水中的重金属离子,其结构如图所示。M的组成元素X、Z、W是原子序数依次增大的短周期主族元素。下列说法错误的是


| A.X、Z的原子半径大小顺序为Z>X |
| B.W的单质难溶于化合物XW2 |
| C.X、Z、W均能形成两种氧化物 |
| D.最高价氧化物对应水化物的酸性:W>X |
您最近一年使用:0次



