请回答下列问题:
(1)下列有关实验操作或结果的说法中正确的是___________ (填字母)。
A.滴定时,眼睛应始终注视滴定管内液面的变化
B.滴定实验都需要指示剂
C.酸碱中和滴定之前,锥形瓶用蒸馏水洗净即可,不能用待测液润洗
D.用pH试纸测量某溶液的pH时要先将试纸润湿
E.滴定管经蒸馏水洗净后,直接注入标准液,将使测得的待测液浓度偏高
F.用广泛pH试纸测量H2SO4溶液的pH时,测得pH=3.2
(2)有pH均为2的CH3COOH、HCl、H2SO4 三种物质的溶液,物质的量浓度由大到小的顺序为___________ ,若分别用这三种酸中和含等物质的量NaOH的溶液,所需酸溶液的体积分别为a、b、c,则a、b、c的大小关系是___________ 。
(3)NaHSO3溶液显酸性的原因是___________ (用化学用语和必要的文字说明)。
(4)常温时,BaSO4的Ksp=1.08×10-10,现将等体积的BaCl2溶液与3.5×10-3mol/L的Na2SO4溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为___________ 。
(1)下列有关实验操作或结果的说法中正确的是
A.滴定时,眼睛应始终注视滴定管内液面的变化
B.滴定实验都需要指示剂
C.酸碱中和滴定之前,锥形瓶用蒸馏水洗净即可,不能用待测液润洗
D.用pH试纸测量某溶液的pH时要先将试纸润湿
E.滴定管经蒸馏水洗净后,直接注入标准液,将使测得的待测液浓度偏高
F.用广泛pH试纸测量H2SO4溶液的pH时,测得pH=3.2
(2)有pH均为2的CH3COOH、HCl、H2SO4 三种物质的溶液,物质的量浓度由大到小的顺序为
(3)NaHSO3溶液显酸性的原因是
(4)常温时,BaSO4的Ksp=1.08×10-10,现将等体积的BaCl2溶液与3.5×10-3mol/L的Na2SO4溶液混合。若要生成BaSO4沉淀,BaCl2溶液的最小浓度为
更新时间:2022-01-08 10:22:06
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】(1)下列有关实验操作或结果的说法中错误的是_________________
A.实验室在配制FeCl3溶液时,先将FeCl3溶于一定量的浓盐酸中,再加蒸馏水稀释至所需浓度
B.用广泛pH试纸测量Na2S溶液的pH时,得pH=10.5
C.滴定管洗净后经蒸馏水润洗后,即可注入标准液进行中和滴定实验
D.电解盐酸溶液后(盐酸过量),再通入一定量HCl气体时,电解质溶液可恢复到和原来一样
(2)氢氧化铝的酸式电离方程式:__________________________________________
(3)向明矾溶液中逐滴加入氢氧化钡溶液至铝离子刚好沉淀完全时,离子反应总方程式为:_____________________________________________________________
(4)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)________________ 。
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH-)减小
(5)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),________________ 和________________ 两种粒子的物质的量之和比OH―多0.05mol。
A.实验室在配制FeCl3溶液时,先将FeCl3溶于一定量的浓盐酸中,再加蒸馏水稀释至所需浓度
B.用广泛pH试纸测量Na2S溶液的pH时,得pH=10.5
C.滴定管洗净后经蒸馏水润洗后,即可注入标准液进行中和滴定实验
D.电解盐酸溶液后(盐酸过量),再通入一定量HCl气体时,电解质溶液可恢复到和原来一样
(2)氢氧化铝的酸式电离方程式:
(3)向明矾溶液中逐滴加入氢氧化钡溶液至铝离子刚好沉淀完全时,离子反应总方程式为:
(4)25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.氯化铵溶于水,电离出大量铵离子,抑制了氨水的电离,使c(OH-)减小
(5)室温下,如果将0.1mol NH4Cl和0.05mol NaOH全部溶于水,形成混合溶液(假设无损失),
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
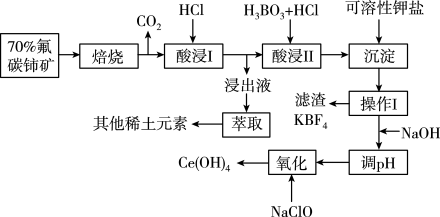
【推荐2】稀土金属是我国战略性资源。氟碳铈矿主要化学成分为CeFCO3,它是提取铈族稀土元素的重要矿物原料。其中一种提取铈的工艺流程如下:
已知:焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物;+ 4价的铈的氧化物有很强的氧化性,通常在酸性条件下易被还原剂还原成+3价而溶于水。请回答下列问题
(1)酸浸l中所用的酸A为(用字母表示)________ (a.盐酸 b.稀硫酸),原因是_______ 。
(2)酸浸Ⅱ后,为避免三价铈以四氟硼酸盐形式损失,需用可溶性钾盐将四氟硼酸根离子沉淀除去,该反应的离子方程式为___________ 。
(3)实验室中进行萃取操作所用到的主要玻璃仪器名称是________ ;在操作I后的溶液中加入NaOH溶液是为了调节溶液pH 获得Ce(OH)3和_______ ,测定该溶液pH的操作是_______ 。
(4)写出氧化步骤的化学方程式_______________ 。
已知:焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物;+ 4价的铈的氧化物有很强的氧化性,通常在酸性条件下易被还原剂还原成+3价而溶于水。请回答下列问题
(1)酸浸l中所用的酸A为(用字母表示)
(2)酸浸Ⅱ后,为避免三价铈以四氟硼酸盐形式损失,需用可溶性钾盐将四氟硼酸根离子沉淀除去,该反应的离子方程式为
(3)实验室中进行萃取操作所用到的主要玻璃仪器名称是
(4)写出氧化步骤的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学欲探究Na2S2O3的有关化学性质,设计如图实验流程图。
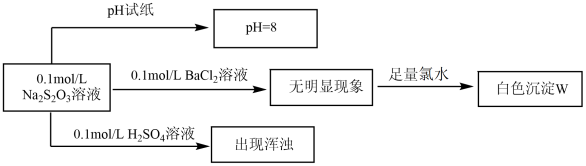
请回答下列问题:
(1)用pH试纸测定溶液pH的操作方法是:_____
(2)写出生成白色沉淀W所涉及的离子方程式:_____
(3)将上述流程中所加BaCl2溶液和氯水的顺序颠倒,也得到白色沉淀,能否说明该白色沉淀与 W 为同种物质_____ (填“能”、“否”);
(4)取三支大小相同的试管,通过测定Na2S2O3溶液与稀硫酸反应出现浑浊的时间,研究外界条件对化学反应速率的影响。设计实验表格如下:
①V=_____ ;
②探究浓度对化学反应速率的影响,应选择_____ (填实验编号)组实验进行对比分析;
③为了准确控制反应的温度,应采用的加热方式为_____

请回答下列问题:
(1)用pH试纸测定溶液pH的操作方法是:
(2)写出生成白色沉淀W所涉及的离子方程式:
(3)将上述流程中所加BaCl2溶液和氯水的顺序颠倒,也得到白色沉淀,能否说明该白色沉淀与 W 为同种物质
(4)取三支大小相同的试管,通过测定Na2S2O3溶液与稀硫酸反应出现浑浊的时间,研究外界条件对化学反应速率的影响。设计实验表格如下:
| 实验 序号 | 实验 温度/℃ | 0.1mol/LNa2S2O3溶液的体积/mL | H2O的体积/mL | 0.1mol/LH2SO4溶液的体积/mL | 所需时间/s |
| 甲 | 25 | 5 | 5 | 2 | / |
| 乙 | 25 | 5 | 6 | 1 | / |
| 丙 | 35 | 5 | 5 | V | / |
①V=
②探究浓度对化学反应速率的影响,应选择
③为了准确控制反应的温度,应采用的加热方式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】测定某品牌洗厕精的酸(盐酸)含量,某学生欲用已知物质的量浓度的NaOH溶液来测定该洗厕精(盐酸)的物质的量浓度,并选择酚酞作指示剂。请填写下列空白:
(1)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是_______ 。
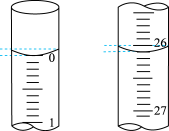
(2)若滴定开始和结束时,碱式滴定管中的液面如图所示:则所用NaOH溶液的体积为_______ mL。
(3)若选择酚酞作指示剂,滴定终点的现象为_______ 。
(4)某学生根据三次实验分别记录有关数据如表:
该洗厕精中酸(盐酸)的物质的量浓度为:c(HCl)=_______ 。
(5)下列操作会导致实验结果偏低的是_______(填序号)。
(1)碱式滴定管用蒸馏水洗净后,接下来应该进行的操作是
(2)若滴定开始和结束时,碱式滴定管中的液面如图所示:则所用NaOH溶液的体积为

(3)若选择酚酞作指示剂,滴定终点的现象为
(4)某学生根据三次实验分别记录有关数据如表:
| 滴定次数 | 待测盐酸的体积/mL | 0.1000mol/LNaOH溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 2.00 | 28.15 | 26.15 |
| 第二次 | 25.00 | 1.50 | 29.50 | 28.00 |
| 第三次 | 25.00 | 0.20 | 26.55 | 26.35 |
(5)下列操作会导致实验结果偏低的是_______(填序号)。
| A.碱式滴定管用蒸馏水洗涤后未用NaOH标准溶液润洗 |
| B.锥形瓶用蒸馏水洗过后未干燥 |
| C.达到滴定终点时,仰视读数 |
| D.滴定过程中振荡锥形瓶,液体不慎溅出 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______ 。直到因加入一滴盐酸后,溶液由黄色变为橙色,并_________ 为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是( )
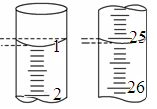
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为________ mL,终点读数为________ mL。
(4)某学生根据3次实验分别记录有关数据如表:
依据上表数据列式计算该NaOH溶液的物质的量浓度为_____________ mol/L。(保留四位有效数字)
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为

(4)某学生根据3次实验分别记录有关数据如表:
| 滴定次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.10 | 26.11 | 26.01 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.32 | 26.31 | 25.99 |
依据上表数据列式计算该NaOH溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】I.实验室用酸碱中和滴定法测定某市售白醋中醋酸的浓度。回答下列问题:
(1)量取待测白醋溶液20.00mL于_______ 中,滴加2滴酚酞作指示剂;将0.1000mol/LNaOH溶液盛装于碱式滴定管中,调至“0”刻度并进行滴定;滴定时两眼注视_______ 。到达滴定终点时停止滴定,并记录NaOH溶液的最终读数。
(2)在完成上述第1次滴定后,重复滴定3次。记录数据如下:
①计算得:c(CH3COOH)= _______ mol•L-1。
②若出现下列情况,测定结果偏高的是_______ 。
A.滴定前用蒸馏水冲洗锥形瓶 B.在振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定至终点时,俯视读数 D碱式滴定管用蒸馏水润洗后,未用标准液润洗
Ⅱ.氧化还原滴定法与酸碱中和滴定法类似,现用0.010 酸性
酸性 溶液滴定未知浓度的
溶液滴定未知浓度的 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为 。回答下列问题:
。回答下列问题:
(3)滴定时,KMnO4 溶液应装在_______ (填“酸式”或“碱式”)滴定管中,该实验_______ (填“需要”或“不需要”)选用指示剂。滴定终点的判断_______ 。
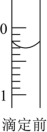
(4)某次滴定前滴定管液面如图所示,读数为_______ mL
(1)量取待测白醋溶液20.00mL于
(2)在完成上述第1次滴定后,重复滴定3次。记录数据如下:
| 实验数据(mL)/滴定次数 | 1 | 2 | 3 | 4 |
| V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
| V[NaOH(aq)](消耗) | 15.95 | 15.00 | 15.02 | 14.98 |
②若出现下列情况,测定结果偏高的是
A.滴定前用蒸馏水冲洗锥形瓶 B.在振荡锥形瓶时不慎将瓶内溶液溅出
C.滴定至终点时,俯视读数 D碱式滴定管用蒸馏水润洗后,未用标准液润洗
Ⅱ.氧化还原滴定法与酸碱中和滴定法类似,现用0.010
 酸性
酸性 溶液滴定未知浓度的
溶液滴定未知浓度的 溶液,有关反应的离子方程式为
溶液,有关反应的离子方程式为 。回答下列问题:
。回答下列问题:(3)滴定时,KMnO4 溶液应装在
(4)某次滴定前滴定管液面如图所示,读数为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】乙二酸俗名草酸,易溶于水。为了探究乙二酸的一些性质,某化学兴趣小组设计了如下实验测定草酸晶体H2C2O4·xH2O中的x值,步骤如下:
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4溶液滴定H2C2O4溶液,至滴定达到终点。
④记录数据,重复实验。整理数据如下:
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒,还缺少的玻璃仪器为_______ (填名称);步骤③滴定过程中,盛装KMnO4溶液的仪器为___________ (填名称)。
(2)本实验滴定达到终点的现象是____________ ;
(3)该反应原理的离子方程式为_____________ ;
(4)根据数据,计算H2C2O4溶液的物质的量浓度为______ mol/L,x=________ ;
(5)若滴定终点读数时俯视滴定管刻度,则x值会________ (填“偏大”、“偏小”或“无影响”)。
方案二:为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是___________ 。
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定0.1mol•L-1草酸溶液的pH
C.将草酸溶液加入Na2CO3溶液中,有CO2放出
D.测定草酸钠溶液的pH
①称取1.260g草酸晶体,配成100mL溶液。
②取25.00mL该H2C2O4溶液加入锥形瓶内,再加入适量稀硫酸。
③用浓度为0.1000mol/L的KMnO4溶液滴定H2C2O4溶液,至滴定达到终点。
④记录数据,重复实验。整理数据如下:
实验序号 | V(KMnO4溶液) | |
滴定前刻度/mL | 滴定后刻度/mL | |
1 | 0.10 | 10.00 |
2 | 1.10 | 11.10 |
3 | 1.50 | 13.50 |
4 | 0.70 | 10.80 |
回答下列问题:
(1)步骤①需要使用烧杯、量筒、玻璃棒,还缺少的玻璃仪器为
(2)本实验滴定达到终点的现象是
(3)该反应原理的离子方程式为
(4)根据数据,计算H2C2O4溶液的物质的量浓度为
(5)若滴定终点读数时俯视滴定管刻度,则x值会
方案二:为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定0.1mol•L-1草酸溶液的pH
C.将草酸溶液加入Na2CO3溶液中,有CO2放出
D.测定草酸钠溶液的pH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如下:
甲:①准确配制0.1mol·L-1的HA、HCl溶液各100mL;
②取纯度相同、质量、大小相等的锌粒放入两支试管中,同时加入0.1mol·L-1的HA、HCl溶液各100mL,按下图装好,观察现象。
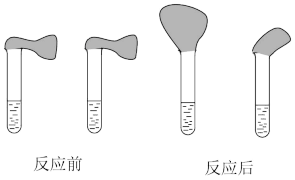
乙:①用pH计测定物质的量浓度均为0.1mol·L-1的HA和HCl溶液的pH;
②再取0.1mol·L-1的HA和HCl溶液各2滴(1滴约为0.05mL)分别稀释至100mL,再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是,测得0.1mol·L-1的HA溶液的pH___________ 1(填“>”“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是___________ 。
A. 装HCl的试管中放出的氢气速率大
B.装HA溶液的试管中放出氢气的速率大
C.两个试管中产生气体速率一样大
(2)乙同学设计的实验第②步,能证明改变条件,弱电解质平衡发生移动。加水稀释,弱酸HA的电离程度___________ (填“增大、减小、不变”)。
(3)甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:使HA的电离程度和c(H+)都减小,c(A)增大,可在0.1mol·L -1的HA溶液中,选择加入___________试剂。
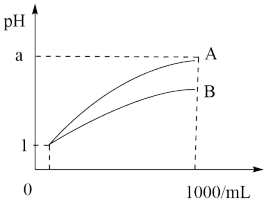
(4)pH=1的两种酸溶液A、B各1mL,分别加水稀释到1000mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的有___________。
甲:①准确配制0.1mol·L-1的HA、HCl溶液各100mL;
②取纯度相同、质量、大小相等的锌粒放入两支试管中,同时加入0.1mol·L-1的HA、HCl溶液各100mL,按下图装好,观察现象。

乙:①用pH计测定物质的量浓度均为0.1mol·L-1的HA和HCl溶液的pH;
②再取0.1mol·L-1的HA和HCl溶液各2滴(1滴约为0.05mL)分别稀释至100mL,再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是,测得0.1mol·L-1的HA溶液的pH
A. 装HCl的试管中放出的氢气速率大
B.装HA溶液的试管中放出氢气的速率大
C.两个试管中产生气体速率一样大
(2)乙同学设计的实验第②步,能证明改变条件,弱电解质平衡发生移动。加水稀释,弱酸HA的电离程度
(3)甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:使HA的电离程度和c(H+)都减小,c(A)增大,可在0.1mol·L -1的HA溶液中,选择加入___________试剂。
| A.NaA固体(可完全溶于水) | B.1mol·L-1 NaOH溶液 |
| C.1mol·L-1 H2SO4 | D.2mol·L-1 HA |

| A.若a=4,则A是强酸,B是弱酸 |
| B.若1<a<4,则A、B都是弱酸 |
| C.两种酸溶液的物质的量浓度一定相等 |
| D.稀释后,A溶液的酸性比B溶液弱 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】弱电解质的研究是重要课题。已知 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)常温下,将 和体积均相同的
和体积均相同的 和
和 溶液分别稀释,溶液
溶液分别稀释,溶液 随加水体积的变化如图。
随加水体积的变化如图。
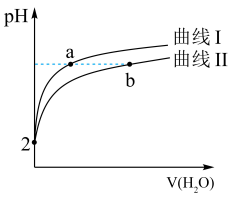
①曲线I代表_______ (填“ ”或“
”或“ ”)溶液。
”)溶液。
②a、b两,点对应的溶液中,水的电离程度:a_______ (填“>”、“<”或“=”)b。
③酸度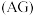 也可表示溶液的酸碱性,
也可表示溶液的酸碱性,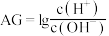 。常温下,
。常温下, 的硝酸溶液的
的硝酸溶液的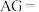
_______ 。
(2)物质的量浓度均为 的下列四种溶液,
的下列四种溶液, 由小到大的顺序是
由小到大的顺序是_______ (用标号填写,例如“ ”)。
”)。
a. b.
b. c.
c. d.
d.
(3)写出向次氯酸钠溶液中通入少量二氧化碳时,发生反应的离子方程式:_______ 。
(4)常温下,含等物质的量浓度的 与
与 的混合溶液显
的混合溶液显_______ (填“酸”、“碱”或“中”)性;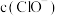
_______ (填“>”、“<”或“=”)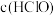 ;该溶液中所含的4种离子浓度由大到小的顺序为
;该溶液中所含的4种离子浓度由大到小的顺序为_______ 。
 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 |  |  |  |  |
| 电离平衡常数 |  | 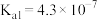  | 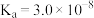 | 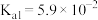 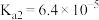 |
(1)常温下,将
 和体积均相同的
和体积均相同的 和
和 溶液分别稀释,溶液
溶液分别稀释,溶液 随加水体积的变化如图。
随加水体积的变化如图。
①曲线I代表
 ”或“
”或“ ”)溶液。
”)溶液。②a、b两,点对应的溶液中,水的电离程度:a
③酸度
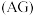 也可表示溶液的酸碱性,
也可表示溶液的酸碱性,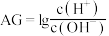 。常温下,
。常温下, 的硝酸溶液的
的硝酸溶液的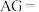
(2)物质的量浓度均为
 的下列四种溶液,
的下列四种溶液, 由小到大的顺序是
由小到大的顺序是 ”)。
”)。a.
 b.
b. c.
c. d.
d.
(3)写出向次氯酸钠溶液中通入少量二氧化碳时,发生反应的离子方程式:
(4)常温下,含等物质的量浓度的
 与
与 的混合溶液显
的混合溶液显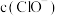
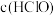 ;该溶液中所含的4种离子浓度由大到小的顺序为
;该溶液中所含的4种离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】用海底锰结核(主要成分为MnO2,含少量MgO、Fe2O3、Al2O3、SiO2)为原料,制备金属锰、镁的一种工艺流程路线如图所示:
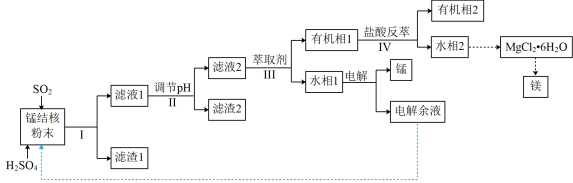
已知:①几种难溶物的溶度积(25℃)如下表所示。
②溶液中某离子浓度≤1.0×10-6mol•L-1时,认为该离子沉淀完全。
完成下列问题:
(1)Mn在周期表中的位置:___________ 。
(2)“滤液1”中c(Mn2+)为0.18mol•L-1,则“调节pH”的范围为___________ ,“滤渣2”的成分为___________ 。
(3)“Ⅲ”处“萃取剂”萃取的成分是___________ 。
(4)MgCl2•6H2O制取无水MgCl2时,需要在干燥的HCl气流中加热分解。HCl的作用为___________ 。
(5)水相1发生电解反应的离子方程式为:___________ 。
(6)一种海生假单孢菌(采自太平洋深海处),在无氧条件下以醋酸为电子供体还原MnO2生成Mn2+的机理如图所示。写出反应②③的总反应的离子方程式___________ 。


已知:①几种难溶物的溶度积(25℃)如下表所示。
| 化学式 | Mg(OH)2 | Mn(OH)2 | Al(OH)3 | Fe(OH)3 |
| Ksp | 1.8×10-11 | 1.8×10-13 | 1.0×10-33 | 4.0×10-38 |
完成下列问题:
(1)Mn在周期表中的位置:
(2)“滤液1”中c(Mn2+)为0.18mol•L-1,则“调节pH”的范围为
(3)“Ⅲ”处“萃取剂”萃取的成分是
(4)MgCl2•6H2O制取无水MgCl2时,需要在干燥的HCl气流中加热分解。HCl的作用为
(5)水相1发生电解反应的离子方程式为:
(6)一种海生假单孢菌(采自太平洋深海处),在无氧条件下以醋酸为电子供体还原MnO2生成Mn2+的机理如图所示。写出反应②③的总反应的离子方程式

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】采用废铁屑还原软锰矿(软锰矿主要成分是MnO2,还含有Fe2O3、MgO、SiO2和NiCO3杂质)来制备Mn的工艺流程如图所示。
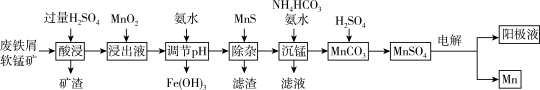
已知:①Ksp(MnS)=2.6×10﹣10,Ksp(NiS)=2.0×10﹣21;
②生成氢氧化物的pH见下表
回答下列问题:
(1)“酸浸”前将原料粉碎的目的是_______ 。
(2)加入量MnO2的目的是_______ 。
(3)常温下,已知K(NH3•H2O)=4×10﹣5,则0.1mol/L的NH3•H2O的pH约为_______ (lg2=0.3)。
(4)“调节pH”操作中pH控制范围为_______ 。
(5)“除杂”加入MnS,请写出此过程发生的离子方程式:_______ 。当该反应完成后,滤液中的Mn2+和Ni2+的物质的量浓度之比是 _______ 。
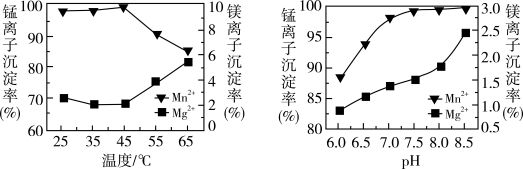
(6)“沉锰”过程中温度和pH对Mn2+和Mg2+沉淀率的影响如图所示。由图可知,“沉锰”的合适条件是_______ 。

已知:①Ksp(MnS)=2.6×10﹣10,Ksp(NiS)=2.0×10﹣21;
②生成氢氧化物的pH见下表
| 离子 | Fe2+ | Fe3+ | Mg2+ | Ni2+ | Mn2+ |
| 开始沉淀的pH | 7.5 | 2.7 | 8.1 | 7.7 | 8.3 |
| 完全沉淀的pH | 9.7 | 3.7 | 9.4 | 8.4 | 9.8 |
回答下列问题:
(1)“酸浸”前将原料粉碎的目的是
(2)加入量MnO2的目的是
(3)常温下,已知K(NH3•H2O)=4×10﹣5,则0.1mol/L的NH3•H2O的pH约为
(4)“调节pH”操作中pH控制范围为
(5)“除杂”加入MnS,请写出此过程发生的离子方程式:
(6)“沉锰”过程中温度和pH对Mn2+和Mg2+沉淀率的影响如图所示。由图可知,“沉锰”的合适条件是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】铋(Bi)的化合物广泛应用于电子、医药等领域。由辉铋碎(主要成分为Bi2S3,含FeS2、CuO、SiO2等杂质)制备NaBiO3的工艺流程如下:
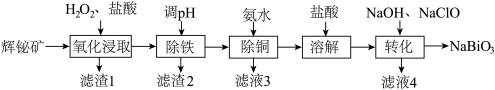
已知:ⅰ.NaBiO3难溶于冷水。
ⅱ.“氧化浸取”时,有单质生成,Bi2S3被氧化,铋元素转化为Bi3+。
ⅲ.Cu(OH)2(s)+4NH3(g)⇌Cu[(NH3)4]2+(aq)+2OH-(aq) K=4.4×10-7
回答下列问题:
(1)滤渣1的主要成份是_______ 。
(2)为提高“氧化浸取”速率,采取的措施有:升高温度、_______ (写出一条)。辉铋矿浸取率随温度的变化曲线如图:
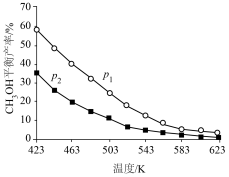
高于40℃时浸取率快速下降,其可能的原因是_______ 。
(3)“除铜”时发生反应:Cu2+(aq)+4NH3(g)⇌Cu[(NH3)4]2+(aq) K=2×1013,则Cu2+(aq)+2OH-(aq)=Cu(OH)2(s)的平衡常数K=_______ 。
(4)“转化”时,生成NaBiO3的离子方程式为_______ 。
(5)已知酸性环境下,NaBiO3可以将Mn2+氧化成MnO (BiO
(BiO 被还原成Bi3+)。可通过一个原电池装置来证明。
被还原成Bi3+)。可通过一个原电池装置来证明。
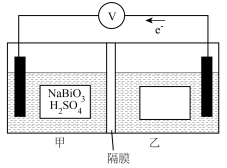
①图中乙池的方框内溶液中溶质的化学式为_______
②写出正极的电极反应式:_______ 。
③若隔膜为质子交换膜,电路中转移0.2mol电子时质子交换膜中通过的H+的个数为_______ 。

已知:ⅰ.NaBiO3难溶于冷水。
ⅱ.“氧化浸取”时,有单质生成,Bi2S3被氧化,铋元素转化为Bi3+。
ⅲ.Cu(OH)2(s)+4NH3(g)⇌Cu[(NH3)4]2+(aq)+2OH-(aq) K=4.4×10-7
回答下列问题:
(1)滤渣1的主要成份是
(2)为提高“氧化浸取”速率,采取的措施有:升高温度、

高于40℃时浸取率快速下降,其可能的原因是
(3)“除铜”时发生反应:Cu2+(aq)+4NH3(g)⇌Cu[(NH3)4]2+(aq) K=2×1013,则Cu2+(aq)+2OH-(aq)=Cu(OH)2(s)的平衡常数K=
(4)“转化”时,生成NaBiO3的离子方程式为
(5)已知酸性环境下,NaBiO3可以将Mn2+氧化成MnO
 (BiO
(BiO 被还原成Bi3+)。可通过一个原电池装置来证明。
被还原成Bi3+)。可通过一个原电池装置来证明。
①图中乙池的方框内溶液中溶质的化学式为
②写出正极的电极反应式:
③若隔膜为质子交换膜,电路中转移0.2mol电子时质子交换膜中通过的H+的个数为
您最近一年使用:0次



