回答下列问题
(1)在微生物作用的条件下,NH 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
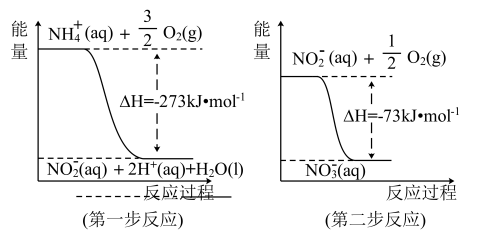
①第一步反应是_______ (填“放热”或“吸热”)反应,判断依据是_______ 。
②1 mol NH (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(2)在80℃时,将0.4mol的N2O4(无色)气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如表数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。该反应的化学方程式为N2O4⇌2NO2。
①0~20s内N2O4的平均反应速率为_______ 。
②在80℃时N2O4的转化率为_______ 。
③写出恒温恒容下,能判断该反应达到平衡状态的依据_______ 。(写出1条即可)
(1)在微生物作用的条件下,NH
 经过两步反应被氧化成NO
经过两步反应被氧化成NO 。两步反应的能量变化示意图如图:
。两步反应的能量变化示意图如图:
①第一步反应是
②1 mol NH
 (aq)全部氧化成NO
(aq)全部氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是(2)在80℃时,将0.4mol的N2O4(无色)气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.20 | a | 0.10 | c | d | e |
| c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
①0~20s内N2O4的平均反应速率为
②在80℃时N2O4的转化率为
③写出恒温恒容下,能判断该反应达到平衡状态的依据
更新时间:2021-12-28 22:58:21
|
相似题推荐
【推荐1】研究化学反应的原理,对掌握物质的应用有重要的意义。
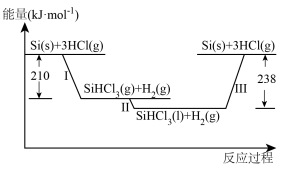
Ⅰ.硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:
(1)工业上用 为原料制备粗硅。
为原料制备粗硅。
①反应的化学方程式为______ 。
② 的用途是
的用途是______ (任写一种)。
(2)反应Ⅲ生成2 mol Si(s)时,______ (填“吸收”或“放出”)______ 热量。
(3)在2L密闭容器中投入过量Si(s)和3 mol HCl(g)发生反应Ⅰ,经过t min反应达到平衡状态,测得容器中HCl的平衡浓度为0.6 mol·L 。
。
①反应开始到t min,用HCl浓度变化表示的平均反应速率为______ mol⋅L ⋅min
⋅min 。
。
②为加快反应速率,可采取的措施为______ (任写一种)。
③下列叙述不能说明反应Ⅰ一定达到平衡状态的是______ (填标号)。
a.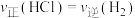 b.硅的质量保持不变
b.硅的质量保持不变
c.HCl的质量分数保持不变 d. 保持不变
保持不变
Ⅱ.用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

(4)电极X为______ (填“正极”、“负极”)。
(5)电池工作时,质子通过交换膜______ (填“从左到右”、“从右到左”)迁移。
(6)正极的电极反应式为______ 。
Ⅰ.硅是太阳能电池的重要材料。“精炼硅”反应历程中的能量变化如下图所示:

(1)工业上用
 为原料制备粗硅。
为原料制备粗硅。①反应的化学方程式为
②
 的用途是
的用途是(2)反应Ⅲ生成2 mol Si(s)时,
(3)在2L密闭容器中投入过量Si(s)和3 mol HCl(g)发生反应Ⅰ,经过t min反应达到平衡状态,测得容器中HCl的平衡浓度为0.6 mol·L
 。
。①反应开始到t min,用HCl浓度变化表示的平均反应速率为
 ⋅min
⋅min 。
。②为加快反应速率,可采取的措施为
③下列叙述不能说明反应Ⅰ一定达到平衡状态的是
a.
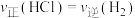 b.硅的质量保持不变
b.硅的质量保持不变c.HCl的质量分数保持不变 d.
 保持不变
保持不变Ⅱ.用于检测酒驾的酸性燃料电池酒精检测仪工作原理如图所示。

(4)电极X为
(5)电池工作时,质子通过交换膜
(6)正极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】合成氨对人类生存具有重大意义,反应为:
 。
。
(1)科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如下图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
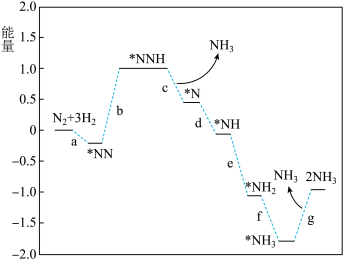
①写出步骤c的化学方程式_______ 。
②由图像可知合成氨反应的
_______ 0(填“>”“<”或“=”),判断的依据是_______ 。
(2)下列有关合成氨的说法中,正确的是_______。
(3)原料气( 、
、 及少量CO、
及少量CO、 的混合气)中CO气体会影响后续反应催化剂活性,可利用如下反应吸收CO:
的混合气)中CO气体会影响后续反应催化剂活性,可利用如下反应吸收CO:
 (注:Ac代表
(注:Ac代表 )。利于CO被吸收的反应条件有
)。利于CO被吸收的反应条件有_______ (写出两点)。
(4)若一定条件下,向体积相同的甲(含催化剂)、乙(不含催化剂)两个恒容密闭容器中分别充入等量的 和等量的
和等量的 进行合成氨反应。反应相同时间时测得两容器中
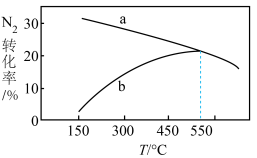
进行合成氨反应。反应相同时间时测得两容器中 的转化率随温度的变化如下图所示,表示甲容器中
的转化率随温度的变化如下图所示,表示甲容器中 的转化率随温度变化的曲线是
的转化率随温度变化的曲线是_______ (填“a”或“b”),随着温度的升高,乙容器中 的转化率变化的原因可能是
的转化率变化的原因可能是_______ 。
(5)一定条件下,若向容积为1.0L的反应容器中投入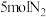 、
、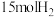 ,平衡时混合气中
,平衡时混合气中 的质量分数为40%,计算平衡常数
的质量分数为40%,计算平衡常数
_______ (可用分数表示)。

 。
。(1)科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如下图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。

①写出步骤c的化学方程式
②由图像可知合成氨反应的

(2)下列有关合成氨的说法中,正确的是_______。
| A.反应物断键吸收的总能量高于生成物成键放出的总能量 |
| B.使用催化剂和施加高压,都能提高反应速率,但都对化学平衡状态无影响 |
| C.合成氨工业温度选择400~500℃,主要是为了提高平衡混合物中氨的含量 |
| D.合成氨生产过程中采用循环操作,主要是为了提高氮气和氢气的利用率 |
(3)原料气(
 、
、 及少量CO、
及少量CO、 的混合气)中CO气体会影响后续反应催化剂活性,可利用如下反应吸收CO:
的混合气)中CO气体会影响后续反应催化剂活性,可利用如下反应吸收CO:
 (注:Ac代表
(注:Ac代表 )。利于CO被吸收的反应条件有
)。利于CO被吸收的反应条件有(4)若一定条件下,向体积相同的甲(含催化剂)、乙(不含催化剂)两个恒容密闭容器中分别充入等量的
 和等量的
和等量的 进行合成氨反应。反应相同时间时测得两容器中
进行合成氨反应。反应相同时间时测得两容器中 的转化率随温度的变化如下图所示,表示甲容器中
的转化率随温度的变化如下图所示,表示甲容器中 的转化率随温度变化的曲线是
的转化率随温度变化的曲线是 的转化率变化的原因可能是
的转化率变化的原因可能是
(5)一定条件下,若向容积为1.0L的反应容器中投入
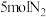 、
、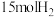 ,平衡时混合气中
,平衡时混合气中 的质量分数为40%,计算平衡常数
的质量分数为40%,计算平衡常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】化学电源广泛地应用于现代社会的生产和生活。请回答下列问题:
(1)原电池是一种化学能转变为电能的装置,所以原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
(2)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图两个实验,已知两个实验除了是否有导线连接两个金属棒外,其余均相同。

①该同学设计这两个实验的目的是___________ 。
②有关反应一段时间后的实验现象,下列说法正确的是___________ ( 填字母)。
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温。
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
(3)若将用导线相连在一起,总质量为80.00 g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为63.75 g,则装置工作时锌片上的电极反应式为___________ ,工作时间内装置所产生氢气的体积为 ___________ L(标准状况)。
(1)原电池是一种化学能转变为电能的装置,所以原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
| A.CaO+H2O=Ca(OH)2 |
B.C+CO2 2CO 2CO |
| C.NaOH+HCl=NaCl+H2O |
| D.2FeCl3+Cu=2FeCl2+CuCl2 |

①该同学设计这两个实验的目的是
②有关反应一段时间后的实验现象,下列说法正确的是
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温。
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
(3)若将用导线相连在一起,总质量为80.00 g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为63.75 g,则装置工作时锌片上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】发展新能源、改善空气质量一直是化学研究的热点。回答下列问题:
(1)甲醇是可再生的清洁能源,可利用 与
与 合成甲醇:
合成甲醇: ,该反应历程如图1所示。合成甲醇过程中产生的有机副产物为
,该反应历程如图1所示。合成甲醇过程中产生的有机副产物为___________ (填分子式);由于该反应速率较慢,需要加入催化剂加快反应速率,则催化剂主要降低___________ (填序号)的能量变化。

A.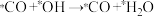
B.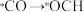
C.
D.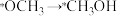
(2)焦炭与水蒸气在恒容密闭容器中反应,可制合成气(CO和 ),主要反应Ⅰ、Ⅱ的lg
),主要反应Ⅰ、Ⅱ的lg (
( 为以分压表示的平衡常数)与
为以分压表示的平衡常数)与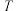 的关系如图2所示。
的关系如图2所示。
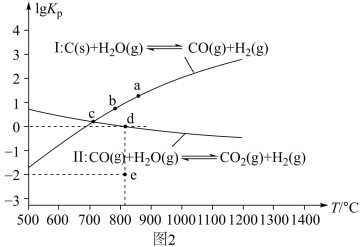
①反应Ⅰ的
_______ (填“>”“=”或“<”)0。
②在容积为10L的密闭容器中充入1molCO、1mol 只发生反应Ⅱ,5min时到达图2中的d点,则0~5min内,用CO表示的反应速率为
只发生反应Ⅱ,5min时到达图2中的d点,则0~5min内,用CO表示的反应速率为_______ ,CO的转化率为_______ 。已知: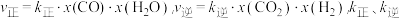 分别为正、逆反应速率常数,x为物质的量分数,计算e点的
分别为正、逆反应速率常数,x为物质的量分数,计算e点的 =
=_________ 。
(3)c点时,若反应容器中CO的浓度为 ,则
,则 的浓度为
的浓度为_______  。
。
(1)甲醇是可再生的清洁能源,可利用
 与
与 合成甲醇:
合成甲醇: ,该反应历程如图1所示。合成甲醇过程中产生的有机副产物为
,该反应历程如图1所示。合成甲醇过程中产生的有机副产物为
A.
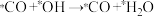
B.
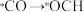
C.

D.
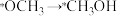
(2)焦炭与水蒸气在恒容密闭容器中反应,可制合成气(CO和
 ),主要反应Ⅰ、Ⅱ的lg
),主要反应Ⅰ、Ⅱ的lg (
( 为以分压表示的平衡常数)与
为以分压表示的平衡常数)与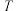 的关系如图2所示。
的关系如图2所示。
①反应Ⅰ的

②在容积为10L的密闭容器中充入1molCO、1mol
 只发生反应Ⅱ,5min时到达图2中的d点,则0~5min内,用CO表示的反应速率为
只发生反应Ⅱ,5min时到达图2中的d点,则0~5min内,用CO表示的反应速率为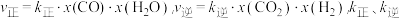 分别为正、逆反应速率常数,x为物质的量分数,计算e点的
分别为正、逆反应速率常数,x为物质的量分数,计算e点的 =
=(3)c点时,若反应容器中CO的浓度为
 ,则
,则 的浓度为
的浓度为 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】CO、CO2是化石燃料燃烧的主要产物。
(1)将含0.02 molCO2和0.01molCO的混合气体通入有足量Na2O2 固体的密闭容器中,同时不断地用电火花点燃,充分反应后,固体质量增加_________ g。
(2)已知:2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ·mol-1,键能Eo=o为499.0kJ·mol-1。
①反应:CO(g)+O2(g) CO2(g)+O(g)的△H=
CO2(g)+O(g)的△H=_________ kJ·mol-1。
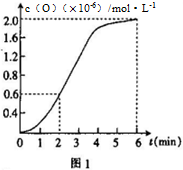
②已知1500℃时,在密闭容器中发生反应:CO2(g) CO(g)+O(g)。反应过程中O(g)的物质的量浓度随时间的变化如图1 所示,则0~2 min 内,CO2 的平均反应速率 υ(CO2)=
CO(g)+O(g)。反应过程中O(g)的物质的量浓度随时间的变化如图1 所示,则0~2 min 内,CO2 的平均反应速率 υ(CO2)=_________ 。
(3)在某密闭容器中发生反应:2CO2(g) 2CO(g)+O2(g),1molCO2 在不同温度下的平衡分解量如图2 所示。
2CO(g)+O2(g),1molCO2 在不同温度下的平衡分解量如图2 所示。

①恒温恒容条件下,能表示该可逆反应达到平衡状态的有_________ (填字母)。
A.CO 的体积分数保持不变
B.容器内混合气体的密度保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内,消耗CO 的浓度等于生成CO2 的浓度
②分析图2,若1500℃时反应达到平衡状态,且容器体积为1L,则此时反应的平衡常数 K=_________ (计算结果保留1 位小数)。
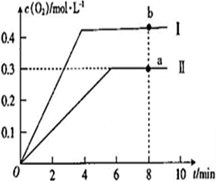
③向恒容密闭容器中充入2molCO2(g),发生反应:2CO2(g) 2CO(g) +O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II 所示。图中曲线I 是相对于曲线II仅改变一种反应条件后c(O2)随时间的变化,则改变的条件是
2CO(g) +O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II 所示。图中曲线I 是相对于曲线II仅改变一种反应条件后c(O2)随时间的变化,则改变的条件是_________ ;a、 b两点用CO浓度变化表示的净反应速率关系为υa(CO)_________ (填“>”“<”或“=”) υb( CO)。
(1)将含0.02 molCO2和0.01molCO的混合气体通入有足量Na2O2 固体的密闭容器中,同时不断地用电火花点燃,充分反应后,固体质量增加
(2)已知:2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ·mol-1,键能Eo=o为499.0kJ·mol-1。
①反应:CO(g)+O2(g)
 CO2(g)+O(g)的△H=
CO2(g)+O(g)的△H=②已知1500℃时,在密闭容器中发生反应:CO2(g)
 CO(g)+O(g)。反应过程中O(g)的物质的量浓度随时间的变化如图1 所示,则0~2 min 内,CO2 的平均反应速率 υ(CO2)=
CO(g)+O(g)。反应过程中O(g)的物质的量浓度随时间的变化如图1 所示,则0~2 min 内,CO2 的平均反应速率 υ(CO2)=
(3)在某密闭容器中发生反应:2CO2(g)
 2CO(g)+O2(g),1molCO2 在不同温度下的平衡分解量如图2 所示。
2CO(g)+O2(g),1molCO2 在不同温度下的平衡分解量如图2 所示。
①恒温恒容条件下,能表示该可逆反应达到平衡状态的有
A.CO 的体积分数保持不变
B.容器内混合气体的密度保持不变
C.容器内混合气体的平均摩尔质量保持不变
D.单位时间内,消耗CO 的浓度等于生成CO2 的浓度
②分析图2,若1500℃时反应达到平衡状态,且容器体积为1L,则此时反应的平衡常数 K=
③向恒容密闭容器中充入2molCO2(g),发生反应:2CO2(g)
 2CO(g) +O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II 所示。图中曲线I 是相对于曲线II仅改变一种反应条件后c(O2)随时间的变化,则改变的条件是
2CO(g) +O2(g),测得温度为T℃时,容器内O2的物质的量浓度随时间的变化如曲线II 所示。图中曲线I 是相对于曲线II仅改变一种反应条件后c(O2)随时间的变化,则改变的条件是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】硫酰氯(SO2Cl2)是重要的化学试剂,可由如下反应制取:SO2(g)+Cl2(g)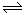 SO2Cl2(g)△H
SO2Cl2(g)△H
针对该反应回答下列问题:
(1)已知:①SO2(g)+Cl2(g)+SCl2(g)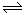 2SOCl2(g)△H1=-akJ/mol
2SOCl2(g)△H1=-akJ/mol
②SO2Cl2(g)+SCl2(g)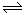 2SOCl2(g)△H2=-bkJ/mol(a>b>0)
2SOCl2(g)△H2=-bkJ/mol(a>b>0)
则△H=________kJ/mol(用a、b的代数式表示)
(2)为了提高该反应中Cl2的平衡转化率,下列措施合理的是________(填字母序号)。
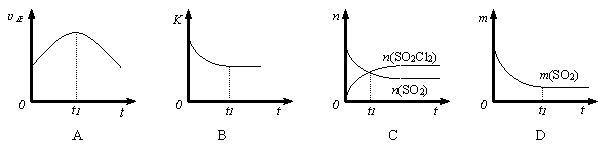
(3)若在绝热、恒容的密闭体系中,投入一定量SO2和Cl2,发生该反应,下列示意图能说明t1 时刻反应达到平衡状态的是(填字母序号)。(下图中υ正、K、n、m分别表示正反应速率、平衡常数、物质的量和质量)
(4)若在催化剂作用下,将n molSO2与nmolCl2充入容积可变的密闭容器中,并始终保持温度为T,压强为P。起始时气体总体积为10L,t min时反应达到平衡状态,此时气体总体积为8L。
①在容积改变的条件下,反应速率可用单位时间内反应物或生成物的物质的量变化来表示。则υ(SO2)= _________。
②此温度下,该反应的K=_________。
③相同条件下,若将0.5nmolSO2与0.5nmolCl2充入该容器,到达平衡状态时,混合物中SO2Cl2的物质的量是_________。
(5)该反应的产物SO2Cl2遇水发生剧烈水解生成两种强酸,写出其化学方程式_______________;已知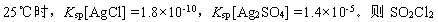 于水所得溶液中逐滴加入AgNO3稀溶液时,最先产生的沉淀是______。
于水所得溶液中逐滴加入AgNO3稀溶液时,最先产生的沉淀是______。
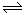 SO2Cl2(g)△H
SO2Cl2(g)△H针对该反应回答下列问题:
(1)已知:①SO2(g)+Cl2(g)+SCl2(g)
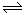 2SOCl2(g)△H1=-akJ/mol
2SOCl2(g)△H1=-akJ/mol②SO2Cl2(g)+SCl2(g)
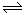 2SOCl2(g)△H2=-bkJ/mol(a>b>0)
2SOCl2(g)△H2=-bkJ/mol(a>b>0)则△H=________kJ/mol(用a、b的代数式表示)
(2)为了提高该反应中Cl2的平衡转化率,下列措施合理的是________(填字母序号)。
| A.缩小容器体积 | B.使用催化剂 | C.增加SO2浓度 | D.升高温度 |
(3)若在绝热、恒容的密闭体系中,投入一定量SO2和Cl2,发生该反应,下列示意图能说明t1 时刻反应达到平衡状态的是(填字母序号)。(下图中υ正、K、n、m分别表示正反应速率、平衡常数、物质的量和质量)

(4)若在催化剂作用下,将n molSO2与nmolCl2充入容积可变的密闭容器中,并始终保持温度为T,压强为P。起始时气体总体积为10L,t min时反应达到平衡状态,此时气体总体积为8L。
①在容积改变的条件下,反应速率可用单位时间内反应物或生成物的物质的量变化来表示。则υ(SO2)= _________。
②此温度下,该反应的K=_________。
③相同条件下,若将0.5nmolSO2与0.5nmolCl2充入该容器,到达平衡状态时,混合物中SO2Cl2的物质的量是_________。
(5)该反应的产物SO2Cl2遇水发生剧烈水解生成两种强酸,写出其化学方程式_______________;已知
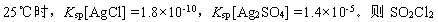 于水所得溶液中逐滴加入AgNO3稀溶液时,最先产生的沉淀是______。
于水所得溶液中逐滴加入AgNO3稀溶液时,最先产生的沉淀是______。
您最近一年使用:0次
【推荐1】含碳物质的转化,有利于“减碳”和可持续性发展,有重要的研究价值,回答下列问题:
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ :2NH3(g)+CO2(g) NH2COONH4(s) △H1
NH2COONH4(s) △H1
反应Ⅱ :NH2COONH4(s) CO(NH2)2(s)+H2O(g) △H2 = +72.5 kJ/mol
CO(NH2)2(s)+H2O(g) △H2 = +72.5 kJ/mol
反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) △H3 = -87.0 kJ/mol
CO(NH2)2(s)+H2O(g) △H3 = -87.0 kJ/mol
①反应Ⅰ的△H1_______ kJ/mol。
②对反应Ⅲ,下列措施中有利于提高NH3平衡转化率的是_______ (填字母)。
A.升高温度
B.增大压强
C.提高原料气中CO2(g)的比例
D.使用高效催化剂
③一定温度下,在体积固定的密闭容器中按化学计量数比投料进行反应Ⅰ,下列不能说明反应Ⅰ达到化学平衡状态的是_______ (填字母)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C. 2v正(NH3)= v逆(CO2)
D.容器内混合气体的密度不再变化
(2)用惰性电极电解KHCO3溶液可将空气中的CO2转化为甲酸根(HCOO-)和HCO ,其电极反应式为
,其电极反应式为_______ ;若电解过程电转移1 mol电子,则阳极生成气体的体积为_______ (标准状况)。
(3)利用工业废气中的CO2制取甲醇:CO2(g)+3H2 (g) CH3OH(g)+ H2O(g),一定条件下往恒容密闭容器中充入1 mol CO2和3 mol H2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2的转化率随温度变化如图所示:
CH3OH(g)+ H2O(g),一定条件下往恒容密闭容器中充入1 mol CO2和3 mol H2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2的转化率随温度变化如图所示:
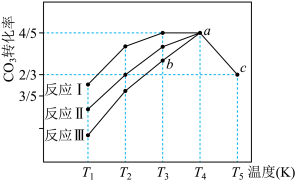
①催化剂效果最佳的反应是_______ (填“反应Ⅰ”“反应Ⅱ”或“反应Ⅲ”)。
②b点v(正)_______ v(逆)(填“> ” “<”或“=”)
③c点时总压强为p,该反应的平衡常数=_______ (用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(1)以CO2和NH3为原料合成尿素是利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ :2NH3(g)+CO2(g)
 NH2COONH4(s) △H1
NH2COONH4(s) △H1反应Ⅱ :NH2COONH4(s)
 CO(NH2)2(s)+H2O(g) △H2 = +72.5 kJ/mol
CO(NH2)2(s)+H2O(g) △H2 = +72.5 kJ/mol反应Ⅲ:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) △H3 = -87.0 kJ/mol
CO(NH2)2(s)+H2O(g) △H3 = -87.0 kJ/mol①反应Ⅰ的△H1
②对反应Ⅲ,下列措施中有利于提高NH3平衡转化率的是
A.升高温度
B.增大压强
C.提高原料气中CO2(g)的比例
D.使用高效催化剂
③一定温度下,在体积固定的密闭容器中按化学计量数比投料进行反应Ⅰ,下列不能说明反应Ⅰ达到化学平衡状态的是
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C. 2v正(NH3)= v逆(CO2)
D.容器内混合气体的密度不再变化
(2)用惰性电极电解KHCO3溶液可将空气中的CO2转化为甲酸根(HCOO-)和HCO
 ,其电极反应式为
,其电极反应式为(3)利用工业废气中的CO2制取甲醇:CO2(g)+3H2 (g)
 CH3OH(g)+ H2O(g),一定条件下往恒容密闭容器中充入1 mol CO2和3 mol H2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2的转化率随温度变化如图所示:
CH3OH(g)+ H2O(g),一定条件下往恒容密闭容器中充入1 mol CO2和3 mol H2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2的转化率随温度变化如图所示:
①催化剂效果最佳的反应是
②b点v(正)
③c点时总压强为p,该反应的平衡常数=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】利用反应NO2(g)+SO2(g) SO3(g)+NO(g) △H=-Q kJ/mol(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。完成下列填空:
SO3(g)+NO(g) △H=-Q kJ/mol(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。完成下列填空:
(1)该反应中被氧化是元素是_________ ;写出该反应的平衡常数表达式:K=_________ 。增大NO2浓度,平衡常数K_________ 。(填“增大”、“减小”或“不变”)
(2)若上述反应在密闭容器中进行,能表明反应达到平衡状态的是_________ (选填编号)。
a. 混合气体颜色保持不变 b. NO2和NO的体积比保持不变
c. 每消耗1 mol SO2的同时生成1 mol SO3 d. 体系中气体平均摩尔质量保持不变
(3)一定温度下,在容积为V L的容器中发生上述反应,t min内,SO2的物质的量下降了a mol,则这段时间内v(NO2)=_________ (用相关字母表示)。
(4)请写出两种能提高平衡转化率的措施____________ 、______________ 。
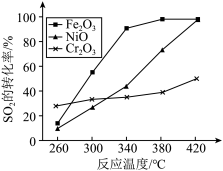
(5)其他条件相同,催化剂不同时,上述反应中SO2的转化率随反应温度的变化如图。不考虑催化剂价格因素,生产中选择Fe2O3作催化剂的主要原因是___________
 SO3(g)+NO(g) △H=-Q kJ/mol(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。完成下列填空:
SO3(g)+NO(g) △H=-Q kJ/mol(Q>0)可处理NO2、SO2等大气污染物,具有十分重要的意义。完成下列填空:(1)该反应中被氧化是元素是
(2)若上述反应在密闭容器中进行,能表明反应达到平衡状态的是
a. 混合气体颜色保持不变 b. NO2和NO的体积比保持不变
c. 每消耗1 mol SO2的同时生成1 mol SO3 d. 体系中气体平均摩尔质量保持不变
(3)一定温度下,在容积为V L的容器中发生上述反应,t min内,SO2的物质的量下降了a mol,则这段时间内v(NO2)=
(4)请写出两种能提高平衡转化率的措施
(5)其他条件相同,催化剂不同时,上述反应中SO2的转化率随反应温度的变化如图。不考虑催化剂价格因素,生产中选择Fe2O3作催化剂的主要原因是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,需要回收处理并加以利用。
(1)已知下列反应的热化学方程式:
①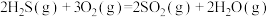
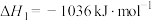
②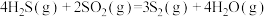
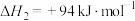
③
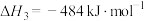
计算 热分解反应④
热分解反应④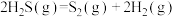 的
的
___________  。
。
(2)反应④的活化能
___________ (填“>”、“<”或“=”) ,在
,在___________ (填“高温”或“低温”)下才可自发进行,判断的理由是___________ 。
(3)已知某温度下,在容积不变的密闭容器中,反应④中 的转化率达到最大值的依据是
的转化率达到最大值的依据是___________ (填字母)。
a.气体的压强不发生变化
b.气体的密度不发生变化
c.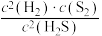 不发生变化
不发生变化
d.单位时间里分解的 和生成的
和生成的 的量一样多
的量一样多
(4)密闭容器中发生反应④,维持体系压强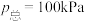 ,反应在不同温度下达到平衡时,混合气体中各组分的体积分数(物质的量分数)如图所示。
,反应在不同温度下达到平衡时,混合气体中各组分的体积分数(物质的量分数)如图所示。
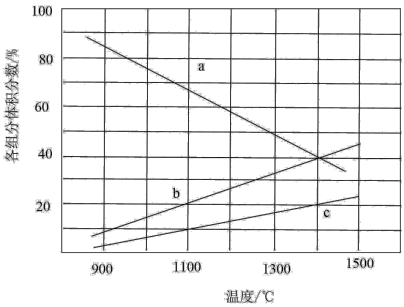
①曲线c代表的物质是___________ (填化学式)。
②反应温度为1300℃时,反应的平衡常数
___________ (写计算式,分压=总压×物质的量分数)。
③若 高温裂解反应在刚性容器中进行,增大
高温裂解反应在刚性容器中进行,增大 的投入量,
的投入量, 的物质的量分数
的物质的量分数___________ (填“增大”、“减小”或“不变”)。
(1)已知下列反应的热化学方程式:
①
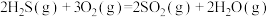
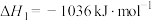
②
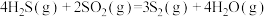
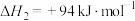
③

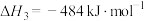
计算
 热分解反应④
热分解反应④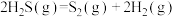 的
的
 。
。(2)反应④的活化能

 ,在
,在(3)已知某温度下,在容积不变的密闭容器中,反应④中
 的转化率达到最大值的依据是
的转化率达到最大值的依据是a.气体的压强不发生变化
b.气体的密度不发生变化
c.
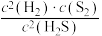 不发生变化
不发生变化 d.单位时间里分解的
 和生成的
和生成的 的量一样多
的量一样多(4)密闭容器中发生反应④,维持体系压强
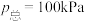 ,反应在不同温度下达到平衡时,混合气体中各组分的体积分数(物质的量分数)如图所示。
,反应在不同温度下达到平衡时,混合气体中各组分的体积分数(物质的量分数)如图所示。
①曲线c代表的物质是
②反应温度为1300℃时,反应的平衡常数

③若
 高温裂解反应在刚性容器中进行,增大
高温裂解反应在刚性容器中进行,增大 的投入量,
的投入量, 的物质的量分数
的物质的量分数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】以 生产甲醇
生产甲醇 实现“碳中和“的重要途径。其原理是:
实现“碳中和“的重要途径。其原理是: 。
。
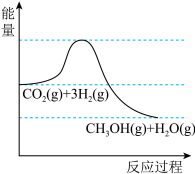
(1)该反应的能量变化如图所示,该反应为___________ (填“放热”成“吸热”)反应。
(2)恒容容器中,对于上述反应,下列措施就加快反应速率的是___________。
(3)在体积为 的密闭容器中,充入
的密闭容器中,充入 和
和 ,测得
,测得 、
、 的物质的量随时间变化如图。从反应开始到
的物质的量随时间变化如图。从反应开始到 末,用
末,用 浓度变化表示的平均反应速率
浓度变化表示的平均反应速率
___________ ;反应从开始达到平衡状态,此时过程 的转化率为
的转化率为___________ 。

(4)在相同温度、容积不变的条件下,能说明该反应已达平衡状态的是___________。
 生产甲醇
生产甲醇 实现“碳中和“的重要途径。其原理是:
实现“碳中和“的重要途径。其原理是: 。
。(1)该反应的能量变化如图所示,该反应为

(2)恒容容器中,对于上述反应,下列措施就加快反应速率的是___________。
| A.升高温度 | B.充入He |
| C.加入合适的催化剂 | D.减少二氧化碳的通入量 |
 的密闭容器中,充入
的密闭容器中,充入 和
和 ,测得
,测得 、
、 的物质的量随时间变化如图。从反应开始到
的物质的量随时间变化如图。从反应开始到 末,用
末,用 浓度变化表示的平均反应速率
浓度变化表示的平均反应速率
 的转化率为
的转化率为
(4)在相同温度、容积不变的条件下,能说明该反应已达平衡状态的是___________。
A. 、 、 的浓度均不再变化 的浓度均不再变化 |
| B.体系压强不变 |
C. |
D. 的消耗速率与 的消耗速率与 的生成速率之比为 的生成速率之比为 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】中国提出要实现“二氧化碳排放力争于2030年前达到峰值,争取在2060年前实现碳中和”的目标,二氧化碳的资源化利用对实现碳中和目标具有促进作用。
甲醇是一种可再生能源,由 制备甲醇可能涉及的反应如下:
制备甲醇可能涉及的反应如下:
反应I:

反应II:
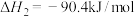
反应III:

已知部分化学键键能如表:
回答下列问题:
(1)反应I自发趋势是___________。
(2)在一密闭容器中充入 和
和 ,分别在
,分别在 、
、 、
、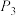 压强下进行反应,测得
压强下进行反应,测得 的平衡转化率随温度的变化如图所示,
的平衡转化率随温度的变化如图所示, 温度后,反应主要以
温度后,反应主要以___________ (填反应I、反应II或反应III)为主。为了提高 生成
生成 的平衡转化率,同时减少反应III的发生,可采取的措施是
的平衡转化率,同时减少反应III的发生,可采取的措施是___________ 。
(3)在一定条件下,向体积为 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,假设仅发生反应I,测得
,假设仅发生反应I,测得 和
和 的物质的量浓度随时间的变化如图所示。
的物质的量浓度随时间的变化如图所示。
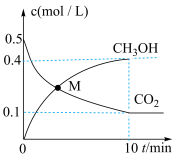
① 内,氢气的平均反应速率为
内,氢气的平均反应速率为___________ 。
②下列叙述中一定能说明该反应达到平衡状态的是___________ 。
A.化学反应速率关系: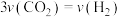
B.容器内混合气体的密度不再改变
C.单位时间内,每断裂2个C=O键,同时断裂3个O—H键
D.容器内混合气体的平均摩尔质量不再改变
(4)加热锅炉时,水中的 可以先转化为
可以先转化为 ,然后转化为
,然后转化为 。已知:
。已知: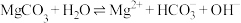 在80℃时的平衡常数为K,水的离子积为
在80℃时的平衡常数为K,水的离子积为 ,碳酸的第一级和第二级电离常数分别为
,碳酸的第一级和第二级电离常数分别为 和
和 ,则该温度下
,则该温度下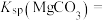
___________ (用相关常数表示)。
(5)二甲醚 直接燃料电池具有启动快、效率高、能量密度大等优点。若电解质溶液呈碱性、二甲醚直接燃料电池的负极反应为
直接燃料电池具有启动快、效率高、能量密度大等优点。若电解质溶液呈碱性、二甲醚直接燃料电池的负极反应为___________ 。
甲醇是一种可再生能源,由
 制备甲醇可能涉及的反应如下:
制备甲醇可能涉及的反应如下:反应I:


反应II:

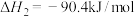
反应III:


已知部分化学键键能如表:
| 化学键 | H—H | O—H | C—H | C—O | C=O |
键能 | 436 | 463 | 414 | 326 | 803 |
(1)反应I自发趋势是___________。
| A.高温自发 | B.低温自发 |
| C.任意温度下自发 | D.任意温度下非自发 |
(2)在一密闭容器中充入
 和
和 ,分别在
,分别在 、
、 、
、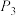 压强下进行反应,测得
压强下进行反应,测得 的平衡转化率随温度的变化如图所示,
的平衡转化率随温度的变化如图所示, 温度后,反应主要以
温度后,反应主要以 生成
生成 的平衡转化率,同时减少反应III的发生,可采取的措施是
的平衡转化率,同时减少反应III的发生,可采取的措施是
(3)在一定条件下,向体积为
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,假设仅发生反应I,测得
,假设仅发生反应I,测得 和
和 的物质的量浓度随时间的变化如图所示。
的物质的量浓度随时间的变化如图所示。
①
 内,氢气的平均反应速率为
内,氢气的平均反应速率为②下列叙述中一定能说明该反应达到平衡状态的是
A.化学反应速率关系:
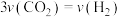
B.容器内混合气体的密度不再改变
C.单位时间内,每断裂2个C=O键,同时断裂3个O—H键
D.容器内混合气体的平均摩尔质量不再改变
(4)加热锅炉时,水中的
 可以先转化为
可以先转化为 ,然后转化为
,然后转化为 。已知:
。已知: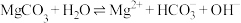 在80℃时的平衡常数为K,水的离子积为
在80℃时的平衡常数为K,水的离子积为 ,碳酸的第一级和第二级电离常数分别为
,碳酸的第一级和第二级电离常数分别为 和
和 ,则该温度下
,则该温度下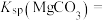
(5)二甲醚
 直接燃料电池具有启动快、效率高、能量密度大等优点。若电解质溶液呈碱性、二甲醚直接燃料电池的负极反应为
直接燃料电池具有启动快、效率高、能量密度大等优点。若电解质溶液呈碱性、二甲醚直接燃料电池的负极反应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】CO可用于合成甲醇,化学方程式为:CO(g)+2H2(g)⇌CH3OH(g)。
(1)图1是反应CO(g)+2H2(g)⇌CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。
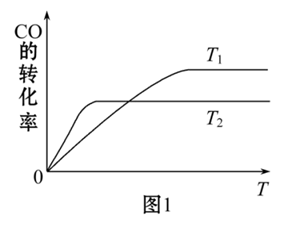
①该反应的焓变ΔH_______ 0(填“>”“<”或“=”)。
②在T1温度下,往体积为1L的密闭容器中,充入1molCO和2molH2,经测得CO和CH3OH的浓度随时间变化如图2所示。则该反应的平衡常数表达式为K=_______ ,H2的平衡转化率为_______ 。
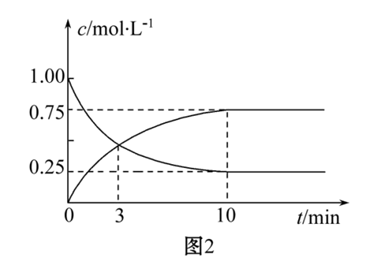
③若容器容积不变,下列措施可增加CO转化率的是_______ (填字母)。
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
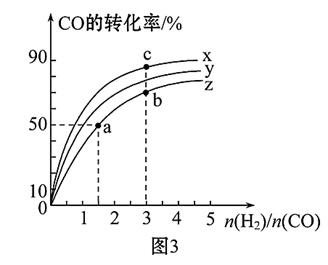
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线z对应的温度是_______ ℃;该温度下上述反应的化学平衡常数为_______ 。曲线上a、b、c点对应的化学平衡常数分别为K1、K2、K3,则K1、K2、K3的大小关系为_______ 。
(1)图1是反应CO(g)+2H2(g)⇌CH3OH(g)在不同温度下CO的转化率随时间变化的曲线。

①该反应的焓变ΔH
②在T1温度下,往体积为1L的密闭容器中,充入1molCO和2molH2,经测得CO和CH3OH的浓度随时间变化如图2所示。则该反应的平衡常数表达式为K=

③若容器容积不变,下列措施可增加CO转化率的是
a.升高温度 b.将CH3OH(g)从体系中分离
c.使用合适的催化剂 d.充入He,使体系总压强增大
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。如图3是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线z对应的温度是

您最近一年使用:0次



