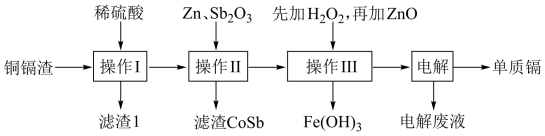
金属回收与利用有利于环境保护,镉可用于制造体积小和电容量大的电池。铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质,湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度均为0.1mol·L-1)
(1)滤渣Ⅰ可用硫酸酸化的双氧水浸取经结晶制取胆矾,试写出浸取过程离子方程式___________ 。
(2)操作Ⅱ“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的化学方程式:___________ 。
(3)操作Ⅲ加入ZnO控制反应液的pH范围为___________ ;若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案加以检验:___________ 。
(4)“电解”过程中以石墨为电极得到粗镉,电解阳极反应式为___________ ;电解废液最好在___________ 加入循环利用。(选择“操作I”、“操作Ⅱ”、“操作Ⅲ”、“电解”工序名称填入横线上)
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的阳极反应式为___________ ;如果用生石灰处理含Cd2+(2.88×10-4mol/L)的电解废液。常温下,当pH=10时,镉的去除率为___________ 。(用百分数表达,小数点后两位有效数字。已知常温下,Ksp[Cd(OH)2]=7.2×10-15)

下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度均为0.1mol·L-1)
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.7 | 6.3 | 7.5 |
| 沉淀完全的pH | 2.8 | 8.4 | 9.3 |
(2)操作Ⅱ“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的化学方程式:
(3)操作Ⅲ加入ZnO控制反应液的pH范围为
(4)“电解”过程中以石墨为电极得到粗镉,电解阳极反应式为
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的阳极反应式为
2021·甘肃金昌·模拟预测 查看更多[6]
甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)安徽省滁州市定远县育才学校2021-2022学年高三下学期开学考试理科综合化学试题湖南省常德市鼎城一中2022-2023学年高三第五次月考化学试题(已下线)T27-工业流程题
更新时间:2022-01-27 23:31:34
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
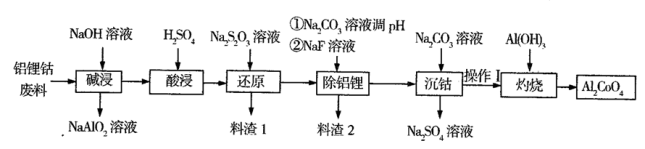
【推荐1】钴蓝(化学式Al2CoO4)是一种耐热、耐光、耐酸、耐碱腐蚀的蓝色颜料。某企业利用含铝锂钴废料(铝箱、CoO和Co2O3、Li2O)制备钴蓝的工艺流程如下:
回答下列问题:
(1)碱浸时要有防火、防爆措施,原因是______ ,操作I的内容是_______ 。
(2)在实验室模拟工业生产时,也可用盐酸酸浸出钴,但实际工业生产中却不用盐酸,请 从反应原理分析不用盐酸浸出钴的主要原因___ 。
(3)写出“还原”过程中反应的离子方程式____ 。
(4)料渣2的主要成分是A1(OH)3 、____ ,写出灼烧时反应的化学方程式______ 。
回答下列问题:
(1)碱浸时要有防火、防爆措施,原因是
(2)在实验室模拟工业生产时,也可用盐酸酸浸出钴,但实际工业生产中却不用盐酸,请 从反应原理分析不用盐酸浸出钴的主要原因
(3)写出“还原”过程中反应的离子方程式
(4)料渣2的主要成分是A1(OH)3 、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】聚合硫酸铁是水处理中重要的絮凝剂。以黄铁矿的烧渣 主要成分为Fe2O3、FeO、SiO2等
主要成分为Fe2O3、FeO、SiO2等 为原料制取聚合硫酸铁(Fe2(OH)x(SO4)(3-
为原料制取聚合硫酸铁(Fe2(OH)x(SO4)(3-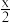 ))的工艺流程如图所示:
))的工艺流程如图所示:

(1)“酸浸”时最合适的酸是___________  写化学式
写化学式 。
。
(2)“酸浸”后溶液中主要的金属阳离子有___________ 。
(3)写出KClO3的与FeSO4反应的离子方程式___________ 。
(4)聚合硫酸铁能净水原因是___________ (用文字描述)。
 主要成分为Fe2O3、FeO、SiO2等
主要成分为Fe2O3、FeO、SiO2等 为原料制取聚合硫酸铁(Fe2(OH)x(SO4)(3-
为原料制取聚合硫酸铁(Fe2(OH)x(SO4)(3-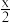 ))的工艺流程如图所示:
))的工艺流程如图所示:
(1)“酸浸”时最合适的酸是
 写化学式
写化学式 。
。(2)“酸浸”后溶液中主要的金属阳离子有
(3)写出KClO3的与FeSO4反应的离子方程式
(4)聚合硫酸铁能净水原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某工厂排出的废水中含有大量的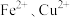 和
和 。为了减少污染并变废为宝,某实验小组在实验室设计了如下流程,以回收铜和硫酸亚铁。请回答:
。为了减少污染并变废为宝,某实验小组在实验室设计了如下流程,以回收铜和硫酸亚铁。请回答:
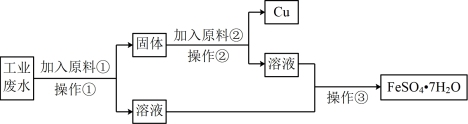
(1)原料①为金属___________ (填元素符号)。
(2)加入原料②是为了溶解过量的①,加入原料②反应的离子方程式___________ 。
(3)操作②要用到的玻璃仪器的名称是漏斗、___________ 、玻璃棒。
(4)操作③要用到蒸发皿,操作③的实验名称是___________ 。
(5)硫酸亚铁分解生成铁红,将反应补充完整: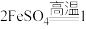
________ 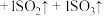 。
。
(6)硫酸亚铁溶液吸收氯气的离子方程式为___________ 。
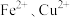 和
和 。为了减少污染并变废为宝,某实验小组在实验室设计了如下流程,以回收铜和硫酸亚铁。请回答:
。为了减少污染并变废为宝,某实验小组在实验室设计了如下流程,以回收铜和硫酸亚铁。请回答:
(1)原料①为金属
(2)加入原料②是为了溶解过量的①,加入原料②反应的离子方程式
(3)操作②要用到的玻璃仪器的名称是漏斗、
(4)操作③要用到蒸发皿,操作③的实验名称是
(5)硫酸亚铁分解生成铁红,将反应补充完整:
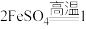
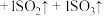 。
。(6)硫酸亚铁溶液吸收氯气的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】按要求填空。
(1) Na2CO3溶液中滴入酚酞试液呈红色,原因是(用离子方程式表示)_____ ;加热后颜色变深,原因_____ 。
(2) FeCl3具有净水作用的原理(用离子方程式表示)_______ 。
(3)将NaHCO3溶液与AlCl3溶液混合(写出反应的离子方程式)_______ 。
(4)已知25℃时,Ksp[Mg(OH)2]=1.6×10-11。向0.01 mol/L的MgCl2溶液中,逐滴加入NaOH溶液,刚好出现沉淀时,溶液的c(OH-)为_____ mol/L;
(5)常温时,Fe(OH)3的溶度积常数Ksp=1×10-38,要使溶液中的Fe3+沉淀完全[残留在溶液中的c(Fe3+)<10-5 mol/L],则溶液的pH应大于_______ 。
(6) 25℃时,在2.0×10-3 mol/L的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-)、c(HF)与溶液 pH的关系如下图。则25℃时,HF电离平衡常数为Ka(HF)=______ 。

(1) Na2CO3溶液中滴入酚酞试液呈红色,原因是(用离子方程式表示)
(2) FeCl3具有净水作用的原理(用离子方程式表示)
(3)将NaHCO3溶液与AlCl3溶液混合(写出反应的离子方程式)
(4)已知25℃时,Ksp[Mg(OH)2]=1.6×10-11。向0.01 mol/L的MgCl2溶液中,逐滴加入NaOH溶液,刚好出现沉淀时,溶液的c(OH-)为
(5)常温时,Fe(OH)3的溶度积常数Ksp=1×10-38,要使溶液中的Fe3+沉淀完全[残留在溶液中的c(Fe3+)<10-5 mol/L],则溶液的pH应大于
(6) 25℃时,在2.0×10-3 mol/L的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-)、c(HF)与溶液 pH的关系如下图。则25℃时,HF电离平衡常数为Ka(HF)=

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、
、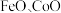 等)为原料制备
等)为原料制备 的工艺流程如图。
的工艺流程如图。
(1)沉淀池1中,先加 充分反应后再加氨水。写出加
充分反应后再加氨水。写出加 时发生反应的离子方程式:
时发生反应的离子方程式:___________ 。
(2)沉淀池2中,选择含硫沉淀剂而不选择 的原因是
的原因是___________ 。
(3)如图为 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取
的溶液”中提取 晶体”的操作为
晶体”的操作为___________ ,洗涤干燥。 。其含量测定方法如下。
。其含量测定方法如下。
称取 废渣,加酸将锰元素全部溶出成
废渣,加酸将锰元素全部溶出成 ,过滤,
,过滤,
i.将滤液定容于 容量瓶中;
容量瓶中;
ii.取 溶液于锥形瓶中,加入少量催化剂和过量
溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热、充分反应后。
溶液,加热、充分反应后。
iii.煮沸溶液使过量的 分解。
分解。
iv.加入指示剂,用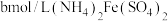 溶液滴定。滴定至终点时消耗
溶液滴定。滴定至终点时消耗 溶液的体积为
溶液的体积为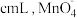 重新变成
重新变成 。
。
①步骤ii中反应的离子方程式是___________ 。
②废渣中锰元素的质量分数为___________ 。
③若省略步骤iii,则测定的结果将___________ (填“偏大”“偏小”或“不变”)。
(5)废渣若长期露置于空气,其中的锰元素会逐渐转化为 。研究者用如图装置提取
。研究者用如图装置提取 中的锰元素。图中“
中的锰元素。图中“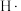 ”代表氢自由基。实验测得电解时间相同时,随外加电流的增大,溶液中
”代表氢自由基。实验测得电解时间相同时,随外加电流的增大,溶液中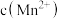 先增大后减小,减小的原因是
先增大后减小,减小的原因是___________ (写出两条)。
 是一种重要的化工产品。以菱锰矿(主要成分为
是一种重要的化工产品。以菱锰矿(主要成分为 ,还含有
,还含有 、
、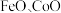 等)为原料制备
等)为原料制备 的工艺流程如图。
的工艺流程如图。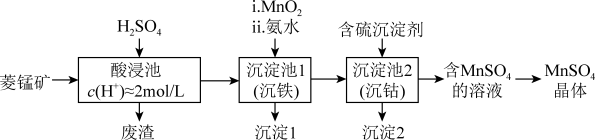
| 难溶物 |  |  |  |  |  |  |
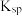 | 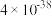 | 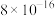 |  | 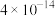 | 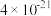 | 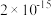 |
(1)沉淀池1中,先加
 充分反应后再加氨水。写出加
充分反应后再加氨水。写出加 时发生反应的离子方程式:
时发生反应的离子方程式:(2)沉淀池2中,选择含硫沉淀剂而不选择
 的原因是
的原因是(3)如图为
 和
和 的溶解度曲线。从“含
的溶解度曲线。从“含 的溶液”中提取
的溶液”中提取 晶体”的操作为
晶体”的操作为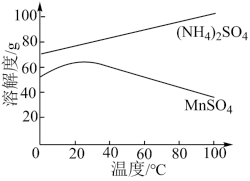
 。其含量测定方法如下。
。其含量测定方法如下。称取
 废渣,加酸将锰元素全部溶出成
废渣,加酸将锰元素全部溶出成 ,过滤,
,过滤,i.将滤液定容于
 容量瓶中;
容量瓶中;ii.取
 溶液于锥形瓶中,加入少量催化剂和过量
溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热、充分反应后。
溶液,加热、充分反应后。iii.煮沸溶液使过量的
 分解。
分解。iv.加入指示剂,用
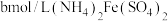 溶液滴定。滴定至终点时消耗
溶液滴定。滴定至终点时消耗 溶液的体积为
溶液的体积为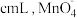 重新变成
重新变成 。
。①步骤ii中反应的离子方程式是
②废渣中锰元素的质量分数为
③若省略步骤iii,则测定的结果将
(5)废渣若长期露置于空气,其中的锰元素会逐渐转化为
 。研究者用如图装置提取
。研究者用如图装置提取 中的锰元素。图中“
中的锰元素。图中“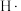 ”代表氢自由基。实验测得电解时间相同时,随外加电流的增大,溶液中
”代表氢自由基。实验测得电解时间相同时,随外加电流的增大,溶液中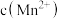 先增大后减小,减小的原因是
先增大后减小,减小的原因是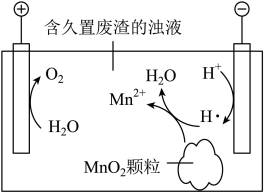
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】碱式碳酸镁不溶于水,用途广泛,主要用作橡胶制品的填充剂,能增强橡胶的耐磨性和强度。也可用作油漆和涂料的添加剂,也可用于牙膏、医药和化妆品等工业。以水氯镁石(主要成分为MgCl2·6H2O)为原料生产碱式碳酸镁的主要流程如下:

(1)上述流程中过滤时所需玻璃仪器除烧杯、玻璃棒外还需_______ ,从滤液中得到NH4Cl固体的主要实验操作有_______ 、_______ 、过滤、洗涤和干燥。
(2)已知:常温下Ka1(H2CO3)=4.4×10-7,Ka2(H2CO3)=4.7×10-11,Kb(NH3·H2O)=1.8×10-5,则NH4HCO3溶液显_______ 性,c( )
)_______ c( )(选填“大于”、“小于”、“等于”),该溶液物料守恒表达式为
)(选填“大于”、“小于”、“等于”),该溶液物料守恒表达式为_______ 。
(3)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Ksp(Mg(OH)2)=1.8×10-11,表示Mg(OH)2沉淀溶解平衡的方程式为_______ ,Mg(OH)2达到沉淀溶解平衡时溶液的pH=_______ (已知:lg36≈1.5)。

(1)上述流程中过滤时所需玻璃仪器除烧杯、玻璃棒外还需
(2)已知:常温下Ka1(H2CO3)=4.4×10-7,Ka2(H2CO3)=4.7×10-11,Kb(NH3·H2O)=1.8×10-5,则NH4HCO3溶液显
 )
) )(选填“大于”、“小于”、“等于”),该溶液物料守恒表达式为
)(选填“大于”、“小于”、“等于”),该溶液物料守恒表达式为(3)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Ksp(Mg(OH)2)=1.8×10-11,表示Mg(OH)2沉淀溶解平衡的方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I:已知反应:H2(g)+ O2(g)=H2O(g) △H1
O2(g)=H2O(g) △H1
N2(g)+2O2=2NO2(g) △H2
 N2(g)+
N2(g)+ H2(g)=NH3(g) △H3
H2(g)=NH3(g) △H3
(1)利用上述三个反应,计算4NH3(g)+7O2(g)=4NO2(g)+6H2O(g)的反应焓变为_______ (用含△H1、△H2、△H3的式子表示)。
(2)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ/mol;
2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol;
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol。
尾气转化的反应之一为NO和CO生成N2和CO2,则该反应的热化学方程式为:_______
II: 二甲醚(CH3-O-CH3)代替氟利昂作为制冷剂可减少臭氧空洞。若用二甲醚-O2燃料电池作为电源,利用电解法制备纳米Cu2O,其装置如下图所示。

(3)上述装置中D电极应连接二甲醚燃料电池中通_______ (“CH3-O-CH3”或“O2”)的一极,该电解池中离子交换膜为_______ 离子交换膜(填“阴”或“阳”)。
(4)该电解池的阳极反应式为_______ 。
 O2(g)=H2O(g) △H1
O2(g)=H2O(g) △H1N2(g)+2O2=2NO2(g) △H2
 N2(g)+
N2(g)+ H2(g)=NH3(g) △H3
H2(g)=NH3(g) △H3(1)利用上述三个反应,计算4NH3(g)+7O2(g)=4NO2(g)+6H2O(g)的反应焓变为
(2)在汽车上安装三效催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5 kJ/mol;
2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ/mol;
C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ/mol。
尾气转化的反应之一为NO和CO生成N2和CO2,则该反应的热化学方程式为:
II: 二甲醚(CH3-O-CH3)代替氟利昂作为制冷剂可减少臭氧空洞。若用二甲醚-O2燃料电池作为电源,利用电解法制备纳米Cu2O,其装置如下图所示。

(3)上述装置中D电极应连接二甲醚燃料电池中通
(4)该电解池的阳极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。请回答:
I.用如图所示装置进行第一组实验。
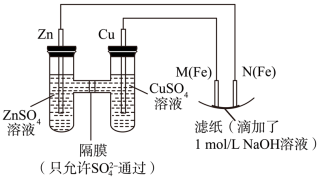
(1)N极发生反应的电极反应式为_________ .
(2)实验过程中,SO42-______ (填“从左向右”、“从右向左”或“不”)移动;
II.用如图所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
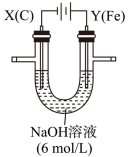
(3)电解过程中,X极区溶液的pH______ (填“增大”、“减小”或“不变”)
(4)电解过程中,Y极发生的电极反应为_____________ 和4OH-- 4e-= 2H2O + O2↑
(5)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少______ g
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极发生的反应的电极反应式为__________
I.用如图所示装置进行第一组实验。

(1)N极发生反应的电极反应式为
(2)实验过程中,SO42-
II.用如图所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。

(3)电解过程中,X极区溶液的pH
(4)电解过程中,Y极发生的电极反应为
(5)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极发生的反应的电极反应式为
您最近一年使用:0次
【推荐3】废旧无汞碱性锌锰电池可用于制造隐形战机的机身涂料MnxZn(1-x)Fe2O4,该电池工作反应原理为Zn+2MnO2+2H2O 2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
A.浸取:将去除表面塑料的旧电池加入水中浸取并过滤,滤液经操作a得KOH固体;
B.溶液:滤渣中加入过量稀硫酸和足量双氧水,至不再出现气泡时,过滤;
C.测成分:测步骤B中滤液成分,然后加入铁粉;
D.氧化:加入双氧水氧化;
E.调pH:滴加氨水调pH,经结晶处理得MnxZn(1-x)Fe2O4。
(1)浸取时的操作有______ 。
A.拆解、粉碎旧电池 B.降低温度 C.搅拌 D.加压
(2)操作a为________ 。
(3)溶渣时生成Mn2+的主要离子方程式为______________________________ 。
(4)若步骤C测得滤液中金属离子组成为:c(Mn2+) +c(Zn2+) =0.8mol/L, c(Fe2+ ) = 0. 1 mol/L。若滤液体积为lm3,要合成MnxZn(1-x)Fe2O4,需加入Fe粉质量为___________ kg(忽略体积变化)。
(5)氧化时,因为分解所需双氧水的量比理论值大得多。其原因可能是①温度过高;②______ 。
(6)最后一步结晶时,处理不当易生成MnFe2O4和ZnFe2O4。要制得MnxZn(1-x)Fe2O4,最后一步结晶时需注意______________________ 。
(7)某小组构想用ZnSO4、MnSO4溶液为原料,以Fe作电极用电解法经过一系列步骤制得MnxZn(1-x)Fe2O4,则开始电解时阳极反应式为___________________________________ 。
 2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:A.浸取:将去除表面塑料的旧电池加入水中浸取并过滤,滤液经操作a得KOH固体;
B.溶液:滤渣中加入过量稀硫酸和足量双氧水,至不再出现气泡时,过滤;
C.测成分:测步骤B中滤液成分,然后加入铁粉;
D.氧化:加入双氧水氧化;
E.调pH:滴加氨水调pH,经结晶处理得MnxZn(1-x)Fe2O4。
(1)浸取时的操作有
A.拆解、粉碎旧电池 B.降低温度 C.搅拌 D.加压
(2)操作a为
(3)溶渣时生成Mn2+的主要离子方程式为
(4)若步骤C测得滤液中金属离子组成为:c(Mn2+) +c(Zn2+) =0.8mol/L, c(Fe2+ ) = 0. 1 mol/L。若滤液体积为lm3,要合成MnxZn(1-x)Fe2O4,需加入Fe粉质量为
(5)氧化时,因为分解所需双氧水的量比理论值大得多。其原因可能是①温度过高;②
(6)最后一步结晶时,处理不当易生成MnFe2O4和ZnFe2O4。要制得MnxZn(1-x)Fe2O4,最后一步结晶时需注意
(7)某小组构想用ZnSO4、MnSO4溶液为原料,以Fe作电极用电解法经过一系列步骤制得MnxZn(1-x)Fe2O4,则开始电解时阳极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O ]为浅绿色晶体,又称摩尔盐,能溶于水,难溶于乙醇。某兴趣小组以废铁屑(含少量硫化物、Fe2O3、油污等杂质)为原料制备摩尔盐的流程如下:

回答下列问题:
(1)“酸溶”在如图所示装置中完成(部分夹持装置省略)。仪器a的名称是_______ ,反应过程中有臭鸡蛋气味气体(H2S)产生,则装置B的作用是_______ 。

(2)“还原”过程主要反应的离子方程式为_______ 。
(3)“系列操作”包括:将转化后溶液蒸发浓缩至有晶膜出现时,_______ ,过滤,用无水乙醇洗涤,晾干。
(4)产品纯度测定:准确称取8.0g产品,加硫酸溶解,用容量瓶配制100mL溶液。取25.00mL上述溶液于锥形瓶中,用0.0500mol·L-1酸性KMnO4标准溶液滴定,消耗标准溶液体积数据如表所示:
(滴定原理:5Fe2+ + MnO + 8H+ = Mn2+ + 5Fe3+ +4H2O)
+ 8H+ = Mn2+ + 5Fe3+ +4H2O)
①配制样品溶液时,用到的玻璃仪器有烧杯、玻璃棒、_______ 、胶头滴管。滴定达到终点的标志是_______ 。
②产品的纯度为_______ [(NH4)2SO4·FeSO4·6H2O 的摩尔质量为392g·mol-1)]。
③滴定前锥形瓶用蒸馏水洗净后没有干燥,则消耗标准溶液体积_______ ;若滴定终点时俯视读数会造成测定结果_______ (填“偏高”“偏低”或“无影响”)。

回答下列问题:
(1)“酸溶”在如图所示装置中完成(部分夹持装置省略)。仪器a的名称是

(2)“还原”过程主要反应的离子方程式为
(3)“系列操作”包括:将转化后溶液蒸发浓缩至有晶膜出现时,
(4)产品纯度测定:准确称取8.0g产品,加硫酸溶解,用容量瓶配制100mL溶液。取25.00mL上述溶液于锥形瓶中,用0.0500mol·L-1酸性KMnO4标准溶液滴定,消耗标准溶液体积数据如表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗酸性 KMnO 4标准溶液的体积/mL | 21.60 | 20.02 | 20.00 | 19.98 |
(滴定原理:5Fe2+ + MnO
 + 8H+ = Mn2+ + 5Fe3+ +4H2O)
+ 8H+ = Mn2+ + 5Fe3+ +4H2O)①配制样品溶液时,用到的玻璃仪器有烧杯、玻璃棒、
②产品的纯度为
③滴定前锥形瓶用蒸馏水洗净后没有干燥,则消耗标准溶液体积
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氮化镓(GaN)被称为“终极半导体材料”,工业生产中利用矿渣(主要含铁酸镓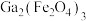 、铁酸锌
、铁酸锌 、
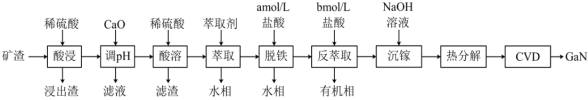
、 )制备GaN的流程如图所示:
)制备GaN的流程如图所示:
已知:①25℃时,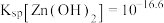 ,
, ,
,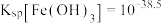 ;
;
②在该工艺条件下 、
、 的反萃取率与盐酸浓度的关系见下表(反萃取率指进入水相中的金属离子百分数)。
的反萃取率与盐酸浓度的关系见下表(反萃取率指进入水相中的金属离子百分数)。
回答下列问题:
(1)基态Ga原子的核外电子排布式为___________ 。
(2)①“酸浸”时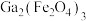 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
②“酸浸”后浸出液中 、
、 浓度分别为
浓度分别为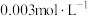 、
、 ,溶液中某离子浓度
,溶液中某离子浓度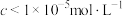 时认为该离子沉淀完全,则常温下,利用CaO调节pH的范围应为
时认为该离子沉淀完全,则常温下,利用CaO调节pH的范围应为___________ (忽略溶液体积变化)。
(3)“反萃取”时,所用盐酸的浓度
___________  (选填上表中盐酸的浓度)。
(选填上表中盐酸的浓度)。
(4)①利用CVD(化学气相沉积)技术,将热分解得到的___________ 与 在高温下反应可制得GaN。②工业上还可用含Ga的有机化合物
在高温下反应可制得GaN。②工业上还可用含Ga的有机化合物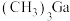 与
与 作为原料,在高温下反应生成GaN,该反应的化学方程式为
作为原料,在高温下反应生成GaN,该反应的化学方程式为___________ 。
(5)GaN的熔点为1700℃,其晶体的一种立方晶胞如图所示。该晶体中与Ga原子距离最近且相等的Ga原子数为___________ 。若晶胞边长为dnm, 为阿伏加德罗常数的值,则晶体密度为
为阿伏加德罗常数的值,则晶体密度为
___________ 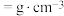 (列出表达式即可)。
(列出表达式即可)。

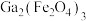 、铁酸锌
、铁酸锌 、
、 )制备GaN的流程如图所示:
)制备GaN的流程如图所示:
已知:①25℃时,
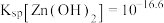 ,
, ,
,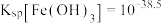 ;
;②在该工艺条件下
 、
、 的反萃取率与盐酸浓度的关系见下表(反萃取率指进入水相中的金属离子百分数)。
的反萃取率与盐酸浓度的关系见下表(反萃取率指进入水相中的金属离子百分数)。盐酸浓度/ | 2.0 | 4.0 | 6.0 |
 反萃取率/% 反萃取率/% | 9.4 | 52.1 | 71.3 |
 反萃取率/% 反萃取率/% | 86.9 | 69.1 | 17.5 |
(1)基态Ga原子的核外电子排布式为
(2)①“酸浸”时
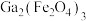 发生反应的离子方程式为
发生反应的离子方程式为②“酸浸”后浸出液中
 、
、 浓度分别为
浓度分别为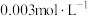 、
、 ,溶液中某离子浓度
,溶液中某离子浓度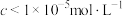 时认为该离子沉淀完全,则常温下,利用CaO调节pH的范围应为
时认为该离子沉淀完全,则常温下,利用CaO调节pH的范围应为(3)“反萃取”时,所用盐酸的浓度

 (选填上表中盐酸的浓度)。
(选填上表中盐酸的浓度)。(4)①利用CVD(化学气相沉积)技术,将热分解得到的
 在高温下反应可制得GaN。②工业上还可用含Ga的有机化合物
在高温下反应可制得GaN。②工业上还可用含Ga的有机化合物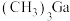 与
与 作为原料,在高温下反应生成GaN,该反应的化学方程式为
作为原料,在高温下反应生成GaN,该反应的化学方程式为(5)GaN的熔点为1700℃,其晶体的一种立方晶胞如图所示。该晶体中与Ga原子距离最近且相等的Ga原子数为
 为阿伏加德罗常数的值,则晶体密度为
为阿伏加德罗常数的值,则晶体密度为
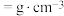 (列出表达式即可)。
(列出表达式即可)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】某化学兴趣小组的四位同学围绕“从含铜废料中回收铜”提出了各自的看法。甲同学根据已学知识,提出了一套回收方案:

乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu+2H2SO4+O2 2CuSO4+2H2O),于是他提出了另一套方案:
2CuSO4+2H2O),于是他提出了另一套方案:

(1)甲方案的②③两个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:②___ ;③___ 。
(2)从环保角度对两套方案的不同部分进行比较,你认为___ (选填“甲”或“乙”)的方案更合理。理由是:___ 。
(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑。丙的理由是:___ 。丁又提出了疑问:“如果铁过量,剩余的铁会混在红色粉末中,该用什么化学方法处理?”请提出你的处理方案:___ 。
(4)最后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益。请写出使“绿矾”结晶的两种可能方法:___ 、___ (“绿矾”溶解度随温度升高而增大)。

乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu+2H2SO4+O2
 2CuSO4+2H2O),于是他提出了另一套方案:
2CuSO4+2H2O),于是他提出了另一套方案:
(1)甲方案的②③两个步骤中,与铜或铜的化合物有关的化学反应方程式分别是:②
(2)从环保角度对两套方案的不同部分进行比较,你认为
(3)丙认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑。丙的理由是:
(4)最后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益。请写出使“绿矾”结晶的两种可能方法:
您最近一年使用:0次



