阅读如下资料:
i.乙烯可在加热条件下催化氧化制得环氧乙烷( );具有强穿透力的环氧乙烷在常温下能杀灭微生物。
);具有强穿透力的环氧乙烷在常温下能杀灭微生物。
ii.环氧乙烷与水在加压、加热的条件下化合为乙二醇;乙二醇的熔点为-12.9℃,沸点197.3℃;能与水、丙酮等互溶。
iii.汽车铝制水箱(即散热器)中盛装的某防冻液(乙二醇与水是主要成分,体积比约1:1),沸点为108℃,冰点为-38℃;其中常加入适量NaH2PO4,用来消除水箱中严生的碱性水垢,从而提高散热效果。
iv.25℃ H3PO4Ka1=6.9×10-3,Ka2=6.2×10-8,Ka3=4.8×10-13。
结合题干信息,请按要求回答下列问题:
(1)环氧乙烷的分子式:____ ,其含有的官能团名称:____ 。
(2)乙二醇能与丙酮互溶的原因可能是乙二醇与丙酮都是极性分子,符合“相似相溶”的规律,还可能是____ 。
(3)结合ii、iii、iv中数据信息解释如下问题。
①NaH2PO4能除水垢的原因为____ ;故NaH2PO4水溶液显弱酸性,可消除碱性水垢。
②防冻液在使用一段时间后pH会降低的可能原因为____ 。
(4)结合已学知识及i、ii中信息,将如下两种合成乙二醇的路线补充完整(方框内填有机产物,箭头上填无机试剂及其反应条件)
①CH2=CH2
 →CH2OHCH2OH
→CH2OHCH2OH____
②CH2=CH2→ →CH2OHCH2OH
→CH2OHCH2OH____
生产乙二醇常采用路线②而不采用路线①,其可能原因(写出一种)是____ 。
i.乙烯可在加热条件下催化氧化制得环氧乙烷(
 );具有强穿透力的环氧乙烷在常温下能杀灭微生物。
);具有强穿透力的环氧乙烷在常温下能杀灭微生物。ii.环氧乙烷与水在加压、加热的条件下化合为乙二醇;乙二醇的熔点为-12.9℃,沸点197.3℃;能与水、丙酮等互溶。
iii.汽车铝制水箱(即散热器)中盛装的某防冻液(乙二醇与水是主要成分,体积比约1:1),沸点为108℃,冰点为-38℃;其中常加入适量NaH2PO4,用来消除水箱中严生的碱性水垢,从而提高散热效果。
iv.25℃ H3PO4Ka1=6.9×10-3,Ka2=6.2×10-8,Ka3=4.8×10-13。
结合题干信息,请按要求回答下列问题:
(1)环氧乙烷的分子式:
(2)乙二醇能与丙酮互溶的原因可能是乙二醇与丙酮都是极性分子,符合“相似相溶”的规律,还可能是
(3)结合ii、iii、iv中数据信息解释如下问题。
①NaH2PO4能除水垢的原因为
②防冻液在使用一段时间后pH会降低的可能原因为
(4)结合已学知识及i、ii中信息,将如下两种合成乙二醇的路线补充完整(方框内填有机产物,箭头上填无机试剂及其反应条件)
①CH2=CH2

 →CH2OHCH2OH
→CH2OHCH2OH②CH2=CH2→
 →CH2OHCH2OH
→CH2OHCH2OH生产乙二醇常采用路线②而不采用路线①,其可能原因(写出一种)是
更新时间:2022-03-13 13:28:53
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】表示有机物组成的方式有多种,根据下列有机物的组成,回答有关问题。
① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨C17H35COOH ⑩CH3CHO
⑨C17H35COOH ⑩CH3CHO
(1)属于烷烃的是_______ (填序号,下同),属于不饱和烃的是_______ 。
(2)属于同分异构体的是_______ ,属于同系物的是_______ 。
(3)有机物⑨和⑩中所含官能团的名称分别为_______ 、_______ 。
(4)有机物⑦的名称为_______ 。
(5)写出④在一定条件下生成高分子化合物的化学方程式:_______ 。
①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨C17H35COOH ⑩CH3CHO
⑨C17H35COOH ⑩CH3CHO(1)属于烷烃的是
(2)属于同分异构体的是
(3)有机物⑨和⑩中所含官能团的名称分别为
(4)有机物⑦的名称为
(5)写出④在一定条件下生成高分子化合物的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】[化学——选修5:有机化学基础]
双安妥明可用于降低血液中的胆固醇,其结构简式为:
该物质合成线路如下图所示:

已知:I.
II.
II.已知:A的密度是同温同压下H2密度的28倍,且支链有一个甲基;G能发生银镜反应,且1molG能与2mol H2发生加成反应;I的结构具有对称性。试回答下列问题:
(1)双安妥明的分子式为___________________ 。
(2)A的结构简式为_____________ ;F的结构简式为 ______________ 。
(3)反应B→C的反应条件是__________ , G→H的反应类型是 ______________ 。
(4)反应“F+I→双安妥明”的化学方程式为_______________________________ 。
(5)符合下列3个条件的F的同分异构体有________ 种:①与FeCl3溶液显色;②苯环上只有两个取代基;③1mol该物质最多消耗3mol NaOH;其中F有五种不同环境氢原子的结构简式为______________ 。
(6)参照上述合成路线,请设计由 (
( 与苯环性质相似)与
与苯环性质相似)与 合成
合成 的路线:
的路线:_______________________________________________________ 。
双安妥明可用于降低血液中的胆固醇,其结构简式为:

该物质合成线路如下图所示:

已知:I.

II.

II.已知:A的密度是同温同压下H2密度的28倍,且支链有一个甲基;G能发生银镜反应,且1molG能与2mol H2发生加成反应;I的结构具有对称性。试回答下列问题:
(1)双安妥明的分子式为
(2)A的结构简式为
(3)反应B→C的反应条件是
(4)反应“F+I→双安妥明”的化学方程式为
(5)符合下列3个条件的F的同分异构体有
(6)参照上述合成路线,请设计由
 (
( 与苯环性质相似)与
与苯环性质相似)与 合成
合成 的路线:
的路线:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙、丙、丁四种有机化合物,它们的组成中均含碳40%,含氢6.67%,含氧53.33%。甲、乙、丙都能发生银镜反应,乙、丙是丁的同分异构体。已知甲在常温下为气体,它有如下反应:甲+C6H5OH →X(高分子化合物)。丁在16.6℃以下凝结为冰状晶体,丁有以下反应:丁+碳酸钠→ 二氧化碳+Y+水,丙不能发生水解反应,但可发生酯化反应。
(1)甲的结构式为 ;乙的名称为 ;丁的结构简式为 。
(2)丙发生银镜反应的方程式为 。
(1)甲的结构式为 ;乙的名称为 ;丁的结构简式为 。
(2)丙发生银镜反应的方程式为 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】近期研究证实,中药甘草中的异甘草素在药理实验中显示明显的促进癌细胞凋亡和抑制肿瘤细胞增殖的活性,且对正常细胞的毒性低于癌细胞。异甘草素可以由有机物A和有机物B合成(A、B均为芳香族含氧衍生物),且由A和B合成异甘草素要用到以下反应:

请回答下列问题:
(1)有机物B分子式为C7H6O2,A和B均能与浓溴水反应生成沉淀。A和B具有一种相同的含氧官能团,其名称为__________ ;B的核磁共振氢谱有四个峰,峰面积之比是2:2:1:1。以下说法正确的是_______ (填序号)。
①有机物B能发生很多类型的反应,例如:中和、取代、氧化、还原、加成反应;
②与B互为同分异构体的芳香族含氧衍生物共有两种(不含B);
③B能与碳酸氢钠溶液反应放出二氧化碳气体。
(2)质谱表明有机物A相对分子质量为152,其碳、氢、氧元素的质量分数比为12:1:6。有机物A的分子式为___________ ;已知A分子中的官能团均处于间位,写出A、B合成异甘草素的化学方程式__________ 。
(3)初步合成的异甘草素需要经过以下处理工艺;
I加入一定量的水,再加入一定量的乙醚提取2次
II用无水MgSO4干燥、过滤减压蒸出。
III洗涤、浓缩得黄色粉末,再用含水乙醇处理得黄色针状晶体。
步骤II蒸出的物质可能是____ 。以上处理工艺中涉及的分离提纯操作依次有__ 。
(4)有机物D符合下列条件,写出D的结构简式_________ 。
①与A互为同分异构体,且能发生水解反应
②1molD能与3moNaOH反应
③苯环上的氢被氯取代的一氯代物有两种
(5)有机物B还可以发生以下变化:
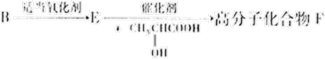
已知:F的单体是由E和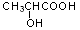 按1:1生成,请写出E→高分子化合物F的化学方程式
按1:1生成,请写出E→高分子化合物F的化学方程式_________ 。

请回答下列问题:
(1)有机物B分子式为C7H6O2,A和B均能与浓溴水反应生成沉淀。A和B具有一种相同的含氧官能团,其名称为
①有机物B能发生很多类型的反应,例如:中和、取代、氧化、还原、加成反应;
②与B互为同分异构体的芳香族含氧衍生物共有两种(不含B);
③B能与碳酸氢钠溶液反应放出二氧化碳气体。
(2)质谱表明有机物A相对分子质量为152,其碳、氢、氧元素的质量分数比为12:1:6。有机物A的分子式为
(3)初步合成的异甘草素需要经过以下处理工艺;
I加入一定量的水,再加入一定量的乙醚提取2次
II用无水MgSO4干燥、过滤减压蒸出。
III洗涤、浓缩得黄色粉末,再用含水乙醇处理得黄色针状晶体。
步骤II蒸出的物质可能是
(4)有机物D符合下列条件,写出D的结构简式
①与A互为同分异构体,且能发生水解反应
②1molD能与3moNaOH反应
③苯环上的氢被氯取代的一氯代物有两种
(5)有机物B还可以发生以下变化:
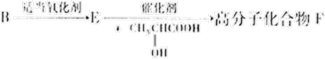
已知:F的单体是由E和
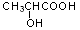 按1:1生成,请写出E→高分子化合物F的化学方程式
按1:1生成,请写出E→高分子化合物F的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】常用于制备食品香料的有机化合物A,其相对分子质量为120,A燃烧只生成二氧化碳和水。A既可以与乙醇发生酯化反应,又可以与乙酸发生酯化反应,且测得A与乙醇完全酯化所得有机产物B的相对分子质量为176。请回答下列问题:
(1)A的分子式为______________ 。
(2)B的结构简式__________________________________________ 。
(3)A与乙酸发生酯化反应的化学方程式____________________________________ 。
(4)由丙烯经过六个步骤可以合成有机化合物A,流程如下:
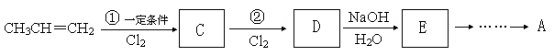
若C的分子式为C3H5Cl,D的分子式为C3H5Cl3,则①的反应类型为_____________ 。
D→E反应的化学方程式为__________________________________________________ 。
请补充完成E→A的反应流程________________________________________________ 。
(1)A的分子式为
(2)B的结构简式
(3)A与乙酸发生酯化反应的化学方程式
(4)由丙烯经过六个步骤可以合成有机化合物A,流程如下:

若C的分子式为C3H5Cl,D的分子式为C3H5Cl3,则①的反应类型为
D→E反应的化学方程式为
请补充完成E→A的反应流程
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请回答以下问题:
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.

Ⅱ.
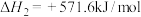
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式__________ 。
(2)在 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(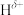 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(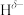 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是__________ 。
(3)100mLpH=10.00的 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为__________ mol。
(4)已知:25℃时碳酸的 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式__________ 。
(5)据文献报道, 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是__________ 。
(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是__________ 。
(7)乙醇的挥发性比水的强,原因是__________ 。
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.


Ⅱ.

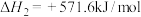
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式
(2)在
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(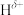 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(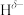 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是(3)100mLpH=10.00的
 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为(4)已知:25℃时碳酸的
 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式(5)据文献报道,
 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是
(7)乙醇的挥发性比水的强,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)解释硝酸铵固体溶于水吸热的原因_______ 。
(2)请把 、
、 、
、 三种物质熔点由高到低排序,并说明原因
三种物质熔点由高到低排序,并说明原因_______ 。
(1)解释硝酸铵固体溶于水吸热的原因
(2)请把
 、
、 、
、 三种物质熔点由高到低排序,并说明原因
三种物质熔点由高到低排序,并说明原因
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】根据要求,回答下列问题:
Ⅰ.已知HClO是比 还弱的酸,氯水中存在下列平衡:
还弱的酸,氯水中存在下列平衡: 、
、 。
。
(1)要使氯水中的HClO浓度增大,可加入___________(填标号)。
(2)由此说明在实验室里可用排饱和食盐水法收集 的理由是
的理由是___________ 。
Ⅱ.如表所示是几种弱酸常温下的电离平衡常数:
(3)常温下,浓度相同的四种酸溶液① 、②
、② 、③
、③ 、④
、④ ,pH值由大到小的顺序是
,pH值由大到小的顺序是___________ (用序号表示)。
(4)常温下,已知某浓度的 溶液pH=9,该溶液中由水电离出的
溶液pH=9,该溶液中由水电离出的
___________ 。
(5)浓度相同的六种溶液① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其碱性由强到弱的顺序是
,其碱性由强到弱的顺序是___________ (用序号表示);其中 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是___________ 。
(6)浓度均为 的三种溶液①
的三种溶液① 、②
、② 、③
、③ ,这三种溶液中
,这三种溶液中 从大到小的顺序为
从大到小的顺序为___________ (用序号表示)。
Ⅰ.已知HClO是比
 还弱的酸,氯水中存在下列平衡:
还弱的酸,氯水中存在下列平衡: 、
、 。
。(1)要使氯水中的HClO浓度增大,可加入___________(填标号)。
A. | B. | C.HCl | D.NaOH |
 的理由是
的理由是Ⅱ.如表所示是几种弱酸常温下的电离平衡常数:
 |  |  |  |
 | 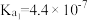 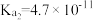 | 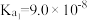 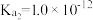 | 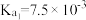 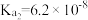 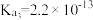 |
 、②
、② 、③
、③ 、④
、④ ,pH值由大到小的顺序是
,pH值由大到小的顺序是(4)常温下,已知某浓度的
 溶液pH=9,该溶液中由水电离出的
溶液pH=9,该溶液中由水电离出的
(5)浓度相同的六种溶液①
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其碱性由强到弱的顺序是
,其碱性由强到弱的顺序是 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(6)浓度均为
 的三种溶液①
的三种溶液① 、②
、② 、③
、③ ,这三种溶液中
,这三种溶液中 从大到小的顺序为
从大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】计算以下数值(以下均为25℃时)。
(1)某浓度的NH3·H2O溶液中,由水电离的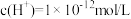 ,该溶液的pH=
,该溶液的pH=______ 。
(2)将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为______ 。
(3)CH3COOH与CH3COONa的混合溶液,若测得pH =6,则溶液中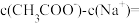
______  (填精确值)。
(填精确值)。
(4)将pH=a的NaOH溶液与pH=b的醋酸溶液等体积混合后,两者恰好完全反应,则该温度下醋酸的电离平衡常数约为______ (用含代数a、b等表示)。
(5)pH=5的H2SO4溶液加水稀释至原溶液体积的1000倍,求稀释后溶液中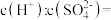
______ 。
(6)盐碱地因含较多的Na2CO3,使得土壤呈碱性,不利于作物生长,通过施加适量石膏粉末(主要含有CaSO4,微溶于水)来降低土壤的碱性。写出该过程中发生反应的化学方程式______ 。
(1)某浓度的NH3·H2O溶液中,由水电离的
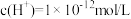 ,该溶液的pH=
,该溶液的pH=(2)将pH=3的H2SO4溶液和pH=12的NaOH溶液混合,混合后所得溶液的pH=10,则H2SO4溶液与NaOH溶液的体积比为
(3)CH3COOH与CH3COONa的混合溶液,若测得pH =6,则溶液中
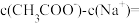
 (填精确值)。
(填精确值)。(4)将pH=a的NaOH溶液与pH=b的醋酸溶液等体积混合后,两者恰好完全反应,则该温度下醋酸的电离平衡常数约为
(5)pH=5的H2SO4溶液加水稀释至原溶液体积的1000倍,求稀释后溶液中
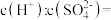
(6)盐碱地因含较多的Na2CO3,使得土壤呈碱性,不利于作物生长,通过施加适量石膏粉末(主要含有CaSO4,微溶于水)来降低土壤的碱性。写出该过程中发生反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】弱电解质的研究是重要课题。
(1)①已知不同pH条件下,水溶液中碳元素的存在形态如图所示。下列说法不 正确的是___________

a.pH=8时,溶液中含碳元素的微粒主要是
b.A点,溶液中 和
和 浓度相同
浓度相同
c.当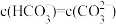 时,
时,
②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是___________ 。
(2)H2CO3以及其它部分弱酸的电离平衡常数如表:
按要求回答下列问题:
①H2S、H2CO3 、 HClO的酸性由强到弱的顺序为___________ 。
②将少量CO2气体通入NaClO溶液中,写出该反应的离子方程式:___________ 。
③测得0.1 mol·L−1 BaS溶液pH≈13,溶液中OH-、S2−、HS-三种离子浓度由大到小的顺序依次是___________ 。
(3)常温下,已知0.1mol/L一元酸HCOOH(甲酸)溶液中
①0.1mol/L HCOOH的 pH=___________ 。
②取10mL0.1mol/L的 HCOOH溶液稀释100倍,有关说法正确的是___________ (填写序号)
A.所有离子的浓度在稀释过程中都会减少
B.稀释后溶液的pH=5
C.稀释后甲酸的电离度会增大
D.与稀释前比较,稀释后水的电离程度增大
(1)①已知不同pH条件下,水溶液中碳元素的存在形态如图所示。下列说法

a.pH=8时,溶液中含碳元素的微粒主要是

b.A点,溶液中
 和
和 浓度相同
浓度相同c.当
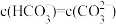 时,
时,
②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是
(2)H2CO3以及其它部分弱酸的电离平衡常数如表:
| 弱酸 | H2S | H2CO3 | HClO |
| 电离平衡常数(25℃) | 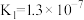 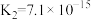 |  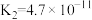 |  |
①H2S、H2CO3 、 HClO的酸性由强到弱的顺序为
②将少量CO2气体通入NaClO溶液中,写出该反应的离子方程式:
③测得0.1 mol·L−1 BaS溶液pH≈13,溶液中OH-、S2−、HS-三种离子浓度由大到小的顺序依次是
(3)常温下,已知0.1mol/L一元酸HCOOH(甲酸)溶液中

①0.1mol/L HCOOH的 pH=
②取10mL0.1mol/L的 HCOOH溶液稀释100倍,有关说法正确的是
A.所有离子的浓度在稀释过程中都会减少
B.稀释后溶液的pH=5
C.稀释后甲酸的电离度会增大
D.与稀释前比较,稀释后水的电离程度增大
您最近一年使用:0次








