根据要求,回答下列问题:
Ⅰ.已知HClO是比 还弱的酸,氯水中存在下列平衡:
还弱的酸,氯水中存在下列平衡: 、
、 。
。
(1)要使氯水中的HClO浓度增大,可加入___________(填标号)。
(2)由此说明在实验室里可用排饱和食盐水法收集 的理由是
的理由是___________ 。
Ⅱ.如表所示是几种弱酸常温下的电离平衡常数:
(3)常温下,浓度相同的四种酸溶液① 、②
、② 、③
、③ 、④
、④ ,pH值由大到小的顺序是
,pH值由大到小的顺序是___________ (用序号表示)。
(4)常温下,已知某浓度的 溶液pH=9,该溶液中由水电离出的
溶液pH=9,该溶液中由水电离出的
___________ 。
(5)浓度相同的六种溶液① 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其碱性由强到弱的顺序是
,其碱性由强到弱的顺序是___________ (用序号表示);其中 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是___________ 。
(6)浓度均为 的三种溶液①
的三种溶液① 、②
、② 、③
、③ ,这三种溶液中
,这三种溶液中 从大到小的顺序为
从大到小的顺序为___________ (用序号表示)。
Ⅰ.已知HClO是比
 还弱的酸,氯水中存在下列平衡:
还弱的酸,氯水中存在下列平衡: 、
、 。
。(1)要使氯水中的HClO浓度增大,可加入___________(填标号)。
A. | B. | C.HCl | D.NaOH |
 的理由是
的理由是Ⅱ.如表所示是几种弱酸常温下的电离平衡常数:
 |  |  |  |
 | 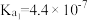 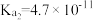 | 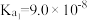 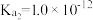 | 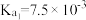 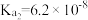 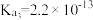 |
 、②
、② 、③
、③ 、④
、④ ,pH值由大到小的顺序是
,pH值由大到小的顺序是(4)常温下,已知某浓度的
 溶液pH=9,该溶液中由水电离出的
溶液pH=9,该溶液中由水电离出的
(5)浓度相同的六种溶液①
 、②
、② 、③
、③ 、④
、④ 、⑤
、⑤ 、⑥
、⑥ ,其碱性由强到弱的顺序是
,其碱性由强到弱的顺序是 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(6)浓度均为
 的三种溶液①
的三种溶液① 、②
、② 、③
、③ ,这三种溶液中
,这三种溶液中 从大到小的顺序为
从大到小的顺序为
更新时间:2023-10-31 08:36:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氨气是重要的化工原料,氨水、硝酸盐、铵盐等均可作化肥产品。
(1)在VL浓度为 的氨水中滴加等体积
的氨水中滴加等体积 的盐酸,使pH=7,则产物中一水合氨浓度为
的盐酸,使pH=7,则产物中一水合氨浓度为___________  。
。
(2)在自然界的氮循环过程中,硝化细菌将土壤中的 转化为
转化为 后,土壤中的O2进一步将
后,土壤中的O2进一步将 氧化为
氧化为 ,在氧气较少的环境下,
,在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以N2形式放出。氧气与
反应,使氮以N2形式放出。氧气与 反应时,反应物
反应时,反应物 与O2的物质的量之比为
与O2的物质的量之比为___________ ,写出 与
与 作用生成N2的离子方程式
作用生成N2的离子方程式___________ 。
(1)在VL浓度为
 的氨水中滴加等体积
的氨水中滴加等体积 的盐酸,使pH=7,则产物中一水合氨浓度为
的盐酸,使pH=7,则产物中一水合氨浓度为 。
。(2)在自然界的氮循环过程中,硝化细菌将土壤中的
 转化为
转化为 后,土壤中的O2进一步将
后,土壤中的O2进一步将 氧化为
氧化为 ,在氧气较少的环境下,
,在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以N2形式放出。氧气与
反应,使氮以N2形式放出。氧气与 反应时,反应物
反应时,反应物 与O2的物质的量之比为
与O2的物质的量之比为 与
与 作用生成N2的离子方程式
作用生成N2的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知常温下部分弱电解质的电离平衡常数如下表:
(1)常温下, 相同的三种溶液a.
相同的三种溶液a. 溶液;b.
溶液;b. 溶液;c.
溶液;c. 溶液,其物质的量浓度由大到小的顺序是
溶液,其物质的量浓度由大到小的顺序是______ 。(填序号)。
(2)已知在常温时,将浓度相等的 与
与 溶液等体积混合,溶液呈酸性。用平衡常数解释溶液呈酸性的原因
溶液等体积混合,溶液呈酸性。用平衡常数解释溶液呈酸性的原因______ 。
(3)同浓度的 溶液和
溶液和 溶液相比:后者溶液中
溶液相比:后者溶液中
______ 前者溶液中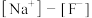 (填字母)。
(填字母)。
A.大于 B.小于
化学式 |
|
|
|
|
电离常数 |
|
|
|
|
 相同的三种溶液a.
相同的三种溶液a. 溶液;b.
溶液;b. 溶液;c.
溶液;c. 溶液,其物质的量浓度由大到小的顺序是
溶液,其物质的量浓度由大到小的顺序是(2)已知在常温时,将浓度相等的
 与
与 溶液等体积混合,溶液呈酸性。用平衡常数解释溶液呈酸性的原因
溶液等体积混合,溶液呈酸性。用平衡常数解释溶液呈酸性的原因(3)同浓度的
 溶液和
溶液和 溶液相比:后者溶液中
溶液相比:后者溶液中
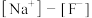 (填字母)。
(填字母)。A.大于 B.小于
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在室温下,下列六种溶液:
①0.1 mol/L NH4Cl;②0.1 mol/L CH3COONH4;⑧0.1 mol/L NH4HSO4;④pH = 12的NH3·H2O和pH = 2 HCl等体积混合液:⑤0.1 mol/L NH3·H2O;⑥0.1 mol/L (NH4)2CO3
请根据要求填写下列空白:
(1)溶液①、③呈酸性的原因不同,分别用方程式解释__________ ;___________ 。
(2)室温下,测得溶液②的pH=7 ,则 CH3COO-与 NH4+浓度的大小关系是:c(CH3COO-)________ c( )(填“>”,“<”或“=”)。
)(填“>”,“<”或“=”)。
(3)比较溶液①、②、③、⑤中c( )的大小关系
)的大小关系_________ 。
(4)写出溶液④中离子浓度的大小关系_______ 。
(5)写出溶液⑥的电荷守恒_________________ 。
①0.1 mol/L NH4Cl;②0.1 mol/L CH3COONH4;⑧0.1 mol/L NH4HSO4;④pH = 12的NH3·H2O和pH = 2 HCl等体积混合液:⑤0.1 mol/L NH3·H2O;⑥0.1 mol/L (NH4)2CO3
请根据要求填写下列空白:
(1)溶液①、③呈酸性的原因不同,分别用方程式解释
(2)室温下,测得溶液②的pH=7 ,则 CH3COO-与 NH4+浓度的大小关系是:c(CH3COO-)
 )(填“>”,“<”或“=”)。
)(填“>”,“<”或“=”)。(3)比较溶液①、②、③、⑤中c(
 )的大小关系
)的大小关系(4)写出溶液④中离子浓度的大小关系
(5)写出溶液⑥的电荷守恒
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】醋酸(CH3COOH)是一种常见的弱酸。
(1)为用实验证明醋酸是弱电解质,实验小组同学设计如下几种方案:
①用pH试纸测出0.1mol/L的醋酸溶液pH:若pH___ 1(填“>”、“<”或“=”),则证明醋酸是弱酸;
②先测0.1mol/L醋酸的pH ;量取该溶液5mL用蒸馏水稀释至500mL,再测其pH,若________________ ,则证明醋酸是弱电解质;
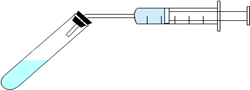
③分别配制pH相同的醋酸和盐酸,各取10mL与足量的锌粒反应(装置如图),测试在不同时间间隔中得到H2的量,即可证明醋酸是弱电解质。下列示意图(X为醋酸,Y为盐酸)中,符合该实验结果的是__________ (选填字母);
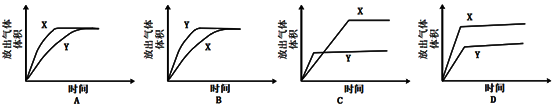
但在该实验中难以实现之处为__________________________________ 。(举例)
(2)醋酸和氢氧化钠反应生成醋酸钠(CH3COONa)。
①将CH3COONa固体溶于蒸馏水后其溶液显碱性,其原因是(用离子方程式表示)______________________________ ;在该溶液中,下列关系式中正确的是________ ;(选填字母)
A.c(Na+)=c(CH3COO-)+c(CH3COOH)
B.c(OH-)=c(H+)+c(CH3COOH)
C.c(CH3COO-)+c(OH-)=c(H+)+c(Na+)
D.c(CH3COO-)>c(OH-)>c(Na+)>c(H+)
②醋酸和氢氧化钠反应后得到溶液中溶质的组成有多种可能:
若得到的溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+),试推断该溶液中的溶质为_____ ;
若得到的溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则可以推断该溶液中的溶质可能为____ ;
③将amol/LCH3COOH稀溶液和bmol/LNaOH稀溶液等体积混合:
若测得溶液中c(OH-)=c(H+),则a___ b;(选填“>”、“<”、“=”、“≤”或“≥”)
若测得溶液中c(OH-)>c(H+),则a___ b;(选填“>”、“<”、“=”、“≤”或“≥”)
(1)为用实验证明醋酸是弱电解质,实验小组同学设计如下几种方案:
①用pH试纸测出0.1mol/L的醋酸溶液pH:若pH
②先测0.1mol/L醋酸的pH ;量取该溶液5mL用蒸馏水稀释至500mL,再测其pH,若

③分别配制pH相同的醋酸和盐酸,各取10mL与足量的锌粒反应(装置如图),测试在不同时间间隔中得到H2的量,即可证明醋酸是弱电解质。下列示意图(X为醋酸,Y为盐酸)中,符合该实验结果的是

但在该实验中难以实现之处为
(2)醋酸和氢氧化钠反应生成醋酸钠(CH3COONa)。
①将CH3COONa固体溶于蒸馏水后其溶液显碱性,其原因是(用离子方程式表示)
A.c(Na+)=c(CH3COO-)+c(CH3COOH)
B.c(OH-)=c(H+)+c(CH3COOH)
C.c(CH3COO-)+c(OH-)=c(H+)+c(Na+)
D.c(CH3COO-)>c(OH-)>c(Na+)>c(H+)
②醋酸和氢氧化钠反应后得到溶液中溶质的组成有多种可能:
若得到的溶液中c(Na+)>c(OH-)>c(CH3COO-)>c(H+),试推断该溶液中的溶质为
若得到的溶液中c(CH3COO-)>c(Na+)>c(H+)>c(OH-),则可以推断该溶液中的溶质可能为
③将amol/LCH3COOH稀溶液和bmol/LNaOH稀溶液等体积混合:
若测得溶液中c(OH-)=c(H+),则a
若测得溶液中c(OH-)>c(H+),则a
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】利用所学化学反应原理,解决以下问题:
(1)KAl(SO4)2·12H2O可做净水剂,其原理是__________ (用离子方程式表示)
(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是__________ (填化学式)。
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式__________ 。
(4)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合:若c(K+)<c (CH3COO−),则a________ b(填>、<、=)。
(5)室温下,1 mol/L相同体积的下列四种溶液:①KCl②FeCl3③HF④Na2CO3中,所含阳离子数由少到多的顺序是________ (用序号填空)。
(1)KAl(SO4)2·12H2O可做净水剂,其原理是
(2)碳酸氢钠溶液蒸干并灼烧得到的固体物质是
(3)向FeCl3溶液中滴加NaHCO3溶液,有沉淀和气体生成的离子方程式
(4)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合:若c(K+)<c (CH3COO−),则a
(5)室温下,1 mol/L相同体积的下列四种溶液:①KCl②FeCl3③HF④Na2CO3中,所含阳离子数由少到多的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】科学研究中观察到的宏观现象能反映微观本质。回答下列问题:
(1)次磷酸分子式为H3PO2,与足量NaOH溶液反应生成NaH2PO2,次磷酸为___________ 元弱酸,次磷酸溶液中微粒有___________ ,次磷酸的电离方程式为___________ 。
(2)根据表中数据(常温下),完成下列填空。
①常温下,NaCN溶液呈___________ (填“酸”、“碱”或“中”)性,其原因是___________ (用离子方程式表示)。
②向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式为___________ ,结合所给数据说明生成该产物的理由:___________ 。
(3)①试计算Na2CO3溶液中CO 的水解常数Kh为
的水解常数Kh为___________ ;
②若加水稀释NaHCO3溶液时,其水解程度___________ ,溶液的pH___________ (填“增大”或“减小”)。
(1)次磷酸分子式为H3PO2,与足量NaOH溶液反应生成NaH2PO2,次磷酸为
(2)根据表中数据(常温下),完成下列填空。
| 物质 | CH3COOH | NH3•H2O | HCN | HClO | H2CO3 | H2SO3 |
| 电离常数(Ka) | 1.7×10﹣5 | 1.7×10﹣5 | 4.9×10﹣10 | 3×10﹣8 | Ka1=4.3×10﹣7 Ka2=4.7×10﹣11 | Ka1=1.5×10﹣2 Ka2=1.0×10﹣7 |
②向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式为
(3)①试计算Na2CO3溶液中CO
 的水解常数Kh为
的水解常数Kh为②若加水稀释NaHCO3溶液时,其水解程度
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】弱酸HA的电离常数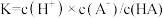 。25℃时,有关弱酸的电离常数如下:
。25℃时,有关弱酸的电离常数如下:
弱酸化学式 | HCOOH | ②CH3COOH | C6H5OH | ④H2A |
电离常数 | 1.810-4 | 1.810-5 | 1.310-10 | K1=4.310-7,K2=5.610-11 |
⑴四种酸的酸性由强到弱的顺序是
⑵向0.1 mol/L CH3COOH溶液中滴加NaOH至溶液中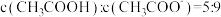 时,此时溶液的pH=
时,此时溶液的pH=
⑶当H2A与NaOH溶液1:1混合溶液显
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】平衡思想是化学研究的一个重要观念,在水溶液中存在多种平衡体系。
(1)①室温下,0.1 mol/L的醋酸在水中有1%发生电离,则该温度下CH3COOH的电离平衡常数Ka ≈___________ 。
②在25℃时,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合(忽略混合时的溶液体积变化),反应平衡时溶液中c(NH )=c(Cl-),则溶液显
)=c(Cl-),则溶液显___________ (填“酸“碱”或“中”)性。
(2)已知,常温下几种物质的电离常数如下:
①三种相同物质的量浓度的Na2CO3、NaClO、NaHSO3的pH从小到大的排序是___________ 。
②下列说法正确的是___________ 。
A.Ca(ClO)2溶液中通入少量SO2:SO2 + H2O+Ca2++2ClO- = CaSO3↓+2HClO
B.常温下,将SO2通入氨水中,当c(OH−)降至1.0×10-7mol/L时,溶液中的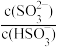 =0.6
=0.6
C.等物质的量浓度的NaHSO3与Na2SO3混合液中,3c(Na+)=2c( )+2c(
)+2c(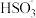 )+2c(H2SO3)
)+2c(H2SO3)
D.Na2CO3溶液中加入少量水,则溶液中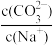 将减小
将减小
③根据表中数据,计算0.03 mol/L NaClO溶液的pH≈___________ 。
(1)①室温下,0.1 mol/L的醋酸在水中有1%发生电离,则该温度下CH3COOH的电离平衡常数Ka ≈
②在25℃时,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合(忽略混合时的溶液体积变化),反应平衡时溶液中c(NH
 )=c(Cl-),则溶液显
)=c(Cl-),则溶液显(2)已知,常温下几种物质的电离常数如下:
| 化学式 | H2CO3 | HClO | H2SO3 |
| 电离平衡常数 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 | Ka1=1.4×10-2 Ka2=6.0×10-8 |
①三种相同物质的量浓度的Na2CO3、NaClO、NaHSO3的pH从小到大的排序是
②下列说法正确的是
A.Ca(ClO)2溶液中通入少量SO2:SO2 + H2O+Ca2++2ClO- = CaSO3↓+2HClO
B.常温下,将SO2通入氨水中,当c(OH−)降至1.0×10-7mol/L时,溶液中的
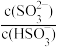 =0.6
=0.6C.等物质的量浓度的NaHSO3与Na2SO3混合液中,3c(Na+)=2c(
 )+2c(
)+2c(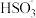 )+2c(H2SO3)
)+2c(H2SO3)D.Na2CO3溶液中加入少量水,则溶液中
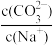 将减小
将减小③根据表中数据,计算0.03 mol/L NaClO溶液的pH≈
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液中c(H+)=2.5 10-6mol/L,c(H2CO3)=1.25
10-6mol/L,c(H2CO3)=1.25 10-5mol/L。则H2CO3⇌HCO
10-5mol/L。则H2CO3⇌HCO +H+的电离平衡常数Ka1=
+H+的电离平衡常数Ka1=_______ 。
(2)现有下列物质:①50 ②25
②25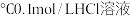 ,③25
,③25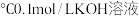 ④25
④25 0.1mol/LBa(OH)2溶液。
0.1mol/LBa(OH)2溶液。
i:这些物质与25 纯水相比,其中水的电离得到促进的是
纯水相比,其中水的电离得到促进的是_______ (填序号,下同),其中水的电离被抑制的是_______ ,水电离的c(OH-)等于溶液中c(OH-)的是_______ ,水电离的c(H+)等于溶液中c(H+)的是_______ 。
ii:从②和③溶液中水的电离程度相等,进而可推出的结论是:同一温度下,当_______ 时,水的电离程度相等。
(1)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液中c(H+)=2.5
 10-6mol/L,c(H2CO3)=1.25
10-6mol/L,c(H2CO3)=1.25 10-5mol/L。则H2CO3⇌HCO
10-5mol/L。则H2CO3⇌HCO +H+的电离平衡常数Ka1=
+H+的电离平衡常数Ka1=(2)现有下列物质:①50
 ②25
②25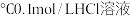 ,③25
,③25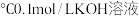 ④25
④25 0.1mol/LBa(OH)2溶液。
0.1mol/LBa(OH)2溶液。i:这些物质与25
 纯水相比,其中水的电离得到促进的是
纯水相比,其中水的电离得到促进的是ii:从②和③溶液中水的电离程度相等,进而可推出的结论是:同一温度下,当
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫及其化合物在生产生活中有广泛的应用。请回答:
(1)室温下, 溶液呈碱性的原因是
溶液呈碱性的原因是___________ (用离子方程式表示)。
(2)下列关于硫及其化合物的说法,正确的是___________(填标号)。
(3)光谱研究表明, 的水溶液中存在下列平衡:
的水溶液中存在下列平衡:
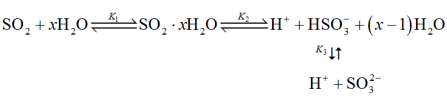
其中K1、K2、K3为各步的平衡常数,且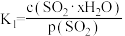 [
[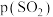 表示
表示 的平衡压强]。
的平衡压强]。
①当 的平衡压强为p时,测得
的平衡压强为p时,测得 ,则溶液
,则溶液
___________  (用含
(用含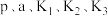 的式子表示)。
的式子表示)。
②滴加 溶液至
溶液至 时,溶液中
时,溶液中 。如果溶液中
。如果溶液中 ,需加
,需加 溶液将
溶液将 调整为约等于
调整为约等于___________ 。
(4)氨水也可吸收 :
: ,
,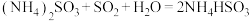 。能提高
。能提高 去除率的措施有___________(填标号)。
去除率的措施有___________(填标号)。
(1)室温下,
 溶液呈碱性的原因是
溶液呈碱性的原因是(2)下列关于硫及其化合物的说法,正确的是___________(填标号)。
| A.硫元素在自然界中只能以化合态形式存在 |
B. 通入紫色石蕊试液,先变红后褪色 通入紫色石蕊试液,先变红后褪色 |
C.酸雨是 的降水,主要是由污染物 的降水,主要是由污染物 造成 造成 |
| D.浓硫酸中加入少量胆矾晶体,搅拌,固体逐渐变成白色 |
 的水溶液中存在下列平衡:
的水溶液中存在下列平衡: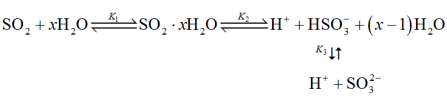
其中K1、K2、K3为各步的平衡常数,且
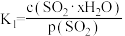 [
[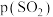 表示
表示 的平衡压强]。
的平衡压强]。①当
 的平衡压强为p时,测得
的平衡压强为p时,测得 ,则溶液
,则溶液
 (用含
(用含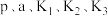 的式子表示)。
的式子表示)。②滴加
 溶液至
溶液至 时,溶液中
时,溶液中 。如果溶液中
。如果溶液中 ,需加
,需加 溶液将
溶液将 调整为约等于
调整为约等于(4)氨水也可吸收
 :
: ,
,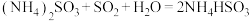 。能提高
。能提高 去除率的措施有___________(填标号)。
去除率的措施有___________(填标号)。| A.增大氨水浓度 | B.加热煮沸 |
| C.降低烟气的流速 | D.补充 ,将 ,将 氧化为 氧化为 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】电离平衡常数是衡量弱电解质电离程度的量。已知如表数据(25℃):
(1)25℃时,等浓度的三种溶液( 溶液、
溶液、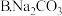 溶液、
溶液、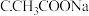 溶液)的
溶液)的 由大到小的顺序为
由大到小的顺序为 _______ 。(填写序号)
(2)25℃时,向 溶液中通入少量
溶液中通入少量 ,所发生反应的化学方程式为
,所发生反应的化学方程式为_______
(3)现有浓度为 的
的 与
与
 等体积混合后,测得
等体积混合后,测得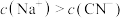 ,下列关系正确的是 _______
,下列关系正确的是 _______
(4)已知 水溶液显酸性,请写出该溶液中各离子浓度的大小
水溶液显酸性,请写出该溶液中各离子浓度的大小 _______ ;
(5)H2C2O4溶液和 酸性溶液可发生反应:
酸性溶液可发生反应: ,反应中每生成标况下
,反应中每生成标况下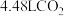 气体,转移的电子的物质的量为
气体,转移的电子的物质的量为 _______ 
| 化学式 | 电离平衡常数 |
 | 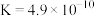 |
 |  |
 | 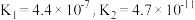 |
(1)25℃时,等浓度的三种溶液(
 溶液、
溶液、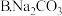 溶液、
溶液、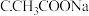 溶液)的
溶液)的 由大到小的顺序为
由大到小的顺序为 (2)25℃时,向
 溶液中通入少量
溶液中通入少量 ,所发生反应的化学方程式为
,所发生反应的化学方程式为(3)现有浓度为
 的
的 与
与
 等体积混合后,测得
等体积混合后,测得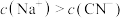 ,下列关系正确的是 _______
,下列关系正确的是 _______A.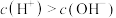 | B.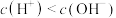 |
C. | D.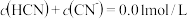 |
 水溶液显酸性,请写出该溶液中各离子浓度的大小
水溶液显酸性,请写出该溶液中各离子浓度的大小 (5)H2C2O4溶液和
 酸性溶液可发生反应:
酸性溶液可发生反应: ,反应中每生成标况下
,反应中每生成标况下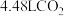 气体,转移的电子的物质的量为
气体,转移的电子的物质的量为 
您最近一年使用:0次



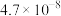
 ;
;

 将
将 )=
)=

