下列有关说法正确的是
| A.化学平衡发生移动,平衡常数必发生变化 |
| B.加入催化剂,单位体积内反应物分子中活化分子百分数不变 |
| C.合成氨时将氨液化分离,可提高原料的利用率,可以用勒夏特列原理解释 |
D.恒温恒容容器中,N2(g)+3H2(g) 2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大 2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大 |
更新时间:2022-02-20 09:59:55
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】2021年Benjamin List和Dave MacMillan因不对称有机催化获得诺贝尔化学奖,脯氨酸可以催化羟醛缩合反应,其反应历程简化如图所示,下列说法正确的是


| A.有机物①能够降低总反应的焓变 |
| B.有机物③和④互为同分异构体 |
| C.反应过程中存在极性键和非极性键的断裂和生成 |
D.如果用 代替 代替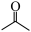 可生成 可生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】甲烷是结构最简单的碳氢化合物。广泛存在于天然气、沼气、煤矿坑井气之中,工业可利用捕捉二氧化碳与氢气制取。甲烷是优质气体燃料,也是制造合成气和许多化工产品的重要原料,还可以用于消除 。
。 加氢制
加氢制 的一种催化机理如图,下列说法正确的是
的一种催化机理如图,下列说法正确的是

 。
。 加氢制
加氢制 的一种催化机理如图,下列说法正确的是
的一种催化机理如图,下列说法正确的是
A.反应中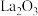 是中间产物 是中间产物 |
B.反应中 可以释放出带负电荷的 可以释放出带负电荷的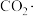 |
C. 经过Ni活性中心裂解产生活化态H·的过程中 经过Ni活性中心裂解产生活化态H·的过程中 |
D.使用 作催化剂可以降低反应的焓变,从而提高化学反应速率 作催化剂可以降低反应的焓变,从而提高化学反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在恒温密闭容器中,充入一定量N2和H2,发生反应N2(g)+3H2(g) 2NH3(g) △H<0,下列说法正确的是
2NH3(g) △H<0,下列说法正确的是
 2NH3(g) △H<0,下列说法正确的是
2NH3(g) △H<0,下列说法正确的是| A.反应过程中,3v消耗(H2)=2v消耗(NH3) |
| B.平衡后,压缩容器体积,平衡正向移动,正反应速率加快,逆反应速率减慢 |
| C.恒容条件下,再充入与原来同样多的N2和H2,体系内活化分子百分数不变,反应速率加快 |
| D.平衡后,仅升高温度,体系内活化分子数增多,反应速率加快,N2的平衡转化率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
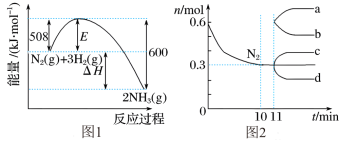
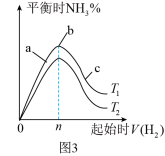
【推荐2】一定条件下,合成氨反应:N2+3H2 2NH3。图1 表示在该反应过程中的 能量的变化,图 2 表示在 2L的密闭容器中反应时 N2的物质的量随时间的变化曲线,图 3 表示在其他条件不变的情况下,改变起始物H2的物质的量对该反应平衡的影响。下列说法不正确的是
2NH3。图1 表示在该反应过程中的 能量的变化,图 2 表示在 2L的密闭容器中反应时 N2的物质的量随时间的变化曲线,图 3 表示在其他条件不变的情况下,改变起始物H2的物质的量对该反应平衡的影响。下列说法不正确的是
 2NH3。图1 表示在该反应过程中的 能量的变化,图 2 表示在 2L的密闭容器中反应时 N2的物质的量随时间的变化曲线,图 3 表示在其他条件不变的情况下,改变起始物H2的物质的量对该反应平衡的影响。下列说法不正确的是
2NH3。图1 表示在该反应过程中的 能量的变化,图 2 表示在 2L的密闭容器中反应时 N2的物质的量随时间的变化曲线,图 3 表示在其他条件不变的情况下,改变起始物H2的物质的量对该反应平衡的影响。下列说法不正确的是

| A.升高温度,正、逆反应速率均加快, N2的转化率减小 |
| B.由图 2 信息,10 min 内该反应速率为v(N2)=0.015mol·L−1·min −1 |
| C.由图 2 信息,从11min 起其他条件不变,增加 N2的量,则 n N 2 的变化曲线为 b |
| D.由图 1 信息,向容器中加入 1molN2和 3molH2,放出的热量为 92kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】氨气去除NO的反应原理为:4NH3(g)+6NO(g) 5N2(g)+6H2O(g) ΔH<0,反应速率与浓度之间存在如下关系:v正=k正·c4(NH3)·c6(NO),v逆=k逆·c5(N2)·c6(H2O),k正、k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9molNH3(g)和1.2molNO(g)发生反应,保持温度不变,5min后反应达平衡,NO的转化率为50%。下列说法正确的是
5N2(g)+6H2O(g) ΔH<0,反应速率与浓度之间存在如下关系:v正=k正·c4(NH3)·c6(NO),v逆=k逆·c5(N2)·c6(H2O),k正、k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9molNH3(g)和1.2molNO(g)发生反应,保持温度不变,5min后反应达平衡,NO的转化率为50%。下列说法正确的是
 5N2(g)+6H2O(g) ΔH<0,反应速率与浓度之间存在如下关系:v正=k正·c4(NH3)·c6(NO),v逆=k逆·c5(N2)·c6(H2O),k正、k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9molNH3(g)和1.2molNO(g)发生反应,保持温度不变,5min后反应达平衡,NO的转化率为50%。下列说法正确的是
5N2(g)+6H2O(g) ΔH<0,反应速率与浓度之间存在如下关系:v正=k正·c4(NH3)·c6(NO),v逆=k逆·c5(N2)·c6(H2O),k正、k逆为速率常数,只受温度影响。350℃时,在2L恒容密闭容器中,通入0.9molNH3(g)和1.2molNO(g)发生反应,保持温度不变,5min后反应达平衡,NO的转化率为50%。下列说法正确的是| A.用NH3表示的化学反应速率为0.06mol·L-1·min-1 |
| B.350℃时,该反应的平衡常数为0.5 |
| C.其他条件不变,往反应后的容器中再通入0.9molNH3(g)和1.2molNO(g),重新达平衡时NO的体积分数增大 |
| D.当温度改变为T°C时,若k正=k逆,则T>350 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:
CO(g)+H2O(g) CO2(g)+H2(g)
CO2(g)+H2(g)
反应过程中测定的部分数据见下表(表中t1>t2),则下列说法正确的是
CO(g)+H2O(g)
 CO2(g)+H2(g)
CO2(g)+H2(g)反应过程中测定的部分数据见下表(表中t1>t2),则下列说法正确的是
| 反应时间/min | n(CO)/mol | H2O/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
| A.反应在t1min内的平均速率为v(H2)=0.40/t1 mol·L-1·min-1 |
| B.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应 |
| C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率减小 |
| D.保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时,n(CO2)=0.40 mol |
您最近一年使用:0次

 加氢制
加氢制 。其反应历程如图所示(*表示吸附在催化剂表面)。
。其反应历程如图所示(*表示吸附在催化剂表面)。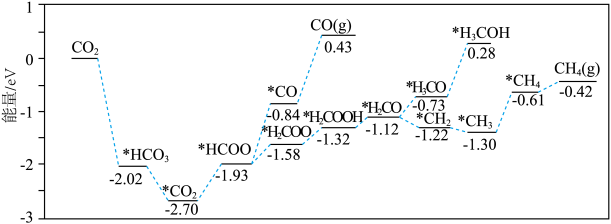
 历程中能垒最大为
历程中能垒最大为
 C(g),反应过程混合物中
C(g),反应过程混合物中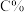 与温度关系如下图,下列说正确的是
与温度关系如下图,下列说正确的是
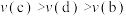
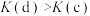
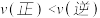

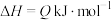 ,CO的平衡转化率与温度、投料比
,CO的平衡转化率与温度、投料比 [
[ ]的关系如下图所示。
]的关系如下图所示。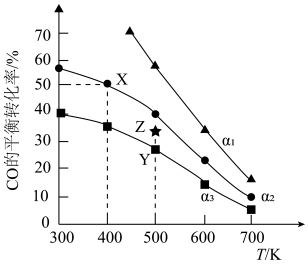
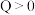

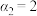 条件下,反应的平衡常数的值为0.25
条件下,反应的平衡常数的值为0.25 条件下,增大压强,CO的平衡转化率能从Y点到Z点
条件下,增大压强,CO的平衡转化率能从Y点到Z点

