石墨烯、高温氯化钠、砷化镉等超导材料应用广泛。回答下列问题:
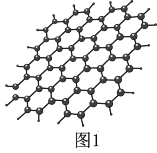
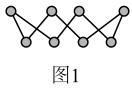
(1)石墨烯结构如图1所示,则碳原子的杂化方式为_______ ,12 g石墨烯中含有六元环个数与σ键个数之比为_______ 。
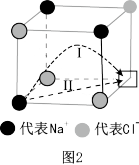
(2)温度升高时,NaCl晶体出现缺陷,如图2方格处填入Na+时,恰好构成氯化钠晶胞的 ,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径
,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径_______ (填图中序号)迁移到空位处。
(3)石墨烯限域单原子铁催化剂使CH4在室温条件下被H2O2直接氧化为HCHO、HCOOH,比较HCHO、HCOOH的沸点高低并说明理由_______ 。
(4)镉(Cd)与Zn同族且相邻,则基态Cd原子的价电子排布式为_______ ;与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3强于PH3,原因是_______ 。
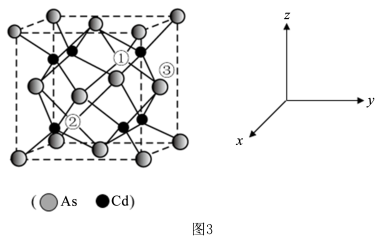
(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构为正方体如图3, 占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为(
占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为( ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为_______ 。晶胞的密度为 ,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为
,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为_______ pm(列计算式即可)。
(1)石墨烯结构如图1所示,则碳原子的杂化方式为

(2)温度升高时,NaCl晶体出现缺陷,如图2方格处填入Na+时,恰好构成氯化钠晶胞的
 ,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径
,此时晶体的导电性大大增强。已知氯化钠晶体中两个相邻Cl-之间的间隙小于Na+直径,则Na+最可能通过途径
(3)石墨烯限域单原子铁催化剂使CH4在室温条件下被H2O2直接氧化为HCHO、HCOOH,比较HCHO、HCOOH的沸点高低并说明理由
(4)镉(Cd)与Zn同族且相邻,则基态Cd原子的价电子排布式为
(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构为正方体如图3,
 占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为(
占据顶点和面心,Cd占据As围成的四面体空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,其中“①”和“②”位是“真空”。建立如图的原子坐标系,①号位的坐标为( ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为 ,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为
,阿伏加德罗常数的值为NA,则该晶胞中距离最远的两个Cd原子之间的距离为
2022·山东聊城·一模 查看更多[4]
山东省聊城市2021-2022学年下学期高三一模化学试题(已下线)必刷卷02-2022年高考化学考前信息必刷卷(山东专用)(已下线)必刷卷05-2022年高考化学考前信息必刷卷(河北专用)河北省石家庄市第二中学2022届高三2.5模化学试题
更新时间:2022-03-29 21:54:07
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】高温乃至室温超导一直是科学家不懈追求目标。科学家合成了一种高温超导材料,其晶胞结构如图所示(B和C原子均位于晶胞面上),该立方晶胞参数为apm。
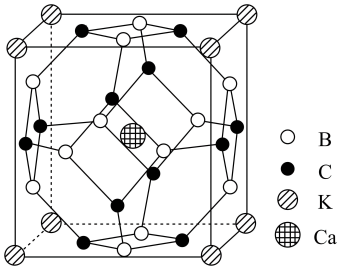
(1)该晶体的四种元素的电负性由大到小的顺序是___________ 。钙元素的焰色实验为砖红色,基于其原理可用于定性与定量分析,这种分析方法称为___________ 光谱。
(2)该晶体中,B原子的杂化轨道类型是_______ ,C原子的杂化轨道类型是________ 。
(3)该晶体中微粒间存在的化学键有_________ 、___________ 。
(4)该晶体的化学式为________ (化成最简整数比),密度为_________  (列出计算式,相对分子质量用M表示无需计算出数值)。
(列出计算式,相对分子质量用M表示无需计算出数值)。
(5)晶胞中B和C原子构成的多面体有_________ 个面
(6)比较 与
与 的沸点并解释原因
的沸点并解释原因_________ ;比较 与
与 的键角并解释原因
的键角并解释原因___________ 。

(1)该晶体的四种元素的电负性由大到小的顺序是
(2)该晶体中,B原子的杂化轨道类型是
(3)该晶体中微粒间存在的化学键有
(4)该晶体的化学式为
 (列出计算式,相对分子质量用M表示无需计算出数值)。
(列出计算式,相对分子质量用M表示无需计算出数值)。(5)晶胞中B和C原子构成的多面体有
(6)比较
 与
与 的沸点并解释原因
的沸点并解释原因 与
与 的键角并解释原因
的键角并解释原因
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】在A、B、C三种元素中,A元素原子的价电子排布为2s22p5,B元素K、L能层上的电子数与M、N层上的电子数相同。C元素的原子序数等于A、B两元素原子序数之和,C的单质在生产生活中具有许多用途,它可在硫酸铜溶液中用电解法进行精炼。请回答以下问题:
(1)已知C元素的电负性数值为1.9,则A、C两元素的原子之间应形成___ 键(填“共价”或“离子”);
(2)C元素的价电子排布式为__________ ;
(3)在A元素氢化物的水溶液中,存在有__________ 种不同类型的氢键;
(4)SO42—中S原子的杂化轨道类型是_________ ,SO42—的立体构型是_________ ;
(5)一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为____________ ;该晶体中,原子之间的作用力是_____________ ;
(6)在A、B两元素所形成晶体的晶胞中,位于六面体顶点和面心上的元素为________ (填具体的元素符号)。
(1)已知C元素的电负性数值为1.9,则A、C两元素的原子之间应形成
(2)C元素的价电子排布式为
(3)在A元素氢化物的水溶液中,存在有
(4)SO42—中S原子的杂化轨道类型是
(5)一种铜金合金晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为
(6)在A、B两元素所形成晶体的晶胞中,位于六面体顶点和面心上的元素为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】[化学——选修 3:物质结构与性质]
(1) 过渡金属元素铁能形成多种配合物,如:[Fe (CN) 6] 4-、[Fe(SCN)6]3-等。
Fe3+的核外电子排布式为______________ ,从原子结构的角度解释Fe3+比Fe2+稳定的理由是_______________ 。
(2) N的基态原子中能量最高的电子,其电子云在空间有________ 个方向,原子轨道呈________ 形。
(3) (NH4)2SO4阴离子的立体构型是________ ,NH4+中心原子的杂化类型是________ 。
(4) Fe 有δ、γ、α三种同素异形体,其晶胞结构如下图所示:
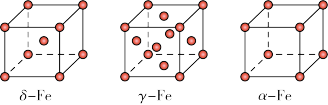
① δ、α两种晶体晶胞中铁原子的配位数之比为_____________ 。
② 1个γ晶体晶胞中所含有的铁原子数为_____________ 。
③ 若Fe原子半径为rpm,NA表示阿伏伽德罗常数的值,则δ-Fe单质的密度为____________ g/cm3(列出算式即可)。
(1) 过渡金属元素铁能形成多种配合物,如:[Fe (CN) 6] 4-、[Fe(SCN)6]3-等。
Fe3+的核外电子排布式为
(2) N的基态原子中能量最高的电子,其电子云在空间有
(3) (NH4)2SO4阴离子的立体构型是
(4) Fe 有δ、γ、α三种同素异形体,其晶胞结构如下图所示:

① δ、α两种晶体晶胞中铁原子的配位数之比为
② 1个γ晶体晶胞中所含有的铁原子数为
③ 若Fe原子半径为rpm,NA表示阿伏伽德罗常数的值,则δ-Fe单质的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】选做人类生活和工业生产都离不开金属。请根据相关信息回答:
(1)235U可用于核能发电。科学家们采用“气体扩散法”从UF6 获得高浓度的235U。已知UF6在常温常压下是固体,在56.4℃升华成气体,说明UF6属于___________________ 晶体。
(2)某丁香酸金属铜配合物的结构简式如下图所示,请回答。
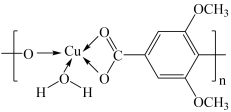
该化合物中碳原子的杂化方式有_______ ,Cu原子的外围电子排布式 ________ 。
(3)某铜的配合物在煤的液化中起催化作用,其阳离子结构如下图。

①在该离子内部含有的化学键类型有_____ (填字母)。
a.离子键
b.极性键
c.非极性键
d.配位键
e.范德华力
f.氢键
②煤液化获得的甲醇经催化氧化可得到重要工业原料甲醛(HCHO)。甲醇的沸点 64.96℃,甲醛的沸点-21℃,甲醛的沸点更低的原因是分子间没有氢键。你认为甲醛分子间没有氢键的原因是_________ 。
③甲醛分子σ键和π键的个数比为____________ 。
(4)具有6 配位的Co3+的配合物[Co(NH3)mCln]Cl(3-n)具有一定的抗肿瘤活性。1 mol该配合物与足量AgNO3溶液反应生成2 mol AgCl沉淀,则m=______ 、n=_____ 。
(1)235U可用于核能发电。科学家们采用“气体扩散法”从UF6 获得高浓度的235U。已知UF6在常温常压下是固体,在56.4℃升华成气体,说明UF6属于
(2)某丁香酸金属铜配合物的结构简式如下图所示,请回答。

该化合物中碳原子的杂化方式有
(3)某铜的配合物在煤的液化中起催化作用,其阳离子结构如下图。

①在该离子内部含有的化学键类型有
a.离子键
b.极性键
c.非极性键
d.配位键
e.范德华力
f.氢键
②煤液化获得的甲醇经催化氧化可得到重要工业原料甲醛(HCHO)。甲醇的沸点 64.96℃,甲醛的沸点-21℃,甲醛的沸点更低的原因是分子间没有氢键。你认为甲醛分子间没有氢键的原因是
③甲醛分子σ键和π键的个数比为
(4)具有6 配位的Co3+的配合物[Co(NH3)mCln]Cl(3-n)具有一定的抗肿瘤活性。1 mol该配合物与足量AgNO3溶液反应生成2 mol AgCl沉淀,则m=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素。X和R属同族元素;Z和U位于第VIIA族;X和Z可形成化合物XZ4;Q基态原子的s轨道和p轨道的电子总数相等;T的一种单质在空气中能够自燃。
请回答下列问题:
(1)R基态原子的电子排布式是_____________________ 。
(2)利用价层电子对互斥理论判断TU3的立体构型是______ 。
(3)X所在周期元素最高价氧化物对应的水化物中,酸性最强的是______ (填化学式);Z和U的氢化物中沸点较高的是_____ (填化学式);Q、R、U的单质形成的晶体,熔点由高到低的排列顺序是_______ (填化学式)。
(4)CuSO4溶液能用作T4中毒的解毒剂,反应可生成T的最高价含氧酸和铜,该反应的化学方程式是_______________________ 。
请回答下列问题:
(1)R基态原子的电子排布式是
(2)利用价层电子对互斥理论判断TU3的立体构型是
(3)X所在周期元素最高价氧化物对应的水化物中,酸性最强的是
(4)CuSO4溶液能用作T4中毒的解毒剂,反应可生成T的最高价含氧酸和铜,该反应的化学方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】2020年1月9日,南京大学物理学院高力波教授团队,探索出了一种可控生长超平整石墨烯的方法,该方法有望推广到新材料、新能源等重要研究领域。
(1)如图图1和图2所示,科学家可以用特殊的胶带将石墨不断地粘撕得到石墨烯,是因为___ 。

(2)石墨烯中碳原子的杂化方式为___ ,12g石墨烯中含有___ 个如图所示的六元环。
(3)石墨晶体中碳碳键的键长___ 金刚石晶体中碳碳键的键长(填“>”“<”或“=”),原因是___ 。
(4)如图图2和图3中,石墨烯转化为氧化石墨烯时,1号C与其相邻C原子间键能的变化是___ (填“变大”、“变小”、“不变”)。
(5)曹原等研制得了具有超导特性的双层石墨烯新材料,手机一旦装上石墨烯电池,充电时间将被缩短为16分钟。将石墨烯逐层叠起来就是石墨,如图图4是石墨晶体的六方晶胞结构。
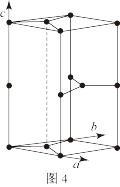

①在下列四边形内画出石墨晶胞沿c轴的投影___ (用“”标出碳原子位置)。
②如果石墨晶胞中最近的两个碳原子之间的距离为apm,层间距为bpm,那么石墨晶体的密度为___ g·cm-3(列出计算式即可))。
(1)如图图1和图2所示,科学家可以用特殊的胶带将石墨不断地粘撕得到石墨烯,是因为

(2)石墨烯中碳原子的杂化方式为
(3)石墨晶体中碳碳键的键长
(4)如图图2和图3中,石墨烯转化为氧化石墨烯时,1号C与其相邻C原子间键能的变化是
(5)曹原等研制得了具有超导特性的双层石墨烯新材料,手机一旦装上石墨烯电池,充电时间将被缩短为16分钟。将石墨烯逐层叠起来就是石墨,如图图4是石墨晶体的六方晶胞结构。


①在下列四边形内画出石墨晶胞沿c轴的投影
②如果石墨晶胞中最近的两个碳原子之间的距离为apm,层间距为bpm,那么石墨晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】IIIA族元素与VA族元素形成的化合物常作为半导体材料,如磷化镓、磷化铝等。磷化镓晶体的晶胞结构可看作金刚石晶胞内部的碳原子被P原子代替,顶点和面心的碳原子被Ga原子代替。
(1)基态P原子中,其电子占据的最高能级共有_______ 个原子轨道,其形状是_______ 。
(2)NH3是一种极易溶于水的气体,其沸点比PH3的沸点高,其原因是_______ 。
(3)①磷化镓晶体中含有的化学键类型为_______ (填字母)。
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
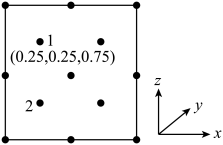
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如图,则原子2的分数坐标为_______ 。 中以获得更好的延展性,具有了磁性,还可以使其显现出优异的光学特性,在磁性器件及光学器件领域具有潜在的应用价值。
中以获得更好的延展性,具有了磁性,还可以使其显现出优异的光学特性,在磁性器件及光学器件领域具有潜在的应用价值。_______ 。
②若图a中晶胞的边长为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为_______  (列出计算式)。
(列出计算式)。
(1)基态P原子中,其电子占据的最高能级共有
(2)NH3是一种极易溶于水的气体,其沸点比PH3的沸点高,其原因是
(3)①磷化镓晶体中含有的化学键类型为
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。若沿y轴投影的晶胞中所有原子的分布图如图,则原子2的分数坐标为
 中以获得更好的延展性,具有了磁性,还可以使其显现出优异的光学特性,在磁性器件及光学器件领域具有潜在的应用价值。
中以获得更好的延展性,具有了磁性,还可以使其显现出优异的光学特性,在磁性器件及光学器件领域具有潜在的应用价值。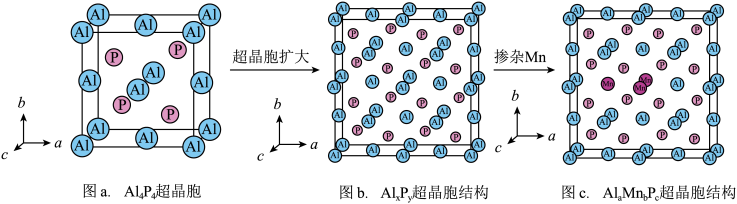
②若图a中晶胞的边长为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的密度为
,则该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)基态B原子中能量最高的电子所在的原子轨道的电子云在空间上有______ 个伸展方向,原子轨道呈______ 形。 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(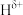 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(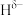 ),H、B、N电负性大小顺序是
),H、B、N电负性大小顺序是______ 。
(2)硼酸( )是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。______ 。
②加热时,硼酸的溶解度增大,主要原因是______ 。
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的 而呈酸性。写出硼酸的电离方程式:
而呈酸性。写出硼酸的电离方程式:______ 。
(3)硼氢化钠( )是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:______ 。
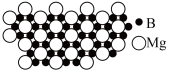
(4)硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为______ 。
(1)基态B原子中能量最高的电子所在的原子轨道的电子云在空间上有
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(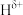 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(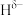 ),H、B、N电负性大小顺序是
),H、B、N电负性大小顺序是(2)硼酸(
 )是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。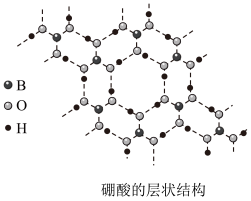
②加热时,硼酸的溶解度增大,主要原因是
③硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的
 而呈酸性。写出硼酸的电离方程式:
而呈酸性。写出硼酸的电离方程式:(3)硼氢化钠(
 )是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:
)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理:(4)硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,如图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】科学家正在研究温室气体CH4和CO2的转化和利用。
(1)CH4和CO2所含的三种元素电负性从小到大的顺序为_____________________________ 。
(2)下列关于CH4和CO2的说法正确的是_______________ (填序号)。
a.固态CO2属于分子晶体
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
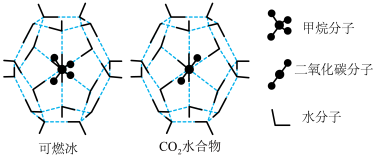
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数见下表.CH4与H2O形成的水合物俗称“可燃冰”
①“可燃冰”中分子间存在的2种作用力是_______________________________________ 。
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想.已知图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是____________________________________________________________________ 。
(1)CH4和CO2所含的三种元素电负性从小到大的顺序为
(2)下列关于CH4和CO2的说法正确的是
a.固态CO2属于分子晶体
b.CH4分子中含有极性共价键,是极性分子
c.因为碳氢键键能小于碳氧键,所以CH4熔点低于CO2
d. CH4和CO2分子中碳原子的杂化类型分别是sp3和sp
(3)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数见下表.CH4与H2O形成的水合物俗称“可燃冰”

| 分子 | 分子直径 | 分子与H2O 的结合能E(kJ/mol) |
| CH4 | 0.436 | 16.40 |
| CO2 | 0.512 | 29.91 |
①“可燃冰”中分子间存在的2种作用力是
②为开采深海海底的“可燃冰”,有科学家提出用CO2置换CH4的设想.已知图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高电子层符号为___________ ,该电子层具有的原子轨道数为___________ 。
②LiBH4由Li+和BH 构成,BH
构成,BH 的立体构型是
的立体构型是___________ ,B原子的杂化轨道类型是___________ 。
③Li、B元素的电负性由小到大的顺序为___________ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+___________ H-(填“>”“=”或“<”)。
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是___________ 族元素。
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488 pm,Na+半径为102 pm,H-的半径为___________ ,NaH的理论密度是___________ g·cm-3。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高电子层符号为
②LiBH4由Li+和BH
 构成,BH
构成,BH 的立体构型是
的立体构型是③Li、B元素的电负性由小到大的顺序为
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1 451 | 7 733 | 10 540 | 13 630 |
M是
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488 pm,Na+半径为102 pm,H-的半径为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】硫铁矿(主要成分FeS2)是接触法制硫酸的主要原料,接触法制硫酸的生产原理分三步。
I.4FeS2+11O2 2Fe2O3+8SO2;
2Fe2O3+8SO2;
II.2SO2+O2 =2SO3;
=2SO3;
III.SO3+H2O=H2SO4
回答下列问题:
(1)①基态Fe2+共有_______ 种不同空间运动状态的电子。
②Fe2+形成的配合物亚铁氰化钾(K4[Fe(CN)6])又称黄血盐,可用于检验Fe2+。与CN-互为等电子体的阴离子为_______ (填离子符号,任写一种)。含有12molσ键的K4[Fe(CN)6]的物质的量为_______ mol。
③已知Fe2+半径为61pm,Co2+半径为65pm,则在隔绝空气条件下分别加热FeCO3和CoCO3,FeCO3受热分解温度_______ (填“低于”或“高于”)CoCO3。
(2)①H2SO4的酸性强于H2SO3的酸性的原因是_______ 。
②过二硫酸的结构式为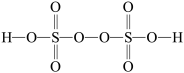 ,S原子的杂化方式为
,S原子的杂化方式为_______ ;S元素的化合价为_______ 。
(3)FeS2晶体的晶胞结构如图所示。
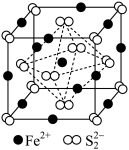
①FeS2晶体的晶胞中,Fe2+位于 所形成的
所形成的_______ (填“正四面体”或“正八面体”,下同)空隙, 位于Fe2+所形成的
位于Fe2+所形成的_______ 空隙。该晶体中距离Fe2+最近的Fe2+的数目为_______ 。
②FeS2晶体的晶胞参数为anm,密度为ρg∙cm-3,阿伏加德罗常数的值为NA,则FeS2的摩尔质量M=_______ g。mol-1(用含a、ρ、NA的代数式表示)。
I.4FeS2+11O2
 2Fe2O3+8SO2;
2Fe2O3+8SO2;II.2SO2+O2
 =2SO3;
=2SO3;III.SO3+H2O=H2SO4
回答下列问题:
(1)①基态Fe2+共有
②Fe2+形成的配合物亚铁氰化钾(K4[Fe(CN)6])又称黄血盐,可用于检验Fe2+。与CN-互为等电子体的阴离子为
③已知Fe2+半径为61pm,Co2+半径为65pm,则在隔绝空气条件下分别加热FeCO3和CoCO3,FeCO3受热分解温度
(2)①H2SO4的酸性强于H2SO3的酸性的原因是
②过二硫酸的结构式为
 ,S原子的杂化方式为
,S原子的杂化方式为(3)FeS2晶体的晶胞结构如图所示。

①FeS2晶体的晶胞中,Fe2+位于
 所形成的
所形成的 位于Fe2+所形成的
位于Fe2+所形成的②FeS2晶体的晶胞参数为anm,密度为ρg∙cm-3,阿伏加德罗常数的值为NA,则FeS2的摩尔质量M=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硫及其化合物在生活、生产中有着广泛的应用。
(1)基态硫原子的价层电子轨道表示式是______ 。
(2)S单质的常见形式为S8,其环状结构如图1所示,其中S原子的杂化方式是______ 。______ 。
(4)大π键可用符号π表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则SO3中的大π键可表示为______ 。
(5)黄铜矿为含硫矿石,这种矿石浑身都是宝。黄铜矿的晶胞如图2所示,原子1的坐标为( ,
, ,2)与Cu(0,0,0)最近的Fe原子的坐标为
,2)与Cu(0,0,0)最近的Fe原子的坐标为______ ;若阿伏加德罗常数的值为NA,则黄铜矿晶体的密度是______ g•cm-3。
(1)基态硫原子的价层电子轨道表示式是
(2)S单质的常见形式为S8,其环状结构如图1所示,其中S原子的杂化方式是
| A.H2S分子的空间构形是直线型 |
| B.六氟化硫(SF6)中心原子的杂化方式为sp3d2 |
| C.第一电离能大小顺序F>O>S |
| D.工业生产硫酸时用水吸收SO3 |
(4)大π键可用符号π表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则SO3中的大π键可表示为
(5)黄铜矿为含硫矿石,这种矿石浑身都是宝。黄铜矿的晶胞如图2所示,原子1的坐标为(
 ,
, ,2)与Cu(0,0,0)最近的Fe原子的坐标为
,2)与Cu(0,0,0)最近的Fe原子的坐标为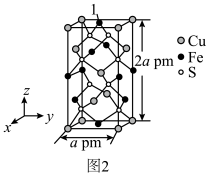
您最近一年使用:0次



