[化学——选修 3:物质结构与性质]
(1) 过渡金属元素铁能形成多种配合物,如:[Fe (CN) 6] 4-、[Fe(SCN)6]3-等。
Fe3+的核外电子排布式为______________ ,从原子结构的角度解释Fe3+比Fe2+稳定的理由是_______________ 。
(2) N的基态原子中能量最高的电子,其电子云在空间有________ 个方向,原子轨道呈________ 形。
(3) (NH4)2SO4阴离子的立体构型是________ ,NH4+中心原子的杂化类型是________ 。
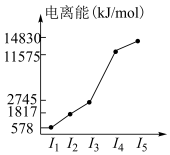
(4) Fe 有δ、γ、α三种同素异形体,其晶胞结构如下图所示:
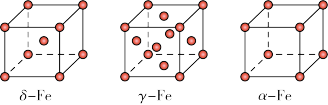
① δ、α两种晶体晶胞中铁原子的配位数之比为_____________ 。
② 1个γ晶体晶胞中所含有的铁原子数为_____________ 。
③ 若Fe原子半径为rpm,NA表示阿伏伽德罗常数的值,则δ-Fe单质的密度为____________ g/cm3(列出算式即可)。
(1) 过渡金属元素铁能形成多种配合物,如:[Fe (CN) 6] 4-、[Fe(SCN)6]3-等。
Fe3+的核外电子排布式为
(2) N的基态原子中能量最高的电子,其电子云在空间有
(3) (NH4)2SO4阴离子的立体构型是
(4) Fe 有δ、γ、α三种同素异形体,其晶胞结构如下图所示:

① δ、α两种晶体晶胞中铁原子的配位数之比为
② 1个γ晶体晶胞中所含有的铁原子数为
③ 若Fe原子半径为rpm,NA表示阿伏伽德罗常数的值,则δ-Fe单质的密度为
更新时间:2018-01-17 20:40:15
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】据世界权威刊物《自然》最近报道,我国科学家选择碲化锆(ZrTe2)和砷化镉(Cd3As2)为材料验证了三维量子霍尔效应,并发现了金属-绝缘体的转换。回答下列问题:
(1)锌原子的价电子排布图:___________
(2)硫和碲位于同主族,H2Te的空间结构为___________ 。H2S的分解温度高于H2Te,其主要原因是___________ 。
(3)Cd2+与NH3等配体形成配离子。1 mol [Cd(NH3)4]2+含___________ molσ键。该配离子中三种元素的电负性大小关系是:___________ 。
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为___________
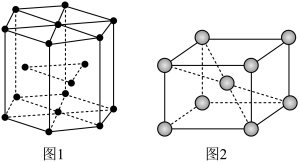
(5)锆晶胞如图1所示,这种堆积方式称为___________ ,镉晶胞如图2所示。已知:NA是阿伏加德罗常数的值,晶体密度为d g·cm-3.在该晶胞中两个镉原子最近核间距为___________ nm(用含NA、d的代数式表示)。
(1)锌原子的价电子排布图:
(2)硫和碲位于同主族,H2Te的空间结构为
(3)Cd2+与NH3等配体形成配离子。1 mol [Cd(NH3)4]2+含
(4)砷与卤素形成多种卤化物。AsCl3、AsF3、AsBr3的熔点由高到低的排序为
(5)锆晶胞如图1所示,这种堆积方式称为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题。_______ (用元素符号表示),1和n的离子半径较大的是_______ (填离子符号)。
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是_______ (填字母)。
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据如下表所示。
比较两元素的 、
、 可知,气态
可知,气态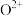 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是_______ 。
(4)第三周期8种元素其中电负性最大的是_______ (填图中的序号)。
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式:_______ 。
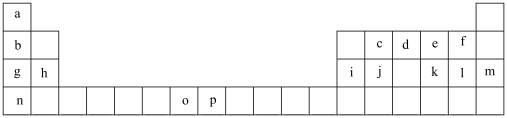
(2)h的单质在空气中燃烧发出耀眼的白光,从原子结构角度解释是涉及电子从能量较高的轨道跃迁到能量较低的轨道时,以光(子)的形式释放能量,以下现象与该原理一样的是
A.燃放焰火 B.棱镜分出的光 C.霓虹灯射出五颜六色的光
(3)o、p两元素的部分电离能数据如下表所示。
电离能/ |  |  |  |
| o | 717 | 1509 | 3248 |
| p | 759 | 1561 | 2957 |
 、
、 可知,气态
可知,气态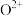 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难。对此,你认为原因可能是
再失去一个电子难。对此,你认为原因可能是(4)第三周期8种元素其中电负性最大的是
(5)表中所列的某主族元素的电离能情况如图所示,写出该元素的最高价氧化物对应的水化物与g的最高价氧化物对应的水化物反应的离子方程式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】[2016·新课标I]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]_______________ ,有__________ 个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是______________________________ 。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________________________ 。
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________________________ 。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______________ ,微粒之间存在的作用力是_______________ 。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______________ 。_____ g·cm−3(列出计算式即可)。
(1)基态Ge原子的核外电子排布式为[Ar]
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为( ,
, ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为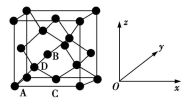
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】(1)基态Fe原子价层电子的电子排布图_______
(2)与NO 互为等电子体的分子是
互为等电子体的分子是_______
(3)比较下列分子或离子中键角大小:H2O_______ H3O+。
(4)OF2分子中,中心原子上的孤电子对数为_______ ,中心原子的杂化方式为_______ 杂化,VSEPR模型为_______ ,分子的立体构型为_______ 。
(5)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑立体构型,[Cu(OH)4]2-结构可用示意图表示为(若有配位键,用箭头表示)_______ 。
(2)与NO
 互为等电子体的分子是
互为等电子体的分子是(3)比较下列分子或离子中键角大小:H2O
(4)OF2分子中,中心原子上的孤电子对数为
(5)向CuSO4溶液中加入过量NaOH溶液可生成[Cu(OH)4]2-。不考虑立体构型,[Cu(OH)4]2-结构可用示意图表示为(若有配位键,用箭头表示)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铂钴合金是以铂为基含钴二元合金,在高温下,铂与钴可无限互溶,其固体为面心立方晶格。铂钴合金磁性极强,磁稳定性较高,耐化学腐蚀性很好,主要用于航天航空仪表、电子钟表、磁控管等。氟及其化合物用途非常广泛。回答下列问题:
(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过____ 方法区分晶体准晶体和非晶体。
(2)基态F原子的价层电子排布图(轨道表达式)为______ 。
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为______ ,与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是______ (各举一例)。
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是______ ;氟化铵中存在______ (填字母)。
A.离子键 B.σ键 C.π键 D.氢键
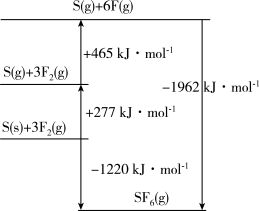
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为______ kJ•mol-1,S-F键的键能为______ kJ•mol-1。
(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是______
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=______ nm(列出计算式)。

(1)聚四氟乙烯是一种准晶体,准晶体是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)基态F原子的价层电子排布图(轨道表达式)为
(3)[H2F]+[SbF6]-(氟锑酸)是一种超强酸,存在[H2F]+,该离子的空间构型为
(4)NH4F(氟化铵)可用于玻璃的蚀刻防腐剂、消毒剂。NH4+中中心原子的杂化类型是
A.离子键 B.σ键 C.π键 D.氢键
(5)SF6被广泛用作高压电气设备的绝缘介质。SF6是一种共价化合物,可通过类似于Born-Haber循环能量构建能量图计算相关键能。则F-F键的键能为

(6)CuCl的熔点为426℃,熔化时几乎不导电;CuF的熔点为908℃,密度为7.1g•cm-3。
①CuF的熔点比CuCl的高,原因是
②已知NA为阿伏加 德罗常数的值,CuF的晶胞结构如图(b)所示,则CuF的晶胞参数a=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】云阳龙缸云端廊桥曾被詟为“世界第一悬挑玻璃景观廊桥”,所用钢化玻璃因其优良的性能广泛应用于日常生活,但由于制作玻璃时里面含有极少量硫化镍,使得钢化玻璃在极限条件下的使用受到限制.
(1)基态硫原子价层电子的轨道表达式(电子排布图)为____________ ,基态镍原子中核外电子占据最高能层的符号为_____________ .
(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为___________ 晶体,Ni(CO)4空间构型与甲烷相同,中心原子的杂化轨道类型为___________ ,写出与配体互为等电子体的阴离子__________________________________________________________ (任写一种).
(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱 > (填化学式)______ ,理由是_______________________________________________________________ .
(4)H2S的键角__________ (填“大于”“小于””等于”)H2O的键角,请从电负性的角度说明理由___________________________________________________ .
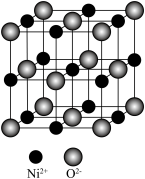
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的空隙__________ 中,已知Ni2+半径为69nm,O2-半径为140nm,阿伏伽德罗常数为NA,NiO晶体的密度为________ g/cm3(只列出计算式).
(1)基态硫原子价层电子的轨道表达式(电子排布图)为
(2)Ni(CO)4常用于制备纯镍,溶于乙醇、CCl4、苯等有机溶剂,为
(3)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱 > (填化学式)
(4)H2S的键角
(5)NiO与NaCl的晶胞结构相似,如图所示,阴离子采取面心立方堆积,阳离子填充在位于阴离子构成的空隙

您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】氨溴索(G)是β-内酰胺类的抗生素,可以治疗多种细菌感染。一种合成路线如下:
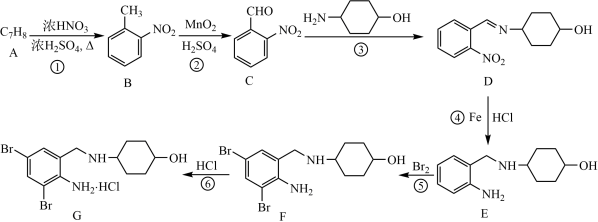
(1)A~C三种物质中_______ (填“有”、“无”)易溶于水的物质。D中氮原子杂化类型为_______ 。
(2)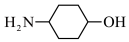 中的官能团名称是
中的官能团名称是_______ ,所涉及到的非金属元素第一电离能由大到小顺序为_______ 。
(3)反应③的化学方程式是_______ 。
(4)反应⑤的反应类型是_______ 。
(5)B的芳香族同分异构体中,满足下列条件的有_______ 种;其中核磁共振氢谱有4组吸收峰且峰面积之比为2∶2∶2∶1的结构简式为_______ 。
①能发生银镜反应;②能水解;③1 mol最多能与2 mol NaOH反应;
(6)写出以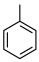 为原料制备
为原料制备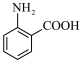 的合成路线
的合成路线_______ (无机试剂任选)。

(1)A~C三种物质中
(2)
 中的官能团名称是
中的官能团名称是(3)反应③的化学方程式是
(4)反应⑤的反应类型是
(5)B的芳香族同分异构体中,满足下列条件的有
①能发生银镜反应;②能水解;③1 mol最多能与2 mol NaOH反应;
(6)写出以
 为原料制备
为原料制备 的合成路线
的合成路线
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硒化物(如KCu4Se8)可用于太阳能电池、光传感器、热电发电与制冷等。回答下列问题:
(1)K与Cu位于同周期,金属钾的熔点比铜的低,这是因为______ 。
(2)O、S、Se均位于元素周期表第ⅥA族,它们的氢化物H2O、H2S及H2Se分子的键角从大到小顺序为______ 。
(3)配合物[Cu(CH3CN)4]BF4中,阴离子的空间构型为______ ,配合离子中与Cu(Ⅱ)形成配位键的原子是______ ,配体中碳原子的杂化方式是______ 。
(4)TMTSF(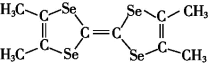 )中共价键的类型是
)中共价键的类型是______ 。
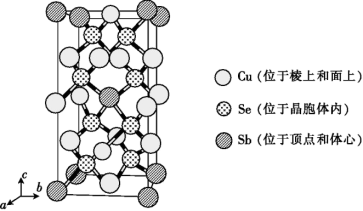
(5)Cu、Sb、Se组成的热电材料,其晶胞结构如图所示,a=b=566pm,c=1128pm,该晶体的密度为______ g·cm-3。
(1)K与Cu位于同周期,金属钾的熔点比铜的低,这是因为
(2)O、S、Se均位于元素周期表第ⅥA族,它们的氢化物H2O、H2S及H2Se分子的键角从大到小顺序为
(3)配合物[Cu(CH3CN)4]BF4中,阴离子的空间构型为
(4)TMTSF(
 )中共价键的类型是
)中共价键的类型是(5)Cu、Sb、Se组成的热电材料,其晶胞结构如图所示,a=b=566pm,c=1128pm,该晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】磷、硫、氯、砷等是农药中的重要组成元素。回答下列问题:
(1)基态砷原子的核外价电子排布式为_______________ 。
(2)生产农药的原料 PSCl3中 P、S、Cl 的第一电离能由大到小的顺序为____ 电负性由大到小的顺序为__________________________ 。
(3)H2SO4为黏稠状难挥发性的酸 ,而 HNO3是易挥发的酸,其原因是__________
(4)COS(羰基硫)可用作粮食的熏蒸剂,其中碳原子的杂化轨道类型为________ ,所含共价 键的类型为_____________ ,N2O与CO2互为等电子体 ,且N2O 分子中O只与一个N相连,则N2O的电子式为_______________ 。
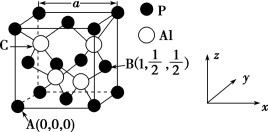
(5)AlP 因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃ ,其晶胞结构如图所示。
①磷化铝的晶体类型为_____________________ 。
②A、B 点的原子坐标如图所示,则C点的原子坐标为__________________ 。
③磷化铝的晶胞参数a = 546.35 pm(l pm=10—12 m),其密度为________ g/cm3( 列出计算式即可,用NA表示阿伏加 德罗常数的数值)。
(1)基态砷原子的核外价电子排布式为
(2)生产农药的原料 PSCl3中 P、S、Cl 的第一电离能由大到小的顺序为
(3)H2SO4为黏稠状难挥发性的酸 ,而 HNO3是易挥发的酸,其原因是
(4)COS(羰基硫)可用作粮食的熏蒸剂,其中碳原子的杂化轨道类型为
(5)AlP 因杀虫效率高、廉价易得而被广泛应用。已知AlP的熔点为2000℃ ,其晶胞结构如图所示。

①磷化铝的晶体类型为
②A、B 点的原子坐标如图所示,则C点的原子坐标为
③磷化铝的晶胞参数a = 546.35 pm(l pm=10—12 m),其密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】碱土金属指II A族的铍(Be)、镁(Mg)、钙(Ca)、锶(Sr)、钡(Ba)等元素,它们的单质及其化合物有着广泛的用途。
(1)Be基态原子的轨道表示式为_________________________ ;
镁和铝的第二电离能:I2(Mg)_____ I2(Al) (填“>”“ <”或“=”)。
(2)在500~600℃气相中,氯化铍以二聚体Be2Cl4, (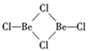 )的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
)的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
①在二聚体Be2Cl4中Be的杂化方式为___________ ,1mol Be2Cl4中含有_________ mol 配位键。
②MgCl2的熔、沸点比BeCl2高的原因是____________________ 。
(3)根据巴索洛规则:一般来讲,盐中阴、阳离子半径相差较大时,其溶解度较大。则在水中溶解度 S(SrF2)____ S(BaF2) (填“>” “<””或“=”)。
(4)石灰氮(CaCN2)—种碱性肥料,可用作除草剂、杀菌剂、杀虫剂等。
①CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和________ (填化学式),写出CN22-的电子式___________ 。
②CaCN2与水反应生成CaCO3和NH3两种物质,则1mol CaCN2与水反应的过程中,反应物断裂的σ键总数_______________ 。
(5) Mg2+与Ni2+、 O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为_________ 。已知该晶胞参数a pm.则该晶体的密度为_________ g·cm-3(用a和NA表示)。
(1)Be基态原子的轨道表示式为
镁和铝的第二电离能:I2(Mg)
(2)在500~600℃气相中,氯化铍以二聚体Be2Cl4, (
 )的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。
)的形式存在,在1000 ℃,氯化铍则以BeCl2形式存在。①在二聚体Be2Cl4中Be的杂化方式为
②MgCl2的熔、沸点比BeCl2高的原因是
(3)根据巴索洛规则:一般来讲,盐中阴、阳离子半径相差较大时,其溶解度较大。则在水中溶解度 S(SrF2)
(4)石灰氮(CaCN2)—种碱性肥料,可用作除草剂、杀菌剂、杀虫剂等。
①CaCN2中阴离子为CN22-,与CN22-互为等电子体的分子有N2O和
②CaCN2与水反应生成CaCO3和NH3两种物质,则1mol CaCN2与水反应的过程中,反应物断裂的σ键总数
(5) Mg2+与Ni2+、 O2-形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为

您最近一年使用:0次
【推荐2】一种从工业锌置换渣(主要含 等)中回收锗、铅的工艺流程如图:
等)中回收锗、铅的工艺流程如图: 能溶于强酸的浓溶液或强碱溶液;
能溶于强酸的浓溶液或强碱溶液; 可溶于热盐酸中:
可溶于热盐酸中: ;常温下,
;常温下,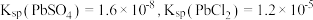 。
。
(1)“还原浸出”时, 的存在可促进
的存在可促进 浸出。
浸出。
① 的空间结构为
的空间结构为___________ 。
②该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)“ 酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是
酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是___________ 。
(3)“碱溶”时, 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)“降温析铅”过程中,体系温度冷却至常温,且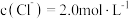 。为防止
。为防止 中混有
中混有 杂质,应控制溶液中
杂质,应控制溶液中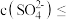
___________ 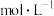 (保留两位有效数字)。
(保留两位有效数字)。
(5)“转化”的意义在于可重复利用___________ (填物质名称)。
(6)通过掺杂硅可将锗单质转化为不同掺杂比例的硅锗合金,锗及硅锗合金的立方晶胞如图所示。 周围与其最近的
周围与其最近的 的个数为
的个数为___________ 。
②若硅锗合金i的晶胞边长为 ,设
,设 为阿伏加德罗常数的值,则硅锗合金i晶体的密度为
为阿伏加德罗常数的值,则硅锗合金i晶体的密度为___________  (列计算式)。
(列计算式)。
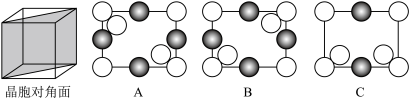
③硅锗合金ii沿晶胞对角面取得的截图为___________ (填标号)。
 等)中回收锗、铅的工艺流程如图:
等)中回收锗、铅的工艺流程如图: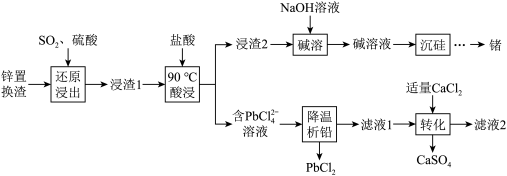
 能溶于强酸的浓溶液或强碱溶液;
能溶于强酸的浓溶液或强碱溶液; 可溶于热盐酸中:
可溶于热盐酸中: ;常温下,
;常温下,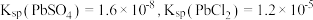 。
。(1)“还原浸出”时,
 的存在可促进
的存在可促进 浸出。
浸出。①
 的空间结构为
的空间结构为②该反应中氧化剂与还原剂的物质的量之比为
(2)“
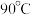 酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是
酸浸”所用盐酸的浓度不宜过大或过小,浓度不宜过大的主要原因是(3)“碱溶”时,
 发生反应的离子方程式为
发生反应的离子方程式为(4)“降温析铅”过程中,体系温度冷却至常温,且
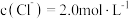 。为防止
。为防止 中混有
中混有 杂质,应控制溶液中
杂质,应控制溶液中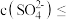
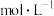 (保留两位有效数字)。
(保留两位有效数字)。(5)“转化”的意义在于可重复利用
(6)通过掺杂硅可将锗单质转化为不同掺杂比例的硅锗合金,锗及硅锗合金的立方晶胞如图所示。
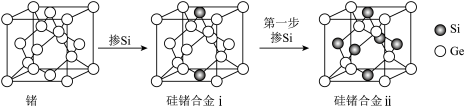
 周围与其最近的
周围与其最近的 的个数为
的个数为②若硅锗合金i的晶胞边长为
 ,设
,设 为阿伏加德罗常数的值,则硅锗合金i晶体的密度为
为阿伏加德罗常数的值,则硅锗合金i晶体的密度为 (列计算式)。
(列计算式)。③硅锗合金ii沿晶胞对角面取得的截图为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】X、Y、Z、W、Q、R均为前四周期元素,且原子序数依次增大。其相关信息如下表所示:
回答下列问题:
(1)Y元素的基态原子中未成对电子数为______ ;X、Y、Z三种元素原子的第一电离能由小到大的顺序为____________ (用元素符号表示)。
(2)W的氯化物的熔点比Q的氯化物的熔点__________ (填“高”或“低”),理由是__________________________________________________ 。
(3)光谱证实元素W的单质与强碱性溶液反应有[W(OH)4]-生成,则[W(OH)4]-中存在(填字母)_____________ 。
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
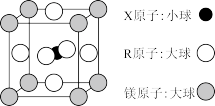
(4)含有X、R和镁三种元素的某种晶体具有超导性,其结构如下图所示。则该晶体的化学式为_______ ;晶体中每个镁原子周围距离最近的R原子有_______ 个。
| X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
| Y元素的气态氢化物与其最高价氧化物对应的水化物能发生化合反应 |
| Z元素的族序数是其周期数的三倍 |
| W原子的第一至第六电离能分别为:I1=578KJ·mol-1I2=1817KJ·mol-1I3=2745KJ·mol-1 I4=11575KJ·mol-1I5=14830KJ·mol-1I6=18376KJ·mol-1 |
| Q为前四周期中电负性最小的元素 |
| 元素R位于周期表的第10列 |
(1)Y元素的基态原子中未成对电子数为
(2)W的氯化物的熔点比Q的氯化物的熔点
(3)光谱证实元素W的单质与强碱性溶液反应有[W(OH)4]-生成,则[W(OH)4]-中存在(填字母)
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
(4)含有X、R和镁三种元素的某种晶体具有超导性,其结构如下图所示。则该晶体的化学式为

您最近一年使用:0次



