东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)硫酸镍溶于氨水形成 蓝色溶液。
蓝色溶液。
① 中阴离子的立体构型是
中阴离子的立体构型是_______ 。
②在 中存在哪些化学键
中存在哪些化学键_______ 。
A.离子键 B.配位键 C.金属键 D.极性共价键
③ 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为_______ (填化学式,下同),还原性由强到弱的顺序为_______ ,键角由大到小的顺序为_______ 。
(2)丁二酮肟是检验 的灵敏试剂。丁二酮肟分子(
的灵敏试剂。丁二酮肟分子(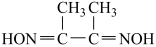 )中C原子轨道杂化类型为
)中C原子轨道杂化类型为_______ ,1mol丁二酮肟分子所含 键的数目为
键的数目为_______ 。
(3)配合物 常温下为液体,易溶于
常温下为液体,易溶于 、苯等有机溶剂。
、苯等有机溶剂。 中
中 与
与 的
的 原子形成配位键。不考虑空间构型,
原子形成配位键。不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为_____ (用“→”表示出配位键)。
(4)①氨硼烷( )分子中,
)分子中, 化学键称为
化学键称为_______ 键,其电子对由_______ 原子提供。 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性(
呈正电性(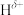 ),与
),与 原子相连的
原子相连的 呈负电性(
呈负电性(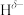 ),组成元素电负性大小顺序是
),组成元素电负性大小顺序是_______ 。与 原子总数相等的等电子体是
原子总数相等的等电子体是_______ (写分子式)。
②氨硼烷在催化剂作用下水解释放氢气: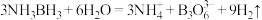 ,
, 的结构为
的结构为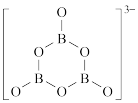 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_______ 变为_______ 。
(1)硫酸镍溶于氨水形成
 蓝色溶液。
蓝色溶液。①
 中阴离子的立体构型是
中阴离子的立体构型是②在
 中存在哪些化学键
中存在哪些化学键A.离子键 B.配位键 C.金属键 D.极性共价键
③
 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(2)丁二酮肟是检验
 的灵敏试剂。丁二酮肟分子(
的灵敏试剂。丁二酮肟分子(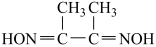 )中C原子轨道杂化类型为
)中C原子轨道杂化类型为 键的数目为
键的数目为(3)配合物
 常温下为液体,易溶于
常温下为液体,易溶于 、苯等有机溶剂。
、苯等有机溶剂。 中
中 与
与 的
的 原子形成配位键。不考虑空间构型,
原子形成配位键。不考虑空间构型, 的结构可用示意图表示为
的结构可用示意图表示为(4)①氨硼烷(
 )分子中,
)分子中, 化学键称为
化学键称为 分子中,与
分子中,与 原子相连的
原子相连的 呈正电性(
呈正电性(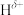 ),与
),与 原子相连的
原子相连的 呈负电性(
呈负电性(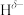 ),组成元素电负性大小顺序是
),组成元素电负性大小顺序是 原子总数相等的等电子体是
原子总数相等的等电子体是②氨硼烷在催化剂作用下水解释放氢气:
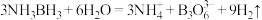 ,
, 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由
更新时间:2022-04-20 06:52:30
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】六方BN与石墨有类似结构。BN纳米片负载纳米 可催化还原对硝基苯酚,生成对氨基苯酚,反应所用还原剂为
可催化还原对硝基苯酚,生成对氨基苯酚,反应所用还原剂为 。
。

回答下列问题:
(1)基态Cu原子的价电子排布式为___________ 。在催化剂 /BN中,O、B、N、Cu电负性由大到小的顺序是
/BN中,O、B、N、Cu电负性由大到小的顺序是___________ ,六方BN晶体中层与层之间的作用力属于___________ 。
(2)还原剂 中,阴离子空间构型是
中,阴离子空间构型是______ ,中心原子的杂化形式为_______ 。 中存在
中存在_______ (填标号)。
A.离子键 B.σ键 C.π键 D.氢键
(3)比较对硝基苯酚与对氨基苯酚,熔点高的是___________ ,原因是___________ 。
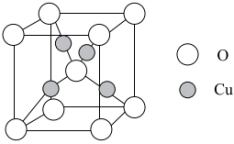
(4) 属立方晶胞,结构如图所示,其边长(晶胞参数)为anm,晶胞中O处于顶角和体心位置,Cu处于晶胞内部,Cu与O间的最短距离为
属立方晶胞,结构如图所示,其边长(晶胞参数)为anm,晶胞中O处于顶角和体心位置,Cu处于晶胞内部,Cu与O间的最短距离为___________ nm,该晶胞中含有的O个数为___________ 。设阿伏加德罗常数的值为 ,则
,则 的密度计算表达式为
的密度计算表达式为___________  。
。
 可催化还原对硝基苯酚,生成对氨基苯酚,反应所用还原剂为
可催化还原对硝基苯酚,生成对氨基苯酚,反应所用还原剂为 。
。
回答下列问题:
(1)基态Cu原子的价电子排布式为
 /BN中,O、B、N、Cu电负性由大到小的顺序是
/BN中,O、B、N、Cu电负性由大到小的顺序是(2)还原剂
 中,阴离子空间构型是
中,阴离子空间构型是 中存在
中存在A.离子键 B.σ键 C.π键 D.氢键
(3)比较对硝基苯酚与对氨基苯酚,熔点高的是
(4)
 属立方晶胞,结构如图所示,其边长(晶胞参数)为anm,晶胞中O处于顶角和体心位置,Cu处于晶胞内部,Cu与O间的最短距离为
属立方晶胞,结构如图所示,其边长(晶胞参数)为anm,晶胞中O处于顶角和体心位置,Cu处于晶胞内部,Cu与O间的最短距离为 ,则
,则 的密度计算表达式为
的密度计算表达式为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】胆矾(CuSO4·5H2O)可用于泳池杀菌消毒。回答下列问题:
(1)铜元素位于元素周期表的_____ 区,基态Cu原子的核外电子排布式为_____ 。
(2)CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如图:
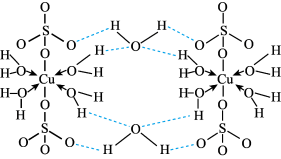
① 的空间构型为
的空间构型为_____ ,其中硫原子的杂化方式为_____ 。
②硫酸铜晶体中Cu2+的配位数为_____ ,[Cu(H2O)4]2+中配位原子是_____ 。
③在上述结构示意图中,存在的化学键有_____ 。
(3)向CuSO4溶液中逐滴加入氨水,溶液最终变为深蓝色,原因是_____ 。
(1)铜元素位于元素周期表的
(2)CuSO4·5H2O可写成[Cu(H2O)4]SO4·H2O,其结构示意图如图:

①
 的空间构型为
的空间构型为②硫酸铜晶体中Cu2+的配位数为
③在上述结构示意图中,存在的化学键有
(3)向CuSO4溶液中逐滴加入氨水,溶液最终变为深蓝色,原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】元素A、B、C、D、E、F、G在元素周期表中的位置如图所示,回答下列问题:

(1)G的基态原子核外电子排布式为____ 。原子的第一电离能:D____ E(填“>”或“<”)。
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l—l>l—b>b—b(l为孤对电子对,b为键合电子对),则关于A2C中的A—C—A键角可得出的结论是____ 。
(3)化合物G(BC)5的熔点为-20℃,沸点为103℃,其固体属于____ 晶体,该物质中存在的化学键类型有___ 。
(4)化合物BCF2的立体构型为____ ,其中B原子的杂化轨道类型是____ 。
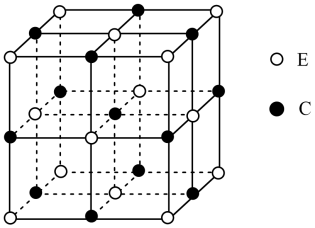
(5)化合物EC的晶胞结构如图所示,晶胞参数a=0.424nm。列式计算EC晶体的密度(g·cm-3)____ 。

(1)G的基态原子核外电子排布式为
(2)根据价层电子互斥理论,价层电子对之间的斥力大小有如下顺序:l—l>l—b>b—b(l为孤对电子对,b为键合电子对),则关于A2C中的A—C—A键角可得出的结论是
| A.180° | B.接近120°,但小于120° |
| C.接近120°,但大于120° | D.接近109°28’,但小于109°28’ |
(4)化合物BCF2的立体构型为
(5)化合物EC的晶胞结构如图所示,晶胞参数a=0.424nm。列式计算EC晶体的密度(g·cm-3)

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】卤素及其化合物在生产生活中应用广泛。请回答:
(1)基态 原子的价层电子轨道表示式为
原子的价层电子轨道表示式为_______ 。
(2)卤族元素可与其他元素形成多种化合物。
①下列说法不正确的是_______ 。
A.能量最低的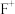 的
的 轨道有一个成单电子
轨道有一个成单电子
B.得到一个电子释放的能量,
C.化学键的极性: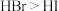
D. 分子的空间构型:直线形
分子的空间构型:直线形
② 中
中 原子的杂化方式是
原子的杂化方式是_______ ,预测该分子可与 、
、 中的
中的_______ 发生化学反应,预测依据是_______ 。
③ 分子之间形成的氢键强于
分子之间形成的氢键强于 分子之间形成的氢键,但在压力相同时
分子之间形成的氢键,但在压力相同时 的沸点仍高于
的沸点仍高于 ,解释原因:
,解释原因:_______ 。
(3)金属元素M与F形成的氟化物晶胞结构如图。已知该物质中M的配位数为8,则氟化物的化学式是_______ ,F的配位数为_______ 。

(1)基态
 原子的价层电子轨道表示式为
原子的价层电子轨道表示式为(2)卤族元素可与其他元素形成多种化合物。
①下列说法不正确的是
A.能量最低的
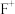 的
的 轨道有一个成单电子
轨道有一个成单电子B.得到一个电子释放的能量,

C.化学键的极性:
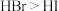
D.
 分子的空间构型:直线形
分子的空间构型:直线形②
 中
中 原子的杂化方式是
原子的杂化方式是 、
、 中的
中的③
 分子之间形成的氢键强于
分子之间形成的氢键强于 分子之间形成的氢键,但在压力相同时
分子之间形成的氢键,但在压力相同时 的沸点仍高于
的沸点仍高于 ,解释原因:
,解释原因:(3)金属元素M与F形成的氟化物晶胞结构如图。已知该物质中M的配位数为8,则氟化物的化学式是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】硼、氮、磷、钴、镍等元素的化合物在现代农业、科技、国防中有着许多独特的用途。
(1)磷原子在成键时,能将一个 电子激发到
电子激发到 能级而参与成键,写出该激发态磷原子的核外电子排布式:
能级而参与成键,写出该激发态磷原子的核外电子排布式:___________ 。
(2)钴位于元素周期表的___________ 区,钴与 易形成正八面体形的
易形成正八面体形的 配离子,试推测
配离子,试推测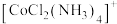 的空间构型有
的空间构型有___________ 种。
(3)制备氮化硼 的一种方法为
的一种方法为 。立方氮化硼(
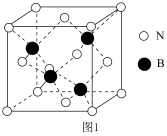
。立方氮化硼( )的晶胞如图1所示,其晶体类型为
)的晶胞如图1所示,其晶体类型为___________ ,N的配位数为___________ 。试用价层电子对互斥理论解释 的键角比
的键角比 大的原因:
大的原因:___________ 。
(4)含有两个或两个以上配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物称为螯合物。 的一种螯合物的结构如图2所示,
的一种螯合物的结构如图2所示, 该配合物中通过螯合作用形成的配位键有
该配合物中通过螯合作用形成的配位键有___________  。
。

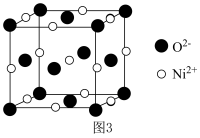
(5) 晶胞为
晶胞为 型结构(如图3)。其中
型结构(如图3)。其中 可看成填充在
可看成填充在 组成的
组成的________ 空隙中,填充率为 。将
。将 在空气中加热,部分
在空气中加热,部分 被氧化为
被氧化为 ,成为
,成为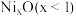 ,晶体仍保持电中性,则会出现晶体缺陷,填充率下降。现有
,晶体仍保持电中性,则会出现晶体缺陷,填充率下降。现有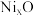 晶胞的质量为
晶胞的质量为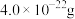 。则填充
。则填充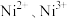 和未填充
和未填充 离子的空隙个数之比为
离子的空隙个数之比为___________ 。
(1)磷原子在成键时,能将一个
 电子激发到
电子激发到 能级而参与成键,写出该激发态磷原子的核外电子排布式:
能级而参与成键,写出该激发态磷原子的核外电子排布式:(2)钴位于元素周期表的
 易形成正八面体形的
易形成正八面体形的 配离子,试推测
配离子,试推测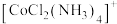 的空间构型有
的空间构型有(3)制备氮化硼
 的一种方法为
的一种方法为 。立方氮化硼(
。立方氮化硼( )的晶胞如图1所示,其晶体类型为
)的晶胞如图1所示,其晶体类型为 的键角比
的键角比 大的原因:
大的原因:
(4)含有两个或两个以上配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物称为螯合物。
 的一种螯合物的结构如图2所示,
的一种螯合物的结构如图2所示, 该配合物中通过螯合作用形成的配位键有
该配合物中通过螯合作用形成的配位键有 。
。
(5)
 晶胞为
晶胞为 型结构(如图3)。其中
型结构(如图3)。其中 可看成填充在
可看成填充在 组成的
组成的 。将
。将 在空气中加热,部分
在空气中加热,部分 被氧化为
被氧化为 ,成为
,成为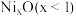 ,晶体仍保持电中性,则会出现晶体缺陷,填充率下降。现有
,晶体仍保持电中性,则会出现晶体缺陷,填充率下降。现有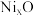 晶胞的质量为
晶胞的质量为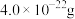 。则填充
。则填充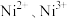 和未填充
和未填充 离子的空隙个数之比为
离子的空隙个数之比为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】化合物G俗称依普黄酮,是一种抗骨质疏松药物的主要成分。以甲苯为原料合成该化合物的路线如下图所示:

已知:I.G的结构简式为
II.
(1)反应①的反应条件为___________ 。
(2)C中碳原子的杂化类型为___________ 。
(3)E中官能团的名称为___________ ,反应F→G的反应类型为___________ 。
(4)E与足量的H2完全加成后所生成的化合物中手性碳原子(碳原子上连接四个不同的原子或基团)的个数为___________ 。
(5)已知N为催化剂,则E+HC(OC2H5)3→F的化学方程式为___________ 。
(6)K是D的同系物,其相对分子质量比D多14,满足下列条件的K的同分异构体共有___________ 种。
①苯环上只有两个取代基;
②能与Na反应生成H2;
③能与银氨溶液发生银镜反应。
(7)根据上述信息,设计以苯酚和为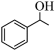 原料,制备
原料,制备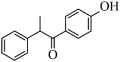 的合成路线
的合成路线___________ (无机试剂任选)。

已知:I.G的结构简式为

II.

(1)反应①的反应条件为
(2)C中碳原子的杂化类型为
(3)E中官能团的名称为
(4)E与足量的H2完全加成后所生成的化合物中手性碳原子(碳原子上连接四个不同的原子或基团)的个数为
(5)已知N为催化剂,则E+HC(OC2H5)3→F的化学方程式为
(6)K是D的同系物,其相对分子质量比D多14,满足下列条件的K的同分异构体共有
①苯环上只有两个取代基;
②能与Na反应生成H2;
③能与银氨溶液发生银镜反应。
(7)根据上述信息,设计以苯酚和为
 原料,制备
原料,制备 的合成路线
的合成路线
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铁触媒常作为合成氨的催化剂,CO会使催化剂中毒。可用CH3COO[Cu(NH3)2]溶液吸收CO。
(1)Cu2+基态核外电子排布式为________________ 。
(2)C、N、O的电负性由大到小的顺序为________________ 。
(3)1 mol CH3COO[Cu(NH3)2]中含有σ键的数目为________________ mol,其中C原子轨道的杂化类型是________________ 。
(4)与CO分子互为等电子体的阴离子为________________ 。
(5)Cu和Fe都可以形成多种氧化物。其中FexO晶胞结构为NaCl型,由于晶体缺陷,x值小于1。若FexO中的x=0.92,则该此晶体化学式为________________ (用Fe2+aFe3+bO形式表示)。
(1)Cu2+基态核外电子排布式为
(2)C、N、O的电负性由大到小的顺序为
(3)1 mol CH3COO[Cu(NH3)2]中含有σ键的数目为
(4)与CO分子互为等电子体的阴离子为
(5)Cu和Fe都可以形成多种氧化物。其中FexO晶胞结构为NaCl型,由于晶体缺陷,x值小于1。若FexO中的x=0.92,则该此晶体化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】中科院大连化学物理研究所科学家用Ni-BaH3/Al2O3、Ni-LiH等作催化剂,实现了在常压、100~300℃的条件下合成氨,这一成果发表在《Nature Energy》杂志上。
(1)基态 的核外电子排布式为
的核外电子排布式为___________ ,若该离子核外电子空间运动状态有15种,则该离子处于___________ (填“基”或“激发”)态。
(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中 的空间构型为
的空间构型为___________ 。
②甘氨酸的晶体类型是___________ ,其熔、沸点远高于相对分子质量几乎相等的丙酸(熔点为-21℃,沸点为141℃)的主要原因:一是甘氨酸能形成内盐;二是___________ 。
(3)比较NH3分子(前者)和在 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者______ 后者。(填“>”、“<”或“=”)
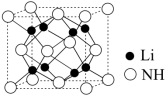
(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为d pm,密度为ρ g/cm3,则阿伏加德罗常数
_______  (列出表达式)。
(列出表达式)。
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨在粮食生产、国防中有着无可替代的地位,也是重要的化工原料,可用于合成氨基酸、硝酸、TNT等。甘氨酸(NH2CH2COOH)是组成最简单的氨基酸,熔点为182℃,沸点为233℃。
①硝酸溶液中
 的空间构型为
的空间构型为②甘氨酸的晶体类型是
(3)比较NH3分子(前者)和在
 中NH3(后者)分子中∠H-N-H的键角大小,前者
中NH3(后者)分子中∠H-N-H的键角大小,前者(4)亚氨基锂(Li2NH,摩尔质量为M g/mol),是一种储氢容量高、安全性能好的固体储氢材料,其晶胞结构如图所示,若晶胞参数为d pm,密度为ρ g/cm3,则阿伏加德罗常数

 (列出表达式)。
(列出表达式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】P可形成许多结构和性质特殊的化合物。请回答下列问题:
(1)P元素位于周期表的第15列。
①基态P原子的价电子轨道表示式为___________ 。
②下列说法不正确的是________ 。
A.非金属性:As<P<N
B.第二电离能( )大小:
)大小: (Si)<
(Si)< (P)<
(P)< (S)<
(S)< (Na)
(Na)
C.电负性:P<As<O
D.O-H键的键能: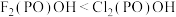
(2)常温下,五氯化磷为白色固体,熔融状态下能导电,气态时以PCl5分子存在。
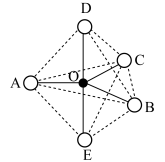
①气态PCl5分子结构如图所示,O位于等边三角形ABC的中心,DOE垂直于ABC的平面,黑球为P,白球为Cl,比较键长大小:键长OD________ OA(填“>”“<”或“=”)。__________ 。
③PCl5不能与金属Ni反应,而PCl3能与金属Ni反应,解释PCl3能与金属Ni反应的原因_____________ 。
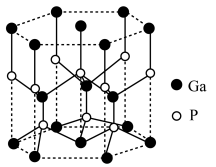
(3)Ga与P形成的某化合物晶体的结构如图。该化合物的化学式为____________ ,P的配位数为____________ 。
(1)P元素位于周期表的第15列。
①基态P原子的价电子轨道表示式为
②下列说法不正确的是
A.非金属性:As<P<N
B.第二电离能(
 )大小:
)大小: (Si)<
(Si)< (P)<
(P)< (S)<
(S)< (Na)
(Na)C.电负性:P<As<O
D.O-H键的键能:
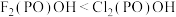
(2)常温下,五氯化磷为白色固体,熔融状态下能导电,气态时以PCl5分子存在。
①气态PCl5分子结构如图所示,O位于等边三角形ABC的中心,DOE垂直于ABC的平面,黑球为P,白球为Cl,比较键长大小:键长OD
③PCl5不能与金属Ni反应,而PCl3能与金属Ni反应,解释PCl3能与金属Ni反应的原因
(3)Ga与P形成的某化合物晶体的结构如图。该化合物的化学式为
您最近一年使用:0次



