绿色植物标本用醋酸铜晶体[(CH3COO)2Cu•H2O]处理后颜色更鲜艳、稳定。制备醋酸铜晶体并测定产品中铜的含量,实验如图。
醋酸铜晶体的制备
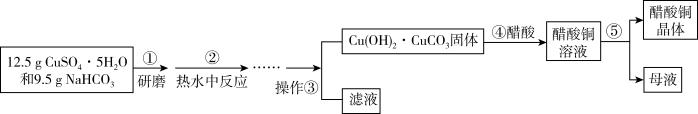
(1)步骤②将研磨后混合物注入热水中反应,写出反应的离子方程式____ ;碱式碳酸铜的制备需在热水中进行反应,且温度需控制在60℃左右,原因是____ 。
(2)操作③的名称为____ 。
(3)写出图中④发生反应的化学方程式____ 。
(4)图中⑤采用的操作为:____ 、____ 、过滤、洗涤、干燥。
醋酸铜晶体的制备

(1)步骤②将研磨后混合物注入热水中反应,写出反应的离子方程式
(2)操作③的名称为
(3)写出图中④发生反应的化学方程式
(4)图中⑤采用的操作为:
更新时间:2022-04-15 19:48:54
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
【推荐1】工业上氯化钠可以制备多种物质。如图是侯德榜联合制碱法的工艺流程图:

已知:侯氏制碱法的原理之一为 。
。
(1)循环物质X的化学式是___________ (填“ ”或“
”或“ ”);
”);
(2)在实验室中进行操作l的名称为___________ (填“过滤”或“蒸馏”);
(3)写出煅烧固体1的化学方程式:___________ :
(4)一定条件下可以发生可逆反应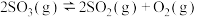 。现在1L容积不变的容器中,通入2mol
。现在1L容积不变的容器中,通入2mol ,10min后生成了1mol
,10min后生成了1mol 。
。
①用 表示该反应的速率
表示该反应的速率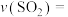
___________  ;
;
②其他条件不变,增大压强,反应速率___________ (填“增大”或“减小”)。

已知:侯氏制碱法的原理之一为
 。
。(1)循环物质X的化学式是
 ”或“
”或“ ”);
”);(2)在实验室中进行操作l的名称为
(3)写出煅烧固体1的化学方程式:
(4)一定条件下可以发生可逆反应
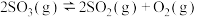 。现在1L容积不变的容器中,通入2mol
。现在1L容积不变的容器中,通入2mol ,10min后生成了1mol
,10min后生成了1mol 。
。①用
 表示该反应的速率
表示该反应的速率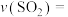
 ;
;②其他条件不变,增大压强,反应速率
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
解题方法
【推荐2】将气体A、B置于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。
2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。
(1)用C表示10s内反应的平均反应速率为_______________ 。
(2)反应前A的物质的量浓度是_______________ 。
(3)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度_______________ ;②增大A的浓度_______________ ;③增大压强_______________ 。
(4)下列叙述能说明该反应已达到化学平衡状态的是_______________ (填标号)。
A.v(B)=2v(C)
B.容器内压强不再发生变化
C.容器内气体密度不再发生变化
D.A的体积分数不再变化
E.相同时间内消耗nmol的B的同时生成2nmol的D
 2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。
2C(g)+2D(g),反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。(1)用C表示10s内反应的平均反应速率为
(2)反应前A的物质的量浓度是
(3)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度
(4)下列叙述能说明该反应已达到化学平衡状态的是
A.v(B)=2v(C)
B.容器内压强不再发生变化
C.容器内气体密度不再发生变化
D.A的体积分数不再变化
E.相同时间内消耗nmol的B的同时生成2nmol的D
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某化学小组为了研究外界条件对化学反应速率的影响,进行了酸性高锰酸钾与草酸(H2C2O4)的反应,记录如表所示的实验数据:
(1)请写出该反应的离子方程式______ ,当该反应以表中数据反应完全时转移电子数为NA。
(2)V1=_______ mL。
(3)根据表中的实验①、②数据,可以得到的结论是_______ 。
(4)探究温度对化学反应速率的影响,应选择_______ (填实验编号)
(5)该小组根据经验绘制了 n (Mn 2+)随时间变化的趋势如图 1 所示,但有同学查阅已有实验资料发现,该实验过程中 n (Mn 2+)随时间变化的实际趋势如图 2 所示。
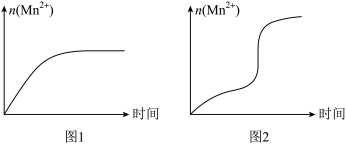
该小组同学根据图 2 所示信息提出了新的假设,并设计实验方案④继续进行实验探究。
②小组同学提出的假设是________ 。
②若该小组同学提出的假设成立,应观察到________ 现象。
| 实验 | 实验 | 试管中所加试剂及其用量/mL | 溶液褪至无 | |||
| 编号 | 温度 | 0.6mol/L H2C2O4溶液 | H2O | 3mol/L H2SO4 稀溶液 | 0.05mol/L KMnO4 溶液 | 色所需时间 /min |
| ① | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
| ② | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
| ③ | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
(1)请写出该反应的离子方程式
(2)V1=
(3)根据表中的实验①、②数据,可以得到的结论是
(4)探究温度对化学反应速率的影响,应选择
| 实验编号 | 实验温度 /℃ | 试管中所加试剂及其用量 | 再加入某种固体 | 溶液褪至无色所需时间/min | |||
| ④ | 25 | 0.6mol/L H2C2O4 | H2O | 3mol/L H2SO4 | 0.05mol/L KMnO4溶液 | ||
| 2.0 | 3.0 | 2.0 | 3.0 | MnSO4 | t | ||

该小组同学根据图 2 所示信息提出了新的假设,并设计实验方案④继续进行实验探究。
②小组同学提出的假设是
②若该小组同学提出的假设成立,应观察到
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐1】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
(1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图:
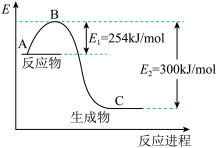
请写出NO2和CO反应的热化学方程式:___ 。
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g) 2NH3(g)+Q(Q>0),其化学平衡常数K与T的关系如下表:
2NH3(g)+Q(Q>0),其化学平衡常数K与T的关系如下表:
请完成下列问题:比较K1、K2的大小:K1___ K2(填写“>”、“=”或“<”)
(3)判断该反应达到化学平衡状态的依据的是___ (选填字母序号)。
A.2v(H2)正=3v(NH3)逆 B.2v(N2)正=v(H2)逆
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。盐酸肼第一步水解反应的离子方程式___ ;
盐酸肼水溶液中离子浓度的排列顺序正确的是___ (填序号)。
a.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
b.c(Cl-)>c([N2H5•H2O]+)>c(H+)>c(OH-)
c.2c(N2H62+)+c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
d.2c(N2H62+)+2c([N2H5•H2O]+)+2c([N2H4•2H2O]=c(Cl-)
(1)如图是1molNO2和1molCO反应生成CO2和NO过程中能量变化示意图:

请写出NO2和CO反应的热化学方程式:
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)
 2NH3(g)+Q(Q>0),其化学平衡常数K与T的关系如下表:
2NH3(g)+Q(Q>0),其化学平衡常数K与T的关系如下表:| T/K | 298 | 398 | 498 | … |
| K/ | 4.1×106 | K1 | K2 | … |
请完成下列问题:比较K1、K2的大小:K1
(3)判断该反应达到化学平衡状态的依据的是
A.2v(H2)正=3v(NH3)逆 B.2v(N2)正=v(H2)逆
C.容器内压强保持不变 D.混合气体的密度保持不变
(4)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。盐酸肼第一步水解反应的离子方程式
盐酸肼水溶液中离子浓度的排列顺序正确的是
a.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
b.c(Cl-)>c([N2H5•H2O]+)>c(H+)>c(OH-)
c.2c(N2H62+)+c([N2H5•H2O]+)+c(H+)=c(Cl-)+c(OH-)
d.2c(N2H62+)+2c([N2H5•H2O]+)+2c([N2H4•2H2O]=c(Cl-)
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
【推荐2】工业上常用微生物法、吸收法、电解法、还原法等消除硫、氮等引起的污染。
(1)微生物法脱硫
富含有机物的弱酸性废水在SBR细菌作用下产生 、
、 等物质,可将废水中
等物质,可将废水中 还原为
还原为 ,同时用
,同时用 或
或 将
将 从水中吹出,再用碱液吸收。
从水中吹出,再用碱液吸收。
① 的空间构型为
的空间构型为_______ 。
② 与
与 在SBR细菌作用下生成
在SBR细菌作用下生成 和
和 的离子方程式为
的离子方程式为_______ 。
③将 从水中吹出时,用
从水中吹出时,用 比
比 效果更好,其原因是
效果更好,其原因是_______ 。
(2)吸收法脱硫
烟气中的 可以用“亚硫酸铵吸收法”处理,发生的反应为
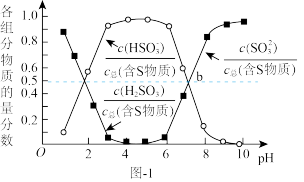
可以用“亚硫酸铵吸收法”处理,发生的反应为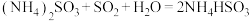 ,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液
,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液 ,则
,则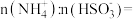
_______ 。
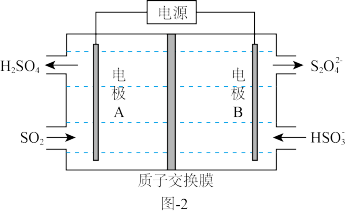
(3)电解法脱硫
用NaOH吸收后 ,所得
,所得 溶液经电解后可制取
溶液经电解后可制取 溶液,反应装置如图-2所示。电解时每有1 mol
溶液,反应装置如图-2所示。电解时每有1 mol  生成有
生成有_______ mol  透过质子交换膜。
透过质子交换膜。
(4)还原法脱氮
用催化剂协同纳米零价铁去除水体中 。其催化还原反应的过程如图-3所示。
。其催化还原反应的过程如图-3所示。
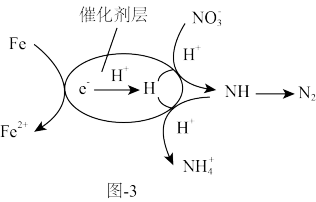
①该反应机理中生成 的过程可描述为
的过程可描述为_______ 。
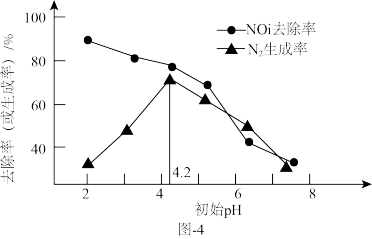
②过程中 去除率及
去除率及 生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当
生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当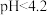 时,随pH减小,
时,随pH减小, 生成率逐渐降低的原因是
生成率逐渐降低的原因是_______ 。
(1)微生物法脱硫
富含有机物的弱酸性废水在SBR细菌作用下产生
 、
、 等物质,可将废水中
等物质,可将废水中 还原为
还原为 ,同时用
,同时用 或
或 将
将 从水中吹出,再用碱液吸收。
从水中吹出,再用碱液吸收。①
 的空间构型为
的空间构型为②
 与
与 在SBR细菌作用下生成
在SBR细菌作用下生成 和
和 的离子方程式为
的离子方程式为③将
 从水中吹出时,用
从水中吹出时,用 比
比 效果更好,其原因是
效果更好,其原因是(2)吸收法脱硫
烟气中的
 可以用“亚硫酸铵吸收法”处理,发生的反应为
可以用“亚硫酸铵吸收法”处理,发生的反应为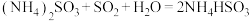 ,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液
,测得25℃时溶液pH与各组分物质的量分数的变化关系如图-1所示。b点时溶液 ,则
,则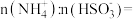

(3)电解法脱硫
用NaOH吸收后
 ,所得
,所得 溶液经电解后可制取
溶液经电解后可制取 溶液,反应装置如图-2所示。电解时每有1 mol
溶液,反应装置如图-2所示。电解时每有1 mol  生成有
生成有 透过质子交换膜。
透过质子交换膜。
(4)还原法脱氮
用催化剂协同纳米零价铁去除水体中
 。其催化还原反应的过程如图-3所示。
。其催化还原反应的过程如图-3所示。
①该反应机理中生成
 的过程可描述为
的过程可描述为②过程中
 去除率及
去除率及 生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当
生成率如图-4所示,为有效降低水体中氮元素的含量,宜调整水体pH为4.2,当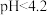 时,随pH减小,
时,随pH减小, 生成率逐渐降低的原因是
生成率逐渐降低的原因是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】痛风是以关节炎反复发作及产生肾结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:① ,②
,②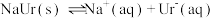 。已知:37℃时,
。已知:37℃时,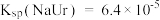 。
。
(1)关节炎发作大多在脚趾和手指的关节处,夏天症状减轻,冬天症状加重,说明反应②是
(2)下列事实可以证明尿酸是弱电解质的是___________
| A.HUr溶液可使石蕊溶液变红 | B.NaUr溶液显碱性 |
| C.常温下,等体积的尿酸溶液导电性比盐酸弱 | D.室温下测10mL0.01mol·L—1HUr溶液pH>2 |
A.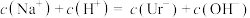 | B.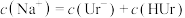 |
C.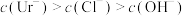 | D.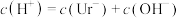 |
 。当向其中加入NaCl(s)至
。当向其中加入NaCl(s)至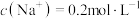 时,NaUr晶体
时,NaUr晶体
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
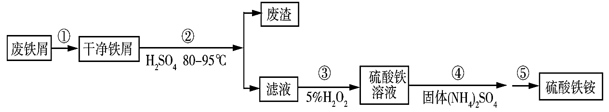
【推荐1】硫酸铁铵[NH4Fe(SO4)2·xH2O]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:
(1)步骤①的目的是去除废铁屑表面的油污,方法是_________________ 。
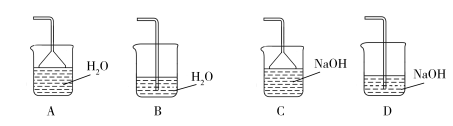
(2)步骤②需要加热的目的是_________________ ,温度保持80~95 ℃,采用的合适加热方式是_________________ 。铁屑中含有少量硫化物,反应产生的气体需要净化处理,合适的装置为_________________ (填标号)。_________________ 。分批加入H2O2,同时为了_________________ ,溶液要保持pH小于0.5。
(4)步骤⑤的具体实验操作有______________ ,经干燥得到硫酸铁铵晶体样品。
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为______________ 。
(1)步骤①的目的是去除废铁屑表面的油污,方法是
(2)步骤②需要加热的目的是
(4)步骤⑤的具体实验操作有
(5)采用热重分析法测定硫酸铁铵晶体样品所含结晶水数,将样品加热到150 ℃时,失掉1.5个结晶水,失重5.6%。硫酸铁铵晶体的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】五氧化二钒(V2O5)在工业生产中常用作催化剂,工业上常以黏土钒矿(钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4)原料制备V2O5,工艺流程如下:
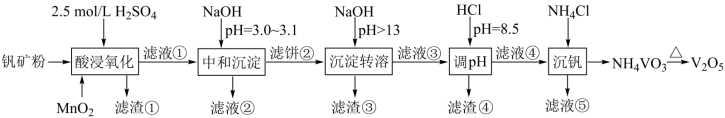
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)“酸浸氧化”中,VO+和VO2+被氧化成 ,同时还有
,同时还有_______ 离子被氧化。写出VO2+转化为 反应的离子方程式
反应的离子方程式_______ 。
(2)“中和沉淀”中,钒水解并沉淀为V2O5·x H2O进入滤饼②,滤饼②中还存在的成分_______ (填化学式)。
(3)“沉淀转溶”中,写出V2O5·x H2O转化为钒酸盐溶解的化学方程式_______ 。溶液③中存在的阴离子除 和OH-外,还存在
和OH-外,还存在_______ 。
(4)我国学者发明的低压高效电催化还原CO2为CO的新方法,用到滤液⑤中的主要溶质,并获得一种家用消毒剂,反应的化学方程式为:_______ 。
(5)接触法制硫酸中,V2O5参与反应的原理如图所示。下列说法正确的是_______ 。
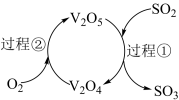
A.该过程中,V2O5和V2O4均为反应的催化剂
B.每转移2mol电子时,过程②中生成1mol V2O5
C.过程①每有1 mol V2O5参与反应,可氧化22.4L SO2
D.整个过程可看作催化剂中氧原子的传递过程

该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 | Fe3+ | Fe2+ | Al3+ | Mn2+ |
开始沉淀pH | 1.9 | 7.0 | 3.0 | 8.1 |
完全沉淀pH | 3.2 | 9.0 | 4.7 | 10.1 |
(1)“酸浸氧化”中,VO+和VO2+被氧化成
 ,同时还有
,同时还有 反应的离子方程式
反应的离子方程式(2)“中和沉淀”中,钒水解并沉淀为V2O5·x H2O进入滤饼②,滤饼②中还存在的成分
(3)“沉淀转溶”中,写出V2O5·x H2O转化为钒酸盐溶解的化学方程式
 和OH-外,还存在
和OH-外,还存在(4)我国学者发明的低压高效电催化还原CO2为CO的新方法,用到滤液⑤中的主要溶质,并获得一种家用消毒剂,反应的化学方程式为:
(5)接触法制硫酸中,V2O5参与反应的原理如图所示。下列说法正确的是

A.该过程中,V2O5和V2O4均为反应的催化剂
B.每转移2mol电子时,过程②中生成1mol V2O5
C.过程①每有1 mol V2O5参与反应,可氧化22.4L SO2
D.整个过程可看作催化剂中氧原子的传递过程
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】高铁酸钾( )是一种高效、无毒的强氧化剂。在工业上,一种通过
)是一种高效、无毒的强氧化剂。在工业上,一种通过 溶液制备
溶液制备 的工艺流程如图所示。回答下列问题:
的工艺流程如图所示。回答下列问题:

(1) 中Fe元素的化合价为
中Fe元素的化合价为______ 价,NaOH的电子式为______ 。
(2)“氧化、沉淀”时,氧化剂和还原剂的物质的量之比为______ 。Fe2+在溶液中放置不稳定,易被氧化成Fe3+,用KSCN溶液检验溶液中的Fe3+是较好的方法,此法的离子方程式为______ 。
(3)通过“氧化”时发生的反应可知,在该条件下物质氧化性:
______ NaClO(填“>”或“<”)。
(4)“转化”时,发生反应的化学方程式为______ ,说明物质的溶解度
______ (填“>”或“<”) 。
。
 )是一种高效、无毒的强氧化剂。在工业上,一种通过
)是一种高效、无毒的强氧化剂。在工业上,一种通过 溶液制备
溶液制备 的工艺流程如图所示。回答下列问题:
的工艺流程如图所示。回答下列问题:
(1)
 中Fe元素的化合价为
中Fe元素的化合价为(2)“氧化、沉淀”时,氧化剂和还原剂的物质的量之比为
(3)通过“氧化”时发生的反应可知,在该条件下物质氧化性:

(4)“转化”时,发生反应的化学方程式为

 。
。
您最近一年使用:0次



