下列实验操作、现象、解释或结论都正确且有因果关系的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向2mL0.1mol/LAgNO3溶液中滴加5mL0.1mol/LNaCl溶液,再滴加5滴0.1mol/LKI溶液 | 先生成白色沉淀,后又产生黄色沉淀 | 该温度下,溶度积:Ksp(AgCl)>Ksp(AgI) |
| B | 常温下用pH试纸分别测定1mol/LCH3COONH4溶液和0.1mol/LCH3COONH4溶液的pH | pH都约等于7 | 常温下,不同浓度的CH3COONH4溶液中水的电离程度相同 |
| C | 用Pt电极电解等物质的量浓度的Fe(NO3)3和Cu(NO3)2的混合溶液 | 阴极有红色固体物质析出 | 金属活动性:Cu>Fe |
| D | 向5mL0.1mol/LFeCl3溶液中滴加2mL0.1mol/LKI溶液,充分反应后,再滴入2滴KSCN溶液 | 溶液变红 | KI与FeCl3的反应为可逆反应。 |
| A.A | B.B | C.C | D.D |
更新时间:2022-04-27 21:57:51
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】25℃时,0.2mol·L-1的HX溶液中c(HX):c(X-)=99:1,下列说法正确的是
| A.升温至30℃时,溶液c(HX):c(X-)=99:1 |
| B.25℃时,K(HX)≈2×10-5 |
| C.向溶液中加入适量NaX固体,酸的电离平衡向左移动,达到新的平衡时c(X-)减小 |
| D.加水稀释后,溶液中c(X-)、c(H+)、c(OH-)均减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的数值,下列说法正确的是
A.常温常压下,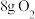 所含的电子数为4NA 所含的电子数为4NA |
B.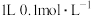 氨水中所含的 氨水中所含的 数为NA 数为NA |
| C.标准状况下,22.4L盐酸中所含的HCl分子数为NA |
D.1mol Na被完全氧化生成 ,失去的电子数为2NA ,失去的电子数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】由菱锰矿(MnCO3,含有少量Si、Fe、Ni、Al等元素)制备锂电池正极材料LiMn2O4的流程如下:

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。下列说法错误的是

已知:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.3×10-33,Ksp[Ni(OH)2]=5.5×10-16。下列说法错误的是
| A.上述流程中有三种元素被氧化 |
| B.从利用率考虑“反应器”中不宜使用H2O2替代MnO2 |
| C.溶矿反应完成后,“反应器”中溶液pH=4,则Fe3+和Al3+都沉淀完全 |
| D.加入少量BaS溶液以除去Ni2+,“滤渣”的成分至少有四种 |
您最近一年使用:0次
单选题
|
适中
(0.65)
真题
【推荐2】草酸( )是二元弱酸。某小组做如下两组实验:
)是二元弱酸。某小组做如下两组实验:
实验I:往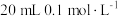
 溶液中滴加
溶液中滴加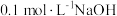 溶液。
溶液。
实验Ⅱ:往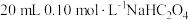 溶液中滴加
溶液中滴加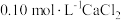 溶液。
溶液。
[已知: 的电离常数
的电离常数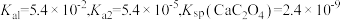 ,溶液混合后体积变化忽略不计],下列说法正确的是
,溶液混合后体积变化忽略不计],下列说法正确的是
 )是二元弱酸。某小组做如下两组实验:
)是二元弱酸。某小组做如下两组实验:实验I:往
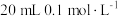
 溶液中滴加
溶液中滴加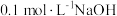 溶液。
溶液。实验Ⅱ:往
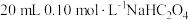 溶液中滴加
溶液中滴加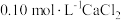 溶液。
溶液。[已知:
 的电离常数
的电离常数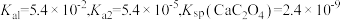 ,溶液混合后体积变化忽略不计],下列说法正确的是
,溶液混合后体积变化忽略不计],下列说法正确的是| A.实验I可选用甲基橙作指示剂,指示反应终点 |
B.实验I中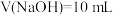 时,存在 时,存在 |
C.实验Ⅱ中发生反应 |
D.实验Ⅱ中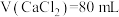 时,溶液中 时,溶液中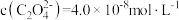 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】如图,石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质。图示装置工作时,生成的金属钙能还原二氧化钛制备金属钛。下列说法不正确的是
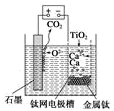

| A.阳极反应式为C+2O2--4e-=CO2↑ |
| B.由TiO2制得1mol金属Ti理论上外电路转移4mol电子 |
| C.制备金属钛前后,装置中CaO的量不变 |
| D.TiO2在阴极放电 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】 是阿伏加德罗常数的值,下列说法不正确的是
是阿伏加德罗常数的值,下列说法不正确的是
 是阿伏加德罗常数的值,下列说法不正确的是
是阿伏加德罗常数的值,下列说法不正确的是A. 中 中 键的个数为 键的个数为 |
B. 碘蒸气和 碘蒸气和 氢气在密闭容器中充分反应,生成的碘化氢分子数小于 氢气在密闭容器中充分反应,生成的碘化氢分子数小于 |
C.电解饱和食盐水时,若阴阳两极产生气体的总质量为 ,则转移电子数为 ,则转移电子数为 |
D.向 溶液中通入氨气至中性,铵根离子数小于 溶液中通入氨气至中性,铵根离子数小于 |
您最近一年使用:0次

 的盐酸,溶液的pH与所加盐酸体积的关系如图所示。下列说法错误的是
的盐酸,溶液的pH与所加盐酸体积的关系如图所示。下列说法错误的是





 方法的示意图如下:T℃时一定量的
方法的示意图如下:T℃时一定量的 溶液吸收后进入再生塔再生,最后利用电化学原理将
溶液吸收后进入再生塔再生,最后利用电化学原理将 (该温度下
(该温度下 的
的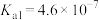 ,
, )。下列有关说法错误的是
)。下列有关说法错误的是
 ,则该溶液的
,则该溶液的
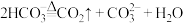
 溶液等体积混合,所得溶液中离子浓度大小为:
溶液等体积混合,所得溶液中离子浓度大小为:
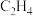 的阴极反应式为
的阴极反应式为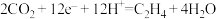 和
和


