一定温度下,在容积为VL的密闭容器中进行反应,M、N两种气体的物质的量随时间的变化曲线如图所示:
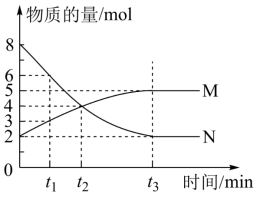
(1)该反应的化学反应方程式是_______ ;
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:_______ ;
(3)若达到平衡状态的时间是4min,N物质在该4min内的平均反应速率为1.5mol·L−1·min−1,则此容器的容积为V=_______ L;
(4)反应A(g)+B(g) 2C(g),当改变下列条件时,会加快反应速率的是
2C(g),当改变下列条件时,会加快反应速率的是_______ (填序号)
①降低温度
②保持容器的体积不变,充入氦气
③加入催化剂
④保持容器的体积不变,增加A(g)的物质的量
(5)用 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
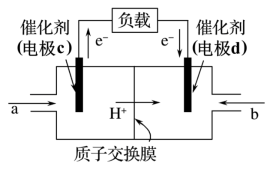
①电极d是_______ (填“正极”或“负极”);能量转化形式_______ 。
②若线路中转移2mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。

(1)该反应的化学反应方程式是
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:
(3)若达到平衡状态的时间是4min,N物质在该4min内的平均反应速率为1.5mol·L−1·min−1,则此容器的容积为V=
(4)反应A(g)+B(g)
 2C(g),当改变下列条件时,会加快反应速率的是
2C(g),当改变下列条件时,会加快反应速率的是①降低温度
②保持容器的体积不变,充入氦气
③加入催化剂
④保持容器的体积不变,增加A(g)的物质的量
(5)用
 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
①电极d是
②若线路中转移2mol电子,则该燃料电池理论上消耗的
 在标准状况下的体积为
在标准状况下的体积为
更新时间:2022-04-29 20:19:36
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.合成氨是人类科学技术发展史上的一项重大成就,是化学和技术对社会发展与进步的巨大贡献之一,其反应原理为:
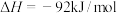 。
。
(1)已知下列数据:
则N-H键的键能是_______ kJ/mol。
(2)T℃时,在2L的密闭容器中发生上述合成氨反应,开始投入 和一定量的
和一定量的 ,体系中
,体系中 随时间的变化如下表:
随时间的变化如下表:
①用 表示从0~2min内该反应的平均速率
表示从0~2min内该反应的平均速率
_______ 。
②第4min时 的体积分数为
的体积分数为_______ 。(保留三位有效数字)
③下列叙述中能说明上述反应达到平衡状态的是_______ 。(用字母表示)
a.该条件下生成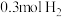 同时生成
同时生成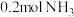
b.该条件下气体的平均相对分子质量保持不变
c.该条件下混合气体的密度保持不变
d.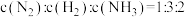
Ⅱ.如图所示的原电池装置,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,若两电极分别为Zn和石墨棒,则:

(3)X为_______ (填“Zn”或“石墨棒”)。
(4)Y上发生的电极反应为_______ 。
(5) 移向
移向_______ 电极(填“Zn”或“石墨棒”)。

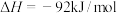 。
。(1)已知下列数据:
| 化学键 | H-H |  |
| 键能(kJ/mol) | 436 | 946 |
则N-H键的键能是
(2)T℃时,在2L的密闭容器中发生上述合成氨反应,开始投入
 和一定量的
和一定量的 ,体系中
,体系中 随时间的变化如下表:
随时间的变化如下表:| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
 的物质的量(mol) 的物质的量(mol) | 0.40 | 0.20 | 0.14 | 0.12 | 0.12 | 0.12 |
①用
 表示从0~2min内该反应的平均速率
表示从0~2min内该反应的平均速率
②第4min时
 的体积分数为
的体积分数为③下列叙述中能说明上述反应达到平衡状态的是
a.该条件下生成
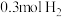 同时生成
同时生成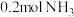
b.该条件下气体的平均相对分子质量保持不变
c.该条件下混合气体的密度保持不变
d.
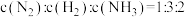
Ⅱ.如图所示的原电池装置,X、Y为两电极,电解质溶液为稀硫酸,外电路中的电子流向如图所示,若两电极分别为Zn和石墨棒,则:

(3)X为
(4)Y上发生的电极反应为
(5)
 移向
移向
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】碳一化学是指从一个碳原子的化合物(如CO、 等)出发合成各种化学品的技术。
等)出发合成各种化学品的技术。
(1)已知:830℃时,反应 的平衡常数为1.0,设起始时投入的
的平衡常数为1.0,设起始时投入的 、
、 均为
均为 ,恒容条件下,反应5min后达到平衡,则
,恒容条件下,反应5min后达到平衡,则 的转化率为
的转化率为___________ ,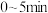 内,
内,
___________  。
。
(2)在带活塞的某容器中,将 和
和 按物质的量之比为
按物质的量之比为 投料,固定活塞使该容器体积为2L,发生反应
投料,固定活塞使该容器体积为2L,发生反应 ,当温度分别
,当温度分别 和
和 时,反应体系中
时,反应体系中 体积分数随时间变化如图。
体积分数随时间变化如图。
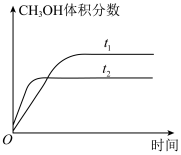
①上述反应的平衡常数的表达式为
___________ ;该反应的
___________ (填“>”、“=”或“<”)0。一定温度下,下列措施能提高 转化率的是
转化率的是___________ (填标号)。
A.增大 和
和 的投料比
的投料比
B.增大压强
C.升高温度
D.加入高效催化剂
②若某温度下,平衡时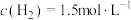 ,保持其他条件不变,移动活塞至该容器体积固定为1L,此时平衡常数
,保持其他条件不变,移动活塞至该容器体积固定为1L,此时平衡常数
___________ (填“增大”、“减小”或“不变”),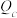
___________ (填“>”、“=”或“<”) ,达到新平衡时
,达到新平衡时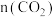
___________ (填“>”、“=”或“<”)1mol。
 等)出发合成各种化学品的技术。
等)出发合成各种化学品的技术。(1)已知:830℃时,反应
 的平衡常数为1.0,设起始时投入的
的平衡常数为1.0,设起始时投入的 、
、 均为
均为 ,恒容条件下,反应5min后达到平衡,则
,恒容条件下,反应5min后达到平衡,则 的转化率为
的转化率为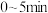 内,
内,
 。
。(2)在带活塞的某容器中,将
 和
和 按物质的量之比为
按物质的量之比为 投料,固定活塞使该容器体积为2L,发生反应
投料,固定活塞使该容器体积为2L,发生反应 ,当温度分别
,当温度分别 和
和 时,反应体系中
时,反应体系中 体积分数随时间变化如图。
体积分数随时间变化如图。
①上述反应的平衡常数的表达式为


 转化率的是
转化率的是A.增大
 和
和 的投料比
的投料比B.增大压强
C.升高温度
D.加入高效催化剂
②若某温度下,平衡时
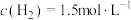 ,保持其他条件不变,移动活塞至该容器体积固定为1L,此时平衡常数
,保持其他条件不变,移动活塞至该容器体积固定为1L,此时平衡常数
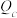
 ,达到新平衡时
,达到新平衡时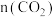
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】按要求回答下列问题:
Ⅰ.某温度时,在2L密闭容器中,加入气体A、B,经过一段时间后,气体A、B的物质的量随时间变化的曲线如图所示,回答下列问题:

(1)该反应的化学方程式为____ 。
(2)0~4min内,用A表示反应速率v(A)=____ mol/(L·min)。
(3)反应达平衡时容器内混合气体的平均相对分子质量比起始时____ (填“变大”、“变小”或“相等”)。
(4)下列措施能加快反应速率的是____ 。
Ⅱ.化学能与电能之间可以相互转化。
(5)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是____ 。
(6)氢氧燃料电池是符合绿色化学理念的新型发电装置。如图为电池示意图,该电池电极表面镀了一层细小的铂粉,铂吸附气体的能力强,性质稳定。请回答:

①电池的负极反应式为____ 。
②电池工作时OH-向____ 移动(填“正极”或“负极”)。
③正极上消耗4.48L(标准状况)气体时,转移电子的物质的量为____ 。
Ⅰ.某温度时,在2L密闭容器中,加入气体A、B,经过一段时间后,气体A、B的物质的量随时间变化的曲线如图所示,回答下列问题:

(1)该反应的化学方程式为
(2)0~4min内,用A表示反应速率v(A)=
(3)反应达平衡时容器内混合气体的平均相对分子质量比起始时
(4)下列措施能加快反应速率的是
| A.缩小体积,使压强增大 | B.恒温恒容充入氦气 |
| C.恒温恒压充入氦气 | D.使用催化剂 |
Ⅱ.化学能与电能之间可以相互转化。
(5)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是
| A.Ba(OH)2·8H2O与NH4Cl反应 | B.氢氧化钠与稀盐酸反应 |
| C.灼热的炭与CO2反应 | D.H2与Cl2燃烧反应 |

①电池的负极反应式为
②电池工作时OH-向
③正极上消耗4.48L(标准状况)气体时,转移电子的物质的量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】甲烷和二氧化碳都是温室气体。随着石油资源日益枯竭,储量丰富的甲烷(天然气、页岩气、可燃冰的主要成分)及二氧化碳的高效利用已成为科学研究的热点。回答下列问题:
(1)在催化剂作用下,将甲烷部分氧化制备合成气(CO和H2)的反应为CH4(g)+ O2(g) =CO(g)+2H2(g)。
O2(g) =CO(g)+2H2(g)。
①已知:25℃,101 kPa,由稳定单质生成1mol化合物的焓变称为该化合物的标准摩尔生成焓。化学反应的反应热ΔH=生成物的标准摩尔生成焓总和反应物的标准摩尔生成焓总和。相关数据如下表:
由此计算CH4(g)+ O2(g) =CO(g)+2H2(g)的∆H=
O2(g) =CO(g)+2H2(g)的∆H=___ kJ·mol-1。
②催化剂能显著提高上述反应的速率,但不能改变下列中的_____ (填标号)。
a.反应的活化能b.活化分子百分数c.化学平衡常数d.反应热(ΔH)
③T℃,向VL密闭容器中充入1 mol CH4和0.5 mol O2,在催化作用下发生上述反应,达到平衡时CO的物质的量为0.9 mol,CH4的平衡转化率为___ ;平衡常数K=____ (mol·L-1)1.5(列出计式即可)。
④欲提高甲烷的平衡转化率,可采取的两条措施是____ 。
(2)甲烷和二氧化碳催化重整制备合成气的反应为CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH>0。我国学者通过计算机模拟对该反应进行理论研究,提出在Pt-Ni合金或Sn-Ni合金催化下,以甲烷逐级脱氢开始反应。脱氢阶段的反应历程如图所示(*表示吸附在催化剂表面,吸附过程产生的能量称为吸附能)。

①该历程中最大能垒(活化能)E正=____ eV·mol-1;两种催化剂比较,脱氢反应阶段催化效果更好的是____ 合金。
②对于CH4*=C*+4H*,其它条件相同,Sn-Ni合金催化下的ΔE=6.357 eV·mol-1,Pt-Ni合金催化下的ΔE=-1.132 eV·mol-1,两者不相等的原因是_______ 。
(1)在催化剂作用下,将甲烷部分氧化制备合成气(CO和H2)的反应为CH4(g)+
 O2(g) =CO(g)+2H2(g)。
O2(g) =CO(g)+2H2(g)。 ①已知:25℃,101 kPa,由稳定单质生成1mol化合物的焓变称为该化合物的标准摩尔生成焓。化学反应的反应热ΔH=生成物的标准摩尔生成焓总和反应物的标准摩尔生成焓总和。相关数据如下表:
| 物质 | CH4 | O2 | CO | H2 |
| 标准摩尔生成焓/kJ∙mol-1 | -74.8 | 0 | -110.5 | 0 |
 O2(g) =CO(g)+2H2(g)的∆H=
O2(g) =CO(g)+2H2(g)的∆H=②催化剂能显著提高上述反应的速率,但不能改变下列中的
a.反应的活化能b.活化分子百分数c.化学平衡常数d.反应热(ΔH)
③T℃,向VL密闭容器中充入1 mol CH4和0.5 mol O2,在催化作用下发生上述反应,达到平衡时CO的物质的量为0.9 mol,CH4的平衡转化率为
④欲提高甲烷的平衡转化率,可采取的两条措施是
(2)甲烷和二氧化碳催化重整制备合成气的反应为CH4(g)+CO2(g)=2CO(g)+2H2(g) ΔH>0。我国学者通过计算机模拟对该反应进行理论研究,提出在Pt-Ni合金或Sn-Ni合金催化下,以甲烷逐级脱氢开始反应。脱氢阶段的反应历程如图所示(*表示吸附在催化剂表面,吸附过程产生的能量称为吸附能)。

①该历程中最大能垒(活化能)E正=
②对于CH4*=C*+4H*,其它条件相同,Sn-Ni合金催化下的ΔE=6.357 eV·mol-1,Pt-Ni合金催化下的ΔE=-1.132 eV·mol-1,两者不相等的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】一定条件下,在体积为5 L的密闭容器中,A、B、C三种气体的物质的量n(mol)随时间t(min)的变化如图1所示。已知达平衡后,降低温度,A的体积分数将减小。

(1)该反应的化学方程式为_____________ ,此反应平衡常数的表达式为K=________ 。
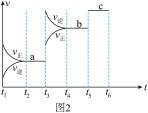
(2)该反应的反应速率v随时间t的关系如图2所示:
①根据图2判断,在t3时刻改变的外界条件是________ ,该反应的△H________ 0。(填“ ”、“
”、“ ”或“=”)
”或“=”)
②a、b、c三点中,C的体积分数最大的是________ 。
③各阶段的平衡常数如下表所示:
K1、K2、K3之间的关系为_______ (用“ ”、“
”、“ ”或“=”连接)。
”或“=”连接)。


(1)该反应的化学方程式为
(2)该反应的反应速率v随时间t的关系如图2所示:
①根据图2判断,在t3时刻改变的外界条件是
 ”、“
”、“ ”或“=”)
”或“=”)②a、b、c三点中,C的体积分数最大的是
③各阶段的平衡常数如下表所示:
| t2~t3 | t4~t5 | t5~t6 |
| K1 | K2 | K3 |
 ”、“
”、“ ”或“=”连接)。
”或“=”连接)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】从银精矿(其化学成分有Ag、Zn、Cu、Pb、S及SiO2)中提取银、铜和铅的工艺流程如图所示。

(1)步骤①中当盐酸的浓度和KClO3的量一定时,写出两点可提高浸取率的措施:___________ ;步骤②中试剂X为___________ (填化学式)。
(2)步骤③中Na2SO3的作用___________ (填序号)
a.氧化剂 b.还原剂 c.提供 溶解沉淀 d.水解以提供碱性环境
溶解沉淀 d.水解以提供碱性环境
(3)步骤④滤渣中主要含有两种杂质。为了回收其中有经济效益的非金属单质,某实验小组选择合理试剂,设计实验流程如下,补充完善___________ 。(已知该单质在碱性溶液中易歧化)

(4)步骤⑤中反应的离子方程式为___________ ;
(5)粗银可用立式电解精炼。纯银作阴极,电解液采用硝酸和硝酸银的混合溶液。硝酸浓度不能过大,可能的原因是___________ ;(答1点)
(6)电解精炼的废水中含有 ,任意排放会造成水体污染。科技人员在碱性条件下用Al粉将
,任意排放会造成水体污染。科技人员在碱性条件下用Al粉将 还原成无污染气体排放,离子方程式为:
还原成无污染气体排放,离子方程式为:___________ ;已知25℃,当调节溶液pH=7时,可以将 的浓度降到1.0×10-6 mol/L,求反应Al(OH)3 + OH-⇌
的浓度降到1.0×10-6 mol/L,求反应Al(OH)3 + OH-⇌  +2 H2O的K值
+2 H2O的K值___________ 。

(1)步骤①中当盐酸的浓度和KClO3的量一定时,写出两点可提高浸取率的措施:
(2)步骤③中Na2SO3的作用
a.氧化剂 b.还原剂 c.提供
 溶解沉淀 d.水解以提供碱性环境
溶解沉淀 d.水解以提供碱性环境(3)步骤④滤渣中主要含有两种杂质。为了回收其中有经济效益的非金属单质,某实验小组选择合理试剂,设计实验流程如下,补充完善

(4)步骤⑤中反应的离子方程式为
(5)粗银可用立式电解精炼。纯银作阴极,电解液采用硝酸和硝酸银的混合溶液。硝酸浓度不能过大,可能的原因是
(6)电解精炼的废水中含有
 ,任意排放会造成水体污染。科技人员在碱性条件下用Al粉将
,任意排放会造成水体污染。科技人员在碱性条件下用Al粉将 还原成无污染气体排放,离子方程式为:
还原成无污染气体排放,离子方程式为: 的浓度降到1.0×10-6 mol/L,求反应Al(OH)3 + OH-⇌
的浓度降到1.0×10-6 mol/L,求反应Al(OH)3 + OH-⇌  +2 H2O的K值
+2 H2O的K值
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示某小组为研究电化学原理,设计如图所示装置。根据原电池原理回答下列问题:

(1)若a和b不连接时,铁片上发生的反应为_______ 。
(2)①若a和b用导线连接时,_______ (填“Cu”或“Fe”)作负极,负极发生的电极反应为_______ ,溶液中SO 离子向
离子向_______ 极移动(填“Cu”或“Fe”)。
②若起始时铁和铜的质量相等,硫酸铜溶液的体积为500mL,将a和b用导线连接。一段时间后,铁片和铜片质量相差1.2g,则导线中流过电子的物质的量为_______ mol(不考虑其他形式能量转化)。
(3)锂锰电池的体积小,性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。
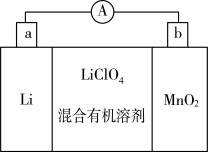
①电池正极反应式为_______ ,每转移2mol电子,生成_______ gLiMnO2。
②不能用水代替电池中的混合有机溶剂,原因是_______ 。
③MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,该反应的化学方程式为_______ 。

(1)若a和b不连接时,铁片上发生的反应为
(2)①若a和b用导线连接时,
 离子向
离子向②若起始时铁和铜的质量相等,硫酸铜溶液的体积为500mL,将a和b用导线连接。一段时间后,铁片和铜片质量相差1.2g,则导线中流过电子的物质的量为
(3)锂锰电池的体积小,性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。

①电池正极反应式为
②不能用水代替电池中的混合有机溶剂,原因是
③MnO2可与KOH和KClO3在高温下反应,生成K2MnO4,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氯、氮、硫等及其化合物性质研究。如图是氮、硫元素的各种价态与物质类别的对应关系:
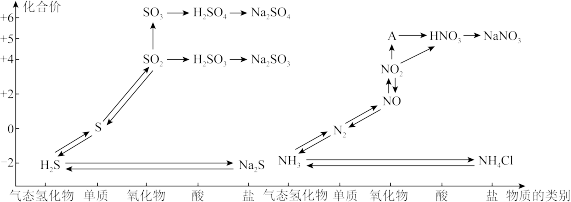
(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的离子方程式为____ 。
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,其中有一种产物是空气的主要成分,写出化学方程式____ 。
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl
b. NO+NO2+H2O 2HNO2
2HNO2
c.HClO+HNO2=HNO3+HCl
下列分析正确的是___ 。
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:
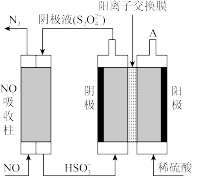
从A口中出来的物质的是____ 。写出电解池阴极的电极反应式____ 。
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
①上述实验中a=____ ,b=____ 。
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是____ (填实验编号)。
(4)氮及其化合物是重要的化工原料。含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
蛋白质 NH3
NH3 HNO2
HNO2 HNO3
HNO3 N2
N2
请回答:
①过程Ⅲ发生反应的化学方程式为____ 。
②根据图1和图2,判断使用亚硝化菌的最佳条件为_______ 。
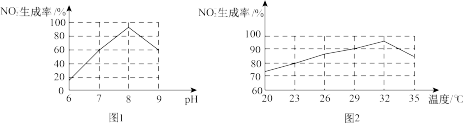
③利用微生物处理含氮废水的优点为_______ 。
(5)肼(N2H4)暴露在空气中容易爆炸,但利用其制作的燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等优点,其工作原理如图所示,写出该电池的正极反应式:_______ 。

(6)下图为制取氨气的装置和选用的试剂,其中错误的是_______ (填字母)。

A. ①② B. ②③ C. ③④ D. ①③
(7)实验室制备氨气的化学反应方程式是_______ ,为了得到干燥的NH3,可用_______ 做干燥剂。若有5.35g氯化铵参加反应,则产生的气体在标准状况下的体积为_______ L。
(8)铵盐受热易分解,如图所示。
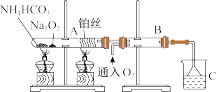
被加热的铂丝处发生反应的化学方程式为_______ 。

(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的离子方程式为
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,其中有一种产物是空气的主要成分,写出化学方程式
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl
b. NO+NO2+H2O
 2HNO2
2HNO2 c.HClO+HNO2=HNO3+HCl
下列分析正确的是
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:

从A口中出来的物质的是
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO
 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:| 实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | b | 124 |
| III | 350 | a | 5.80×10-3 | 82 |
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是
(4)氮及其化合物是重要的化工原料。含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
蛋白质
 NH3
NH3 HNO2
HNO2 HNO3
HNO3 N2
N2请回答:
①过程Ⅲ发生反应的化学方程式为
②根据图1和图2,判断使用亚硝化菌的最佳条件为
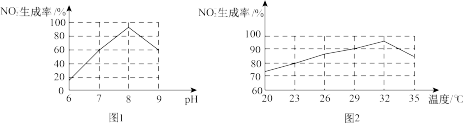
③利用微生物处理含氮废水的优点为
(5)肼(N2H4)暴露在空气中容易爆炸,但利用其制作的燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等优点,其工作原理如图所示,写出该电池的正极反应式:

(6)下图为制取氨气的装置和选用的试剂,其中错误的是

A. ①② B. ②③ C. ③④ D. ①③
(7)实验室制备氨气的化学反应方程式是
(8)铵盐受热易分解,如图所示。
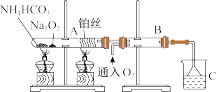
被加热的铂丝处发生反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】KMnO4常作氧化剂、防腐剂、消毒剂、漂白剂和水处理剂等。
(1)向K2MnO4溶液中通入足量CO2可制得KMnO4,副产物是黑色沉淀M。该反应中氧化剂与还原剂的质量之比为_____ 。在锂离子有机高聚物中锂与M构成原电池,消耗8.7 g M时转移 0.1 mol电子。该电池正极的电极反应式为_____________ 。
(2)实验室用KMnO4制备O2和Cl2。取0.4 mol KMnO4固体加热一段时间后,收集到a mol O2,在反应后的残留固体中加入足量浓盐酸,加热又收集到b mol Cl2。设锰元素全部转化成Mn2+存在于溶液中,当a+b=0.8时,在标准状况下生成Cl2的体积为____ L。
(3)电解K2MnO4溶液可以制备KMnO4。工业上,通常以软锰矿(主要成分是MnO2)与KOH的混合物在铁坩埚中混合均匀,小火加热至熔融,即可得到绿色的K2MnO4,该反应的化学方程式为____________ 。用镍片(不参与反应)作阳极,铁板作阴极,电解K2MnO4溶液可制备KMnO4。上述过程用流程图表示如下:

则D的化学式为____ ;阳极的电极反应式为___________ ;阳离子的迁移方向是____________ 。
(4)废液中c(Mn2+)较大时会污染水体。实验室可用过二硫酸铵[(NH4)2S2O8]溶液检验废水中的Mn2+,实验现象是溶液变紫红色(还原产物为 )。过二硫酸可以看成是H2O2的衍生物,过二硫酸铵中含有过氧键(—O—O—)。写出检验Mn2+时发生反应的离子方程式:
)。过二硫酸可以看成是H2O2的衍生物,过二硫酸铵中含有过氧键(—O—O—)。写出检验Mn2+时发生反应的离子方程式:____________ ;如果将这个反应设计成双液(或双桶)电池,盐桥中的溶液用____ (填“饱和KCl溶液”、“饱和K2SO4溶液”或“饱和NH4Cl溶液”)。
(1)向K2MnO4溶液中通入足量CO2可制得KMnO4,副产物是黑色沉淀M。该反应中氧化剂与还原剂的质量之比为
(2)实验室用KMnO4制备O2和Cl2。取0.4 mol KMnO4固体加热一段时间后,收集到a mol O2,在反应后的残留固体中加入足量浓盐酸,加热又收集到b mol Cl2。设锰元素全部转化成Mn2+存在于溶液中,当a+b=0.8时,在标准状况下生成Cl2的体积为
(3)电解K2MnO4溶液可以制备KMnO4。工业上,通常以软锰矿(主要成分是MnO2)与KOH的混合物在铁坩埚中混合均匀,小火加热至熔融,即可得到绿色的K2MnO4,该反应的化学方程式为

则D的化学式为
(4)废液中c(Mn2+)较大时会污染水体。实验室可用过二硫酸铵[(NH4)2S2O8]溶液检验废水中的Mn2+,实验现象是溶液变紫红色(还原产物为
 )。过二硫酸可以看成是H2O2的衍生物,过二硫酸铵中含有过氧键(—O—O—)。写出检验Mn2+时发生反应的离子方程式:
)。过二硫酸可以看成是H2O2的衍生物,过二硫酸铵中含有过氧键(—O—O—)。写出检验Mn2+时发生反应的离子方程式:
您最近一年使用:0次



