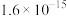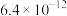三氯化铬(CrCl3)是常用的媒染剂和催化剂,易潮解,实验室利用重铬酸钠制备CrCl3·6H2O及其
相关产物的实验如下。回答相关问题:
[实验1]制备CrCl3·6H2O的实验流程如下。

(1)甲醛( HCHO)的作用为_______ ;“混合”时发生反应的化学方程式为_______ 。
(2)“一系列操作”的具体步骤包括_______ 、过滤。
[实验2]高温下氨气与无水CrCl3反应制备CrN。(夹持和加热仪器省略)
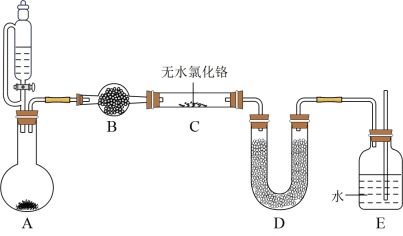
(3)仪器B的名称是_______ 。
(4)B中的试剂名称是_______ ,其作用为_______ 。
(5)处理尾气时,用E装置的优点是_______ 。
(6)整套装置的不足之处为_______ ,改进的措施是_______ 。
相关产物的实验如下。回答相关问题:
[实验1]制备CrCl3·6H2O的实验流程如下。

(1)甲醛( HCHO)的作用为
(2)“一系列操作”的具体步骤包括
[实验2]高温下氨气与无水CrCl3反应制备CrN。(夹持和加热仪器省略)

(3)仪器B的名称是
(4)B中的试剂名称是
(5)处理尾气时,用E装置的优点是
(6)整套装置的不足之处为
更新时间:2022-05-19 14:31:39
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】三氧乙醛( )是生产农药、医药的重要中间体,实验室可用无水乙醇和氯气制备三氯乙醛:
)是生产农药、医药的重要中间体,实验室可用无水乙醇和氯气制备三氯乙醛: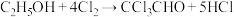 。反应装置示意图(加热装置未画出)和有关数据如下:
。反应装置示意图(加热装置未画出)和有关数据如下:
(1)恒压漏斗中所装的液体是_______ ,D中干燥管的作用是_______ 。
(2)E的具体名称是_______ ,冷凝水从_______ 口流入。(填“a”或“b”)
(3)反应时,装置C温度应保持在70℃左右,其原因是_______ 。(任答两点)
(4)已知 能被次氯酸氧化生成
能被次氯酸氧化生成 (三氯乙酸),所以该实验装置在设计流程中存在的一处明显缺陷是
(三氯乙酸),所以该实验装置在设计流程中存在的一处明显缺陷是_______ 。
(5)反应结束后,分离得到 的实验方法是应控制温度为
的实验方法是应控制温度为_______ 。
(6)某次实验用9.2g 进行实验,最终得到
进行实验,最终得到 20.0g,则产率为
20.0g,则产率为_______ %。(保留3位有效数字)
 )是生产农药、医药的重要中间体,实验室可用无水乙醇和氯气制备三氯乙醛:
)是生产农药、医药的重要中间体,实验室可用无水乙醇和氯气制备三氯乙醛: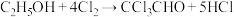 。反应装置示意图(加热装置未画出)和有关数据如下:
。反应装置示意图(加热装置未画出)和有关数据如下:| 物质 | 物质 | 相对分子质量 | 熔点/℃ | 沸点/℃ |
 | 46 | -114.1 | 78.3 | 与水互溶 |
 | 147.5 | -57.5 | 97.8 | 可溶于水、乙醇 |
 | 163.5 | 58 | 198 | 可溶于水、乙醇、三氯乙醛 |
 | 64.5 | -138.7 | 12.3 | 微溶于水,可溶于乙醇 |
(2)E的具体名称是
(3)反应时,装置C温度应保持在70℃左右,其原因是
(4)已知
 能被次氯酸氧化生成
能被次氯酸氧化生成 (三氯乙酸),所以该实验装置在设计流程中存在的一处明显缺陷是
(三氯乙酸),所以该实验装置在设计流程中存在的一处明显缺陷是(5)反应结束后,分离得到
 的实验方法是应控制温度为
的实验方法是应控制温度为(6)某次实验用9.2g
 进行实验,最终得到
进行实验,最终得到 20.0g,则产率为
20.0g,则产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某化学兴趣小组的同学在乙醛溶液中加入溴水,溴水褪色。分析乙醛的结构和性质,同学们认为溴水褪色的原因有三种可能(请补充完整):
(1)________________________________________________________________________ 。
为确定此反应的机理,同学们作了如下探究:
(2)向反应后的溶液中加入硝酸银溶液,若有沉淀产生,则上述第________ 种可能被排除。
(3)有同学提出通过检测反应后溶液的酸碱性作进一步验证,就可确定该反应究竟是何种反应原理。此方案是否可行?________ ,理由是_______________________ 。
(4)若反应物Br2与生成物Br-的物质的量之比是1∶2,则乙醛与溴水反应的化学方程式为___________ 。
(1)
为确定此反应的机理,同学们作了如下探究:
(2)向反应后的溶液中加入硝酸银溶液,若有沉淀产生,则上述第
(3)有同学提出通过检测反应后溶液的酸碱性作进一步验证,就可确定该反应究竟是何种反应原理。此方案是否可行?
(4)若反应物Br2与生成物Br-的物质的量之比是1∶2,则乙醛与溴水反应的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】由丙烯经下列反应可得到F和高分子化合物G,它们都是常用的塑料。
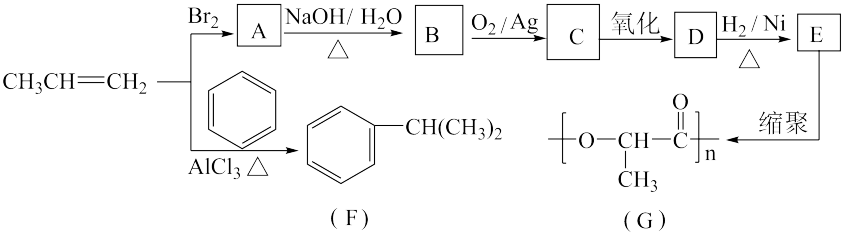
完成下列埴空:
(1)F的分子式为___________ ,E中含氧官能团的名称是 ___________ 。
(2)写出反应类型:丙烯直接形成高分子______ :A →B __________ 。
(3)B 转化为 C 的化学方程式为______________________________ 。
(4)E的一种同分异构体M具有如下性质:
①能发生银镜反应;②l molM与足量的金属钠反应可产生l molH2
则M的结构简式为______________________ 。
(5)写出由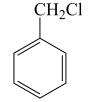 合成
合成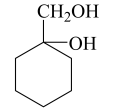
___________________ (合成路线常用表示方法为:X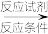 Y......
Y......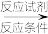 目标产物)
目标产物)

完成下列埴空:
(1)F的分子式为
(2)写出反应类型:丙烯直接形成高分子
(3)B 转化为 C 的化学方程式为
(4)E的一种同分异构体M具有如下性质:
①能发生银镜反应;②l molM与足量的金属钠反应可产生l molH2
则M的结构简式为
(5)写出由
 合成
合成
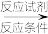 Y......
Y......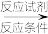 目标产物)
目标产物)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】以低品位铜钴矿(主要成分为 、
、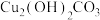 、
、 ,还有少量的FeO、
,还有少量的FeO、 、CaO、MgO等杂质)为原料制备硫酸铜晶体和
、CaO、MgO等杂质)为原料制备硫酸铜晶体和 的一种工艺流程如下:
的一种工艺流程如下:
②萃取时发生反应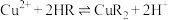
(1)铜钴矿浸出前要预先粉碎,其目的是______ 。
(2)浸出步骤铜钴矿中的 转化为
转化为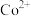 ,该反应的离子方程式为
,该反应的离子方程式为______ 。
(3)加入试剂a______ 可使萃取剂再生。
(4)对于过程I:
①加 溶液作用是
溶液作用是______ 。
②通过计算判断 是否沉淀完全并简述理由
是否沉淀完全并简述理由______ 。(一般认为溶液中离子浓度小于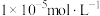 时沉淀完全)
时沉淀完全)
(5)滤渣1成分______ 。
(6) 在足量空气中煅烧生成
在足量空气中煅烧生成 ,写出煅烧过程中的化学反应方程式
,写出煅烧过程中的化学反应方程式______ 。
(7)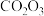 产品纯度测定方法如下:
产品纯度测定方法如下: 与EDTA-2Na按物质的量1:1反应,若滴定至终点时消耗EDTA-2Na标准液体积为20.00mL,则
与EDTA-2Na按物质的量1:1反应,若滴定至终点时消耗EDTA-2Na标准液体积为20.00mL,则 产品纯度为
产品纯度为______ 。( 的摩尔质量是
的摩尔质量是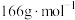 )
)
 、
、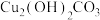 、
、 ,还有少量的FeO、
,还有少量的FeO、 、CaO、MgO等杂质)为原料制备硫酸铜晶体和
、CaO、MgO等杂质)为原料制备硫酸铜晶体和 的一种工艺流程如下:
的一种工艺流程如下: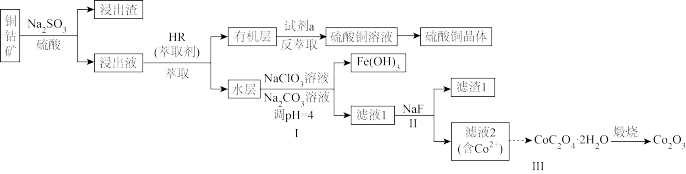
物质 |
|
|
|
|
|
|
|
|
|
|
|
|
|
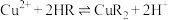
(1)铜钴矿浸出前要预先粉碎,其目的是
(2)浸出步骤铜钴矿中的
 转化为
转化为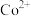 ,该反应的离子方程式为
,该反应的离子方程式为(3)加入试剂a
(4)对于过程I:
①加
 溶液作用是
溶液作用是②通过计算判断
 是否沉淀完全并简述理由
是否沉淀完全并简述理由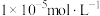 时沉淀完全)
时沉淀完全)(5)滤渣1成分
(6)
 在足量空气中煅烧生成
在足量空气中煅烧生成 ,写出煅烧过程中的化学反应方程式
,写出煅烧过程中的化学反应方程式(7)
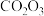 产品纯度测定方法如下:
产品纯度测定方法如下: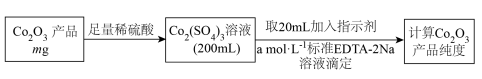
 与EDTA-2Na按物质的量1:1反应,若滴定至终点时消耗EDTA-2Na标准液体积为20.00mL,则
与EDTA-2Na按物质的量1:1反应,若滴定至终点时消耗EDTA-2Na标准液体积为20.00mL,则 产品纯度为
产品纯度为 的摩尔质量是
的摩尔质量是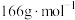 )
)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】黄铁矿石是制取硫酸的主要原料,主要成分为FeS2和少量FeS(假设其它杂质中不含铁、硫元素,且高温下不发生化学变化)。某化学兴趣小组对该黄铁矿石进行如下实验探究。将m1g该黄铁矿石的样品放入如图装置(夹持和加热装置略)的石英管中,从a处不断地缓缓通入空气,高温灼烧黄铁矿样品至反应完全。其反应的化学方程式为4FeS2+11O2=2Fe2O3+8SO2,4FeS+7O2=2Fe2O3+4SO2
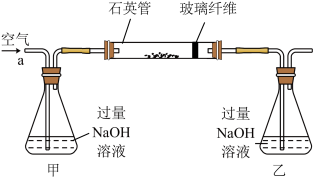
(1)鼓人空气的作用是___________ ,锥形瓶乙中NaOH溶液的作用是___________ 。
【实验一】测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:
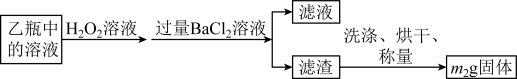
(2)反应结束后,给乙瓶溶液中加入足量H2O2溶液的目的是___________ (用化学方程式表示)。
(3)洗涤滤渣的方法是______________________ 。
(4)该黄铁矿石中硫元素的质量分数为___________ (列出表达式即可)。
【实验二】测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣;②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤;③将滤液稀释至250mL;④取25.00mL稀释液,用0.1000mol·L-1的酸性KMnO4溶液滴定,三次滴定实验,平均消耗酸性KMnO4溶液25.00mL。
(5)操作②中用铁粉作还原剂,测定铁的含量___________ (填“偏高”或“偏低”或“不变”),操作④中滴定时酸性KMnO4溶液盛装在___________ 填“酸式滴定管”或“碱式滴定管”),③中稀释液中Fe2+的物质的量浓度c(Fe2+)=___________ 。

(1)鼓人空气的作用是
【实验一】测定硫元素的含量
反应结束后,将乙瓶中的溶液进行如下处理:

(2)反应结束后,给乙瓶溶液中加入足量H2O2溶液的目的是
(3)洗涤滤渣的方法是
(4)该黄铁矿石中硫元素的质量分数为
【实验二】测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣;②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤;③将滤液稀释至250mL;④取25.00mL稀释液,用0.1000mol·L-1的酸性KMnO4溶液滴定,三次滴定实验,平均消耗酸性KMnO4溶液25.00mL。
(5)操作②中用铁粉作还原剂,测定铁的含量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】已知:FeC2O4∙nH2O加热至300℃完全失去结晶水,继续加热至400℃,剩余固体又变成黑色,黑色固体为铁的氧化物,同时生成气体,为确定分解产物及n的值,设计了如图所示实验,实验时先打开弹簧夹a、b,鼓入一段时间氮气,然后关闭a,加热热分解装置,资料:无水硫酸铜是白色固体,遇水变蓝;FeO和Fe3O4都是黑色固体。
【实验设计】
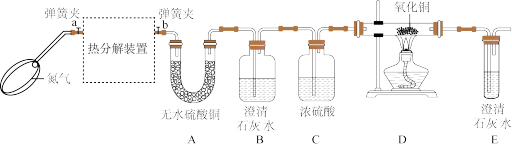
【实验分析】
(1)先鼓入氮气,再加热热分解装置的原因是_____________ 。
(2)实验过程中观察到:A中白色固体变蓝,证明产物有_____________ ;B中石灰水变浑浊,证明产物有CO2;D中_____________ (填实验现象),证明产物有CO。
(3)现测得装置D中硬质玻璃管固体质量减轻0.32g,则草酸亚铁晶体分解得到的CO的质量为_____________ 。
(4)上述实验装置不足之处是_____________ 。
(5)为进一步探究加热至400℃时固体产物的成分,另取1.80gFeC2O4·nH2O重新实验,测得热分解装置中固体质量随温度变化如图所示。
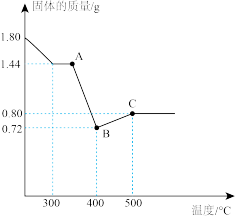
①FeC2O4·nH2O中n的值为_____________ ,若草酸亚铁晶体中混有杂质(杂质不参与反应),会导致测得的值_____________ (填“偏大”、“偏小”或“不变”)。
②AB段发生反应的化学方程式_____________ 。
③将B点物质在空气中继续加热至500℃得到C点物质,BC段发生反应的化学反应方程式为_____________ 。
【实验设计】

【实验分析】
(1)先鼓入氮气,再加热热分解装置的原因是
(2)实验过程中观察到:A中白色固体变蓝,证明产物有
(3)现测得装置D中硬质玻璃管固体质量减轻0.32g,则草酸亚铁晶体分解得到的CO的质量为
(4)上述实验装置不足之处是
(5)为进一步探究加热至400℃时固体产物的成分,另取1.80gFeC2O4·nH2O重新实验,测得热分解装置中固体质量随温度变化如图所示。

①FeC2O4·nH2O中n的值为
②AB段发生反应的化学方程式
③将B点物质在空气中继续加热至500℃得到C点物质,BC段发生反应的化学反应方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】硫酸亚铁在空气中易被氧化,与硫酸铵反应生成硫酸亚铁铵[化学式为FeSO4·(NH4)2SO4·6H2O]后就不易被氧化。模拟工业制备硫酸亚铁铵晶体的实验装置如下图所示。请回答下列问题:
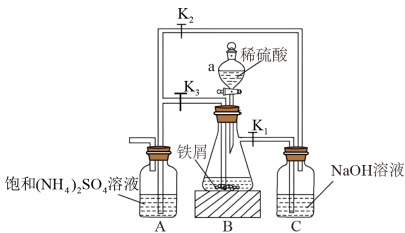
(1)仪器a的名称是______________________ 。
(2)铁屑中常含有Fe2O3、FeS等杂质,则装置C的作用是___________ ,装置B中发生反应的离子方程式可能是___________ (填序号)。
A. Fe+2H+=Fe2++H2↑
B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=2Fe2+
(3)按上图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中有气体产生,该气体的作用是___________ 。反应一段时间后,打开K3,关闭K1和K2。装置B中的溶液会流入装置A,其原因是______________________ 。
(4)按上图所示装置制备硫酸亚铁铵晶体的安全隐患是______________________ 。
(5)根据相关物质的溶解度判断,从装置A中分离出硫酸亚铁铵晶体,需采用的操作有___________ 、___________ 、洗涤、干燥。
三种盐的溶解度(单位为g/100gH2O)

(1)仪器a的名称是
(2)铁屑中常含有Fe2O3、FeS等杂质,则装置C的作用是
A. Fe+2H+=Fe2++H2↑
B.Fe2O3+6H+=2Fe3++3H2O
C.2Fe3++S2-=2Fe2++S↓
D.2Fe3++Fe=2Fe2+
(3)按上图连接好装置,经检验气密性良好后加入相应的药品,打开K1、K2,关闭K3,装置B中有气体产生,该气体的作用是
(4)按上图所示装置制备硫酸亚铁铵晶体的安全隐患是
(5)根据相关物质的溶解度判断,从装置A中分离出硫酸亚铁铵晶体,需采用的操作有
三种盐的溶解度(单位为g/100gH2O)
温度 | FeSO4 | (NH4)2SO4 | 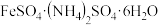 |
| 10 | 20.0 | 73 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78 | 28.1 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】乙酸正丁酯(CH3CH2CH2CH2OOCCH3)是一种优良的有机溶剂。实验室制备少量乙酸正丁酯的反应为CH3COOH+CH3CH2CH2CH2OH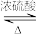 CH3CH2CH2CH2OOCCH3+H2O。
CH3CH2CH2CH2OOCCH3+H2O。
实验步骤如下:
步骤1:向仪器A中加入11.5 mL正丁醇(微溶于水)、1 mL浓H2SO4、7.2 mL冰醋酸及沸石少许。
步骤2:按如图连接装置。
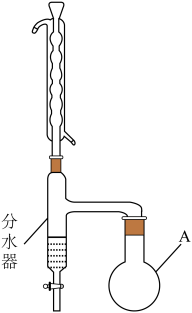
步骤3:向分水器中预先加少量水(略低于支管口)。通入冷却水,加热回流。
步骤4:将分水器分出的酯层和反应液合并转入分液漏斗中,依次用5% Na2CO3溶液、水洗涤,分离出有机相。
步骤5:将有机相用无水硫酸镁干燥、过滤、蒸馏,收集乙酸正丁酯。
(1)仪器A的名称是________ ;向其中加入碎瓷片的目的是________ 。
(2)装置中分水器的作用是________ ,判断反应已经完成的标志是________ 。
(3)反应时生成的主要有机副产物有丁醚和________ (用结构简式表示)。
(4)步骤4中,分离出有机相的具体操作是___________________ 。
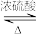 CH3CH2CH2CH2OOCCH3+H2O。
CH3CH2CH2CH2OOCCH3+H2O。实验步骤如下:
步骤1:向仪器A中加入11.5 mL正丁醇(微溶于水)、1 mL浓H2SO4、7.2 mL冰醋酸及沸石少许。
步骤2:按如图连接装置。

步骤3:向分水器中预先加少量水(略低于支管口)。通入冷却水,加热回流。
步骤4:将分水器分出的酯层和反应液合并转入分液漏斗中,依次用5% Na2CO3溶液、水洗涤,分离出有机相。
步骤5:将有机相用无水硫酸镁干燥、过滤、蒸馏,收集乙酸正丁酯。
(1)仪器A的名称是
(2)装置中分水器的作用是
(3)反应时生成的主要有机副产物有丁醚和
(4)步骤4中,分离出有机相的具体操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】乙酰乙酸乙酯是有机合成中非常重要的原料,实验室制备乙酰乙酸乙酯的反应原理、装置示意图和有关数据如下所示:
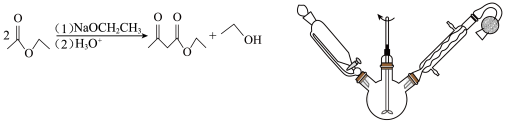
实验步骤:
Ⅰ.合成:向三颈烧瓶中加入9.8ml无水乙酸乙酯,迅速加入0.1g切细的金属钠。水浴加热反应液,缓慢回流约2h至金属钠全部反应完。停止加热,冷却后向反应混合物中加入50%乙酸至反应液呈弱酸性。
Ⅱ.分离与提纯:
①向反应混合物中加入等体积的饱和食盐水,分离得到有机层。
②水层用5mL无水乙酸乙酯萃取,分液。
③将①②所得有机层合并,洗涤、干燥、蒸馏得到乙酰乙酸乙酯粗产品。
④蒸馏粗产品得到乙酰乙酸乙酯3.9g。
(1)球形冷凝管中冷却水从______ (填“上”或“下”)口进入,上方干燥管中盛无水CaCl2,其作用是________ 。
(2)实验室制备乙酰乙酸乙酯时,通常在无水乙酸乙酯中加入微量的无水乙醇,其作用是___ 。
(3)分离与提纯操作①中使用的分离仪器是________ 。加入饱和食盐水的作用是 _______ 。
(4)分离与提纯操作③用饱和NaHCO3溶液洗涤的目的是_______ 。
(5)本实验的产率为_______ %(结果保留两位有效数字)。

| 密度/(g·cm-3) | 沸点/℃ | 水中 溶解性 | |
| 乙酸乙酯 | 0.90 | 77.2 | 难溶 |
| 乙酰乙酸乙酯 | 1.02 | 181 | 微溶 |
| 乙酸 | 1.05 | 118 | 易溶 |
Ⅰ.合成:向三颈烧瓶中加入9.8ml无水乙酸乙酯,迅速加入0.1g切细的金属钠。水浴加热反应液,缓慢回流约2h至金属钠全部反应完。停止加热,冷却后向反应混合物中加入50%乙酸至反应液呈弱酸性。
Ⅱ.分离与提纯:
①向反应混合物中加入等体积的饱和食盐水,分离得到有机层。
②水层用5mL无水乙酸乙酯萃取,分液。
③将①②所得有机层合并,洗涤、干燥、蒸馏得到乙酰乙酸乙酯粗产品。
④蒸馏粗产品得到乙酰乙酸乙酯3.9g。
(1)球形冷凝管中冷却水从
(2)实验室制备乙酰乙酸乙酯时,通常在无水乙酸乙酯中加入微量的无水乙醇,其作用是
(3)分离与提纯操作①中使用的分离仪器是
(4)分离与提纯操作③用饱和NaHCO3溶液洗涤的目的是
(5)本实验的产率为
您最近一年使用:0次