TIC、TiN、MnS、MnSe在电化学领域均有巨大的应用潜力。回答下列问题:
(1)基态Ti2+和Mn2+中未成对电子数之比为_______ ;N、S、Mn的第一电离能由大到小的顺序为_______ 。
(2)键能:H—S_______ H—Se(填“>”或“<"),理由为_______ 。
(3)C3N4的硬度可以和金刚石媲美,其中N原子的杂化方式为_______ 。
(4)SeO2的VSEPR模型为_______ 。
(5)H2S2O8是一种强氧化剂,可看作两个H2SO4分子通过形成过氧键结合而成。1molH2S2O8中σ键的数目为_______ 。
(6)MnSe具有NaCl型结构,其立方晶胞结构如图1所示。
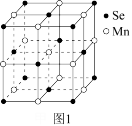
①MnSe晶体可以看成是由Se原子堆成的正八面体中空隙被Mn原子填充,填充率为_______ 。
②图2所示单元不是MnSe的晶胞单元,原因为_______ 。

③若阿伏加德罗常数的值为NA,晶体密度为ρg·cm-3,则该晶体中Se原子与Mn原子之间最短距离为_______ pm。
(1)基态Ti2+和Mn2+中未成对电子数之比为
(2)键能:H—S
(3)C3N4的硬度可以和金刚石媲美,其中N原子的杂化方式为
(4)SeO2的VSEPR模型为
(5)H2S2O8是一种强氧化剂,可看作两个H2SO4分子通过形成过氧键结合而成。1molH2S2O8中σ键的数目为
(6)MnSe具有NaCl型结构,其立方晶胞结构如图1所示。

①MnSe晶体可以看成是由Se原子堆成的正八面体中空隙被Mn原子填充,填充率为
②图2所示单元不是MnSe的晶胞单元,原因为

③若阿伏加德罗常数的值为NA,晶体密度为ρg·cm-3,则该晶体中Se原子与Mn原子之间最短距离为
更新时间:2022-06-13 16:28:01
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+ 原子核外有3层电子且M层3d轨道电子全充满。请回答:
(1)E元素基态原子的电子排布式为_________ 。
(2)B、C、D三种元素的第一电离能数值由小到大 的顺序为____ (填元素符号)
(3)D元素与氟元素相比,电负性:D______ F(填“>”、“=”或“<”),下列表述中能证明这一事实的是_______ (填选项序号)
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物,其电子式为______ ,它的晶体中含有多种化学键,但一定不含有的化学键是______ (填选项序号)。
A.极性键 B.非极性键 C.离子键 D.金属键
(5)B2A4是重要的基本石油化工原料。lmolB2A4分子中含 键
键______ mol。
(1)E元素基态原子的电子排布式为
(2)B、C、D三种元素的第一电离能数值由
(3)D元素与氟元素相比,电负性:D
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)只含C、A两元素的离子化合物,其电子式为
A.极性键 B.非极性键 C.离子键 D.金属键
(5)B2A4是重要的基本石油化工原料。lmolB2A4分子中含
 键
键
您最近一年使用:0次
【推荐2】原子序数小于等于36的Q、W、X、Y、Z五种元素,其中Q是原子半径最小的元素,W和Y的基态原子2p能级所含成单电子数均为2,Z的基态原子核外含有13种运动状态不同的电子。回答下列问题(涉及元素时用对应的元素符号表示):
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是_______ 。
(2) 与
与 所含
所含 键的比值为
键的比值为_______ 。
(3)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为_______ 。

(4)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为:_______ 。
②预测该化合物熔点应_______ 金刚石(填“高于”或“低于”)。
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是
(2)
 与
与 所含
所含 键的比值为
键的比值为(3)一种由X和Z两种元素形成化合物的晶胞如图所示,该晶胞的化学式为

(4)实验室合成一种由W和X两种元素形成的化合物,该化合物具有空间网状结构,其中每个W原子与4个X原子形成共价键,每个X原子与3个W原子形成共价键。
①该化合物的化学式为:
②预测该化合物熔点应
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、F、G是前四周期元素,原子序数依次增大,根据表中提供的有关信息,回答问题:
(1)E元素在周期表中的位置是______ ,F元素原子最外层电子排布式为______ ,BD2的立体构型为______ 。
(2)由D、E、F三种元素形成的一种常见物质的水溶液显碱性,用离子方程式表示其显碱性的原因:______ 。
(3)氢化物稳定性:B______ D;最高价氧化物对应的水化物酸性:C______ F。(填“<”或“>”)
(4)每个B2A4分子中含有______ 个σ键,______ 个π键。
| 元素 | 相关信息 |
| A | 所有单质中密度最小 |
| B | 形成化合物种类最多的元素 |
| D | 基态原子中只有3个能级,有2个未成对电子 |
| E | 短周期中原子半径最大 |
| F | 第三周期中电负性最大的元素 |
| G | 最外层只有一个电子,内层填满电子 |
(2)由D、E、F三种元素形成的一种常见物质的水溶液显碱性,用离子方程式表示其显碱性的原因:
(3)氢化物稳定性:B
(4)每个B2A4分子中含有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体类型为______ ,晶体中原子间通过_____ 作用形成面心立方密堆积,其中M原子的配位数为______ 。
(2)元素Y基态原子的核外电子排布式为________ ,其同周期元素中,第一电离能最大的是______ (写元素符号)。元素Y的含氧酸中,酸性最强的是________ (写化学式),该酸根离子的立体构型为________ 。
(3)M与Y形成的一种化合物的立方晶胞如图所示。
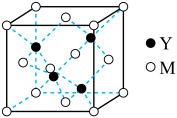
①该化合物的化学式为_______ ,已知晶胞参数a=0.542 nm,此晶体的密度为_______ g·cm–3。(写出计算式,不要求计算结果。阿伏加德罗常数为NA)
②该化合物难溶于水但易溶于氨水,其原因是________ 。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______ 。
(1)单质M的晶体类型为
(2)元素Y基态原子的核外电子排布式为
(3)M与Y形成的一种化合物的立方晶胞如图所示。

①该化合物的化学式为
②该化合物难溶于水但易溶于氨水,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
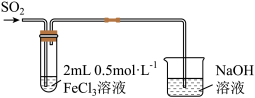
【推荐2】某小组探究 与
与 溶液的反应。
溶液的反应。
(1)小组同学预测向 溶液中通入
溶液中通入 ,溶液颜色将由黄色变为浅绿色,预测的依据是
,溶液颜色将由黄色变为浅绿色,预测的依据是___ 。
进行实验
资料: 与
与 可以发生可逆反应,形成红棕色的配离子
可以发生可逆反应,形成红棕色的配离子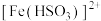 。
。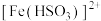 可以将
可以将 还原为
还原为 。
。
(2) 的空间结构是
的空间结构是__________ ,Fe在周期表中属于______________ 区。
(3) 与
与 可以形成配离子的原因是
可以形成配离子的原因是______________________ 。
(4) 溶液中通入
溶液中通入 至饱和,形成
至饱和,形成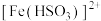 配离子的方程式是
配离子的方程式是_________________ 。
(5)溶液中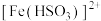 将
将 还原为
还原为 的离子方程式是
的离子方程式是______________________ 。
(6)由实验现象分析,溶液先变为红色,最后慢慢变为浅绿色的可能原因是________ 。
 与
与 溶液的反应。
溶液的反应。(1)小组同学预测向
 溶液中通入
溶液中通入 ,溶液颜色将由黄色变为浅绿色,预测的依据是
,溶液颜色将由黄色变为浅绿色,预测的依据是进行实验
实验装置(夹持仪器略) | 实验现象 |
| 向 溶液中通入 溶液中通入 至饱和,溶液变为红色,静置5min后,溶液的颜色从红色慢慢变为黄色,静置9h后,溶液慢慢由黄色变为浅绿色。 至饱和,溶液变为红色,静置5min后,溶液的颜色从红色慢慢变为黄色,静置9h后,溶液慢慢由黄色变为浅绿色。 |
 与
与 可以发生可逆反应,形成红棕色的配离子
可以发生可逆反应,形成红棕色的配离子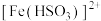 。
。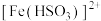 可以将
可以将 还原为
还原为 。
。(2)
 的空间结构是
的空间结构是(3)
 与
与 可以形成配离子的原因是
可以形成配离子的原因是(4)
 溶液中通入
溶液中通入 至饱和,形成
至饱和,形成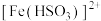 配离子的方程式是
配离子的方程式是(5)溶液中
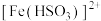 将
将 还原为
还原为 的离子方程式是
的离子方程式是(6)由实验现象分析,溶液先变为红色,最后慢慢变为浅绿色的可能原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】卤素是典型的非金属元素,它们在自然界中大多以盐的形式存在。回答下列问题:
(1)卤素互化物是指两种卤素形成的化合物,因中心原子的成单电子数为奇数,故配体数目也为奇数,如IF7、ICl3、ClF3等。基态溴原子的价电子排布式为________ ,分析上述卤素互化物中中心原子和配体的电负性特点,推测卤素互化物BrXa中,X可能是__________ (填元素符号);
(2)CsBrCl2属于多卤化物,受热分解存在如下两种可能:
CsBrCl2= CsBr+Cl2①
CsBiCl2=CsCl+BrCl ②
由于晶格能的原因,实际进行的是反应②,则晶格能:CsCl________ CsBr。(填“>”或 “<”)
(3)(CN)2、(SCN)2的性质与卤素单质相似,称为拟卤素。其分子内各原子均达到8电子结构,则(CN)2分子中σ键和π键的个数比为___________ ,SCN-离子的空间构型为_______________ 形,C原子的轨道杂化方式为_____________ 。 SCN-离子用于检验Fe3+时,SCN-与Fe3+间形成的化学键为_____________ 键;
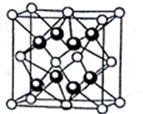
(4)一种天然宝石萤石的主要成分是CaF2。下图是CaF2的晶胞结构示意图,其中与每个Ca2+距离最近的Ca2+有__________ 个;该晶胞边长为α cm,晶体密度为________ g•cm-3(用NA表示阿伏伽德罗常数值)。
(1)卤素互化物是指两种卤素形成的化合物,因中心原子的成单电子数为奇数,故配体数目也为奇数,如IF7、ICl3、ClF3等。基态溴原子的价电子排布式为
(2)CsBrCl2属于多卤化物,受热分解存在如下两种可能:
CsBrCl2= CsBr+Cl2①
CsBiCl2=CsCl+BrCl ②
由于晶格能的原因,实际进行的是反应②,则晶格能:CsCl
(3)(CN)2、(SCN)2的性质与卤素单质相似,称为拟卤素。其分子内各原子均达到8电子结构,则(CN)2分子中σ键和π键的个数比为
(4)一种天然宝石萤石的主要成分是CaF2。下图是CaF2的晶胞结构示意图,其中与每个Ca2+距离最近的Ca2+有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;C原子基态成对电子数是未成对电子数的3倍;原子D的简单离子半径在第三周期元素形成的简单离子中最小;E是前四周期中未成对电子数最多的元素。回答下列问题:
(1)元素B、C、D第一电离能由小到大的顺序为_______ 。
(2)BC 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为_______ 。
(3)下列含B元素的微粒与CO2分子不是互为等电子体的是_______ (填字母)。
A. SCB- B. B2O C. BO2 D.OCB-
(4)E元素的价电子轨道表示式_______ 。
(5)+6价E的化合物毒性较大,常用NaHSO3将酸性废液中的E2O 还原成E3+,反应的离子方程式为
还原成E3+,反应的离子方程式为_______ 。
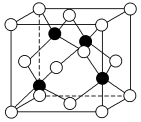
(6)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为_______ g·cm-3(用NA表示阿伏加德罗常数)。
(1)元素B、C、D第一电离能由小到大的顺序为
(2)BC
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为(3)下列含B元素的微粒与CO2分子不是互为等电子体的是
A. SCB- B. B2O C. BO2 D.OCB-
(4)E元素的价电子轨道表示式
(5)+6价E的化合物毒性较大,常用NaHSO3将酸性废液中的E2O
 还原成E3+,反应的离子方程式为
还原成E3+,反应的离子方程式为(6)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数依次增大,其中基态A原子价电子排布式为nsnnpn;化合物B2E为离子化合物,E原子核外的M层中只有两对成对电子;C元素基态原子没有不成对电子;D单质常用于制作太阳能电池和集成电路芯片;F原子最外层只有1个电子,其余各内层轨道均充满电子。请根据以上信息,回答下列问题(答题时,A、B、C、D、E、F用所对应的元素符号表示):
(1)C的同周期相邻元素的第一电离能由小到大的顺序为______
(2)氢化物A2H4分子中A原子采取______ 杂化
(3)元素F在周期表的位置为______ ,E的气态氢化物通入二价阳离子F2+的水溶液反应的离子方程式为______
(4)元素A和D可形成一种无机非金属材料,其晶体具有很高的硬度和熔点,其化合物中所含的化学键类型为______ (从原子轨道重叠方式看),A、D的最高价氧化物的熔沸点大小顺序_________ ;原因________ 。
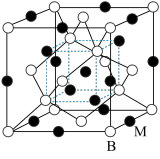
(5)B与同主族原子半径最小的元素M形成的晶胞结构所示的立方晶胞,则其化学式为______ 。设阿伏加 德罗常数为NA,距离最近的两个B、M原子的核间距为a nm,则该化合物的晶胞密度为(用含a和NA的代数式表示)______ g/cm3
(1)C的同周期相邻元素的第一电离能由小到大的顺序为
(2)氢化物A2H4分子中A原子采取
(3)元素F在周期表的位置为
(4)元素A和D可形成一种无机非金属材料,其晶体具有很高的硬度和熔点,其化合物中所含的化学键类型为
(5)B与同主族原子半径最小的元素M形成的晶胞结构所示的立方晶胞,则其化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】前4周期元素X、Y、Z、M、Q的原子序数依次增大,其中元素X的基态原子中电子占据了三种能量不同的原子轨道,且这三种轨道中的电子数相同;元素Y的2p轨道有3个未成对电子,元素Z的基态原子的2p轨道有1个成对电子,M是第4周期核外未成对电子数最多的元素,元素Q位于周期表Ⅷ族,是应用最广泛的金属。请用化学符号 回答下列问题:
(1)基态Q原子的核外电子排布式为_____ 。
(2)X、Y、Z的简单气态氢化物中沸点最高的是_____ ,主要原因是_____ 。
(3)化合物H2Z2中Z原子的杂化方式为_____ 。
(4)XZ2中σ与π键数目之比为_____ 。
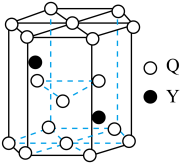
(5)某种由元素Y、Q组成的晶体,其晶胞如图所示,该晶体的化学式为_____ 。_____ 。
(1)基态Q原子的核外电子排布式为
(2)X、Y、Z的简单气态氢化物中沸点最高的是
(3)化合物H2Z2中Z原子的杂化方式为
(4)XZ2中σ与π键数目之比为
(5)某种由元素Y、Q组成的晶体,其晶胞如图所示,该晶体的化学式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】第四周期的过渡元素在工业、农业、科学技术以及人类生活等方面有重要作用。请回答:
(1)科学研究表明用TiO2作光催化剂可将废水中CN-转化为OCN-、并最终氧化为N2、CO2。OCN-中三种元素的电负性由大到小的顺序为_______ 。与CN-互为等电子体的一种分子为_______ (填化学式)。
(2)Ti(BH4)2是一种储氢材料。写出基态Ti的价电子排布式_______ ,BH 的空间构型是
的空间构型是_______ 。
(3)[Cr(H2O)4Cl2]Cl·2H2O中提供孤对电子的原子为_______ ;
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,该物质晶胞呈正四面体构型。试推测Ni(CO)4的晶体类型为_______
(5)FeO、NiO晶体中r(Ni2+)和r(Fe2+)分别为69 pm和78 pm,则熔点FeO_______ NiO (填“>”或“<”)。
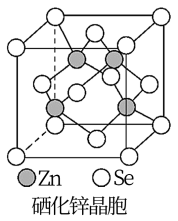
(6)硒化锌(SnSe)是一种重要的半导体材料,其晶胞结构如图所示,则该晶胞中硒原子的配位数为_______ ;若该晶胞密度为d g·cm-3, 硒化锌的摩尔质量为mg/mol。NA代表阿伏加德罗常数,则晶胞参数a为_______ cm。
(1)科学研究表明用TiO2作光催化剂可将废水中CN-转化为OCN-、并最终氧化为N2、CO2。OCN-中三种元素的电负性由大到小的顺序为
(2)Ti(BH4)2是一种储氢材料。写出基态Ti的价电子排布式
 的空间构型是
的空间构型是(3)[Cr(H2O)4Cl2]Cl·2H2O中提供孤对电子的原子为
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,该物质晶胞呈正四面体构型。试推测Ni(CO)4的晶体类型为
(5)FeO、NiO晶体中r(Ni2+)和r(Fe2+)分别为69 pm和78 pm,则熔点FeO
(6)硒化锌(SnSe)是一种重要的半导体材料,其晶胞结构如图所示,则该晶胞中硒原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有 NOx、 (PAN)、HCOOH、等二次污染物。
(PAN)、HCOOH、等二次污染物。
① 1mol PAN中含有的σ键数目为_______ 。PAN中C、N、O种元素的第一电离能由大到小的顺序为_________________ 。
② NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配位数为________ ,中心离子的核外电子排布式为_______________ 。
③相同压强下,HCOOH的沸点比CH3OCH3____ (填“高”或“低”),其原因是__________________ 。
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
① (NH4)2SO4晶体中各种微粒间的作用力不涉及___________ (填序号)。
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
② NH4NO3中阳离子的空间构型为_______ ,阴离子的中心原子轨道采用_______ 杂化。
(3)测定大气中PM2.5的浓度方法之一是β—射线吸收法,β—射线放射源可用85Kr。已知Kr晶体的晶胞结构如图(甲)所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则m/n=_____ (填数字)。
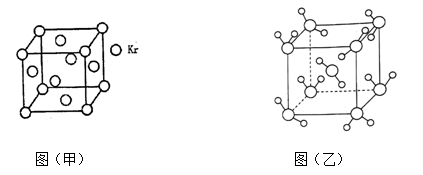
(4)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图(乙)所示。已知晶胞参数a=333.7 pm,阿伏伽德罗常数的值取6.02×1023,则重冰的密度为_______ g.cm-3(计算结果精确到0.01)。
 (PAN)、HCOOH、等二次污染物。
(PAN)、HCOOH、等二次污染物。① 1mol PAN中含有的σ键数目为
② NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配位数为
③相同压强下,HCOOH的沸点比CH3OCH3
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
① (NH4)2SO4晶体中各种微粒间的作用力不涉及
a.离子键 b.共价键 c.配位键 d.范德华力 e.氢键
② NH4NO3中阳离子的空间构型为
(3)测定大气中PM2.5的浓度方法之一是β—射线吸收法,β—射线放射源可用85Kr。已知Kr晶体的晶胞结构如图(甲)所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则m/n=

(4)最新研究发现,水能凝结成13种类型的结晶体。除普通冰外,还有-30℃才凝固的低温冰,180℃依然不变的热冰,比水密度大的重冰等。重冰的结构如图(乙)所示。已知晶胞参数a=333.7 pm,阿伏伽德罗常数的值取6.02×1023,则重冰的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】(1)PM2.5富含大量的有毒、有害物质,易引发二次光化学烟雾,光化学烟雾中含有NOx、HCOOH、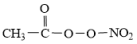 (PAN)等二次污染物。
(PAN)等二次污染物。
①1mol PAN中含有的σ键数目为_______ 。PAN中除H外其余三种元素的第一电离能由大到小的顺序为_________________ 。
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配位数为_______ ,中心离子的核外电子排布式为_______________ 。
③相同压强下,HCOOH的沸点比CH3OCH3____ (填“高”或“低”),其原因是___________________ 。
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
①(NH4)2SO4晶体中各种微粒间的作用力不涉及___________ (填序号)。
a.离子键
b.共价键
c.配位键
d.范德华力
e.氢键
②NH4NO3中阳离子的空间构型为_____ ,阴离子的中心原子轨道采用_______ 杂化。
(3)测定大气中PM2.5的浓度方法之一是β—射线吸收法,β—射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则m/n=_____ (填数字)。

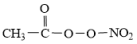 (PAN)等二次污染物。
(PAN)等二次污染物。①1mol PAN中含有的σ键数目为
②NO能被FeSO4溶液吸收生成配合物[Fe(NO)(H2O)5]SO4,该配合物中中心离子的配位数为
③相同压强下,HCOOH的沸点比CH3OCH3
(2)PM2.5微细粒子包含(NH4)2SO4、NH4NO3等。
①(NH4)2SO4晶体中各种微粒间的作用力不涉及
a.离子键
b.共价键
c.配位键
d.范德华力
e.氢键
②NH4NO3中阳离子的空间构型为
(3)测定大气中PM2.5的浓度方法之一是β—射线吸收法,β—射线放射源可用85Kr。已知Kr晶体的晶胞结构如图所示,设晶体中与每个Kr原子紧相邻的Kr原子有m个,晶胞中Kr原子为n个,则m/n=

您最近一年使用:0次