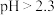黄铁矿(主要成分FeS2),在空气中会被缓慢氧化,氧化过程如图所示。下列说法正确的是
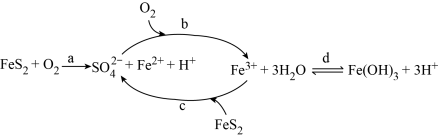

| A.发生反应a时,每1 mol FeS2被还原,转移14 mol e- |
| B.已知25°C时,Ksp[Fe(OH)3]=2.79 ×10-39,则该温度下d逆反应的平衡常数为K=2.79 ×103 |
C.c发生反应的离子方程式为:4Fe3++FeS2+8H2O=5Fe2++2 +16H+ +16H+ |
| D.为了验证b过程反应后溶液中是否含Fe2+,可选用氯水和KSCN溶液 |
更新时间:2022/06/06 06:34:04
|
相似题推荐
单选题
|
适中
(0.65)
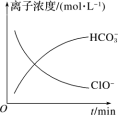
【推荐1】在处理废水时,某特定反应体系中反应物和生成物共有 6 种粒子:NO 、HCO
、HCO 、ClO-、CNO-(N 的价态为-3)、H2O、Cl-,在反应过程中部分离子浓度与反应进程关系如图所示。下列有关该反应的说法正确的是
、ClO-、CNO-(N 的价态为-3)、H2O、Cl-,在反应过程中部分离子浓度与反应进程关系如图所示。下列有关该反应的说法正确的是
 、HCO
、HCO 、ClO-、CNO-(N 的价态为-3)、H2O、Cl-,在反应过程中部分离子浓度与反应进程关系如图所示。下列有关该反应的说法正确的是
、ClO-、CNO-(N 的价态为-3)、H2O、Cl-,在反应过程中部分离子浓度与反应进程关系如图所示。下列有关该反应的说法正确的是
| A.在上述反应体系中,CNO-是氧化剂 |
| B.还原产物与氧化产物的物质的量之比为1∶3 |
| C.在标准状况下,产生 4.48 L N2 时转移 0.8 mol 电子 |
| D.上述反应中,只有两种元素化合价发生了变化 |
您最近一年使用:0次
【推荐2】某反应的反应机理、能量与反应进程的关系如图所示,下列说法不正确的是
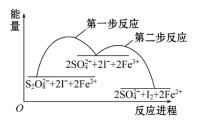

| A.Fe2+是该反应的催化剂 |
B.反应的总离子方程式为 +2I- +2I- 2 2 + I2 + I2 |
C. 在第一步反应中作氧化剂 在第一步反应中作氧化剂 |
| D.两步反应都是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】宏观辨识与微观探析是化学学科核心素养之一、下列对应离子方程式书写正确,且能完整解释对应实验现象或应用的是
A.和面时用小苏打和食醋能使馒头蓬松:HCO +H+=H2O+CO2↑ +H+=H2O+CO2↑ |
| B.氯化亚铁溶液中通入氯气,溶液变黄色:Fe2++Cl2=Fe3++2Cl- |
C.向滴有酚酞的Ba(OH)2溶液中加入NaHSO4溶液,至溶液恰好变为无色:Ba2++2OH-+SO +2H+=BaSO4↓+2H2O +2H+=BaSO4↓+2H2O |
D.NaAlO2溶液中通入过量CO2,产生白色沉淀:2AlO +CO2+3H2O=2Al(OH)3↓+CO +CO2+3H2O=2Al(OH)3↓+CO |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验能达到目的的是
| A.用Na2CO3溶液除去CO2中的SO2气体 |
| B.加热除去Na2CO3固体中的NaHCO3 |
| C.用Cl2除去Fe2(SO4)3溶液中的少量FeSO4 |
| D.用BaCl2溶液除去NaCl溶液中的K2SO4 |
您最近一年使用:0次
【推荐1】一定温度下,在三个容积均为2L的恒容密闭容器中按不同方式投入反应物,发生反应CO(g)+H2O(g) CO2(g)+H2(g) △H<0,测得反应的相关数据如下表所示。下列说法错误的是( )
CO2(g)+H2(g) △H<0,测得反应的相关数据如下表所示。下列说法错误的是( )
 CO2(g)+H2(g) △H<0,测得反应的相关数据如下表所示。下列说法错误的是( )
CO2(g)+H2(g) △H<0,测得反应的相关数据如下表所示。下列说法错误的是( )| 容器 | 温度/K (T1>T2) | 起始时物质的量/mol | 平衡时物质的量/mol | |
| CO(g) | H2O(g) | H2(g) | ||
| I | T1 | 3.00 | 2.00 | 1.75 |
| II | T2 | 2.00 | 3.00 | |
| II | T1 | 2.00 | 3.00 | |
| A.达到平衡时,容器I和容器II中正反应速率:v I(H2)>vII(H2) |
| B.达到平衡时,容器II中c(CO2)>1.75mol·L-1 |
| C.达到平衡时,容器I和容器II中的转化率:αI (CO)=αII(H2O) |
| D.达到平衡时,容器II和容器I中的平衡常数:KII>KI |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
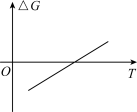
【推荐2】一定温度和压强下,在催化剂作用下可发生反应: 。该反应的自由能(ΔG)与温度(T)的关系如图所示。已知:分压=总压×物质的量分数,浓度平衡常数用K表示。下列说法正确的是
。该反应的自由能(ΔG)与温度(T)的关系如图所示。已知:分压=总压×物质的量分数,浓度平衡常数用K表示。下列说法正确的是
 。该反应的自由能(ΔG)与温度(T)的关系如图所示。已知:分压=总压×物质的量分数,浓度平衡常数用K表示。下列说法正确的是
。该反应的自由能(ΔG)与温度(T)的关系如图所示。已知:分压=总压×物质的量分数,浓度平衡常数用K表示。下列说法正确的是
| A.增大CO的浓度,v正和K均增大 |
B.当反应达到平衡状态时,体系的总压强为p,其中H2(g)、CO(g)、CH3OH(g)的物质的量均为1mol,则用分压表示的平衡常数为 |
C.由图像可知  |
| D.加入更多的固体酸催化剂,有利于提高甲醇的平衡产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列叙述正确的是
A.浓度均为 的下列溶液,pH由大到小的顺序为 的下列溶液,pH由大到小的顺序为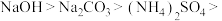  |
B.常温下,为确定 是强酸还是弱酸,可测NaHA溶液的pH,若 是强酸还是弱酸,可测NaHA溶液的pH,若 ,则 ,则 是弱酸,若 是弱酸,若 ,则 ,则 是强酸 是强酸 |
C.常温下,将 的 的 溶液稀释10倍,稀释后溶液的 溶液稀释10倍,稀释后溶液的 |
D.常温下 ,此时将足量AgCl固体分别投入相同体积的①蒸馏水、② ,此时将足量AgCl固体分别投入相同体积的①蒸馏水、② 盐酸、③ 盐酸、③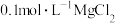 溶液、④ 溶液、④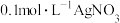 溶液中,则溶液中 溶液中,则溶液中 浓度由大到小的顺序为 浓度由大到小的顺序为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,将11.65 g BaSO4粉末置于盛有250mL蒸馏水的烧杯中,然后向烧杯中加入Na2CO3固体(忽视溶液体积的变化)并充分搅拌,加入Na2CO3固体的过程中,溶液中几种离子的浓度变化曲线如图所示,下列说法中不正确的是


| A.相同温度时,Ksp(BaSO4)<Ksp(BaCO3) |
| B.若使0.05 mol BaSO4全部转化为BaCO3,至少加入1.3 mol Na2CO3 |
| C.BaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小为:c(CO32-)>c(SO42-)>c(OH-)>c(Ba2+) |
| D.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 |
您最近一年使用:0次


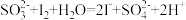
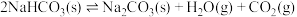
 ,一定温度下,在密闭容器中放入
,一定温度下,在密闭容器中放入 固体,反应达平衡时容器中压强为
固体,反应达平衡时容器中压强为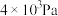 。下列说法正确的是
。下列说法正确的是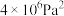
 、
、 、
、 和
和 等离子,以这种废液为原料设计制备高纯
等离子,以这种废液为原料设计制备高纯 的工艺流程如图所示(部分操作和条件略)。下列说法正确的是
的工艺流程如图所示(部分操作和条件略)。下列说法正确的是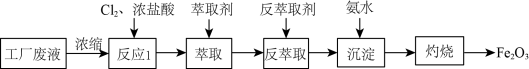
 (浓)
(浓) (易溶于有机溶剂);
(易溶于有机溶剂);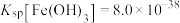 ,
, 。
。 使
使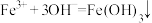
 ),需调节溶液
),需调节溶液