金属镓被称为“电子工业脊梁”,性质与铝相似,金属活动性介于锌和铁之间。氮化镓是5G技术中广泛应用的新型半导体材料,利用粉煤灰(主要成分为 、
、 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
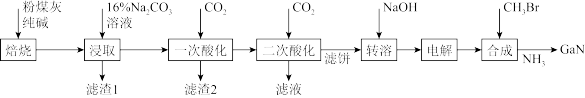
已知:常温下,相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度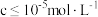 时,可认为已除尽。
时,可认为已除尽。
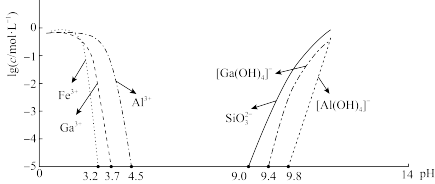
回答下列问题:
(1)“焙烧”的目的是将 转化为
转化为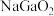 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(2)“滤渣1”主要成分为_______ 。
(3)“二次酸化”的pH≈_______ ,其中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)“电解”可得金属Ga,写出阴极电极反应式_______ 。
(5)“合成”得到的三甲基镓与NH3反应时,两者物质的量之比为_______ 。
(6)常温下,反应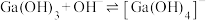 的平衡常数K=
的平衡常数K=_______ 。
 、
、 、
、 ,还有少量
,还有少量 等杂质)制备氮化镓流程如下:
等杂质)制备氮化镓流程如下:
已知:常温下,相关元素可溶性组分物质的量浓度c与pH的关系如图所示。当溶液中可溶组分浓度
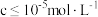 时,可认为已除尽。
时,可认为已除尽。
回答下列问题:
(1)“焙烧”的目的是将
 转化为
转化为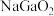 ,该反应的化学方程式为
,该反应的化学方程式为(2)“滤渣1”主要成分为
(3)“二次酸化”的pH≈
 发生反应的离子方程式为
发生反应的离子方程式为(4)“电解”可得金属Ga,写出阴极电极反应式
(5)“合成”得到的三甲基镓与NH3反应时,两者物质的量之比为
(6)常温下,反应
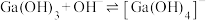 的平衡常数K=
的平衡常数K=
更新时间:2022-08-12 17:54:43
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】钴是稀有的贵重金属,废旧锂离子电池正极材料[钴酸锂(LiCoO2) 、石墨、铝箔及其他杂质]的回收再生意义重大。一种钴酸锂回收再生工艺流程如图:
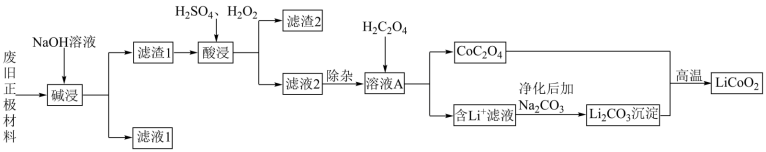
已知: H2C2O4: Ka1=5.6 ×10-2, Ka2=1.5 ×10-4; Ksp(CoC2O4) =4.0 ×10-6
回答下列问题:
(1)为加快“碱浸”效率可采取的措施有_______ 。(任写一条) 。
(2)“ 酸浸”时反应的离子方程式为_______ ,“滤渣2”的成分为_______ , 相同条件下,酸浸时钴的浸出率随温度变化如表所示,酸浸时温度控制在50°C左右的原因_______ 。
(3)“滤液2”中各种金属离子的沉淀率随pH的变化如图所示,向“滤液2”中加入氨水,可除去杂质离子_______ (填离子符号),应调节pH范围为_______ 。
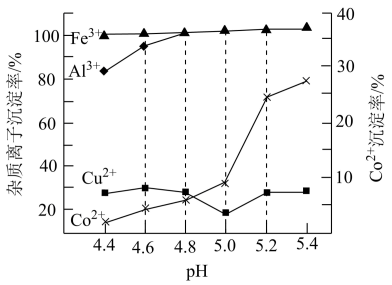
(4)溶液A中加入H2C2O4产生CoC2O4沉淀,常温下Co2+与H2C2O4反应生成CoC2O4的平衡常数K=_______ 。
(5)高温下,纯净的CoC2O4与Li2CO3再生LiCoO2的化学方程式为_______ 。

已知: H2C2O4: Ka1=5.6 ×10-2, Ka2=1.5 ×10-4; Ksp(CoC2O4) =4.0 ×10-6
回答下列问题:
(1)为加快“碱浸”效率可采取的措施有
(2)“ 酸浸”时反应的离子方程式为
| 反应温度/°C | 30 | 40 | 50 | 60 |
| 钴的浸出率/% | 88 | 90.5 | 93 | 89 |

(4)溶液A中加入H2C2O4产生CoC2O4沉淀,常温下Co2+与H2C2O4反应生成CoC2O4的平衡常数K=
(5)高温下,纯净的CoC2O4与Li2CO3再生LiCoO2的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸锰是一种重要的化工中间体,是锰行业研究的热点。一种以高硫锰矿(主要成分为含锰化合物及FeS)为原料制备硫酸锰的工艺流程如下:

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
② Ksp(MgF2)=6.4×10-10 (mol/L)3;Ksp(CaF2)=3.6×10-12 (mol/L)3
③离子浓度≤10-5mol·L-1时,离子沉淀完全。请回答:
(1)“氧化”时,发生反应的离子方程式为___________ 。
(2)“中和除杂”时,生成沉淀的主要成分为___________ (填化学式)。
(3)“氟化除杂”时,使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于___________ mol/L。
(4)“碳化结晶”时,发生反应的离子方程式为___________ 。
(5)用惰性电极电解MnSO4溶液可制备MnO2,电解过程中阳极的电极反应式为___________ 。

已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
② Ksp(MgF2)=6.4×10-10 (mol/L)3;Ksp(CaF2)=3.6×10-12 (mol/L)3
③离子浓度≤10-5mol·L-1时,离子沉淀完全。请回答:
(1)“氧化”时,发生反应的离子方程式为
(2)“中和除杂”时,生成沉淀的主要成分为
(3)“氟化除杂”时,使溶液中的Mg2+和Ca2+沉淀完全,需维持c(F-)不低于
(4)“碳化结晶”时,发生反应的离子方程式为
(5)用惰性电极电解MnSO4溶液可制备MnO2,电解过程中阳极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】碳酸锂是一种白色粉末,微溶于水,是常用的锂离子电池原料,也可用于制备陶瓷和催化剂。此外,碳酸锂有明显的抑制躁狂症作用,可以改善精神分裂症的情感障碍,因此碳酸锂也是一种重要的药物。工业上使用锂辉石(主要成分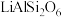 ,含少量
,含少量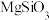 和
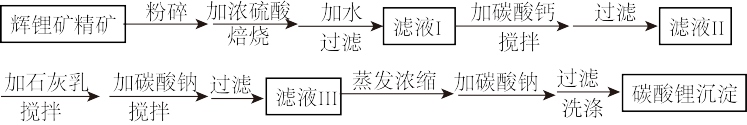
和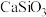 )制备碳酸锂,我国目前主要采用三种方法:石灰石焙烧法、硫酸法和硫酸盐法。硫酸法的主要流程如下图所示:
)制备碳酸锂,我国目前主要采用三种方法:石灰石焙烧法、硫酸法和硫酸盐法。硫酸法的主要流程如下图所示:
已知: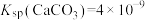 ,
,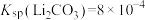 。
。
(1)将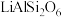 写成氧化物的形式
写成氧化物的形式___________ 。
(2)滤液Ⅰ中所含的浓度较大的两种金属阳离子是___________ 。在滤液Ⅰ中加碳酸钙的目的是___________ 。
(3)在滤液Ⅱ中加入石灰乳的目的之一是除去 ,写出发生反应的离子方程式
,写出发生反应的离子方程式___________ 。
(4)向滤液Ⅱ中加完石灰乳再加碳酸钠时,为了将 恰好沉淀完全[
恰好沉淀完全[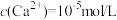 ]),此时
]),此时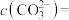
___________ mol/L。假设此时溶液中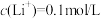 ,试通过计算说明此时是否会生成碳酸锂沉淀:
,试通过计算说明此时是否会生成碳酸锂沉淀:___________ 。
(5)有人研究出一种从碳酸锂制备锂单质的新方法:将碳酸锂和氧化铝混合后加强热,该反应有一种常见温室气体生成;充分反应后再加入铝粉继续加强热,反应后进行分离即可得到锂单质,写出这两步反应的化学方程式:___________ ,___________ 。
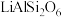 ,含少量
,含少量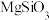 和
和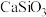 )制备碳酸锂,我国目前主要采用三种方法:石灰石焙烧法、硫酸法和硫酸盐法。硫酸法的主要流程如下图所示:
)制备碳酸锂,我国目前主要采用三种方法:石灰石焙烧法、硫酸法和硫酸盐法。硫酸法的主要流程如下图所示:
已知:
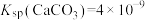 ,
,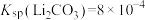 。
。(1)将
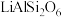 写成氧化物的形式
写成氧化物的形式(2)滤液Ⅰ中所含的浓度较大的两种金属阳离子是
(3)在滤液Ⅱ中加入石灰乳的目的之一是除去
 ,写出发生反应的离子方程式
,写出发生反应的离子方程式(4)向滤液Ⅱ中加完石灰乳再加碳酸钠时,为了将
 恰好沉淀完全[
恰好沉淀完全[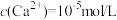 ]),此时
]),此时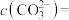
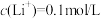 ,试通过计算说明此时是否会生成碳酸锂沉淀:
,试通过计算说明此时是否会生成碳酸锂沉淀:(5)有人研究出一种从碳酸锂制备锂单质的新方法:将碳酸锂和氧化铝混合后加强热,该反应有一种常见温室气体生成;充分反应后再加入铝粉继续加强热,反应后进行分离即可得到锂单质,写出这两步反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】电化学原理在工业生产、物质制备、污染物理处理等方面应用广泛,请按要求回答下列问题。
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。
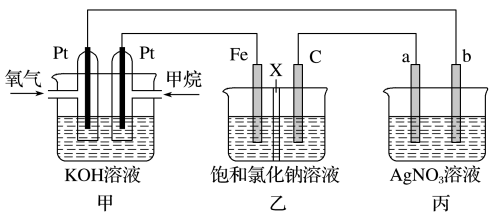
请按要求回答相关问题:
(1)乙中X是_______ 交换膜,甲烷燃料电池负极电极反应式是_______ 。
(2)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成气体的物质的量为_______ 。
(3)欲用丙装置给铜镀银,b应是_______ (填化学式)。
(4)将0.2 mol AgNO3、0.4 mol Cu(NO3)2、0.6 mol KCl溶于水,配成100 mL溶液,用惰性电极电解一段时间后,某一电极上析出了0.3 mol Cu,此时在另一电极上产生的气体体积(标准状况)为_______ L
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。

请按要求回答相关问题:
(1)乙中X是
(2)若在标准状况下,有4.48 L氧气参加反应,则乙装置中C电极上生成气体的物质的量为
(3)欲用丙装置给铜镀银,b应是
(4)将0.2 mol AgNO3、0.4 mol Cu(NO3)2、0.6 mol KCl溶于水,配成100 mL溶液,用惰性电极电解一段时间后,某一电极上析出了0.3 mol Cu,此时在另一电极上产生的气体体积(标准状况)为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】铝是应用广泛的金属。以铝土矿(主要成分为 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如下:
等杂质)为原料制备铝的一种工艺流程如下:
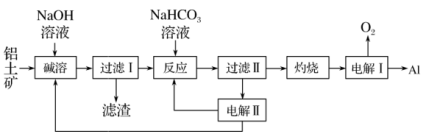
注: 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式:___________ 。
(2)向“过滤Ⅰ”所得滤液中加入 溶液,溶液的
溶液,溶液的
___________ (填“增大”“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融 ,电解过程中作阳极的石墨易消耗,原因是
,电解过程中作阳极的石墨易消耗,原因是___________ 。
(4)“电解Ⅱ”是电解 溶液,原理如图所示。阳极的电极反应式:
溶液,原理如图所示。阳极的电极反应式:___________ 。
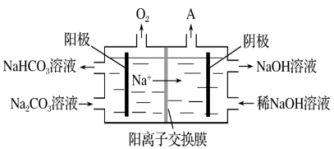
(5)铝粉在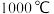 时可与
时可与 反应制备
反应制备 。在铝粉中添加少量
。在铝粉中添加少量 固体并充分混合,有利于
固体并充分混合,有利于 的制备,其主要原因是
的制备,其主要原因是___________ 。
 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如下:
等杂质)为原料制备铝的一种工艺流程如下:
注:
 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。(1)“碱溶”时生成偏铝酸钠的离子方程式:
(2)向“过滤Ⅰ”所得滤液中加入
 溶液,溶液的
溶液,溶液的
(3)“电解Ⅰ”是电解熔融
 ,电解过程中作阳极的石墨易消耗,原因是
,电解过程中作阳极的石墨易消耗,原因是(4)“电解Ⅱ”是电解
 溶液,原理如图所示。阳极的电极反应式:
溶液,原理如图所示。阳极的电极反应式:
(5)铝粉在
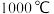 时可与
时可与 反应制备
反应制备 。在铝粉中添加少量
。在铝粉中添加少量 固体并充分混合,有利于
固体并充分混合,有利于 的制备,其主要原因是
的制备,其主要原因是
您最近一年使用:0次
【推荐3】科学家一直致力于“人工固氮”的研究,现已有多种方法。
【方法一】1918年,德国化学家哈伯因发明工业合成氨【N2(g)+3H2(g) 2NH3(g) H<0】的方法而荣获诺贝尔化学奖。
2NH3(g) H<0】的方法而荣获诺贝尔化学奖。
(1)若将1molN2和3molH2放入1L的密闭容器中,5min后N2的浓度为0.8mol/L,这段时间内用N2的浓度变化表示的反应速率为_____ mol/(L·min)。
(2)在一定温度下的定容密闭容器中发生上述反应,下列叙述能说明反应已经达到平衡状态的是____ 。
a. v(N2)正=3v(H2)逆
b. 容器中气体的密度不随时间而变化
c. 容器中气体的分子总数不随时间而变化
d. 容器中气体的平均相对分子质量不随时间而变化
(3)合成氨反应的生产条件选择中,能用勒夏特列原理解释的是________ 。
①使用催化剂 ②高温 ③高压 ④及时将氨气液化从体系中分离出来
A. ①③ B. ②③ C. ③④ D. ②④
【方法二】1998年,两位希腊化学家提出了电解合成氨的新思路:
(4)采用高质子导电性的SCY陶瓷(能传递H+)为介质,实现了高温(570℃)常压下高转化率的电解法合成氨,转化率可达到78%,装置如下图:

钯电极A是电解池的___ 极(填“阳”或“阴”),阳极反应式为________ 。
【方法三】最新的“人工固氮”研究报道:在常温、常压、光照条件下,N2在催化剂表面与水发生反应,直接生成氨气和氧气:
已知:N2(g)+3H2(g) 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol
2H2(g)+O2(g)=2H2O(1) △H=-571.6 kJ/mol
(5)写出上述固氮反应的热化学方程式___________ 。
【方法一】1918年,德国化学家哈伯因发明工业合成氨【N2(g)+3H2(g)
 2NH3(g) H<0】的方法而荣获诺贝尔化学奖。
2NH3(g) H<0】的方法而荣获诺贝尔化学奖。(1)若将1molN2和3molH2放入1L的密闭容器中,5min后N2的浓度为0.8mol/L,这段时间内用N2的浓度变化表示的反应速率为
(2)在一定温度下的定容密闭容器中发生上述反应,下列叙述能说明反应已经达到平衡状态的是
a. v(N2)正=3v(H2)逆
b. 容器中气体的密度不随时间而变化
c. 容器中气体的分子总数不随时间而变化
d. 容器中气体的平均相对分子质量不随时间而变化
(3)合成氨反应的生产条件选择中,能用勒夏特列原理解释的是
①使用催化剂 ②高温 ③高压 ④及时将氨气液化从体系中分离出来
A. ①③ B. ②③ C. ③④ D. ②④
【方法二】1998年,两位希腊化学家提出了电解合成氨的新思路:
(4)采用高质子导电性的SCY陶瓷(能传递H+)为介质,实现了高温(570℃)常压下高转化率的电解法合成氨,转化率可达到78%,装置如下图:

钯电极A是电解池的
【方法三】最新的“人工固氮”研究报道:在常温、常压、光照条件下,N2在催化剂表面与水发生反应,直接生成氨气和氧气:
已知:N2(g)+3H2(g)
 2NH3(g) △H=-92 kJ/mol
2NH3(g) △H=-92 kJ/mol2H2(g)+O2(g)=2H2O(1) △H=-571.6 kJ/mol
(5)写出上述固氮反应的热化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】五氧化二钒(V2O5)在冶金、化工等领域有重要应用。实验室以含钒废料(含V2O3、FeO、CuO、MnO、SiO2、Al2O3、有机物)为原料制备V2O5的一种流程如图:
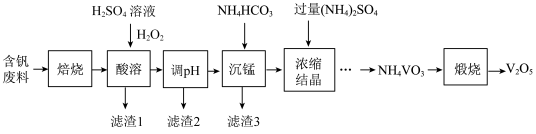
已知:25℃时,难溶电解质的溶度积常数如表所示:
(1)“焙烧”的目的是______ 。
(2)酸溶时加入H2O2的目的是_______ 。
(3)常温下,若“调pH”为7,Cu2+是否能沉淀完全:______ (填“是”或“否”)(溶液中离子浓度小于10-5mol•L-1时,认为该离子沉淀完全)。
(4)“沉锰”需将温度控制在70℃左右,温度不能过高或过低的原因为______ 。
(5)结晶所得的NH4VO3需进行水洗、干燥。证明NH4VO3已洗涤干净的实验操作及现象_____ 。
(6)为测定该产品的纯度,兴趣小组同学准确称取V2O5产品2.000g,加入过量稀硫酸使其完全反应,生成(VO2)2SO4,并配成100mL溶液。取10.00mL溶液用0.1000mol•L-1的H2C2O4标准溶液滴定,滴定到终点时消耗标准液10.00mL。已知滴定过程中H2C2O4被氧化为CO2,VO 黄色(被还原为VO2+蓝色),该反应的离子方程式:
黄色(被还原为VO2+蓝色),该反应的离子方程式:______ ;该产品的纯度为______ 。

已知:25℃时,难溶电解质的溶度积常数如表所示:
| 难溶电解质 | Cu(OH)2 | Mn(OH)2 | Al(OH)3 |
| Ksp | 2.2×10-20 | 4×10-14 | 1.9×10-33 |
(2)酸溶时加入H2O2的目的是
(3)常温下,若“调pH”为7,Cu2+是否能沉淀完全:
(4)“沉锰”需将温度控制在70℃左右,温度不能过高或过低的原因为
(5)结晶所得的NH4VO3需进行水洗、干燥。证明NH4VO3已洗涤干净的实验操作及现象
(6)为测定该产品的纯度,兴趣小组同学准确称取V2O5产品2.000g,加入过量稀硫酸使其完全反应,生成(VO2)2SO4,并配成100mL溶液。取10.00mL溶液用0.1000mol•L-1的H2C2O4标准溶液滴定,滴定到终点时消耗标准液10.00mL。已知滴定过程中H2C2O4被氧化为CO2,VO
 黄色(被还原为VO2+蓝色),该反应的离子方程式:
黄色(被还原为VO2+蓝色),该反应的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】三盐基硫酸铅简称“三盐”,是一种重要的工业原料,其化学式为 (相对分子质量为990)。以
(相对分子质量为990)。以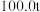 铅泥(主要成分为
铅泥(主要成分为 、
、 及
及 等,
等, 、
、 不与
不与 溶液反应)为原料制备三盐的工艺流程如图所示。
溶液反应)为原料制备三盐的工艺流程如图所示。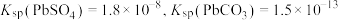 。
。
回答下列问题:
(1)“转化”时 发生反应的离子方程式为
发生反应的离子方程式为_______ ,反应达到平衡时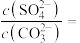
_______ 。
(2)“酸溶”时若有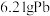 发生反应,则生成
发生反应,则生成 的体积(标准状况)为
的体积(标准状况)为_______  ,为提高“酸溶”速率,可采取的措施是
,为提高“酸溶”速率,可采取的措施是_______ (任意写出一条)。
(3)“滤液2”中溶质的主要成分的化学式为_______ 。
(4)“合成”时主要反应的化学方程式为_______ 。
(5)若得到纯净干燥的三盐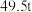 ,假设铅泥中的铅元素有
,假设铅泥中的铅元素有 转化为三盐,则铅泥中央铅元素的质量分数为
转化为三盐,则铅泥中央铅元素的质量分数为_______  。
。
 (相对分子质量为990)。以
(相对分子质量为990)。以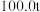 铅泥(主要成分为
铅泥(主要成分为 、
、 及
及 等,
等, 、
、 不与
不与 溶液反应)为原料制备三盐的工艺流程如图所示。
溶液反应)为原料制备三盐的工艺流程如图所示。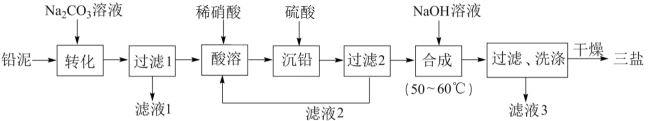
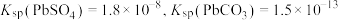 。
。回答下列问题:
(1)“转化”时
 发生反应的离子方程式为
发生反应的离子方程式为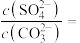
(2)“酸溶”时若有
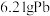 发生反应,则生成
发生反应,则生成 的体积(标准状况)为
的体积(标准状况)为 ,为提高“酸溶”速率,可采取的措施是
,为提高“酸溶”速率,可采取的措施是(3)“滤液2”中溶质的主要成分的化学式为
(4)“合成”时主要反应的化学方程式为
(5)若得到纯净干燥的三盐
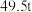 ,假设铅泥中的铅元素有
,假设铅泥中的铅元素有 转化为三盐,则铅泥中央铅元素的质量分数为
转化为三盐,则铅泥中央铅元素的质量分数为 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】以废旧电池[主要含MnO2、MnOOH、Zn、Zn(OH)2、Fe、KOH、、石墨棒]为原料,制备锰锌铁氧体[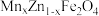 ]的流程如下:
]的流程如下: 在煮沸时易分解。
在煮沸时易分解。
(1)将电池“粉碎”前应先放电,其目的是______________ 。
(2)“酸浸”过程中含锰物质被溶液中的 ,还原为
,还原为 ,其中
,其中 参与反应的离子方程式为
参与反应的离子方程式为______________ 。
(3)“氧化”时加入 将
将 氧化,取氧化后的溶液加入
氧化,取氧化后的溶液加入 ,调节溶液
,调节溶液 为1~2,可制得黄钾铁矾[
为1~2,可制得黄钾铁矾[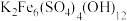 ]沉淀。
]沉淀。
①复杂的含氧酸盐可以表示为氧化物的形式,如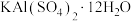 可表示为
可表示为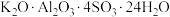 ,则
,则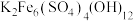 以氧化物的形式可表示为
以氧化物的形式可表示为______________ 。
②写出加入Na2CO3生成黄钾铁矾反应的离子方程式:______________ 。
③检验“氧化”后的溶液中是否还存在Fe2+,可使用的试剂是_______________ (填化学式)。
(4)“共沉淀”前,需测定溶液中锰元素含量。操作步骤:
a.准确量取1.00mL“氧化”后的溶液于锥形瓶中,加入少量硫酸、磷酸和硝酸银溶液,振荡;
b.将溶液加热至 ,加入
,加入 充分反应(
充分反应( 被氧化为
被氧化为 )后,再将溶液煮沸;
)后,再将溶液煮沸;
c.冷却后,用 的
的 标准溶液滴定至终点,平行滴定3次,平均消耗
标准溶液滴定至终点,平行滴定3次,平均消耗 溶液
溶液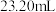 。
。
①步骤b中,煮沸的目的是_______________ 。
②“氧化”后的溶液中 的物质的量浓度为
的物质的量浓度为_________  。
。
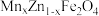 ]的流程如下:
]的流程如下: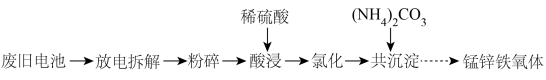
 在煮沸时易分解。
在煮沸时易分解。(1)将电池“粉碎”前应先放电,其目的是
(2)“酸浸”过程中含锰物质被溶液中的
 ,还原为
,还原为 ,其中
,其中 参与反应的离子方程式为
参与反应的离子方程式为(3)“氧化”时加入
 将
将 氧化,取氧化后的溶液加入
氧化,取氧化后的溶液加入 ,调节溶液
,调节溶液 为1~2,可制得黄钾铁矾[
为1~2,可制得黄钾铁矾[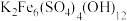 ]沉淀。
]沉淀。①复杂的含氧酸盐可以表示为氧化物的形式,如
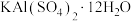 可表示为
可表示为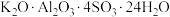 ,则
,则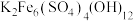 以氧化物的形式可表示为
以氧化物的形式可表示为②写出加入Na2CO3生成黄钾铁矾反应的离子方程式:
③检验“氧化”后的溶液中是否还存在Fe2+,可使用的试剂是
(4)“共沉淀”前,需测定溶液中锰元素含量。操作步骤:
a.准确量取1.00mL“氧化”后的溶液于锥形瓶中,加入少量硫酸、磷酸和硝酸银溶液,振荡;
b.将溶液加热至
 ,加入
,加入 充分反应(
充分反应( 被氧化为
被氧化为 )后,再将溶液煮沸;
)后,再将溶液煮沸;c.冷却后,用
 的
的 标准溶液滴定至终点,平行滴定3次,平均消耗
标准溶液滴定至终点,平行滴定3次,平均消耗 溶液
溶液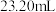 。
。①步骤b中,煮沸的目的是
②“氧化”后的溶液中
 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】以辉铋矿(主要成分为Bi2S3,含有CuS、FeS2、SiO2杂质)和软锰矿(主要成分为MnO2)为原料联合制备BiOCl和MnSO4•H2O的工艺流程如图:
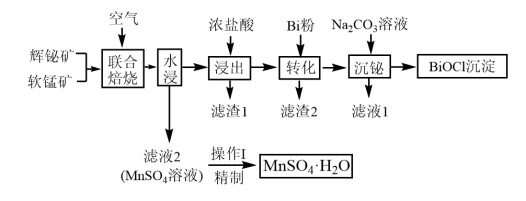
已知:①金属活动性:Fe>Bi>Cu。
②Bi3+易水解为BiOCl沉淀;常温下,BiOCl存在的pH范围约为2.0~11.0。
③常温下,该工艺中有关金属离子开始沉淀和完全沉淀的pH见表。
(1)“联合焙烧”时Bi2S3、FeS2、CuS分别转化为Bi2O3、Fe2O3、CuO,写出生成MnSO4和Bi2O3的化学方程式:_______ 。
(2)“浸出”时需及时补充浓盐酸调节浸取液的pH≈l.4,其目的是_______ 。
(3)“滤渣1”的主要成分为_______ (填化学式)。
(4)“转化”时加入足量金属Bi的目的是________ (用离子方程式表示)。
(5)为保证BiOCl产品的纯度,理论上“沉铋”时应控制溶液的pH范围为_______ 。
(6)将100kg辉铋矿进行“联合焙烧”,“转化”时消耗2.0kg金属Bi,假设其余各步损失不计,干燥后称量BiOCl产品质量为47.5kg,滴定测得产品中Bi的质量分数为80.0%。辉铋矿中Bi元素的质量分数为_______ %(保留3位有效数字)。
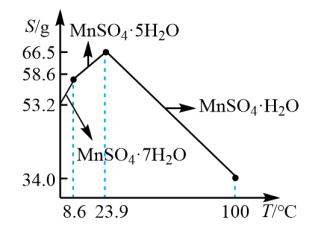
(7)已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。则从“滤液2”中获得较高纯度MnSO4•H2O的“操作I”为控制温度在80~90℃、_______ 、_______ 、用80~90℃蒸馏水洗涤2~3次、真空干燥。

| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe2+ | 6.3 | 8.3 |
| Fe3+ | 1.6 | 3.1 |
②Bi3+易水解为BiOCl沉淀;常温下,BiOCl存在的pH范围约为2.0~11.0。
③常温下,该工艺中有关金属离子开始沉淀和完全沉淀的pH见表。
(1)“联合焙烧”时Bi2S3、FeS2、CuS分别转化为Bi2O3、Fe2O3、CuO,写出生成MnSO4和Bi2O3的化学方程式:
(2)“浸出”时需及时补充浓盐酸调节浸取液的pH≈l.4,其目的是
(3)“滤渣1”的主要成分为
(4)“转化”时加入足量金属Bi的目的是
(5)为保证BiOCl产品的纯度,理论上“沉铋”时应控制溶液的pH范围为
(6)将100kg辉铋矿进行“联合焙烧”,“转化”时消耗2.0kg金属Bi,假设其余各步损失不计,干燥后称量BiOCl产品质量为47.5kg,滴定测得产品中Bi的质量分数为80.0%。辉铋矿中Bi元素的质量分数为
(7)已知硫酸锰在不同温度下的溶解度和析出晶体的组成如图所示。则从“滤液2”中获得较高纯度MnSO4•H2O的“操作I”为控制温度在80~90℃、

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】对废催化剂进行回收可有效利用金属资源。某废催化剂主要含 、
、 、
、 。一种回收利用废催化剂的工艺流程如下图。
。一种回收利用废催化剂的工艺流程如下图。
(1)“焙烧”时, 转化为
转化为 ,
, 中Mo的化合价为
中Mo的化合价为_______ ,出该步骤相应的化学方程式_______ 。
(2)溶浸后的溶液中,铝元素以 的形态存在。写出“沉铝”时使铝元素恰好沉淀完全的离子方程式为
的形态存在。写出“沉铝”时使铝元素恰好沉淀完全的离子方程式为_______ 。
(3)“沉钼”后,滤液X的溶质主要是_______ (写化学式)。
(4)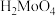 在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是
在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是_______ 。
(5)已知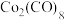 中
中 元素的化合价为0价。
元素的化合价为0价。
①在“反应”中的氧化剂和还原剂物质的量之比为_______ 。
② 是一种可以循环利用的物质,
是一种可以循环利用的物质, 是
是_______ (填化学式)。
 、
、 、
、 。一种回收利用废催化剂的工艺流程如下图。
。一种回收利用废催化剂的工艺流程如下图。 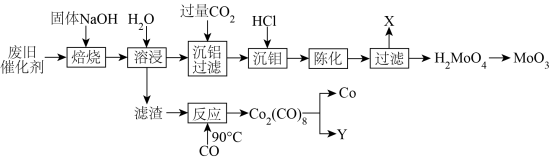
(1)“焙烧”时,
 转化为
转化为 ,
, 中Mo的化合价为
中Mo的化合价为(2)溶浸后的溶液中,铝元素以
 的形态存在。写出“沉铝”时使铝元素恰好沉淀完全的离子方程式为
的形态存在。写出“沉铝”时使铝元素恰好沉淀完全的离子方程式为(3)“沉钼”后,滤液X的溶质主要是
(4)
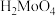 在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是
在水中呈胶状,陈化是指将溶液静止存放一段时间,陈化的作用是(5)已知
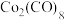 中
中 元素的化合价为0价。
元素的化合价为0价。①在“反应”中的氧化剂和还原剂物质的量之比为
②
 是一种可以循环利用的物质,
是一种可以循环利用的物质, 是
是
您最近一年使用:0次
【推荐3】【化学一选修2:化学与技术】三氧化二镍(Ni2O3)是一种重要的蓄电池材料。工业上利用镍废料(镍、铁、钙、镁合金为主)制取草酸镍晶体(NiC2O4-2H2O),再高温煅烧草酸镍晶体制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水。下列工艺流程示意图如下;
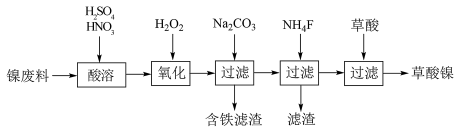
回答下列问题
(1)为提高酸溶操作中镍废料的转化率,可采取的措施有_________ (答出三条)。
(2)加入H2O2发生的主要反应的离子方程式为______________ 。
(3)加入NH4F后除掉的杂质是____
(4)上述反应制出的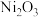 ,可用于镍氢电池的原料,在碱性条件下,镍氢电池的反应为
,可用于镍氢电池的原料,在碱性条件下,镍氢电池的反应为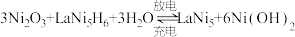 。该电池放电时,负极电极反应式为
。该电池放电时,负极电极反应式为___________________ 。
(5)工业上还可用电解法制取Ni2O3。用NaOH溶液调节NiCl2溶液的pH至7.5,加入适量Na2SO4后采用惰性电极电解。电解过程中产生的Cl2有80%在弱碱性条件下生成ClO-,再把二价镍氧化为三价镍。当amol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为____ 。电解法制取Ni2O3的实际过程中,先获得一种结晶水合物,已知含1 mol Ni的该结晶水合物中含有0.5 mol结晶水。取该化合物20.2 g进行充分加热,获得Ni2O3固体和0.2 mol水,则该结晶水合物的化学式为_______________ .

回答下列问题
(1)为提高酸溶操作中镍废料的转化率,可采取的措施有
(2)加入H2O2发生的主要反应的离子方程式为
(3)加入NH4F后除掉的杂质是
(4)上述反应制出的
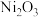 ,可用于镍氢电池的原料,在碱性条件下,镍氢电池的反应为
,可用于镍氢电池的原料,在碱性条件下,镍氢电池的反应为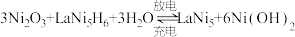 。该电池放电时,负极电极反应式为
。该电池放电时,负极电极反应式为(5)工业上还可用电解法制取Ni2O3。用NaOH溶液调节NiCl2溶液的pH至7.5,加入适量Na2SO4后采用惰性电极电解。电解过程中产生的Cl2有80%在弱碱性条件下生成ClO-,再把二价镍氧化为三价镍。当amol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为
您最近一年使用:0次



