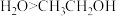下列描述中正确的是
| A.CS2为V形的极性分子 | B. 的空间构型为平面三角形 的空间构型为平面三角形 |
C.SiF4和 的中心原子均为sp3杂化 的中心原子均为sp3杂化 | D.SF6中有4对完全相同的成键电子对 |
更新时间:2022-04-06 13:45:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某种含铜微粒可用于汽车尾气脱氮的催化剂,催化机理如图甲,金属铜的晶胞如图乙,下列说法不正确的是
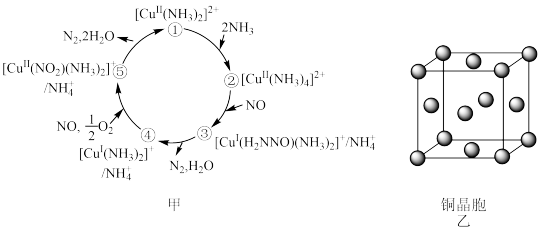

| A.图甲中所有铜的配合物中铜的配位数有2,3,4三种情况 |
B.图甲配合物 中 中 和配位原子形成的空间结构名称为V形 和配位原子形成的空间结构名称为V形 |
| C.图乙铜的晶胞中含有的铜原子数为4 |
| D.图乙铜的晶胞中与Cu距离最近且相等的Cu原子数为12 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】电催化是利用催化剂电极进行电解以实现物质转化的前沿方法.使用单原子催化剂电催化将 转化为CO的部分机理如下所示.下列说法不正确的是
转化为CO的部分机理如下所示.下列说法不正确的是
 转化为CO的部分机理如下所示.下列说法不正确的是
转化为CO的部分机理如下所示.下列说法不正确的是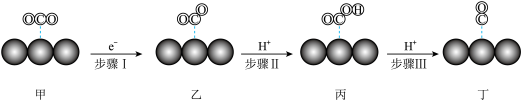
| A.该催化过程在电解池的阴极进行 | B. 的空间构型为直线形 的空间构型为直线形 |
| C.甲、乙中的C原子的杂化类型相同 | D.催化剂原子吸附 中带正电的部分 中带正电的部分 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】离子液体广泛应用于科研和生产中。某离子液体结构如下图,其中阳离子有类似苯环的特殊稳定性,下列说法错误的是
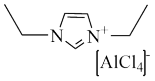

| A.阳离子中C有两种不同的杂化方式 | B.阳离子中存在大π键 |
| C.阳离子中所有C、N原子不可能共面 | D.阴离子中含有配位键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】科学家成功将 转化为类似
转化为类似 结构的共价晶体,下列说法正确的是
结构的共价晶体,下列说法正确的是
 转化为类似
转化为类似 结构的共价晶体,下列说法正确的是
结构的共价晶体,下列说法正确的是A. 共价晶体易升华 共价晶体易升华 |
B. 共价晶体硬度小于 共价晶体硬度小于 |
C. 共价晶体中C原子的杂化方式为sp 共价晶体中C原子的杂化方式为sp |
D. 由分子晶体转化为共价晶体是化学变化 由分子晶体转化为共价晶体是化学变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】 和
和 均可发生水解反应,其中
均可发生水解反应,其中 的水解机理示意图如下:
的水解机理示意图如下:
 和
和 均可发生水解反应,其中
均可发生水解反应,其中 的水解机理示意图如下:
的水解机理示意图如下: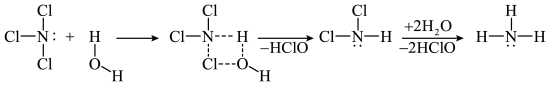
A. 和 和 均为极性分子 均为极性分子 | B. 和 和 中的 中的 均为 均为 杂化 杂化 |
C. 和 和 的水解反应机理相同 的水解反应机理相同 | D.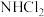 和 和 均能与 均能与 形成氢键 形成氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】BP晶体超硬、耐磨,是耐高温飞行器的红外增透的理想材料,其合成途径之一为:BBr3+PBr3+3H2 BP+6HBr。BP立方晶胞结构如图所示(已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标)
BP+6HBr。BP立方晶胞结构如图所示(已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标)

下列说法正确的是
 BP+6HBr。BP立方晶胞结构如图所示(已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标)
BP+6HBr。BP立方晶胞结构如图所示(已知:以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标)
下列说法正确的是
| A.BBr3是由极性键构成的极性分子 |
| B.PBr3分子的空间构型是平面三角形 |
| C.BP属于分子晶体 |
D.图中若原子1的坐标为( , , ,0),则原子2的坐标为( ,0),则原子2的坐标为( , , , , ) ) |
您最近一年使用:0次

 原子的价电子排布式为
原子的价电子排布式为
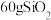 晶体中有
晶体中有 分子
分子 在水溶液中水解的离子方程式:
在水溶液中水解的离子方程式: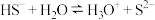
 和
和 中
中 均为
均为 杂化
杂化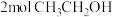 与足量Na反应置换出
与足量Na反应置换出 ,乙醇分子中断裂氢氧键
,乙醇分子中断裂氢氧键