现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外电子有六种空间运动状态,其最高能层容纳的电子数是核外电子总数的 ;E元素基态原子的未成对电子是第四周期最多的;F元素正三价离子的3d轨道为半充满状态;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子的未成对电子是第四周期最多的;F元素正三价离子的3d轨道为半充满状态;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)C元素的电子排布图为___ 。
(2)D元素与氯元素形成的简单化合物的电子式为____ 。
(3)E元素基态原子的价层电子的电子排布式为____ 。
(4)F3+的常见检验方法为取其溶液适量于试管中,滴入____ 溶液形成某种带颜色的配合物。
(5)G元素可能的性质____ 。
 ;E元素基态原子的未成对电子是第四周期最多的;F元素正三价离子的3d轨道为半充满状态;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子的未成对电子是第四周期最多的;F元素正三价离子的3d轨道为半充满状态;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)C元素的电子排布图为
(2)D元素与氯元素形成的简单化合物的电子式为
(3)E元素基态原子的价层电子的电子排布式为
(4)F3+的常见检验方法为取其溶液适量于试管中,滴入
(5)G元素可能的性质
| A.其单质可作为半导体材料 | B.其电负性大于磷 |
| C.其原子半径大于锗 | D.其第一电离能小于硒 |
更新时间:2022-09-20 00:57:04
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】根据物质结构和元素周期表的相关知识回答下列问题:
I.用A+、B-、C2-、D表示含有18个电子的离子或分子。请填空:
(1)A元素是__________ ,B元素是__________ ,C元素是__________ 。(用元素符号表示)
(2)物质D由两种元素组成,每个分子中含有三个原子,其分子式是________ ,电子式是______________ 。
Ⅱ.X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
回答下列问题:
(1)Y在元素周期表中的位置为______________ ,
(2)上述元素的最高价氧化物对应的水化物酸性最强的是______________ (写化学式),非金属气态氢化物还原性最强的是______________ (写化学式)。
(3)Y和Z的两元素之间形成的原子个数比为1:1的化合物的电子式为______________ 。
I.用A+、B-、C2-、D表示含有18个电子的离子或分子。请填空:
(1)A元素是
(2)物质D由两种元素组成,每个分子中含有三个原子,其分子式是
Ⅱ.X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
回答下列问题:
(1)Y在元素周期表中的位置为
(2)上述元素的最高价氧化物对应的水化物酸性最强的是
(3)Y和Z的两元素之间形成的原子个数比为1:1的化合物的电子式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】如表为四种短周期元素的相关信息
回答下列问题(注:涉及元素的均要用对应元素的元素符号书写作答)
(1)Y元素的最简单氢化物的空间构型是___ 。
(2)Z、Q、R相比,其原子半径由大到小的顺序是___ 。
(3)最高价的R与Z元素组成的化合物中R原子的杂化方式为___ ,其中R在周期表中的位置是__ ,R的基态原子电子排布式为___ 。
(4)与O3分子互为等电子体的一种分子为___ ,阴离子为__ 。
(5)Y与R相比,非金属性较强的是___ ,能证明这一结论的事实是___ 。(用化学方程式表示)
| 元素 | 元素的相关信息 |
| Y | 原子最外层电子数是次外层电子数的2倍 |
| Z | 地壳中含量最多的元素 |
| Q | 短周期中金属性最强 |
| R | 常温下,R的单质是淡黄色固体,常在火山喷口附近沉积 |
(1)Y元素的最简单氢化物的空间构型是
(2)Z、Q、R相比,其原子半径由大到小的顺序是
(3)最高价的R与Z元素组成的化合物中R原子的杂化方式为
(4)与O3分子互为等电子体的一种分子为
(5)Y与R相比,非金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】短周期五种主族元素合A、B、C、D、E的原子序数依次增大。A、C的单质在常温下呈气态;C原子最外层电子数是其电子层数的3倍;B是形成有机物的主要元素;D能在BC2中燃烧重新生成B单质,其氧化物是一种耐高温材料;E和C位于同主族。回答下列问题:
(1)写出 的电子式:
的电子式:___________ ;
(2)D、E的简单离子中,离子半径大小关系是:_______ (用离子符号表示);
(3)D的单质能在BC2气体中燃烧,写出化学方程式:____________ ;
(4) 碱性燃料电池放电效率高,其正极反应式为:
碱性燃料电池放电效率高,其正极反应式为:_____________ 。
(1)写出
 的电子式:
的电子式:(2)D、E的简单离子中,离子半径大小关系是:
(3)D的单质能在BC2气体中燃烧,写出化学方程式:
(4)
 碱性燃料电池放电效率高,其正极反应式为:
碱性燃料电池放电效率高,其正极反应式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】①②③④⑤五种元素,在元素周期表中的位置如图所示。回答下列问题:

(1)①②③④⑤五种元素中,写出属于金属的元素在周期表中的位置_______ 。
(2)元素①和③可以形成众多的化合物,其中最简单的是(写化学式)____________ ,该化合物中,化学键的类型为 _________ (填“离子键”或“共价键”)。
(3)写出元素④的核外电子排布式__________ ,该元素的氢化物的电子式是_______ 。
(4)写出元素⑤最外层轨道表示式__________ ,其单质在常温下为黄绿色的气体,实验中可以用NaOH溶液吸收,反应的离子方程式为___________________ 。
(5)写出与氯元素同周期的元素形成的简单离子中半径最小的离子的化学式_________ ,该元素的最高价氧化物的水化物在强酸环境下的电离方程式是_________________ 。

(1)①②③④⑤五种元素中,写出属于金属的元素在周期表中的位置
(2)元素①和③可以形成众多的化合物,其中最简单的是(写化学式)
(3)写出元素④的核外电子排布式
(4)写出元素⑤最外层轨道表示式
(5)写出与氯元素同周期的元素形成的简单离子中半径最小的离子的化学式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】含锌废料具有毒性,若随意排放会对环境和人体造成较大的危害。现有一种湿法回收含锌废料(主要成分为 ,还含有少量
,还含有少量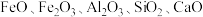 和
和 )生产硫酸锌晶体(
)生产硫酸锌晶体( )的工艺流程如下:
)的工艺流程如下:

查阅资料:①几种离子形成氢氧化物沉淀时的 如下:
如下:
② 时,
时,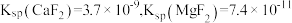 。
。
请回答下列问题:
(1)基态锌原子的价电子排布图为__________________ 。
(2)滤渣a的成分是__________________ (写化学式)。
(3)“氧化除杂”时,加入 的目的是
的目的是___________________________ ,“氧化除杂”过程Fe2+发生反应的总离子方程式为___________________________ 。
(4)25℃时,“脱钙镁”后的滤液中,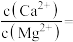
_________ 。
(5)滤渣c与浓 反应所得某一产物,可进入“
反应所得某一产物,可进入“_________ ”(填“酸浸”“氧化除杂”或“脱钙镁”)工序循环利用。
(6)“一系列操作”有_________ 、_________ 过滤、洗涤、干燥。
 ,还含有少量
,还含有少量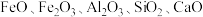 和
和 )生产硫酸锌晶体(
)生产硫酸锌晶体( )的工艺流程如下:
)的工艺流程如下:
查阅资料:①几种离子形成氢氧化物沉淀时的
 如下:
如下:待沉淀离子 |
|
|
|
|
|
开始沉淀的 | 6.2 | 6.5 | 1.5 | 3.2 | 9.3 |
沉淀完全的 | 8.1 | 9.7 | 3.7 | 5.3 | 10.8 |
 时,
时,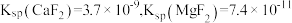 。
。请回答下列问题:
(1)基态锌原子的价电子排布图为
(2)滤渣a的成分是
(3)“氧化除杂”时,加入
 的目的是
的目的是(4)25℃时,“脱钙镁”后的滤液中,
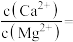
(5)滤渣c与浓
 反应所得某一产物,可进入“
反应所得某一产物,可进入“(6)“一系列操作”有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】金属钠及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)基态Na原子的价层电子轨道表示式为_______ 。
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式如下:2NaCl(l)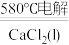 2Na(l)+Cl2(g)。加入CaCl2的目的是
2Na(l)+Cl2(g)。加入CaCl2的目的是_______ 。
(3)Na2O2的电子式为______ 。在25℃和101kPa时,Na与O2反应生成1molNa2O2放热510.9kJ,写出该反应的热化学方程式:_______ 。
(4)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过______ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
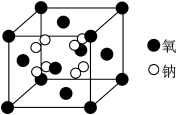
(5)钠的某氧化物晶胞如图,图中所示钠离子全部位于晶胞内。由晶胞图判断该氧化物的化学式为_______ 。晶胞参数为apm,则该晶体的密度为______ g/cm3。(列计算式)
(1)基态Na原子的价层电子轨道表示式为
(2)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式如下:2NaCl(l)
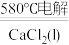 2Na(l)+Cl2(g)。加入CaCl2的目的是
2Na(l)+Cl2(g)。加入CaCl2的目的是(3)Na2O2的电子式为
(4)采用空气和Na为原料可直接制备Na2O2。空气与熔融金属Na反应前需依次通过
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.KMnO4溶液
(5)钠的某氧化物晶胞如图,图中所示钠离子全部位于晶胞内。由晶胞图判断该氧化物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】W、R、X、Y、Z是原子序数依次增大的前四周期元素(只有Z是第四周期),其元素性质或原子结构如表:
回答下列问题:
(1)W、Y的最高价氧化物对应的水化物酸性更强的是___________ (填化学式)。
(2)W、R、X的简单氢化物中,三元素的原子的轨道杂化方式均为___________ ,键角由大到小的顺序是___________ (用对应的分子式表示),原因是___________ 。
(3)Z的价电子排布式为___________ ,Z位于元素周期表第___________ 族,属于___________ 区。
(4)R、X和Z元素的电负性由大到小的顺序是___________ (填元素符号)。
| 元素 | 元素性质或原子结构 |
| W | 基态原子L能层所有能级上电子数相同 |
| R | 第二周期元素基态原子中未成对电子最多 |
| X | 基态原子核外s能级上电子总数与p能级上电子总数相等,且第一电离能低于同周期相邻元素 |
| Y | 其价电子中,在不同形状的原子轨道中运动的电子数相等 |
| Z | 属于副族元素,且最外层只有1个电子,其他内层各能级所有轨道电子均成对 |
(1)W、Y的最高价氧化物对应的水化物酸性更强的是
(2)W、R、X的简单氢化物中,三元素的原子的轨道杂化方式均为
(3)Z的价电子排布式为
(4)R、X和Z元素的电负性由大到小的顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】砷化铝(AlAs)常用作光谱分析试剂和制备电子组件的原料,是一种新型半导体材料。回答下列问题:
(1)基态As原子的核外价电子排布图为_______ ;第一电离能I1(As)_______ I1(Se) (填“大于”或“小于”),其原因是_______ 。
(2)As4S4的分子结构中均为单键,且每个原子最外层均满足8e-稳定结构,则该分子中所含共价键数目为_______ ;分子中As、S原子的杂化轨道类型分别为_______ 、_______ 。
(3)AlF3的熔点约为1 040 ℃,AlCl3的熔点为194 ℃,其晶体类型分别是_______ 、_______ 。
(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止H2O2刻蚀液与下层GaAs(砷化镓)反应。

已知AlAs的立方晶胞如图2所示,其中As的配位数为_______ ;该晶体密度为ρ g·cm-3,设NA为阿伏加德罗常数的值,晶胞参数为_______ pm。

(1)基态As原子的核外价电子排布图为
(2)As4S4的分子结构中均为单键,且每个原子最外层均满足8e-稳定结构,则该分子中所含共价键数目为
(3)AlF3的熔点约为1 040 ℃,AlCl3的熔点为194 ℃,其晶体类型分别是
(4)高纯AlAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图1所示,其中的致密保护膜可阻止H2O2刻蚀液与下层GaAs(砷化镓)反应。

已知AlAs的立方晶胞如图2所示,其中As的配位数为

您最近一年使用:0次
【推荐3】根据信息回答下列问题:
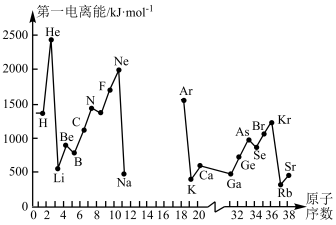
A.第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的最低能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
B.不同元素的原子在分子内吸引电子的能力大小可用数值表示,该数值称为电负性。一般认为:如果两个成键原子间的电负性差值大于1.7,原子之间通常形成离子键;如果两个成键原子间的电负性差值小于1.7,通常形成共价键。下表是某些元素的电负性值:

(1)认真分析信息A图中同周期元素第一电离能的变化规律,推断第三周期Na~Ar这几种元素中,Al的第一电离能的大小范围为______ <Al<________ (填元素符号)。
(2)从信息A图中分析可知,同一主族元素原子的第一电离能I1的变化规律是______________ :
(3)信息A图中第一电离能最小的元素在周期表中的位置是_______ 周期__________ 族。
(4)根据对角线规则,Be、Al元素最高价氧化物对应水化物的性质相似,它们都具有_______ 性,其中Be(OH)2显示这种性质的离子方程式是____________ 。
(5)通过分析电负性值的变化规律,确定Mg元素的电负性值的最小范围_________ 。
(6)请归纳元素的电负性和金属性、非金属性的关系是__________ 。
(7)从电负性角度,判断AlCl3是离子化合物还是共价化合物___________ ,说出理由并写出判断的方法_________ 。
A.第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的最低能量。下图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。

B.不同元素的原子在分子内吸引电子的能力大小可用数值表示,该数值称为电负性。一般认为:如果两个成键原子间的电负性差值大于1.7,原子之间通常形成离子键;如果两个成键原子间的电负性差值小于1.7,通常形成共价键。下表是某些元素的电负性值:

(1)认真分析信息A图中同周期元素第一电离能的变化规律,推断第三周期Na~Ar这几种元素中,Al的第一电离能的大小范围为
(2)从信息A图中分析可知,同一主族元素原子的第一电离能I1的变化规律是
(3)信息A图中第一电离能最小的元素在周期表中的位置是
(4)根据对角线规则,Be、Al元素最高价氧化物对应水化物的性质相似,它们都具有
(5)通过分析电负性值的变化规律,确定Mg元素的电负性值的最小范围
(6)请归纳元素的电负性和金属性、非金属性的关系是
(7)从电负性角度,判断AlCl3是离子化合物还是共价化合物
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E、F为原子序数依次增大的六种元素,其中A、B、C、D、E为短周期元素,F为第四周期元素。已知:A原子核外电子只有一种自旋取向;B元素原子核外有三个未成对电子;C原子的第一至第四电离能数据分别为: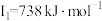 、
、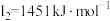 、
、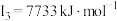 、
、 ;D原子核外最外层所有p轨道均为半充满;E元素的族序数与周期序数的差为4;F元素原子的最外层只有一个电子,其次外层的所有电子均成对。
;D原子核外最外层所有p轨道均为半充满;E元素的族序数与周期序数的差为4;F元素原子的最外层只有一个电子,其次外层的所有电子均成对。
回答下列问题:
(1)写出A的元素符号_______ ,写出C元素在周期表中位置_______ ;
(2)B元素基态原子的轨道表示式为_______ ,其中电子占据最高能级的电子云轮廓图为_______ 形
(3)比较D、E的电负性:_______ >_______ (用元素符号表示);
(4)写出元素F的基态原子简化电子排布式_______ ;
(5)B、C、D三种元素的原子半径由大到小的顺序_______ (用元素符号表示)。
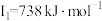 、
、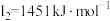 、
、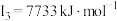 、
、 ;D原子核外最外层所有p轨道均为半充满;E元素的族序数与周期序数的差为4;F元素原子的最外层只有一个电子,其次外层的所有电子均成对。
;D原子核外最外层所有p轨道均为半充满;E元素的族序数与周期序数的差为4;F元素原子的最外层只有一个电子,其次外层的所有电子均成对。回答下列问题:
(1)写出A的元素符号
(2)B元素基态原子的轨道表示式为
(3)比较D、E的电负性:
(4)写出元素F的基态原子简化电子排布式
(5)B、C、D三种元素的原子半径由大到小的顺序
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有五种短周期元素,它们的结构、性质等信息如下表所示:
请根据表中信息回答下列问题。
(1)A元素原子的核外电子排布式为___ 。
(2)B元素在元素周期表中的位置为___ ;离子半径:B___ (填“>”或“<”)A。
(3)C元素原子的轨道表示式为___ ,其原子核外有___ 个未成对电子,能量最高的电子排布在轨道上,该轨道呈___ 形。
(4)D元素原子的核外电子排布式为___ ,D-的结构示意图为___ 。
(5)C、E元素的第一电离能的大小关系是___ (用元素符号表示)。
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是CD3___ (用元素符号表示),CD3与水反应后的产物是___ (填化学式)。
| 元素 | 结构、性质等信息 |
| A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时常用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的杀菌消毒剂 |
| E | 元素原子的L电子层上有2对成对电子 |
(1)A元素原子的核外电子排布式为
(2)B元素在元素周期表中的位置为
(3)C元素原子的轨道表示式为
(4)D元素原子的核外电子排布式为
(5)C、E元素的第一电离能的大小关系是
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是CD3
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E都是短周期元素,原子序数依次增大,B、C同周期,A、D同主族。A、B能形成两种常温下的液态化合物甲和乙,原子个数比分别为2∶1和1∶1。根据以上信息回答下列问题:
(1)甲、乙两分子中含有非极性共价键的物质的电子式是________ ,C元素在周期表中的位置是_____ 。
(2)C和D的离子中,半径较小的是____ (离子符号),以上元素中电负性最大的是____ (元素符号)
(3)常温下将D的单质投入甲中,待D消失后再向上述溶液中加入E的固体单质,此时发生反应的化学方程式是______________ 。
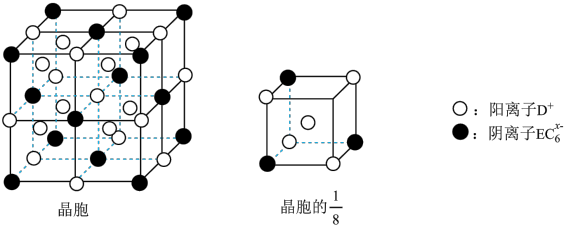
(4)C、D、E可组成离子化合物DxEC6,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如下图所示,阳离子D+(用○表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是_________ 。
(1)甲、乙两分子中含有非极性共价键的物质的电子式是
(2)C和D的离子中,半径较小的是
(3)常温下将D的单质投入甲中,待D消失后再向上述溶液中加入E的固体单质,此时发生反应的化学方程式是
(4)C、D、E可组成离子化合物DxEC6,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如下图所示,阳离子D+(用○表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是

您最近一年使用:0次








