下列事实中,不能用勒·夏特列原理加以解释的是
| A.缩小容器的体积,由H2(g)、I2(g)、HI(g)组成的平衡体系颜色变深 |
| B.浓氨水中加入氢氧化钠固体时产生较多的刺激性气味的气体 |
| C.合成氨时选择加压作为反应条件 |
| D.新制的氯水在光照下颜色变浅 |
更新时间:2022-09-26 19:22:55
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】CuCl2溶液中存在如下平衡:[Cu(H2O)4]2+(蓝色)+4Cl- [CuCl4]2-(黄色)+4H2O △H>0。下列可使黄绿色的CuCl2溶液变成蓝色的方法是
[CuCl4]2-(黄色)+4H2O △H>0。下列可使黄绿色的CuCl2溶液变成蓝色的方法是
 [CuCl4]2-(黄色)+4H2O △H>0。下列可使黄绿色的CuCl2溶液变成蓝色的方法是
[CuCl4]2-(黄色)+4H2O △H>0。下列可使黄绿色的CuCl2溶液变成蓝色的方法是| A.升温 | B.加NaCl(s) | C.加压 | D.加AgNO3(s) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】氯水中存在平衡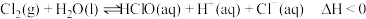 ,下列说法正确的是
,下列说法正确的是
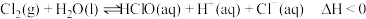 ,下列说法正确的是
,下列说法正确的是A.升高温度,氯水中的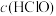 增大 增大 |
| B.氯水中加入少量醋酸钠固体,平衡不发生移动 |
C.该平衡可解释用饱和食盐水除去氯气中混有的 气体的原因 气体的原因 |
D.取两份氯水,分别滴加 溶液和淀粉 溶液和淀粉 溶液,若前者产生白色沉淀,后者溶液变蓝色,可以证明上述反应为可逆反应 溶液,若前者产生白色沉淀,后者溶液变蓝色,可以证明上述反应为可逆反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的是
A.恒温恒压容器中,反应A(s)+2B(g) 2C(g)达平衡后,再通入气体C,平衡不移动,气体B的浓度保持不变 2C(g)达平衡后,再通入气体C,平衡不移动,气体B的浓度保持不变 |
| B.1molN2和3molH2反应达到平衡时H2转化率为10%,放出的热量为Q1;在相同温度和压强下,当2molNH3分解为N2和H2的转化率为10%时,吸收的热量为Q2,Q2≠Q1 |
C.恒温下,向密闭容器中加入NH2COONH4固体,反应NH2COONH4(s) 2NH3(g)+CO2(g)达平衡后,缩小容器的容积,再达平衡时,CO2的浓度不变 2NH3(g)+CO2(g)达平衡后,缩小容器的容积,再达平衡时,CO2的浓度不变 |
D.恒温恒容容器中,N2(g)+3H2(g) 2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大 2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度下,体积一定的密闭容器中发生如下可逆反应:2X(g)+Y(s) 3Z(g)△H=+QkJ/mol,一段时间后达到平衡状态,下列说法正确的是
3Z(g)△H=+QkJ/mol,一段时间后达到平衡状态,下列说法正确的是
 3Z(g)△H=+QkJ/mol,一段时间后达到平衡状态,下列说法正确的是
3Z(g)△H=+QkJ/mol,一段时间后达到平衡状态,下列说法正确的是| A.消耗2molX同时生成3molZ,说明达到了平衡状态 |
| B.加入少量的Y正反应速率加快,平衡向正反应方向移动 |
| C.若Z为有色气体,此时充入少量Z,则平衡向左移动,颜色最终比原平衡的深 |
| D.加入少量的X,Q变大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用勒夏特列原理解释的是
A.溴水中有化学平衡Br2+H2O HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 HBr+HBrO,当加入硝酸银溶液后,溶液颜色变浅 |
| B.合成氨反应(正反应为放热反应),为提高氨的产率,理论上应采取降低温度的措施 |
C.反应CO(g)+NO2(g) CO2(g)+NO(g)(正反应放热),平衡后,升高温度体系颜色变深 CO2(g)+NO(g)(正反应放热),平衡后,升高温度体系颜色变深 |
D.对于2HI(g) H2(g)+I2(g),达到平衡后,缩小容器容积可使体系颜色变深 H2(g)+I2(g),达到平衡后,缩小容器容积可使体系颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关说法正确的是
A.可以用勒夏特列原理解释2NO2(g) N2O4(g)体系加压后颜色变深 N2O4(g)体系加压后颜色变深 |
B.N2(g)+3H2(g) 2NH3(g) ΔH<0可通过加压方式增大其平衡常数 2NH3(g) ΔH<0可通过加压方式增大其平衡常数 |
| C.合成氨时将氨液化分离,可提高原料的转化率 |
| D.工业上合成氨,其他条件相同时恒温恒容比恒温恒压条件下的N2的转化率大 |
您最近一年使用:0次

 KCrO2溶液
KCrO2溶液 K2Cr2O4溶液
K2Cr2O4溶液 K2Cr2O7溶液
K2Cr2O7溶液 +2H+
+2H+ +H2O。KCrO2溶液绿色,K2CrO4溶液黄色,K2Cr2O7溶液橙红色。
+H2O。KCrO2溶液绿色,K2CrO4溶液黄色,K2Cr2O7溶液橙红色。 ,平衡时测得C的浓度为
,平衡时测得C的浓度为 。保持温度不变,将容器的容积压缩到原来的一半,再次达到平衡时,测得C的浓度为
。保持温度不变,将容器的容积压缩到原来的一半,再次达到平衡时,测得C的浓度为 。下列有关判断正确的是
。下列有关判断正确的是 N2O4(g) ΔH<0, 增大压强,下列说法正确的是( )
N2O4(g) ΔH<0, 增大压强,下列说法正确的是( )

