研究 之间的转化具有重要意义。
之间的转化具有重要意义。
(1)已知:
 ,将一定量
,将一定量 气体充入恒容的密闭容器中,控制反应温度为
气体充入恒容的密闭容器中,控制反应温度为 。
。
①该反应自发进行的条件是_______ 。
②下列不能 作为反应达到平衡的判据是_______ 。
A. 的物质的量不变 B.
的物质的量不变 B. C.
C. 不变
不变
D.容器内气体的平均相对分子质量不变 E.容器内颜色不变
③ 时刻反应达到平衡,混合气体平衡总压强为p,
时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为
气体的平衡转化率为 ,则反应
,则反应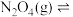
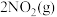 的平衡常数
的平衡常数
_______ (用含有 的表达式表示。对于气相反应,用某组分B的平衡压强
的表达式表示。对于气相反应,用某组分B的平衡压强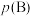 代替物质的量浓度
代替物质的量浓度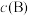 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如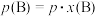 ,p为平衡总压强,
,p为平衡总压强,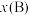 为平衡系统中B的物质的量分数)。
为平衡系统中B的物质的量分数)。
(2) 氧化反应:
氧化反应: 分两步基元反应进行:
分两步基元反应进行:
I.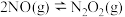
 快反应
快反应
II.
 慢反应
慢反应
已知: 。
。
①在下图中绘制“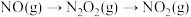 ”的“能量~反应过程”示意图
”的“能量~反应过程”示意图_______ 。

② 法是工业上消除氮氧化物的常用方法,反应原理为:
法是工业上消除氮氧化物的常用方法,反应原理为: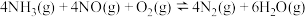
 。消除汽车尾气中的
。消除汽车尾气中的 时,可用尿素[
时,可用尿素[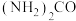 ]还原NO,既安全又高效,且产物都是空气中含有的成分。与
]还原NO,既安全又高效,且产物都是空气中含有的成分。与 法相比,等物质的量的尿素与氨气可消除的
法相比,等物质的量的尿素与氨气可消除的 物质的量之比为
物质的量之比为_______ 。(不考虑副反应)
 之间的转化具有重要意义。
之间的转化具有重要意义。(1)已知:

 ,将一定量
,将一定量 气体充入恒容的密闭容器中,控制反应温度为
气体充入恒容的密闭容器中,控制反应温度为 。
。①该反应自发进行的条件是
②下列
A.
 的物质的量不变 B.
的物质的量不变 B. C.
C. 不变
不变D.容器内气体的平均相对分子质量不变 E.容器内颜色不变
③
 时刻反应达到平衡,混合气体平衡总压强为p,
时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为
气体的平衡转化率为 ,则反应
,则反应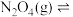
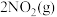 的平衡常数
的平衡常数
 的表达式表示。对于气相反应,用某组分B的平衡压强
的表达式表示。对于气相反应,用某组分B的平衡压强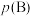 代替物质的量浓度
代替物质的量浓度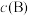 也可表示平衡常数,记作
也可表示平衡常数,记作 ,如
,如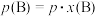 ,p为平衡总压强,
,p为平衡总压强,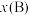 为平衡系统中B的物质的量分数)。
为平衡系统中B的物质的量分数)。(2)
 氧化反应:
氧化反应: 分两步基元反应进行:
分两步基元反应进行:I.
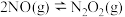
 快反应
快反应II.

 慢反应
慢反应已知:
 。
。①在下图中绘制“
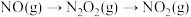 ”的“能量~反应过程”示意图
”的“能量~反应过程”示意图
②
 法是工业上消除氮氧化物的常用方法,反应原理为:
法是工业上消除氮氧化物的常用方法,反应原理为: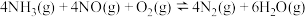
 。消除汽车尾气中的
。消除汽车尾气中的 时,可用尿素[
时,可用尿素[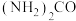 ]还原NO,既安全又高效,且产物都是空气中含有的成分。与
]还原NO,既安全又高效,且产物都是空气中含有的成分。与 法相比,等物质的量的尿素与氨气可消除的
法相比,等物质的量的尿素与氨气可消除的 物质的量之比为
物质的量之比为
更新时间:2022-10-11 20:59:05
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
真题
解题方法
【推荐1】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
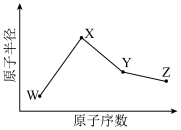
(1) X位于元素周期表中第______ 周期第______ 族;W的基态原子核外有_______ 个未成对电子。
(2)X的单质子和Y的单质相比,熔点较高的是______ (写化学式);Z的气态氢化物和溴化氢相比,较稳定的是_________ (写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是_____________ 。
(4)在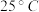 、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是
、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是_____________ 。

(1) X位于元素周期表中第
(2)X的单质子和Y的单质相比,熔点较高的是
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
(4)在
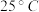 、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是
、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】与氨气相关的化学变化是氮循环和转化的重要一环,对生产、生活有重要的价值。
(1)下图转化途径中属于“固氮”的是___________。

(2)合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中 表示物质吸附在催化剂表面时的状态)
表示物质吸附在催化剂表面时的状态)

①由图可知合成氨反应 的
的
___________  ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤___________ 。(填写编号)
②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是___________ 。
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用 的燃烧反应(
的燃烧反应( )能设计成燃料电池,其工作原理如图所示。电极
)能设计成燃料电池,其工作原理如图所示。电极 为
为___________ (选填“正”或“负”)极;电极 的电极反应式为
的电极反应式为___________ ;当正负极共消耗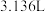 (标准状况)气体时,通过负载的电子数为
(标准状况)气体时,通过负载的电子数为___________ 个。

合成氨厂的可用于合成重要化工原料 ,主要反应为:
,主要反应为: ,向两个容积固定为
,向两个容积固定为 的密闭容器中分别充入比例相同,但总量不同的
的密闭容器中分别充入比例相同,但总量不同的 和气体,
和气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
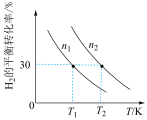
(4)①若 时,向容器中充入
时,向容器中充入 气体(
气体( 和
和 ),反应至
),反应至 时达到平衡,则
时达到平衡,则 内
内 的平均反应速率
的平均反应速率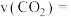
___________ 。
②由上图可判断该反应是___________ (选填“吸热”或“放热”)反应,在___________ (填“较高”或“较低”)温度下有利于该反应自发进行。
③判断图中 、
、 相对大小,并说明理由。
相对大小,并说明理由。___________ 。
(1)下图转化途径中属于“固氮”的是___________。

| A.④⑤⑥ | B.①③④ | C.①⑤⑦ | D.②⑧⑨ |
(2)合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中
 表示物质吸附在催化剂表面时的状态)
表示物质吸附在催化剂表面时的状态)
①由图可知合成氨反应
 的
的
 ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤②若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是
A.升高温度,使单位体积内活化分子百分数增加
B.增加反应物的浓度,使单位体积内活化分子百分数增加
C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加
D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加
(3)氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用
 的燃烧反应(
的燃烧反应( )能设计成燃料电池,其工作原理如图所示。电极
)能设计成燃料电池,其工作原理如图所示。电极 为
为 的电极反应式为
的电极反应式为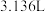 (标准状况)气体时,通过负载的电子数为
(标准状况)气体时,通过负载的电子数为
合成氨厂的可用于合成重要化工原料
 ,主要反应为:
,主要反应为: ,向两个容积固定为
,向两个容积固定为 的密闭容器中分别充入比例相同,但总量不同的
的密闭容器中分别充入比例相同,但总量不同的 和气体,
和气体, 的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
的平衡转化率与初始充入物质的量(n)、反应温度(T)的关系如下图所示。
(4)①若
 时,向容器中充入
时,向容器中充入 气体(
气体( 和
和 ),反应至
),反应至 时达到平衡,则
时达到平衡,则 内
内 的平均反应速率
的平均反应速率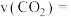
②由上图可判断该反应是
③判断图中
 、
、 相对大小,并说明理由。
相对大小,并说明理由。
您最近一年使用:0次
【推荐3】氨气在农业和国防工业都有很重要的作用,历史上诺贝尔化学奖曾经有3次颁给研究氮气与氢气合成氨气的化学家。
(1)下图表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答
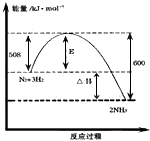
①写出氮气和氢气合成氨的热化学方程式:_____________ 。
②对于合成氨的反应下列说法正确的是_____________ (填编号)。
A.该反应在任意条件下都可以自发进行
B.加入催化剂,能使该反应的E和△H都减小
C.若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1>K2
D.该反应属于人工固氮
(2)现在普遍应用的工业合成氨的方法为N2+3H2 2NH3,是哈伯于1905年发明的,但此法达到平衡时反应物的转化率不高。
2NH3,是哈伯于1905年发明的,但此法达到平衡时反应物的转化率不高。
①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是_________________ 。
A.使用的更高效催化剂 B.升高温度
C.及时分离出氨气 D.充入氮气,增大氮气的浓度(保持容器体积不变)
②若在某温度下,2L的密闭容器中发生N2+3H2 2NH3的反应,左下图表示N2的物质的量随时间的变化曲线。用H2表示0~10min内该反应的平均速率v(H2)=
2NH3的反应,左下图表示N2的物质的量随时间的变化曲线。用H2表示0~10min内该反应的平均速率v(H2)=_______________ 。从11min起,压缩容器的体积为1L,则n(N2)的变化曲线为_____________________ 。
A. a B.b C.c D.d
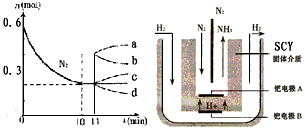
(3)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到500℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质里,用吸附在它内外表面上的金属钯多晶薄膜作电极,实现了常压、570℃条件下高转化率的电解法合成氮(装置如右上图)。则钯电极上的电极反应式是_____________________ 。
(1)下图表示了298K时氮气与氢气合成氨反应过程中的能量变化,据此请回答

①写出氮气和氢气合成氨的热化学方程式:
②对于合成氨的反应下列说法正确的是
A.该反应在任意条件下都可以自发进行
B.加入催化剂,能使该反应的E和△H都减小
C.若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1>K2
D.该反应属于人工固氮
(2)现在普遍应用的工业合成氨的方法为N2+3H2
 2NH3,是哈伯于1905年发明的,但此法达到平衡时反应物的转化率不高。
2NH3,是哈伯于1905年发明的,但此法达到平衡时反应物的转化率不高。①能使该反应的反应速率增大,且平衡向正反应方向移动的措施是
A.使用的更高效催化剂 B.升高温度
C.及时分离出氨气 D.充入氮气,增大氮气的浓度(保持容器体积不变)
②若在某温度下,2L的密闭容器中发生N2+3H2
 2NH3的反应,左下图表示N2的物质的量随时间的变化曲线。用H2表示0~10min内该反应的平均速率v(H2)=
2NH3的反应,左下图表示N2的物质的量随时间的变化曲线。用H2表示0~10min内该反应的平均速率v(H2)=A. a B.b C.c D.d

(3)随着对合成氨研究的发展,2001年两位希腊化学家提出了电解合成氨的方法,即在常压下把氢气和用氦气稀释的氮气,分别通入一个加热到500℃的电解池中,采用高质子导电性的SCY陶瓷(能传递H+)为介质里,用吸附在它内外表面上的金属钯多晶薄膜作电极,实现了常压、570℃条件下高转化率的电解法合成氮(装置如右上图)。则钯电极上的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】 是当今最主要的温室气体,全球各国都面临着严峻的减排压力。与此同时,
是当今最主要的温室气体,全球各国都面临着严峻的减排压力。与此同时, 也是一种“碳源”,转化为高附加值的燃料或化学品不仅可以解决
也是一种“碳源”,转化为高附加值的燃料或化学品不仅可以解决 的问题,还可变废为宝得到有用的化学品。
的问题,还可变废为宝得到有用的化学品。 加氢制甲醇是实现这一过程的理想方法之一。
加氢制甲醇是实现这一过程的理想方法之一。
主要发生以下反应:
反应I:

反应Ⅱ:

反应Ⅲ:

(1)已知部分化学键的键能如下表,则x=___________ 
(2)Fujta等学者开展了在Cu/ZnO催化剂上进行CO2+H2合成甲醇机理的研究。机理如下:

①过程2的化学方程式为___________ ;
②研究表明,过程3的活化能小但实际反应速率慢,是速控步骤,导致该步反应速率小的原因可能是___________
A.温度变化导致活化能增大
B. 的存在削弱了同一吸附位上
的存在削弱了同一吸附位上 的吸附
的吸附
C. 对该反应有阻碍作用
对该反应有阻碍作用
D.温度变化导致平衡常数减小
(3)一定温度下,在容积恒定的密闭容器中充入amol (g)和3amol
(g)和3amol (g),起始压强为
(g),起始压强为 在达到平衡,测得容器内的压强为起始的0.8倍,
在达到平衡,测得容器内的压强为起始的0.8倍, (g)的物质的量为0.6amol。在此条件下,
(g)的物质的量为0.6amol。在此条件下, 的转化率=
的转化率=________ ,反应Ⅲ的平衡常数
_______ (以分压表示,分压=总压×物质的量分数)
(4)甲醇水蒸气重整制氢(SRM)系统可作为电动汽车燃料电池的理想氢源。系统中的两个反应如下:
主反应: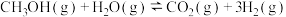

副反应: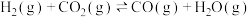

单位时间内, 转化率与CO生成率随温度的变化如图所示:
转化率与CO生成率随温度的变化如图所示:

升温过程中 实际反应转化率不断接近平衡状态转化率的原因是
实际反应转化率不断接近平衡状态转化率的原因是___________ ;温度升高,CO实际反应生成率并没有不断接近平衡状态的生成率,其原因可能是___________ 。
 是当今最主要的温室气体,全球各国都面临着严峻的减排压力。与此同时,
是当今最主要的温室气体,全球各国都面临着严峻的减排压力。与此同时, 也是一种“碳源”,转化为高附加值的燃料或化学品不仅可以解决
也是一种“碳源”,转化为高附加值的燃料或化学品不仅可以解决 的问题,还可变废为宝得到有用的化学品。
的问题,还可变废为宝得到有用的化学品。 加氢制甲醇是实现这一过程的理想方法之一。
加氢制甲醇是实现这一过程的理想方法之一。主要发生以下反应:
反应I:


反应Ⅱ:


反应Ⅲ:


(1)已知部分化学键的键能如下表,则x=

| 化学键 | H-H | H-O | C-H | 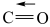 | C-O |
键能/( ) ) | 436 | 465 | 413 | 1076.8 | x |

①过程2的化学方程式为
②研究表明,过程3的活化能小但实际反应速率慢,是速控步骤,导致该步反应速率小的原因可能是
A.温度变化导致活化能增大
B.
 的存在削弱了同一吸附位上
的存在削弱了同一吸附位上 的吸附
的吸附C.
 对该反应有阻碍作用
对该反应有阻碍作用 D.温度变化导致平衡常数减小
(3)一定温度下,在容积恒定的密闭容器中充入amol
 (g)和3amol
(g)和3amol (g),起始压强为
(g),起始压强为 在达到平衡,测得容器内的压强为起始的0.8倍,
在达到平衡,测得容器内的压强为起始的0.8倍, (g)的物质的量为0.6amol。在此条件下,
(g)的物质的量为0.6amol。在此条件下, 的转化率=
的转化率=
(4)甲醇水蒸气重整制氢(SRM)系统可作为电动汽车燃料电池的理想氢源。系统中的两个反应如下:
主反应:
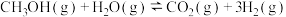

副反应:
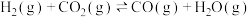

单位时间内,
 转化率与CO生成率随温度的变化如图所示:
转化率与CO生成率随温度的变化如图所示:
升温过程中
 实际反应转化率不断接近平衡状态转化率的原因是
实际反应转化率不断接近平衡状态转化率的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】雾霾中含有颗粒物(PM2.5)、氮氧化物(NOx)、CO等多种污染物。
(1)NO在空气中存在如下反应:2NO(g)+O2(g)⇌2NO2(g),上述反应分两步完成,其反应历程如图所示:(纵坐标从上到下依次是:E1、E2、E3、E4、E5)
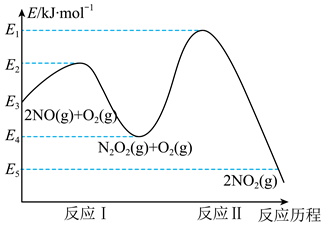
反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g)⇌ 2NO2(g)反应速率的是___________ (填“反应I”或“反应II”);快反应的正反应活化能为___________ kJ/mol(用含E1~E5的代数式表示)。
(2)用活性炭还原法处理氮氧化物的有关反应为:C(s)+2NO(g)⇌N2(g)+CO2(g)。向恒容密闭容器中加入一定量(足量)的活性炭和NO,T℃时,各物质起始浓度及10min和20min各物质平衡浓度如表所示:
在10min时,若只改变某一条件使平衡发生移动,20min时重新达到平衡,则改变的条件是_____ 。
(3)我国学者研究了用反应[ ]来治理雾霾中的污染性气体。T℃时,向容积为2L的恒容密闭容器中加入2molNO和2molCO发生上述反应,5min时达到平衡状态,平衡时测得N2的体积分数为
]来治理雾霾中的污染性气体。T℃时,向容积为2L的恒容密闭容器中加入2molNO和2molCO发生上述反应,5min时达到平衡状态,平衡时测得N2的体积分数为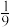 。
。
①T℃时,该反应的化学平衡常数为___________ (用最简整数比表示)。
②下列能说明该反应已经达到平衡状态的是___________ (填字母)。
A.c(N2)和c(CO2)的浓度比保持不变 B.混合气体的密度保持不变
C.NO的消耗速率等于CO2的生成速率 D.容器内气体压强保持不变
(1)NO在空气中存在如下反应:2NO(g)+O2(g)⇌2NO2(g),上述反应分两步完成,其反应历程如图所示:(纵坐标从上到下依次是:E1、E2、E3、E4、E5)

反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。决定2NO(g)+O2(g)⇌ 2NO2(g)反应速率的是
(2)用活性炭还原法处理氮氧化物的有关反应为:C(s)+2NO(g)⇌N2(g)+CO2(g)。向恒容密闭容器中加入一定量(足量)的活性炭和NO,T℃时,各物质起始浓度及10min和20min各物质平衡浓度如表所示:
| 浓度/mol·L-1 时间/min | NO | N2 | CO2 |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.040 | 0.030 | 0.030 |
| 20 | 0.032 | 0.034 | 0.017 |
在10min时,若只改变某一条件使平衡发生移动,20min时重新达到平衡,则改变的条件是
(3)我国学者研究了用反应[
 ]来治理雾霾中的污染性气体。T℃时,向容积为2L的恒容密闭容器中加入2molNO和2molCO发生上述反应,5min时达到平衡状态,平衡时测得N2的体积分数为
]来治理雾霾中的污染性气体。T℃时,向容积为2L的恒容密闭容器中加入2molNO和2molCO发生上述反应,5min时达到平衡状态,平衡时测得N2的体积分数为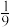 。
。①T℃时,该反应的化学平衡常数为
②下列能说明该反应已经达到平衡状态的是
A.c(N2)和c(CO2)的浓度比保持不变 B.混合气体的密度保持不变
C.NO的消耗速率等于CO2的生成速率 D.容器内气体压强保持不变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】上饶市正在创建“全国文明城市”,对碳的化合物做广泛深入的研究并妥善处理具有重要意义。
I.CO2与H2合成甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:

(1)容易得到的副产物有CO和CH2O,其中相对较少的副产物为______ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中______ (填字母)的能量变化。
A.•OCH3 •CH3OH B.•CO
•CH3OH B.•CO •OCH
•OCH
C. •OCH2 •OCH3 D.•CO + •OH
•OCH3 D.•CO + •OH •CO + •H2O
•CO + •H2O
II.天然气一个重要的用途是制取H2,其原理为CO2(g)+ CH4(g)⇌2CO(g)+2H2(g)。
(2)在密闭容器中通入物质的量均为 0.1 mol 的CH4和CO2,在一定条件下发生反应,CH4的平衡转化率与温度及压强(单位Pa)的关系如图所示。

y点:v(CO)正______ v(H2)逆(填“大于”“小于”或“等于”)。已知气体分压(p分)=气体总压(p总)×气体的物质的量分数。若平衡时气体的总压强为3×106Pa,求x点对应温度下反应的平衡常数Kp=______ Pa2。
(3)天然气中少量的杂质通常用氨水吸收,产物为硫氢化铵。一定条件下向硫氢化铵溶液中通入空气,得到单质硫并使吸收液再生。写出再生反应的化学方程式:______ 。
III.利用铜基配合1,10-phenanthroline-Cu催化剂电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段,其装置原理如图所示。

(4)电池工作过程中,阴极的电极反应式为______ 。
(5)每转移0.2mol电子,阳极室溶液质量减少______ g。
I.CO2与H2合成甲醇:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。最近采用真空封管法制备磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:

(1)容易得到的副产物有CO和CH2O,其中相对较少的副产物为
A.•OCH3
 •CH3OH B.•CO
•CH3OH B.•CO •OCH
•OCHC. •OCH2
 •OCH3 D.•CO + •OH
•OCH3 D.•CO + •OH •CO + •H2O
•CO + •H2OII.天然气一个重要的用途是制取H2,其原理为CO2(g)+ CH4(g)⇌2CO(g)+2H2(g)。
(2)在密闭容器中通入物质的量均为 0.1 mol 的CH4和CO2,在一定条件下发生反应,CH4的平衡转化率与温度及压强(单位Pa)的关系如图所示。

y点:v(CO)正
(3)天然气中少量的杂质通常用氨水吸收,产物为硫氢化铵。一定条件下向硫氢化铵溶液中通入空气,得到单质硫并使吸收液再生。写出再生反应的化学方程式:
III.利用铜基配合1,10-phenanthroline-Cu催化剂电催化CO2还原制备碳基燃料(包括CO、烷烃和酸等)是减少CO2在大气中累积和实现可再生能源有效利用的关键手段,其装置原理如图所示。

(4)电池工作过程中,阴极的电极反应式为
(5)每转移0.2mol电子,阳极室溶液质量减少
您最近一年使用:0次
【推荐1】火法炼铜是目前世界上最主要的冶炼铜的方法,其产量可占到铜总产量的85%以上,火法炼铜相关的方程式有
Cu2S(s)+O2(g)=2Cu(s)+SO2(g) ΔH1=-271.4kJ/mol 反应①
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g) ΔH2=+123.2kJ/mol 反应②
(1)Cu2S(s)在空气中煅烧生成Cu2O(s)和SO2(g)的热化学方程式是__ 。
(2)在2L的恒温密闭容器中通入5mol氧气并加入足量Cu2S发生反应①(不考虑其它反应),容器中的起始压强为akPa,反应过程中某气体的体积分数随时间变化如图所示,反应前3min平均反应速率v(SO2)=__ mol/(L·min),该温度下反应的平衡常数KP=__ (KP为以分压表示的平衡常数)。若保持温度不变向平衡体系中再通入1mol氧气,达到新平衡后氧气的体积分数__ (填“大于”“小于”或“等于”)原平衡时氧气的体积分数。
Cu2S(s)+O2(g)=2Cu(s)+SO2(g) ΔH1=-271.4kJ/mol 反应①
Cu2S(s)+2Cu2O(s)=6Cu(s)+SO2(g) ΔH2=+123.2kJ/mol 反应②
(1)Cu2S(s)在空气中煅烧生成Cu2O(s)和SO2(g)的热化学方程式是
(2)在2L的恒温密闭容器中通入5mol氧气并加入足量Cu2S发生反应①(不考虑其它反应),容器中的起始压强为akPa,反应过程中某气体的体积分数随时间变化如图所示,反应前3min平均反应速率v(SO2)=

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】近几年我国大面积发生雾霾天气,其主要原因是SO2、NOx等挥发性有机物等发生二次转化,研究碳、氮、硫及其化合物的转化对于环境的改善有重大意义。
(1)在一定条件下,CH4可与NOx反应除去NOx,已知有下列热化学方程式:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ·mol-1
②N2(g)+2O2(g) 2NO2(g) △H=+67.0 kJ·mol-1
2NO2(g) △H=+67.0 kJ·mol-1
③H2O(g)=H2O(l) △H=-41.0 kJ·mol-1
则CH4(g)+2NO2(g) CO2(g)+2H2O(g)+N2 (g) △H=
CO2(g)+2H2O(g)+N2 (g) △H=____ kJ·mol-1;该反应在____ (高温,低温,任何温度)下可自发进行
(2)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g) 2SO3(g) △H< 0,在一定温度下的定容容器中,能说明上述平衡达到平衡状态的是:
2SO3(g) △H< 0,在一定温度下的定容容器中,能说明上述平衡达到平衡状态的是:_____________ 。
A. 混合气体的密度不再发生变化 B.混合气体的平均摩尔质量不再发生变化
C. (SO2):
(SO2): (O2):
(O2): (SO3)=2:1:2 D.混合气体的总物质的量不再发生变化
(SO3)=2:1:2 D.混合气体的总物质的量不再发生变化
(3)若在T1℃、0.1 MPa条件下,往一密闭容器通入SO2和O2 [其中n(SO2):n(O2)= 2:1],测得容器内总压强与反应时间如下图所示。

①图中A点时,SO2的转化率为________ 。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率 0(正)与A点的逆反应速率
0(正)与A点的逆反应速率 A(逆)的大小关系为
A(逆)的大小关系为 0(正)
0(正)_____  A(逆) (填“>"、“<”或“ = ”)。
A(逆) (填“>"、“<”或“ = ”)。
③图中B点的平衡常数Kp=______ 。(Kp=压强平衡常数,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)为了清除NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理。现有由a mol NO、b molNO2、c molN2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为____________ 。
(1)在一定条件下,CH4可与NOx反应除去NOx,已知有下列热化学方程式:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ·mol-1
②N2(g)+2O2(g)
 2NO2(g) △H=+67.0 kJ·mol-1
2NO2(g) △H=+67.0 kJ·mol-1③H2O(g)=H2O(l) △H=-41.0 kJ·mol-1
则CH4(g)+2NO2(g)
 CO2(g)+2H2O(g)+N2 (g) △H=
CO2(g)+2H2O(g)+N2 (g) △H=(2)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g)
 2SO3(g) △H< 0,在一定温度下的定容容器中,能说明上述平衡达到平衡状态的是:
2SO3(g) △H< 0,在一定温度下的定容容器中,能说明上述平衡达到平衡状态的是:A. 混合气体的密度不再发生变化 B.混合气体的平均摩尔质量不再发生变化
C.
 (SO2):
(SO2): (O2):
(O2): (SO3)=2:1:2 D.混合气体的总物质的量不再发生变化
(SO3)=2:1:2 D.混合气体的总物质的量不再发生变化(3)若在T1℃、0.1 MPa条件下,往一密闭容器通入SO2和O2 [其中n(SO2):n(O2)= 2:1],测得容器内总压强与反应时间如下图所示。

①图中A点时,SO2的转化率为
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率
 0(正)与A点的逆反应速率
0(正)与A点的逆反应速率 A(逆)的大小关系为
A(逆)的大小关系为 0(正)
0(正) A(逆) (填“>"、“<”或“ = ”)。
A(逆) (填“>"、“<”或“ = ”)。③图中B点的平衡常数Kp=
(4)为了清除NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理。现有由a mol NO、b molNO2、c molN2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】 是危害最为严重的大气污染物之一,它主要来自化石燃料的燃烧。工业上常采用催化还原法或吸收法处理
是危害最为严重的大气污染物之一,它主要来自化石燃料的燃烧。工业上常采用催化还原法或吸收法处理 。回答下列问题:
。回答下列问题:
(1)用 还原
还原 生成S的反应分两步完成(部分产物略去),如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示。
生成S的反应分两步完成(部分产物略去),如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示。___________ (写化学式),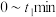 时间段的温度为
时间段的温度为___________ ,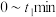 时间段用
时间段用 表示的平均反应速率为
表示的平均反应速率为___________ 。
②总反应的化学方程式为___________ (可不写条件)。
(2)焦炭催化还原 生成
生成 ,化学方程式为
,化学方程式为 ,恒容容器中,
,恒容容器中,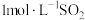 与足量的焦炭反应,
与足量的焦炭反应, 的转化率随温度的变化如图3所示。
的转化率随温度的变化如图3所示。
___________ 0(填“>”或“<”)。
②a点的平衡常数为___________ 。
(3)工业上可用 溶液吸收
溶液吸收 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。 时用
时用 的
的 溶液吸收
溶液吸收 ,当溶液中的溶质为
,当溶液中的溶质为 时,溶液中各离子浓度的大小关系为
时,溶液中各离子浓度的大小关系为___________ (已知: 的电离平衡常数
的电离平衡常数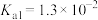 ,
, )。
)。
 是危害最为严重的大气污染物之一,它主要来自化石燃料的燃烧。工业上常采用催化还原法或吸收法处理
是危害最为严重的大气污染物之一,它主要来自化石燃料的燃烧。工业上常采用催化还原法或吸收法处理 。回答下列问题:
。回答下列问题:(1)用
 还原
还原 生成S的反应分两步完成(部分产物略去),如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示。
生成S的反应分两步完成(部分产物略去),如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示。
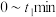 时间段的温度为
时间段的温度为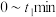 时间段用
时间段用 表示的平均反应速率为
表示的平均反应速率为②总反应的化学方程式为
(2)焦炭催化还原
 生成
生成 ,化学方程式为
,化学方程式为 ,恒容容器中,
,恒容容器中,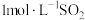 与足量的焦炭反应,
与足量的焦炭反应, 的转化率随温度的变化如图3所示。
的转化率随温度的变化如图3所示。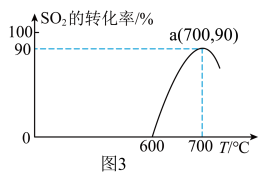

②a点的平衡常数为
(3)工业上可用
 溶液吸收
溶液吸收 ,该反应的离子方程式为
,该反应的离子方程式为 时用
时用 的
的 溶液吸收
溶液吸收 ,当溶液中的溶质为
,当溶液中的溶质为 时,溶液中各离子浓度的大小关系为
时,溶液中各离子浓度的大小关系为 的电离平衡常数
的电离平衡常数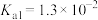 ,
, )。
)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】煤制甲醇工艺是煤高效利用的途径之一,生产工艺如图所示:
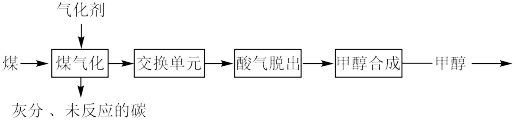
(1)“煤气化”涉及反应:C(s)+H2O(g) CO(g)+H2(g) ∆H=+135kJ∙mol-1,气化剂为H2O(g)和O2(g),关于“煤气化”说法正确的是_______(填序号)。
CO(g)+H2(g) ∆H=+135kJ∙mol-1,气化剂为H2O(g)和O2(g),关于“煤气化”说法正确的是_______(填序号)。
(2)甲醇合成过程中涉及的主要反应如下:
反应I:CO(g)+2H2(g) CH3OH(g) ∆H1=-90.94kJ∙mol-1
CH3OH(g) ∆H1=-90.94kJ∙mol-1
反应II:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ∆H2=-49.47kJ∙mol-1
CH3OH(g)+H2O(g) ∆H2=-49.47kJ∙mol-1
反应III:CO(g)+H2O(g) CO2(g)+H2(g) ∆H3
CO2(g)+H2(g) ∆H3
①反应Ⅰ在_______ (填“高温”或“低温”)下能自发进行。
②∆H3=_______ kJ/mol。
③若要大幅度提高单位时间内反应Ⅱ的选择性,可采取的最佳措施是_______ 。
④反应Ⅲ中,调控反应条件,CO和OH(羟基自由基)在催化剂上相互作用得到CO2和H的氧化还原机理和羧基机理如图所示:

若仅从第一步来看,_______ (填“氧化还原机理”或“羧基机理”)对合成更有利,但最终选择另一反应机理途径的原因是_______ 。
⑤在一定温度下,向2L刚性容器中充入1molCO2和3molH2初始压强为3.2MPa,5min后体系达到平衡态,此时容器中含有0.5molCH3OH和0.3molCO,则5min时,H2O的浓度是_______ mol/L,反应Ⅰ的压强平衡常数Kp为_______ 。

(1)“煤气化”涉及反应:C(s)+H2O(g)
 CO(g)+H2(g) ∆H=+135kJ∙mol-1,气化剂为H2O(g)和O2(g),关于“煤气化”说法正确的是_______(填序号)。
CO(g)+H2(g) ∆H=+135kJ∙mol-1,气化剂为H2O(g)和O2(g),关于“煤气化”说法正确的是_______(填序号)。| A.适量的氧气浓度有利于水煤气的生成 |
| B.适当降低水氧比有利于提高碳的转化率 |
| C.氧气的百分含量越高,对煤气化反应越有利 |
| D.煤气化反应会产生灰分和未反应的碳粉,故煤气化反应过程不适合使用催化剂 |
反应I:CO(g)+2H2(g)
 CH3OH(g) ∆H1=-90.94kJ∙mol-1
CH3OH(g) ∆H1=-90.94kJ∙mol-1反应II:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ∆H2=-49.47kJ∙mol-1
CH3OH(g)+H2O(g) ∆H2=-49.47kJ∙mol-1反应III:CO(g)+H2O(g)
 CO2(g)+H2(g) ∆H3
CO2(g)+H2(g) ∆H3①反应Ⅰ在
②∆H3=
③若要大幅度提高单位时间内反应Ⅱ的选择性,可采取的最佳措施是
④反应Ⅲ中,调控反应条件,CO和OH(羟基自由基)在催化剂上相互作用得到CO2和H的氧化还原机理和羧基机理如图所示:

若仅从第一步来看,
⑤在一定温度下,向2L刚性容器中充入1molCO2和3molH2初始压强为3.2MPa,5min后体系达到平衡态,此时容器中含有0.5molCH3OH和0.3molCO,则5min时,H2O的浓度是
您最近一年使用:0次
【推荐2】金属钛( )在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:
)在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:
(1)目前生产钛的方法之一是将金红石( )转化为
)转化为 ,再进一步还原
,再进一步还原 得到钛。
得到钛。 转化为
转化为 有直接氯化法和碳氯化法。在
有直接氯化法和碳氯化法。在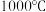 时反应的热化学方程式及其平衡常数如下:
时反应的热化学方程式及其平衡常数如下:
直接氯化: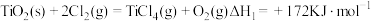 ,
,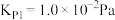
碳氯化: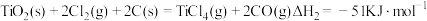 ,
,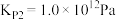
运用以上数据分析,你认为以上两个方法更优越的是__________ ,理由是__________ 。
(2)已知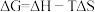 ,
, 和
和 类似,只取决于反应体系的始态和终态。根据如图回答问题。
类似,只取决于反应体系的始态和终态。根据如图回答问题。

①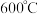 时,反应
时,反应
________ 自发进行(填“能”或“不能”)。
②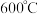 时,
时,
________  。
。
(3)钛酸锂是一种理想的嵌入型电极材料。某新型钛酸锂电池与普通石墨烯锂电池相比,电位比较高,安全性相较好,工作原理如图所示。
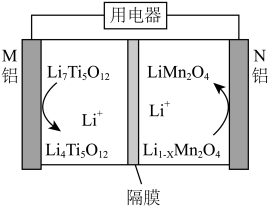
①电池的正极为______ (填“M”或“N”)
②放电时, 通过隔膜向
通过隔膜向______ 极(填“M”或“N”)移动。
③放电时,电极N的电极反应式为______ 。
 )在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:
)在航空航天、医疗器械等工业领域有着重要用途。回答下列问题:(1)目前生产钛的方法之一是将金红石(
 )转化为
)转化为 ,再进一步还原
,再进一步还原 得到钛。
得到钛。 转化为
转化为 有直接氯化法和碳氯化法。在
有直接氯化法和碳氯化法。在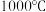 时反应的热化学方程式及其平衡常数如下:
时反应的热化学方程式及其平衡常数如下:直接氯化:
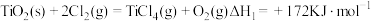 ,
,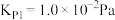
碳氯化:
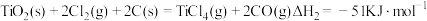 ,
,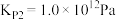
运用以上数据分析,你认为以上两个方法更优越的是
(2)已知
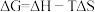 ,
, 和
和 类似,只取决于反应体系的始态和终态。根据如图回答问题。
类似,只取决于反应体系的始态和终态。根据如图回答问题。
①
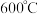 时,反应
时,反应
②
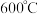 时,
时,
 。
。(3)钛酸锂是一种理想的嵌入型电极材料。某新型钛酸锂电池与普通石墨烯锂电池相比,电位比较高,安全性相较好,工作原理如图所示。

①电池的正极为
②放电时,
 通过隔膜向
通过隔膜向③放电时,电极N的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】甲醇水蒸气重整制氢(SRM)系统简单,产物中H2含量高、CO含量低(CO会损坏燃料电池的交换膜),是电动汽车氢氧燃料电池理想的氢源。反应如下:
反应Ⅰ(主):CH3OH(g)+H2O(g) CO2(g)+3H2(g) ΔH1=+49kJ/mol
CO2(g)+3H2(g) ΔH1=+49kJ/mol
反应Ⅱ(副):H2(g)+CO2(g) CO(g)+H2O(g) ΔH2=+41kJ/mol
CO(g)+H2O(g) ΔH2=+41kJ/mol
温度高于300℃则会同时发生反应Ⅲ:CH3OH(g) CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3
(1)计算反应Ⅲ的ΔH3=___ 。
(2)反应1能够自发进行的原因是___ ,升温有利于提高CH3OH转化率,但也存在一个明显的缺点是___ 。
(3)如图为某催化剂条件下,CH3OH转化率、CO生成率与温度的变化关系。
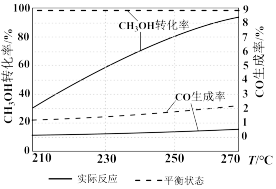
①随着温度的升高,CO的实际反应生成率没有不断接近平衡状态生成率的原因是___ (填标号)。
A.反应Ⅱ逆向移动
B.部分CO转化为CH3OH
C.催化剂对反应Ⅱ的选择性低
D.催化剂对反应Ⅲ的选择性低
②随着温度的升高,CH3OH实际反应转化率不断接近平衡状态转化率的原因是___ 。
③写出一条能提高CH3OH转化率而降低CO生成率的措施___ 。
(4)250℃,一定压强和催化剂条件下,1.00molCH3OH和1.32molH2O充分反应(已知此条件下可忽略反应Ⅲ),平衡时测得H2为2.70mol,CO有0.030mol,试求反应Ⅰ中CH3OH的转化率___ 。
反应Ⅰ(主):CH3OH(g)+H2O(g)
 CO2(g)+3H2(g) ΔH1=+49kJ/mol
CO2(g)+3H2(g) ΔH1=+49kJ/mol反应Ⅱ(副):H2(g)+CO2(g)
 CO(g)+H2O(g) ΔH2=+41kJ/mol
CO(g)+H2O(g) ΔH2=+41kJ/mol温度高于300℃则会同时发生反应Ⅲ:CH3OH(g)
 CO(g)+2H2(g) ΔH3
CO(g)+2H2(g) ΔH3(1)计算反应Ⅲ的ΔH3=
(2)反应1能够自发进行的原因是
(3)如图为某催化剂条件下,CH3OH转化率、CO生成率与温度的变化关系。

①随着温度的升高,CO的实际反应生成率没有不断接近平衡状态生成率的原因是
A.反应Ⅱ逆向移动
B.部分CO转化为CH3OH
C.催化剂对反应Ⅱ的选择性低
D.催化剂对反应Ⅲ的选择性低
②随着温度的升高,CH3OH实际反应转化率不断接近平衡状态转化率的原因是
③写出一条能提高CH3OH转化率而降低CO生成率的措施
(4)250℃,一定压强和催化剂条件下,1.00molCH3OH和1.32molH2O充分反应(已知此条件下可忽略反应Ⅲ),平衡时测得H2为2.70mol,CO有0.030mol,试求反应Ⅰ中CH3OH的转化率
您最近一年使用:0次



