为比较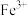 和
和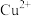 对
对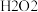 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验,请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验,请回答相关问题:
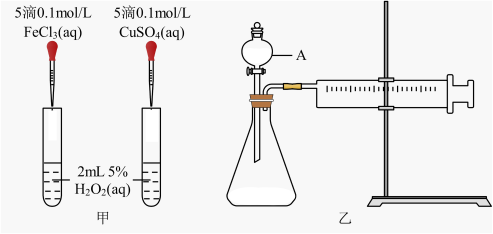
(1)定性分析:如图甲可通过观察_______ 的快慢,定性比较得出结论,有同学提出将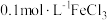 改为
改为_______  更为合理,其理由是
更为合理,其理由是_______ 。
(2)定量分析:如图乙所示,实验时均以生成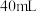 气体为准,其他可能影响实验的因素均已忽略,实验中需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略,实验中需要测量的数据是_______ 。
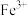 和
和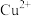 对
对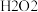 分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验,请回答相关问题:
分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验,请回答相关问题:
(1)定性分析:如图甲可通过观察
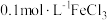 改为
改为 更为合理,其理由是
更为合理,其理由是(2)定量分析:如图乙所示,实验时均以生成
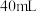 气体为准,其他可能影响实验的因素均已忽略,实验中需要测量的数据是
气体为准,其他可能影响实验的因素均已忽略,实验中需要测量的数据是
更新时间:2022-10-15 13:47:55
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】某小组拟用含稀硫酸的KMnO4溶液与H2C2O4溶液(弱酸)的反应(此反应为放热反应)来探究“条件对化学反应速率的影响”,并设计了如表的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol/LH2C2O4溶液、0.010mol/L KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
回答下列问题:
(1)完成上述反应原理的离子方程式:___________________________ 。
(2)上述实验①②是探究________________ 对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则 a为_________ ;
(3)乙是实验需要测量的物理量,则表格中“乙”应填写________ 。上述实验②④是探究___________________ 对化学反应速率的影响。
(4)实验③中加入amL蒸馏水的目的是__________________
(5)为了观察紫色褪去,草酸与高锰酸钾初始的物质的量需要满足的关系n(H2C2O4):n (KMnO4)最小为:_____________ 。
| 物理量 编号 | V(0.20 mol/L H2C2O4溶液)/mL | V(蒸馏水)/mL | V(0.010mol/L KMnO4溶液)/mL | M(MnSO4 固体)/g | T/℃ | 乙 |
| ① | 2.0 | 0 | 4.0 | 0 | 50 | |
| ② | 2.0 | 0 | 4.0 | 0 | 25 | |
| ③ | 1.0 | a | 4.0 | 0 | 25 | |
| ④ | 2.0 | 0 | 4.0 | 0.1 | 25 |
(1)完成上述反应原理的离子方程式:
(2)上述实验①②是探究
(3)乙是实验需要测量的物理量,则表格中“乙”应填写
(4)实验③中加入amL蒸馏水的目的是
(5)为了观察紫色褪去,草酸与高锰酸钾初始的物质的量需要满足的关系n(H2C2O4):n (KMnO4)最小为:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】实验目的:探究(一)同周期元素性质的递变规律
探究(二)影响化学反应速率的因素
供选试剂:锌片、锌粉、铁片、铁粉、镁条、铝条、新制Na2S溶液、新制氯水、
0.5mol/L盐酸、3mol/L盐酸等试剂(实验仪器自选)。
现有A同学设计的部分实验方案,请你帮他填写完整,并作出评价。
【实验探究一】同周期元素金属性和非金属性的递变规律
【实验探究二】影响化学反应速率的因素
A同学在[实验探究二]中所得结论不够严谨。原因是___________________________ 。
在不改变实验探究二所做实验的前提下,再补充一些实验即可完成有关探究,补充实验是(写最简方案,可不填满,也可增加):
①_________________________________ ;
②_________________________________ ;
③_________________________________ 。
探究(二)影响化学反应速率的因素
供选试剂:锌片、锌粉、铁片、铁粉、镁条、铝条、新制Na2S溶液、新制氯水、
0.5mol/L盐酸、3mol/L盐酸等试剂(实验仪器自选)。
现有A同学设计的部分实验方案,请你帮他填写完整,并作出评价。
【实验探究一】同周期元素金属性和非金属性的递变规律
| 实验步骤 (画图表示,参照下图) | 实验现象 | 实验结论 | |
| 非金属性递变 | |||
| 金属性递变 |
【实验探究二】影响化学反应速率的因素
实验步骤 | 实验现象 | 实验结论 |
 (锌片和锌粉的质量相同,盐酸均过量) | 均有气体生成,锌粉比锌片消失快。 | 反应物接触面积越大,反应速率越快 |
A同学在[实验探究二]中所得结论不够严谨。原因是
在不改变实验探究二所做实验的前提下,再补充一些实验即可完成有关探究,补充实验是(写最简方案,可不填满,也可增加):
①
②
③
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】为探究反应条件对 溶液与
溶液与 稀硫酸反应的化学反应速率的影响,某小组设计的实验方案及测定的结果如下表所示,请回答下列问题。
稀硫酸反应的化学反应速率的影响,某小组设计的实验方案及测定的结果如下表所示,请回答下列问题。
(1)请写出上述反应的离子方程式:_______ 。
(2)若实验①和③的目的是探究反应物浓度对上述化学反应速率的影响,则
_______ 。
(3)若 ,则实验②和③的目的是
,则实验②和③的目的是_______ ,可预测表中y和z的关系应为y_______ (填“>”、“<”或“=”)z。
 溶液与
溶液与 稀硫酸反应的化学反应速率的影响,某小组设计的实验方案及测定的结果如下表所示,请回答下列问题。
稀硫酸反应的化学反应速率的影响,某小组设计的实验方案及测定的结果如下表所示,请回答下列问题。| 编号 | 反应温度/℃ |  溶液/mL 溶液/mL | 稀硫酸/mL | 蒸馏水/mL | 出现浑浊时间/s |
| ① | 25 | 5.0 | 10.0 | a | x |
| ② | 40 | 10.0 | 10.0 | b | y |
| ③ | 25 | 10.0 | 10.0 | 0 | z |
(2)若实验①和③的目的是探究反应物浓度对上述化学反应速率的影响,则

(3)若
 ,则实验②和③的目的是
,则实验②和③的目的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】同学们测定和探究影响反应速率的因素,设计了如下系列实验。
Ⅰ.甲同学测定室温下H2C2O4溶液与用硫酸酸化的KMnO4溶液的反应速率。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时。该小组设计了如下的方案。
(1)写出H2C2O4与KMnO4(H+)反应的离子反应方程式:___________
(2)该实验是通过测定___________ 来计算反应速率。
(3)实验测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=___________ 。
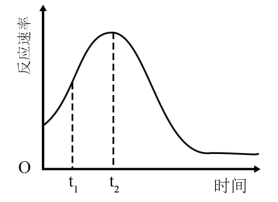
(4)该小组发现室温下反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:___________ ,若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是___________ (填序号)。
A.硫酸钾 B.硫酸锰 C.稀硫酸 D.二氯化锰
Ⅱ.乙同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
(5)该实验①、②可探究___________ 对反应速率的影响,因此V1和V3分别是___________ 、___________ 。实验①、③可探究硫酸浓度对反应速率的影响,因此V5=___________ 。
(6)硫代硫酸钠与稀硫酸反应离子反应方程式:___________ 。
Ⅰ.甲同学测定室温下H2C2O4溶液与用硫酸酸化的KMnO4溶液的反应速率。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时。该小组设计了如下的方案。
| H2C2O4溶液 | 酸性KMnO4溶液 | ||
| 浓度/mol·L-1 | 体积/mL | 浓度/mol·L-1 | 体积/mL |
| 0.50 | 6.0 | 0.020 | 4.0 |
(2)该实验是通过测定
(3)实验测得反应所用的时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=
(4)该小组发现室温下反应速率走势如图,其中t1~t2时间内速率变快的主要原因可能是:
A.硫酸钾 B.硫酸锰 C.稀硫酸 D.二氯化锰

Ⅱ.乙同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
| 实验序号 | 反应温度/℃ | Na2S2O3浓度 | 稀硫酸 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| ② | 40 | V1 | 0.10 | V2 | 0.50 | V3 |
| ③ | 20 | V4 | 0.10 | 4.0 | 0.50 | V5 |
(6)硫代硫酸钠与稀硫酸反应离子反应方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】某研究性学习小组拟从盐卤液(含Na+、Cl-、Mg2+、Ca2+、I-、SO42-),来制取较纯净的氯化钠晶体及单质碘(I2),他们设计了如下实验:
第一步:提取碘
(1)在盐卤液中通入Cl2可使I-氧化为碘单质(I2),反应的离子方程式为_______________
(2)要将此反应后的溶液中的碘单质分离出来,先加入一种试剂可以得到一种紫红色液体,这种试剂是___________ (填字母编号)
A.盐酸 B.四氯化碳 C.氢氧化钠溶液 D.酒精
该分离方法称为___________ 。
(3)要从紫红色液体中再分离出单质碘,还需要采取下图的分离操作,该分离方法称为___________ 。(填分离操作名称)
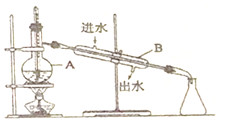
①指出图中的两处明显错误_________________ ;___________________ 。
②写出仪器名称:A_____________ ,B________________ 。
第二步:粗盐提纯
(4)提取碘后,溶液中主要含有Na+、Cl-、Ca2+、Mg2+、SO42-,为了得到纯净的NaCl,然后在下列操作中选取必要的步骤和正确的操作顺序______________ (有多少选多少)
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
第一步:提取碘
(1)在盐卤液中通入Cl2可使I-氧化为碘单质(I2),反应的离子方程式为
(2)要将此反应后的溶液中的碘单质分离出来,先加入一种试剂可以得到一种紫红色液体,这种试剂是
A.盐酸 B.四氯化碳 C.氢氧化钠溶液 D.酒精
该分离方法称为
(3)要从紫红色液体中再分离出单质碘,还需要采取下图的分离操作,该分离方法称为

①指出图中的两处明显错误
②写出仪器名称:A
第二步:粗盐提纯
(4)提取碘后,溶液中主要含有Na+、Cl-、Ca2+、Mg2+、SO42-,为了得到纯净的NaCl,然后在下列操作中选取必要的步骤和正确的操作顺序
①过滤②加过量NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某校化学研究性学习小组欲设计实验验证Fe、Cu的金属活动性,他们提出了以下两种方案。请你帮助他们完成有关实验项目。
(1)方案Ⅰ:有人提出将大小相等的铁片和铜片同时放入稀硫酸(或稀盐酸)中,观察产生气泡的快慢,据此确定它们的活动性。该原理的离子方程式为___ 。
(2)方案Ⅱ:有人利用Fe、Cu作电极设计成原电池,以确定它们的活动性。试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出负极的电极反应式___ 。

(3)方案Ⅲ:结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案及现象(与方案Ⅰ、Ⅱ不能雷同):___ 。
(1)方案Ⅰ:有人提出将大小相等的铁片和铜片同时放入稀硫酸(或稀盐酸)中,观察产生气泡的快慢,据此确定它们的活动性。该原理的离子方程式为
(2)方案Ⅱ:有人利用Fe、Cu作电极设计成原电池,以确定它们的活动性。试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出负极的电极反应式

(3)方案Ⅲ:结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案及现象(与方案Ⅰ、Ⅱ不能雷同):
您最近一年使用:0次



