2SO2(g)+O2(g) 2SO2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
2SO2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
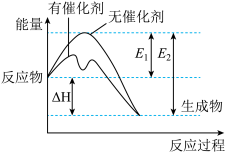
 2SO2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
2SO2(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列有关叙述正确的是
| A.E1-E2=△H |
| B.该反应为吸热反应 |
| C.增大氧气的浓度,能使活化分子百分数增大 |
| D.使用催化剂可以提高SO2的转化率 |
更新时间:2022-10-16 09:24:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下, 与
与 反应可得到
反应可得到 、
、 及少量副产物
及少量副产物 的混合气体,图是用
的混合气体,图是用 与
与 制备
制备 和
和 的反应历程,关于该过程的说法中错误的是
的反应历程,关于该过程的说法中错误的是

已知: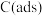 表示吸附性活性炭,TS表示反应中的过渡态
表示吸附性活性炭,TS表示反应中的过渡态
 与
与 反应可得到
反应可得到 、
、 及少量副产物
及少量副产物 的混合气体,图是用
的混合气体,图是用 与
与 制备
制备 和
和 的反应历程,关于该过程的说法中错误的是
的反应历程,关于该过程的说法中错误的是 
已知:
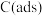 表示吸附性活性炭,TS表示反应中的过渡态
表示吸附性活性炭,TS表示反应中的过渡态A.反应②为 ⇌ ⇌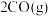 ,与TS2相比,TS1更稳定 ,与TS2相比,TS1更稳定 |
B.反应②活化能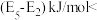 反应①活化能 反应①活化能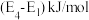 ,总反应的活化能为 ,总反应的活化能为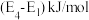 |
| C.若加入固体X能提高CO的选择性,则X为CH4与CO2转化为CO的催化剂 |
| D.反应①决定总反应的快慢,增大CO2浓度能明显增大总反应的速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列依据热化学方程式得出的结论正确的是
A.已知  ,则 ,则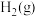 的能量一定高于 的能量一定高于 |
B.在一定的温度和压强下, 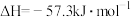 。若将含有 。若将含有 的某溶液与含 的某溶液与含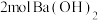 的某溶液混合,则放出的热量小于 的某溶液混合,则放出的热量小于 |
C.工业上常用SO2将CO氧化为CO2,二氧化硫转化为单质硫,若生成1 g单质硫放出的能量为8.5 kJ,则该反应的热化学方程式可以写为 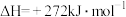 |
D.已知 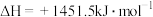 ,则 ,则 和 和 中化学键的总键能大于 中化学键的总键能大于 和 和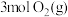 中化学键的总键能 中化学键的总键能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列有关概念的理解正确的是
A. 燃烧所放出的热量即为 燃烧所放出的热量即为 的燃烧热 的燃烧热 |
| B.升高温度,化学反应速率加快,K值也一定增大 |
| C.活化能最大的基元反应决定总反应速率的快慢 |
| D.分子间的碰撞会导致分子能量升高,必然会发生化学反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】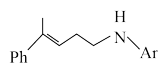 是一系列具有合成价值的高烯丙胺类化合物(Ph代表苯基、Ar代表芳香基),以羰基钼[
是一系列具有合成价值的高烯丙胺类化合物(Ph代表苯基、Ar代表芳香基),以羰基钼[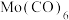 ]为催化剂合成该物质的反应机理如图所示:
]为催化剂合成该物质的反应机理如图所示:
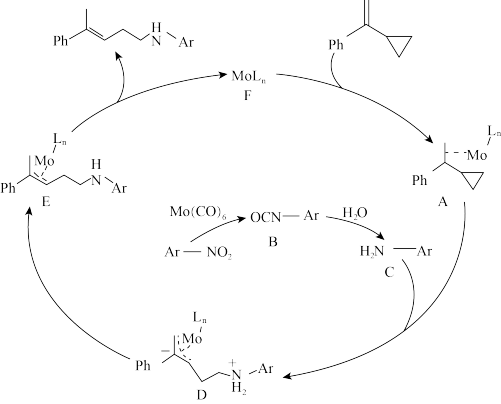
下列说法正确的是
 是一系列具有合成价值的高烯丙胺类化合物(Ph代表苯基、Ar代表芳香基),以羰基钼[
是一系列具有合成价值的高烯丙胺类化合物(Ph代表苯基、Ar代表芳香基),以羰基钼[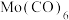 ]为催化剂合成该物质的反应机理如图所示:
]为催化剂合成该物质的反应机理如图所示:
下列说法正确的是
A.催化剂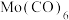 中不含配位键 中不含配位键 |
| B.该反应机理不涉及非极性键的断裂和形成 |
C.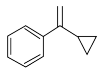 与 与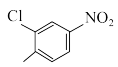 在该条件下反应可合成 在该条件下反应可合成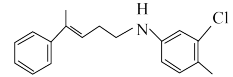 |
| D.炭基钼催化剂能有效降低总反应的焓变,加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列图示与对应的叙述相符的是
 |  |  |  |
| A.用盐酸滴定NaOH溶液 | B.反应开始后,注射器活塞向右移,该反应为放热反应 | C.读取滴定管读数 | D.研究不同金属离子对过氧化氢分解速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】不同催化剂会改变反应的选择性[CH3OCH3的选择性=  ],在某催化剂催化下发生的两个反应的能量变化如图所示,下列说法错误的是
],在某催化剂催化下发生的两个反应的能量变化如图所示,下列说法错误的是

 ],在某催化剂催化下发生的两个反应的能量变化如图所示,下列说法错误的是
],在某催化剂催化下发生的两个反应的能量变化如图所示,下列说法错误的是
| A.ΔH1< ΔH2 |
| B.反应①、反应②均为放热反应 |
| C.在该条件下,CH3OCH3(g)的生成速率比C2H4(g)的大 |
| D.改变加入的催化剂,可使E2- E1的值变小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在密闭容器中的一定量混合气体发生反应: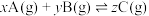 ,达到平衡时,测得A的浓度为
,达到平衡时,测得A的浓度为 ,在温度不变的条件下,将容器的容积压缩到原来的一半,再达到平衡,测得A的浓度为
,在温度不变的条件下,将容器的容积压缩到原来的一半,再达到平衡,测得A的浓度为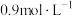 。下列有关判断不正确的是
。下列有关判断不正确的是
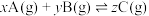 ,达到平衡时,测得A的浓度为
,达到平衡时,测得A的浓度为 ,在温度不变的条件下,将容器的容积压缩到原来的一半,再达到平衡,测得A的浓度为
,在温度不变的条件下,将容器的容积压缩到原来的一半,再达到平衡,测得A的浓度为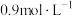 。下列有关判断不正确的是
。下列有关判断不正确的是| A.x+y>z | B.平衡向正反应方向移动 |
| C.C的体积分数减小 | D.B的物质的量减小 |
您最近一年使用:0次
【推荐2】一定温度下,在2个容积均为1L的恒容密闭容器中,加入一定量的反应物,发生反应: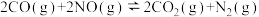 ,相关数据见下表。
,相关数据见下表。
下列说法不正确的是
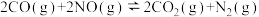 ,相关数据见下表。
,相关数据见下表。| 容器编号 | 温度/℃ | 起始物质的量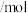 | 平衡物质的量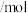 | |
 |  |  | ||
| Ⅰ |  | 0.2 | 0.2 | 0.1 |
| Ⅱ |  | 0.2 | 0.2 | 0.12 |
A.若 ;则 ;则 |
B.Ⅰ中反应达到平衡时, 的转化率为50% 的转化率为50% |
C. 条件下的平衡常数为5 条件下的平衡常数为5 |
D.对于Ⅱ,平衡后向容器中再充入0.2  和0.2 和0.2  平衡逆向移动 平衡逆向移动 |
您最近一年使用:0次


 。反应历程如图所示(*表示吸附在催化剂表面)。下列叙述错误的是
。反应历程如图所示(*表示吸附在催化剂表面)。下列叙述错误的是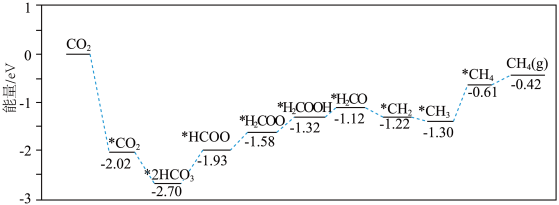
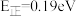

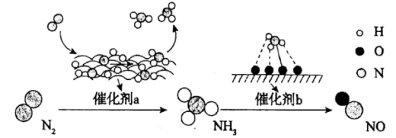
 的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是
的催化剂可用于汽车尾气脱硝。催化机理如图甲,反应历程如图乙。下列说法正确的是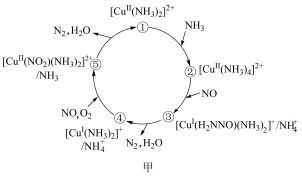

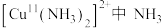 的键角小于氨气中
的键角小于氨气中 分子的键角
分子的键角

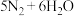
 可加快脱硝速率,提高脱硝的平衡转化率
可加快脱硝速率,提高脱硝的平衡转化率

