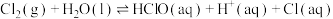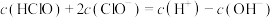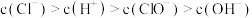已知 N2(g)+3H2(g) 2NH3(g) ∆H=-92.3kJ∙mol-1。在一定温度和催化剂条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态Ⅰ;相同条件下,向另一体积相同的密闭容器中通入0.7molN2、2.1molH2和0.6molNH3,达到平衡状态Ⅱ,下列说法正确的是
2NH3(g) ∆H=-92.3kJ∙mol-1。在一定温度和催化剂条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态Ⅰ;相同条件下,向另一体积相同的密闭容器中通入0.7molN2、2.1molH2和0.6molNH3,达到平衡状态Ⅱ,下列说法正确的是
 2NH3(g) ∆H=-92.3kJ∙mol-1。在一定温度和催化剂条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态Ⅰ;相同条件下,向另一体积相同的密闭容器中通入0.7molN2、2.1molH2和0.6molNH3,达到平衡状态Ⅱ,下列说法正确的是
2NH3(g) ∆H=-92.3kJ∙mol-1。在一定温度和催化剂条件下,向一密闭容器中,通入1molN2和3molH2,达到平衡状态Ⅰ;相同条件下,向另一体积相同的密闭容器中通入0.7molN2、2.1molH2和0.6molNH3,达到平衡状态Ⅱ,下列说法正确的是| A.反应放出的热量:QⅠ>QⅡ |
| B.H2的转化率:平衡Ⅰ<平衡Ⅱ |
| C.平衡Ⅰ和平衡Ⅱ中H2的百分含量不相同 |
| D.两个平衡状态的平衡常数的关系:KⅠ>KⅡ |
更新时间:2022-10-28 21:18:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在一定温度下,向一个容积固定的容器中通入3mol SO2和2mol O2及固体催化剂,使之反应:2SO2(g)+O2(g) 2SO3(g)△H=-196.6kJ•mol-1,平衡时容器内气体的压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4mol SO2、3mol O2、2mol SO3(g),下列说法正确的是( )
2SO3(g)△H=-196.6kJ•mol-1,平衡时容器内气体的压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4mol SO2、3mol O2、2mol SO3(g),下列说法正确的是( )
 2SO3(g)△H=-196.6kJ•mol-1,平衡时容器内气体的压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4mol SO2、3mol O2、2mol SO3(g),下列说法正确的是( )
2SO3(g)△H=-196.6kJ•mol-1,平衡时容器内气体的压强为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为4mol SO2、3mol O2、2mol SO3(g),下列说法正确的是( )| A.达平衡时用O2表示的反应速率为0.25mol·L-1·min-1 |
B.第二次达平衡时SO3的体积分数大于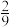 |
| C.第一次平衡时反应放出的热量为294.9kJ |
| D.两次平衡SO2的转化率相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列有关说法正确的是
| A.合成氨为放热反应,所以在实际生产过程中温度越低越好 |
B.在恒温恒容条件下,发生2SO2(g)+O2(g) 2SO3(g)。当反应达到平衡后,若再充入少量O2,再次达到平衡后,SO3的浓度降低 2SO3(g)。当反应达到平衡后,若再充入少量O2,再次达到平衡后,SO3的浓度降低 |
C.在恒温恒压条件下,发生2NO2(g) N2O4(g)。当反应达到平衡后,若再充入少量N2O4,再次达到平衡后,体系颜色不变 N2O4(g)。当反应达到平衡后,若再充入少量N2O4,再次达到平衡后,体系颜色不变 |
D.CaCO3(s)+2NH (aq) (aq) Ca2+(aq)+2NH3(aq)+CO2(g)+H2O(l) Ca2+(aq)+2NH3(aq)+CO2(g)+H2O(l)  H=+68.9kJ•mol-1、 H=+68.9kJ•mol-1、 S=+37.3J/(mol•K)该反应可在沸水中自发进行 S=+37.3J/(mol•K)该反应可在沸水中自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】在一个固定体积的密闭容器中,向容器内充入2molA和1molB,发生如下反应:2A(g) + B(g) 3C(g) + D(s),反应达到平衡时C的物质的量浓度为1.2 mol/L。若维持容器的温度和体积不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2 mol/L的是
3C(g) + D(s),反应达到平衡时C的物质的量浓度为1.2 mol/L。若维持容器的温度和体积不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2 mol/L的是
 3C(g) + D(s),反应达到平衡时C的物质的量浓度为1.2 mol/L。若维持容器的温度和体积不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2 mol/L的是
3C(g) + D(s),反应达到平衡时C的物质的量浓度为1.2 mol/L。若维持容器的温度和体积不变,按下列方法改变起始物质,达到平衡时C的浓度仍为1.2 mol/L的是| A.4molA + 2molB | B.3molC+ 1molD+ 1molB |
| C.6molC + 0.8molD | D.1.6molA+0.8molB + 0.6molC+0.3molD |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】t ℃时,某平衡体系中含有 X、Y、Z、W 四种物质,此温度下发生反应的平衡常数表达式如右: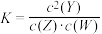 。有关该平衡体系的说法正确的是
。有关该平衡体系的说法正确的是
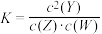 。有关该平衡体系的说法正确的是
。有关该平衡体系的说法正确的是 | A.当混合气体的平均相对分子质量保持不变时,反应达平衡 |
| B.增大压强,各物质的浓度不变 |
| C.升高温度,平衡常数K增大 |
| D.增加X的量,平衡既可能正向移动,也可能逆向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】大气固氮(闪电时N2转化为NO)和工业固氮(合成氨)是固氮的重要形式,下表列举了不同温度下大气固氮和工业固氮的部分K值:
下列说法正确的是
N2+O2  2NO 2NO | N2+3H2 2NH3 2NH3 | |||
| 温度 | 25℃ | 2000℃ | 25℃ | 400℃ |
| K | 3.84×10-31 | 0.1 | 5×108 | 1.88×104 |
| A.在常温下,工业固氮非常容易进行 |
| B.人类可以通过大规模模拟大气固氮利用氮资源 |
| C.大气固氮与工业固氮的K值受温度和压强等的影响较大 |
| D.大气固氮是吸热反应,工业固氮是放热反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】甲酸乙酯在OH-存在下发生水解:HCOOC2H5+OH- HCOO-+C2H5OH,两种反应物的初始浓度均为0.500 mol/L,不同温度下测得HCOOC2H5的浓度(mol/L)随时间变化的数据如表所示。下列有关说法正确的是
HCOO-+C2H5OH,两种反应物的初始浓度均为0.500 mol/L,不同温度下测得HCOOC2H5的浓度(mol/L)随时间变化的数据如表所示。下列有关说法正确的是
 HCOO-+C2H5OH,两种反应物的初始浓度均为0.500 mol/L,不同温度下测得HCOOC2H5的浓度(mol/L)随时间变化的数据如表所示。下列有关说法正确的是
HCOO-+C2H5OH,两种反应物的初始浓度均为0.500 mol/L,不同温度下测得HCOOC2H5的浓度(mol/L)随时间变化的数据如表所示。下列有关说法正确的是 | 0 | 120 | 180 | 240 | 330 | 530 | 600 | 700 | 800 |
 | 0.500 | 0.335 | 0.2910 | 0.256 | 0.210 | 0.156 | 0.148 | 0.145 | 0.145 |
 | 0.500 | 0.325 | 0.2775 | 0.238 | 0.190 | … | 0.130 | 0.130 | 0.130 |
A.该反应在15℃,120s~180s区间的v(HCOOC2H5)为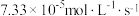 |
| B.530 s时,表格中35℃对应的数据一定是0.130 |
| C.由表中数据可知,温度升高,反应速率加快 |
| D.其他条件不变,提高c(OH-),可使该反应的化学平衡常数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将4mol SO2与2molO2放入4L的密闭容器中,在一定条件下反应达到平衡:2SO2(g)+ O2(g) 2SO3(g),测得平衡时SO3的浓度为0.5mol·L-1。则此条件下的平衡常数K为
2SO3(g),测得平衡时SO3的浓度为0.5mol·L-1。则此条件下的平衡常数K为
 2SO3(g),测得平衡时SO3的浓度为0.5mol·L-1。则此条件下的平衡常数K为
2SO3(g),测得平衡时SO3的浓度为0.5mol·L-1。则此条件下的平衡常数K为| A.4 | B.0.4 | C.0.25 | D.0.2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在化学平衡体系中,由各气体物质的分压替代浓度,计算的平衡常数叫压强平衡常数,用符号Kp表示。在温度为T时,将NH4HS(s)置于抽真空的容器中,当反应NH4HS(s) NH3(g)+H2S(g)达到平衡时,测得总压强为p,则该反应的压强平衡常数Kp为
NH3(g)+H2S(g)达到平衡时,测得总压强为p,则该反应的压强平衡常数Kp为
 NH3(g)+H2S(g)达到平衡时,测得总压强为p,则该反应的压强平衡常数Kp为
NH3(g)+H2S(g)达到平衡时,测得总压强为p,则该反应的压强平衡常数Kp为A.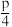 | B.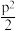 | C.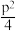 | D.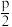 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】CO2催化加氢合成甲醇是重要的碳捕获利用与封存技术,该过程发生下列反应:
反应I:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H=-58.6kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g) △H=41.2kJ·mol-1
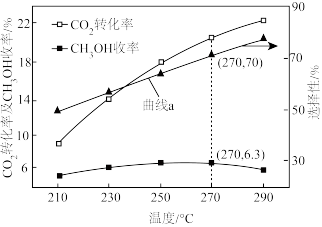
0.5MPa下,将n(H2):n(CO2)=3的混合气体以一定流速通过装有催化剂的反应器,测得CO2的转化率、CH3OH或CO的选择性[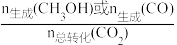 ×100%]以及CH3OH的收率(CO2的转化率×CH3OH的选择性)随温度的变化如图所示。下列说法正确的是
×100%]以及CH3OH的收率(CO2的转化率×CH3OH的选择性)随温度的变化如图所示。下列说法正确的是
反应I:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H=-58.6kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g) △H=41.2kJ·mol-1
0.5MPa下,将n(H2):n(CO2)=3的混合气体以一定流速通过装有催化剂的反应器,测得CO2的转化率、CH3OH或CO的选择性[
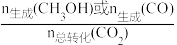 ×100%]以及CH3OH的收率(CO2的转化率×CH3OH的选择性)随温度的变化如图所示。下列说法正确的是
×100%]以及CH3OH的收率(CO2的转化率×CH3OH的选择性)随温度的变化如图所示。下列说法正确的是
| A.CO(g)+2H2(g)=CH3OH(g) △H=99.8kJ·mol-1 |
| B.曲线a表示CH3OH的选择性随温度的变化 |
| C.图中所示270℃时,对应CO2的转化率为21% |
| D.在210℃~250℃之间,CH3OH的收率增大是由于CH3OH的选择性增大导致 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】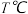 时,在
时,在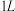 的密闭容器中充入
的密闭容器中充入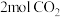 和
和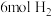 ,一定条件下发生反应:
,一定条件下发生反应: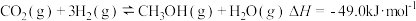 ,测得
,测得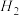 和
和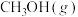 的浓度随时间变化如下表所示。下列说法不正确的是
的浓度随时间变化如下表所示。下列说法不正确的是
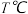 时,在
时,在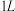 的密闭容器中充入
的密闭容器中充入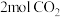 和
和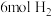 ,一定条件下发生反应:
,一定条件下发生反应: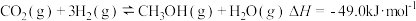 ,测得
,测得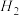 和
和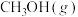 的浓度随时间变化如下表所示。下列说法不正确的是
的浓度随时间变化如下表所示。下列说法不正确的是时间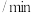 | 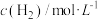 |  | 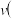 正 正 和 和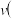 逆 逆 比较 比较 |
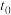 | 6 | 0 | ? |
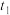 | 3 | 1 | 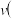 正 正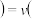 逆 逆 |
A. 时间内 时间内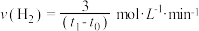 |
B.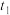 时,若升高温度或再充入 时,若升高温度或再充入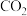 气体,都可以提高 气体,都可以提高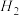 的转化率 的转化率 |
C.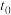 时, 时,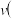 正 正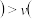 逆 逆 |
D.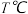 时,平衡常数 时,平衡常数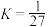 , ,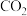 与 与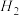 的转化率相等 的转化率相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用CO2、C3H8为原料可制备丙烯(C3H6),反应为CO2(g)+C3H8(g)⇌C3H6(g)+CO(g)+H2O(g)。一定温度下,向2L恒容密闭容器中通入3mol CO2、2mol C3H8,测得C3H8与H2O的物质的量随时间的变化关系如下表所示,下列说法错误的是
| t/min | 0 | t1 | t2 | t3 | t4 |
| n(C3H8)/mol | 2 | 1.4 | 1 | 0.8 | 0.8 |
| n(H2O)/mol | 0 | 0.6 | 1 | 1.2 | 1.2 |
| A.t3时,该反应达到平衡 |
| B.t2=10时, 0~10min内用C3H8表示的平均反应速率为0.1mol·L-1·min-1 |
| C.当容器中气体压强不再改变时,该反应达到平衡 |
| D.平衡时与起始时气体的压强之比是31:25 |
您最近一年使用:0次

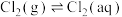
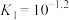
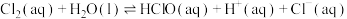
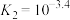
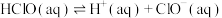
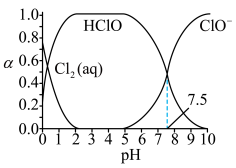
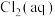 、
、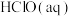 和
和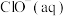 分别在三者总量中所占物质的量分数
分别在三者总量中所占物质的量分数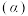 随pH变化的关系如图所示。下列表述正确的是
随pH变化的关系如图所示。下列表述正确的是