周期表中VIIA族元素及其化合物应用广泛。Cl2是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、燃料和药品等;ClO2用作自来水消毒剂;NaClO、Ca(ClO)2既可用作漂白棉麻、纸张的漂白剂,又可用作游泳池等场所的消毒剂;氯可形成多种含氧酸HClO、HClO2、HClO3、HClO4;AgBr可用作感光材料;AgI可用于人工降雨;KIO3常用作食盐中的补碘剂。下列说法正确的是
A.ClO 中O-Cl-O夹角大于ClO 中O-Cl-O夹角大于ClO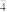 中O-Cl-O夹角 中O-Cl-O夹角 |
| B.ClO2是由极性键构成的非极性分子 |
| C.碘原子(53I)基态核外电子排布式为5s25p5 |
| D.前五周期的VIIA族元素单质的晶体类型相同 |
22-23高三上·江苏南通·阶段练习 查看更多[2]
更新时间:2022-10-18 16:35:25
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列化学用语的表达正确的是
A.原子核内有10个中子的氧原子: |
B. 的电子式: 的电子式: |
C. 的最外层电子排布式: 的最外层电子排布式: |
D. 电离: 电离: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】镓 与铝同主族,曾被称为“类铝”,其氧化物、氢氧化物均为两性化合物。工业制备的流程如图所示。下列判断合理的是
与铝同主族,曾被称为“类铝”,其氧化物、氢氧化物均为两性化合物。工业制备的流程如图所示。下列判断合理的是
 与铝同主族,曾被称为“类铝”,其氧化物、氢氧化物均为两性化合物。工业制备的流程如图所示。下列判断合理的是
与铝同主族,曾被称为“类铝”,其氧化物、氢氧化物均为两性化合物。工业制备的流程如图所示。下列判断合理的是
A.基态 原子有3个单电子 原子有3个单电子 | B.酸性: |
C. 可由 可由 与水反应得到 与水反应得到 | D.金属 可从 可从 溶液中置换得到金属 溶液中置换得到金属 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】我国力争于2060年前实现碳中和。 与
与 重整是
重整是 利用的研究热点之一。下列关于
利用的研究热点之一。下列关于 和
和 说法正确的是
说法正确的是
 与
与 重整是
重整是 利用的研究热点之一。下列关于
利用的研究热点之一。下列关于 和
和 说法正确的是
说法正确的是
| A.CO2中C原子采用sp2杂化 |
B. 键角大于 键角大于 键角 键角 |
C. 分子中含有极性共价键,是极性分子 分子中含有极性共价键,是极性分子 |
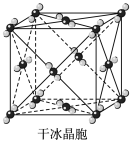
D.干冰中每个 分子周围紧邻12个 分子周围紧邻12个 分子 分子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】乙二酸(HOOC-COOH)受热分解产物为CO、CO2和H2O。下列有关说法正确的是
| A.CO的结构式为C=O |
| B.C、H、O元素电负性由大到小的顺序为O>H>C |
| C.HOOC-COOH分子和CO2分子中碳原子轨道杂化类型相同 |
| D.HOOC-COOH分子内σ键与π键个数之比为7:2 |
您最近一年使用:0次
【推荐1】下列结论与解释不匹配的是
| 选项 | 结论 | 解释 |
| A | CH4的稳定性强于SiH4的 | C-H键键长比Si-H键的短,C-H键键能更大 |
| B | 冰中1个水分子周围只有4个紧邻分子 | 水分子之间存在氢键,氢键具有方向性 |
| C | 氟乙酸的酸性强于氯乙酸的 | 氟的电负性大于氯的电负性 |
| D | CH3CH2OH的沸点比CH3OCH3的沸点高 | CH3CH2OH是极性分子,CH3OCH3是非极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】二氯化二硫(S2Cl2)可用于橡胶的低温硫化剂和黏接剂。其分子结构与H2O2相似,室温下稳定,100℃时分解为相应单质,与氯气反应能生成SO2。下列说法错误的是
| A.H2O2是含有极性键和非极性键的非极性分子 | B.Cl2中Cl-Cl是p-pσ键 |
| C.SO2中硫原子的杂化方式为sp2 | D.酸性:H2SO4<HClO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】氧、硫、铁可形成多种用途广泛的物质。 具有较强的氧化性。亚硫酰氯
具有较强的氧化性。亚硫酰氯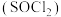 遇水发生水解反应生成
遇水发生水解反应生成 与
与 。
。 可用作锂离子电池的电极材料,电池工作时有
可用作锂离子电池的电极材料,电池工作时有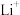 嵌入其中生成
嵌入其中生成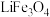 。
。 可用于生产
可用于生产 ,其一种晶胞结构如图1所示。工业上可电解
,其一种晶胞结构如图1所示。工业上可电解 与
与 混合溶液制备过二硫酸铵
混合溶液制备过二硫酸铵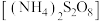 ,其结构如图2所示。酸与碱反应时放热,中和热为
,其结构如图2所示。酸与碱反应时放热,中和热为 。
。

对下列物质性质的解释不合理 的是
 具有较强的氧化性。亚硫酰氯
具有较强的氧化性。亚硫酰氯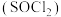 遇水发生水解反应生成
遇水发生水解反应生成 与
与 。
。 可用作锂离子电池的电极材料,电池工作时有
可用作锂离子电池的电极材料,电池工作时有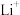 嵌入其中生成
嵌入其中生成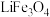 。
。 可用于生产
可用于生产 ,其一种晶胞结构如图1所示。工业上可电解
,其一种晶胞结构如图1所示。工业上可电解 与
与 混合溶液制备过二硫酸铵
混合溶液制备过二硫酸铵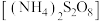 ,其结构如图2所示。酸与碱反应时放热,中和热为
,其结构如图2所示。酸与碱反应时放热,中和热为 。
。
对下列物质性质的解释
A. 的热稳定性强于 的热稳定性强于 , , 分子间存在氢键 分子间存在氢键 |
B. 易液化, 易液化, 是极性分子,分子间作用力较大 是极性分子,分子间作用力较大 |
C.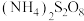 具有较强的氧化性, 具有较强的氧化性,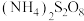 中含过氧键( 中含过氧键( ) ) |
D. 晶体中可嵌入 晶体中可嵌入 形成 形成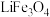 , , 可转化为 可转化为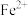 |
您最近一年使用:0次

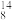 C
C
 、
、 、
、 、
、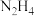 等,下列说法正确的是
等,下列说法正确的是 、
、 两种
两种 的键角相等
的键角相等 、
、 两种阳离子,且两种阳离子都可以与强碱反应
两种阳离子,且两种阳离子都可以与强碱反应 的氨水溶液中,
的氨水溶液中,

