电子工业对超细银粉的需求不断增加,制备过程如下:先将纯银粉溶于浓硝酸,室温下加氨水调节pH至8~9,搅拌下加入分散剂PEG与水合肼混合液,过滤、干燥、研磨得产品。
(1)Ag在周期表中与Cu相邻,Ag原子的基态外围电子排布式为_______ 。
(2)银粉溶于浓硝酸的离子方程式为_______ 。
(3) Ag+直接与水合肼反应过于激烈,加入氨水使反应更加平稳的原因是_______ 。
(4)在pH<4时,加入分散剂PEG与水合肼混合液未发现银单质生成,原因是_______ 。
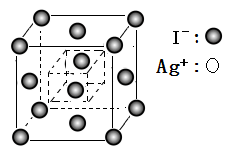
(5)I-在AgI晶胞中位置如图所示,已知Ag+周围有距离最近且相等的4个I-,请画出Ag+在晶胞中的位置_______ 。
(1)Ag在周期表中与Cu相邻,Ag原子的基态外围电子排布式为
(2)银粉溶于浓硝酸的离子方程式为
(3) Ag+直接与水合肼反应过于激烈,加入氨水使反应更加平稳的原因是
(4)在pH<4时,加入分散剂PEG与水合肼混合液未发现银单质生成,原因是
(5)I-在AgI晶胞中位置如图所示,已知Ag+周围有距离最近且相等的4个I-,请画出Ag+在晶胞中的位置

更新时间:2022/10/19 18:06:41
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
【推荐1】用 NaOH溶液制备
NaOH溶液制备 溶液。
溶液。
步骤一:取一定体积的 NaOH溶液,等分成两份;
NaOH溶液,等分成两份;
步骤二:向其中一份中通入过量 ,获得溶液1;
,获得溶液1;
步骤三:将另一份NaOH溶液与溶液1混合即可得到 溶液。
溶液。
(1)“溶液1”中溶质的电离方程式为______ ;“步骤三”中发生反应的离子方程式为______ .
(2)忽略溶液体积变化,最终所得 溶液的物质的量浓度为
溶液的物质的量浓度为______ .
 NaOH溶液制备
NaOH溶液制备 溶液。
溶液。步骤一:取一定体积的
 NaOH溶液,等分成两份;
NaOH溶液,等分成两份;步骤二:向其中一份中通入过量
 ,获得溶液1;
,获得溶液1;步骤三:将另一份NaOH溶液与溶液1混合即可得到
 溶液。
溶液。(1)“溶液1”中溶质的电离方程式为
(2)忽略溶液体积变化,最终所得
 溶液的物质的量浓度为
溶液的物质的量浓度为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】一包固体粉末可能含有Na+、K+、Fe3+、Cl-、NO 、SO
、SO 、HCO
、HCO 中的若干种,小明同学为探究该固体成分,进行如图实验:
中的若干种,小明同学为探究该固体成分,进行如图实验:
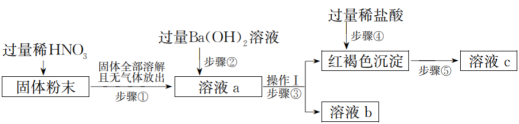
回答下列问题:
(1)由步骤①可推知该粉末中一定不存在的离子为__ (填离子符号,下同),步骤②中涉及的离子方程式为__ 。
(2)操作I的名称为__ ,根据步骤③、步骤⑤的现象可确定该粉末中一定不存在的离子为___ ,步骤④中发生反应的离子方程式为__ 。
(3)检验固体粉末中是否含Cl-的具体操作为__ 。
 、SO
、SO 、HCO
、HCO 中的若干种,小明同学为探究该固体成分,进行如图实验:
中的若干种,小明同学为探究该固体成分,进行如图实验:
回答下列问题:
(1)由步骤①可推知该粉末中一定不存在的离子为
(2)操作I的名称为
(3)检验固体粉末中是否含Cl-的具体操作为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】氨基甲酸铵(NH2COONH4)为白色粉末,易溶于水,难溶于CCl4,水解生成NH4HCO3,受热分解生成CO(NH2)2,是一种优良的氨化剂,其工业制取原理为2NH3(g) +CO2(g) NH2COONH4 (s) ΔH<0。某化学小组模拟工业原理制备少量NH2COONH4,实验装置(夹持仪器及冷却装置已省略)如图所示。
NH2COONH4 (s) ΔH<0。某化学小组模拟工业原理制备少量NH2COONH4,实验装置(夹持仪器及冷却装置已省略)如图所示。

回答下列问题:
(1)装置Ⅰ中胶皮管a的作用为___________ ,仪器 b中发生反应的离子方程式为___________ 。
(2)装置Ⅱ中盛放的试剂为___________ ,若某同学实验时忘记安装装置V,其导致的后果是___________ 。
(3)装置Ⅳ可采取的冷却方式为___________ ,若没有冷却装置会导致氨基甲酸铵的产量降低,其原因是___________ 。
(4)尾气处理装置如图所示,浓硫酸的作用是___________ 。
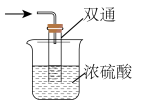
(5)测量氨基甲酸铵样品的纯度:称取含有NH4HCO3的NH2COONH4样品0.782g,用足量石灰水充分处理后,使碳元素完全转化为CaCO3,过滤、洗涤、干燥,所得固体的质量为1. 000 g。则样品中NH2COONH4的纯度为___________ (保留三位有效数字)。
 NH2COONH4 (s) ΔH<0。某化学小组模拟工业原理制备少量NH2COONH4,实验装置(夹持仪器及冷却装置已省略)如图所示。
NH2COONH4 (s) ΔH<0。某化学小组模拟工业原理制备少量NH2COONH4,实验装置(夹持仪器及冷却装置已省略)如图所示。
回答下列问题:
(1)装置Ⅰ中胶皮管a的作用为
(2)装置Ⅱ中盛放的试剂为
(3)装置Ⅳ可采取的冷却方式为
(4)尾气处理装置如图所示,浓硫酸的作用是

(5)测量氨基甲酸铵样品的纯度:称取含有NH4HCO3的NH2COONH4样品0.782g,用足量石灰水充分处理后,使碳元素完全转化为CaCO3,过滤、洗涤、干燥,所得固体的质量为1. 000 g。则样品中NH2COONH4的纯度为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:
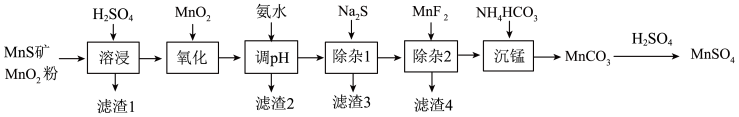
相关金属离子[c(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
(1)Fe2+的价电子排布式为_______ ,在元素周期表中Zn处于_______ 区。
(2)“滤渣1”含有S和_______ ;写出“溶浸”中二氧化锰与硫化锰反应的化学方程式_______ 。
(3)“氧化”中添加适量的MnO2的作用是_______ 。
(4)“调pH”除铁和铝,溶液的pH范围应调节为_______ ~6之间。
(5)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是_______ 。
(6)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_______ 。
(7)写出“沉锰”的离子方程式_______ 。
(8)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y= 时,z=
时,z=_______ 。

相关金属离子[c(Mn+)=0.1mol/L]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)Fe2+的价电子排布式为
(2)“滤渣1”含有S和
(3)“氧化”中添加适量的MnO2的作用是
(4)“调pH”除铁和铝,溶液的pH范围应调节为
(5)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
(6)“除杂2”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(7)写出“沉锰”的离子方程式
(8)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNixCoyMnzO2,其中Ni、Co、Mn的化合价分别为+2、+3、+4。当x=y=
 时,z=
时,z=
您最近一年使用:0次
【推荐2】Q、R、X、M、Y、Z是元素周期表前四周期的六种元素,原子序数依次递增。已知:
①Z位于 区,最外层没有单电子,其余的均为短周期主族元素;
区,最外层没有单电子,其余的均为短周期主族元素;
②基态Y原子的价电子排布式为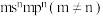 ;
;
③基态Q、X原子p轨道的未成对电子数都是2;
④基态M原子的 能级有1个单电子。
能级有1个单电子。
请回答下列问题:
(1)Z在周期表中的位置为______ 。
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为______ (用对应元素的符号填写)。
(3)分析下表中两种物质的键能数据(单位: )。
)。
结合数据说明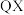 比
比 活泼的原因:
活泼的原因:__________________ 。
①Z位于
 区,最外层没有单电子,其余的均为短周期主族元素;
区,最外层没有单电子,其余的均为短周期主族元素;②基态Y原子的价电子排布式为
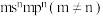 ;
;③基态Q、X原子p轨道的未成对电子数都是2;
④基态M原子的
 能级有1个单电子。
能级有1个单电子。请回答下列问题:
(1)Z在周期表中的位置为
(2)Q、R、X、M四种元素第一电离能由大到小的顺序为
(3)分析下表中两种物质的键能数据(单位:
 )。
)。 |  |  | |
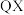 | 351 | 745 | 1076 |
 | 196 | 418 | 945 |
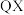 比
比 活泼的原因:
活泼的原因:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】氧族元素是元素周期表中第VIA族元素,包含氧 、硫
、硫 、硒
、硒 、碲
、碲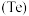 、钋
、钋 五种元素,它们及其化合物在生产、生活中有着广泛的应用。请回答下列问题:
五种元素,它们及其化合物在生产、生活中有着广泛的应用。请回答下列问题:
(1)基态 原子的简化核外电子排布式为
原子的简化核外电子排布式为___________ 。
(2) 、
、 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为___________ 。
(3)依布硒是一种有机硒化物,具有良好的抗炎活性,其结构简式为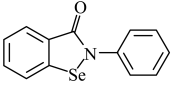 。依布硒分子中
。依布硒分子中 、
、 原子的杂化类型分别为
原子的杂化类型分别为___________ 、___________ 。
(4)国家速滑馆又称为“冰丝带”,所用的碲化镉(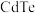 )“发电玻璃”被誉为“挂在墙上的油田”。碲化镉立方晶胞结构如图。
)“发电玻璃”被誉为“挂在墙上的油田”。碲化镉立方晶胞结构如图。 、
、 原子的分数坐标分别为
原子的分数坐标分别为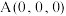 ,
, ,则
,则 点原子的分数坐标为
点原子的分数坐标为___________ 。
②碲化镉晶体的密度为 ,设
,设 为阿伏加德罗常数的值,则其晶胞边长为
为阿伏加德罗常数的值,则其晶胞边长为
___________  。
。
 、硫
、硫 、硒
、硒 、碲
、碲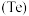 、钋
、钋 五种元素,它们及其化合物在生产、生活中有着广泛的应用。请回答下列问题:
五种元素,它们及其化合物在生产、生活中有着广泛的应用。请回答下列问题:(1)基态
 原子的简化核外电子排布式为
原子的简化核外电子排布式为(2)
 、
、 、
、 、
、 的沸点由高到低的顺序为
的沸点由高到低的顺序为(3)依布硒是一种有机硒化物,具有良好的抗炎活性,其结构简式为
 。依布硒分子中
。依布硒分子中 、
、 原子的杂化类型分别为
原子的杂化类型分别为(4)国家速滑馆又称为“冰丝带”,所用的碲化镉(
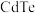 )“发电玻璃”被誉为“挂在墙上的油田”。碲化镉立方晶胞结构如图。
)“发电玻璃”被誉为“挂在墙上的油田”。碲化镉立方晶胞结构如图。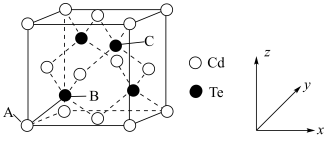
 、
、 原子的分数坐标分别为
原子的分数坐标分别为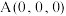 ,
, ,则
,则 点原子的分数坐标为
点原子的分数坐标为②碲化镉晶体的密度为
 ,设
,设 为阿伏加德罗常数的值,则其晶胞边长为
为阿伏加德罗常数的值,则其晶胞边长为
 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】(1)氢键作用常表示为“A—H…B”,其中A、B为电负性很强的一类原子,用氢键的表示方法写出HF溶液中存在的所有氢键________________________ 。
(2)已知某配合物中有如下结构,则N原子的杂化方式为___________ ,在结构式上用“→”标出配位键。___________
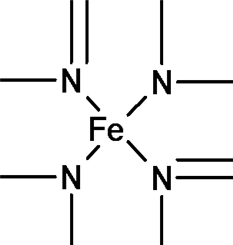
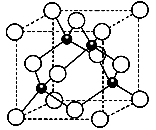
(3)Al和N组成的晶胞结构如下图一所示(“O”表示Al原子):
①则其化学式为_____ ,Al原子的配位数是___ ;
②一个N原子周围距离最近且等距的N原子有_____ 个。
(2)已知某配合物中有如下结构,则N原子的杂化方式为
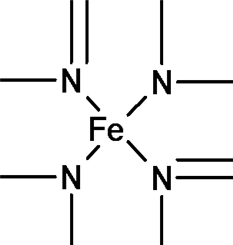
(3)Al和N组成的晶胞结构如下图一所示(“O”表示Al原子):
①则其化学式为
②一个N原子周围距离最近且等距的N原子有

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】镍的合金及其配合物用途非常广泛。回答下列问题:
(1)Ni与Ca均位于第四周期,最外层电子数也相同,但Ni的熔点和沸点均比Ca的高,这是因为_______ 。
(2)Ni2 MnGa晶体的立方晶胞结构如图a所示。

①已知Ni2MnGa的晶胞参数为0.5822nm,设NA为阿伏加德罗常数的数值,则Ni2MnGa晶体的密度为_______ (列出计算式)g· cm-3。
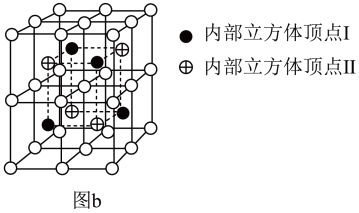
②Ni2MnGa晶体的晶胞结构还可以用图b表示,若●表示的是Mn,则 表示的是
表示的是_______ ,⊕表示的是_______ 。
(1)Ni与Ca均位于第四周期,最外层电子数也相同,但Ni的熔点和沸点均比Ca的高,这是因为
(2)Ni2 MnGa晶体的立方晶胞结构如图a所示。

①已知Ni2MnGa的晶胞参数为0.5822nm,设NA为阿伏加德罗常数的数值,则Ni2MnGa晶体的密度为
②Ni2MnGa晶体的晶胞结构还可以用图b表示,若●表示的是Mn,则
 表示的是
表示的是
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】根据晶体的微观结构,试回答有关问题:
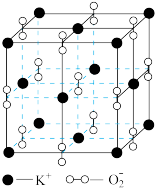
(1)高温下,超氧化钾(KO2)晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。下图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,K+的配位数为_______ ,0价氧原子与-2价氧原子的数目比为_______ 。
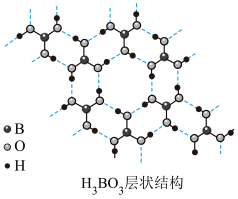
(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的有_______ 。
①硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1 mol H3BO3的晶体中有3 mol氢键
⑤含1 mol H3BO3的晶体中有6 mol极性共价键
(3)确定该合金(如图)的化学式为_____ ,与Fe原子等距离且最短的Fe原子个数为____ ,若晶胞的边长为a nm,此合金的密度为_____ g·cm-3。

(1)高温下,超氧化钾(KO2)晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。下图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,K+的配位数为

(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子通过氢键相连(如图)。下列有关说法正确的有

①硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1 mol H3BO3的晶体中有3 mol氢键
⑤含1 mol H3BO3的晶体中有6 mol极性共价键
(3)确定该合金(如图)的化学式为

您最近一年使用:0次



