回答下列问题:
(1)冰晶石(Na3AlF6)是工业上冶炼铝的助熔剂,制取冰晶石的化学方程式为:2Al(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2+9H2O。上述反应中有两种元素在元素周期表中的位置相邻,二者的电负性较小的是____ (填元素符号),上述反应的生成物中极性分子的立体构型呈____ 。
(2)已知NF3与NH3的组成结构相似,但NF3的沸点比NH3的沸点(-33℃)低得多,其主要原因是____ 。
(3)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式____ 。
(4)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是____ 。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为____ 。
(6)一种有机EL材料结构如图,该分子内存在的作用力有____ (填字母)。
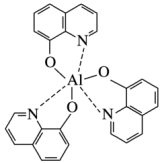
A.σ键 B.π键 C.配位键 D.氢键 E.离子键
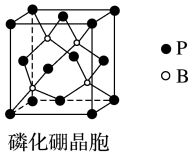
(7)2019年电子科技大学孙旭平教授团队报道了一种磷化硼纳米颗粒作为高选择性CO2电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用,其晶胞结构如图所示。立方氮化硼是一种新型无机非金属材料,熔点很高,硬度很大,立方氮化硼晶体属于____ (填晶体类型),氮化硼与磷化硼具有相似的结构,比较BN和BP的熔点大小并说明原因:____ 。
(1)冰晶石(Na3AlF6)是工业上冶炼铝的助熔剂,制取冰晶石的化学方程式为:2Al(OH)3+12HF+3Na2CO3=2Na3AlF6+3CO2+9H2O。上述反应中有两种元素在元素周期表中的位置相邻,二者的电负性较小的是
(2)已知NF3与NH3的组成结构相似,但NF3的沸点比NH3的沸点(-33℃)低得多,其主要原因是
(3)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式
(4)2020年新冠肺炎疫情席卷全球,酒精(CH3CH2OH)成为家庭必备品,乙醇分子中碳原子轨道的杂化类型是
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数为6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为
(6)一种有机EL材料结构如图,该分子内存在的作用力有

A.σ键 B.π键 C.配位键 D.氢键 E.离子键
(7)2019年电子科技大学孙旭平教授团队报道了一种磷化硼纳米颗粒作为高选择性CO2电化学还原为甲醇的非金属电催化剂。磷化硼熔点特别高,处于极高温的空气环境时也具有抗氧化作用,其晶胞结构如图所示。立方氮化硼是一种新型无机非金属材料,熔点很高,硬度很大,立方氮化硼晶体属于

更新时间:2022-10-24 15:49:13
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】二氧化钛/氧化锌纳米复合材料是重要且广泛使用的无机紫外防晒剂,某研究小组设计了由钛铁矿(主要成分FeTiO2,杂质有Fe2O3、SiO2等)制备二氧化钛/氧化锌纳米复合材料的工艺流程如下:
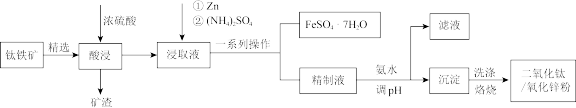
已知:溶液中钛元素均以TiO2+形式存在;几种沉淀难溶物的溶度积常数如下:
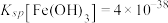
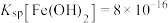
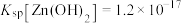
(1)为提高钛铁矿酸浸时的浸出率,除了采用适当升温和增大酸的浓度外,还可以采用___________ 、___________ (写两种方法)。
(2)酸浸的矿渣主要成分是___________ 。
(3)加入锌粉的目的是___________ ,判断该反应完全的操作是___________ 。
(4)浸取率与时间和温度关系分别如图1和图2
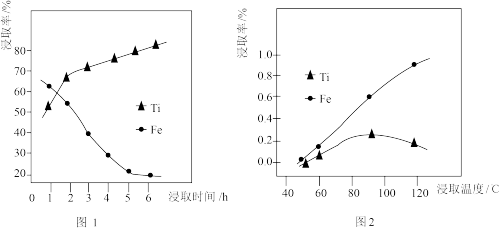
应该选择合适的浸取时间和温度是___________ h,___________ ℃。
(5)调整pH时,TiOSO4水解生成TiO2•xH2O的化学反应方程式为___________ 。
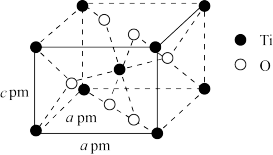
(6)基态Ti原子的电子排布式为___________ ,金红石型TiO2的四方晶胞结构及参数如图所示,密度为d ,则c=
,则c=___________ pm(NA表示阿佛加德罗常数的值)。

已知:溶液中钛元素均以TiO2+形式存在;几种沉淀难溶物的溶度积常数如下:
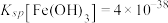
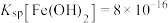
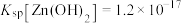
(1)为提高钛铁矿酸浸时的浸出率,除了采用适当升温和增大酸的浓度外,还可以采用
(2)酸浸的矿渣主要成分是
(3)加入锌粉的目的是
(4)浸取率与时间和温度关系分别如图1和图2

应该选择合适的浸取时间和温度是
(5)调整pH时,TiOSO4水解生成TiO2•xH2O的化学反应方程式为
(6)基态Ti原子的电子排布式为
 ,则c=
,则c=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】氨、磷、砷在农药、肥料等农业生产方面有广泛的应用。回答相关问题:
(1)氨水是一种速效氮肥:
①氨水中存在_______ 种氢键,根据氨水的性质,可推知 与
与 之间形成的最主要氢键是
之间形成的最主要氢键是_______ ;(用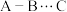 表示)
表示)
②氨水中含有配位键的粒子有 和X,则X的离子符号为
和X,则X的离子符号为_______ 。X离子中形成的配位键中提供孤电子对的原子是_______ 。
(2)甲胺磷是一种剧毒农药,分子结构如下,试回答下列问题
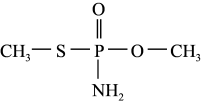
①甲胺磷分子中P原子的杂化方式为_______ ;P元素的化合价为_______ 。
②O、N、S的第一电离能由大到小的排列顺序为_______ 。
③甲胺磷易溶于水,其主要原因是_______ 。
(3)As的简化电子排布式为:_______ ;它有两种含氧酸: 和
和 ,其中酸性较强的是
,其中酸性较强的是_______ 。
(1)氨水是一种速效氮肥:
①氨水中存在
 与
与 之间形成的最主要氢键是
之间形成的最主要氢键是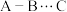 表示)
表示)②氨水中含有配位键的粒子有
 和X,则X的离子符号为
和X,则X的离子符号为(2)甲胺磷是一种剧毒农药,分子结构如下,试回答下列问题
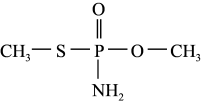
①甲胺磷分子中P原子的杂化方式为
②O、N、S的第一电离能由大到小的排列顺序为
③甲胺磷易溶于水,其主要原因是
(3)As的简化电子排布式为:
 和
和 ,其中酸性较强的是
,其中酸性较强的是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】镍、铜等金属及其化合物在工农业生产上有重要用途。回答下列问题:
(1)基态Ni的核外电子排布式为_______ ,Ni位于元素周期表中_______ 区(填“s”“p”“d”或“ds”),其核外电子占据的最高能层符号为_______ 。
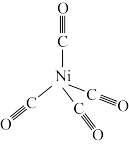
(2)Ni与CO能形成如图所示的配合物 ,该分子中σ键与π键个数比为
,该分子中σ键与π键个数比为_______ 。 易溶于
易溶于_______ (填标号)。
A.水 B.四氯化碳 C.苯 D.稀
(3)将Cu粉加入浓氨水中,并通入 ,充分反应后溶液呈深蓝色,该反应的离子方程式为
,充分反应后溶液呈深蓝色,该反应的离子方程式为_______ 。
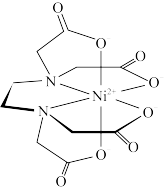
(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有_______ 个,其中提供孤对电子的原子为_______ (写元素符号)。
(5)钴的一种化合物的晶胞结构如下图所示:

①已知A点的原子坐标参数为(0,0,0),B点为( ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为_______ 。
②已知晶胞参数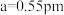 ,则该晶体的密度为
,则该晶体的密度为_______  (用NA表示阿伏加德罗常数,只列出计算表达式即可。
(用NA表示阿伏加德罗常数,只列出计算表达式即可。
(1)基态Ni的核外电子排布式为
(2)Ni与CO能形成如图所示的配合物
 ,该分子中σ键与π键个数比为
,该分子中σ键与π键个数比为 易溶于
易溶于
A.水 B.四氯化碳 C.苯 D.稀

(3)将Cu粉加入浓氨水中,并通入
 ,充分反应后溶液呈深蓝色,该反应的离子方程式为
,充分反应后溶液呈深蓝色,该反应的离子方程式为(4)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
与EDTA形成的螯合物的结构如图所示,1个该配合物中通过螯合作用形成的配位键有
(5)钴的一种化合物的晶胞结构如下图所示:

①已知A点的原子坐标参数为(0,0,0),B点为(
 ,0,
,0, ),则C点的原子坐标参数为
),则C点的原子坐标参数为②已知晶胞参数
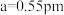 ,则该晶体的密度为
,则该晶体的密度为 (用NA表示阿伏加德罗常数,只列出计算表达式即可。
(用NA表示阿伏加德罗常数,只列出计算表达式即可。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】前四周期元素A、B、C、D、E的原子序数依次增大,A元素原子的核外电子只有一种运动状态;基态B原子s能级的电子总数比p能级的多1;基态C原子和基态E原子中成对电子数均是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题:
(1)E的元素名称为___________ 。
(2)元素A、B、C中,电负性最大的是___________ (填元素符号 ) 。
(3)BC 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为___________ ,BC 的空间结构为
的空间结构为___________ 。
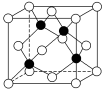
(4)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为___________ g·cm-3(用NA表示阿伏加德罗常数的值)。
(1)E的元素名称为
(2)元素A、B、C中,电负性最大的是
(3)BC
 中B原子轨道的杂化类型为
中B原子轨道的杂化类型为 的空间结构为
的空间结构为(4)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB的晶胞参数为a pm,则晶体的密度为
您最近一年使用:0次
【推荐2】丁二酮肟(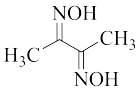 )可与
)可与 反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定
反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定 的存在。请回答下列问题:
的存在。请回答下列问题:
(1)Ni在元素周期表中的位置为___________ 。
(2)基态氧原子的核外电子的运动状态有___________ 种。
(3)丁二酮肟(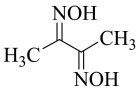 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为___________ ;与氮同周期的硼在成键时,能将一个 电子激发进入
电子激发进入 能级参与形成化学键,请写出该激发态原子的价电子轨道表示式:
能级参与形成化学键,请写出该激发态原子的价电子轨道表示式:___________ ,该过程形成的原子光谱为___________ (填“吸收”或“发射”)光谱。
(4)与Ni同周期的铜、锌两种元素位于元素周期表的___________ 区,两元素的第一电离能 、第二电离能
、第二电离能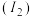 数据如表所示:
数据如表所示:
铜的 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是___________ 。
 )可与
)可与 反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定
反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定 的存在。请回答下列问题:
的存在。请回答下列问题:(1)Ni在元素周期表中的位置为
(2)基态氧原子的核外电子的运动状态有
(3)丁二酮肟(
 )中涉及元素的电负性由大到小的顺序为
)中涉及元素的电负性由大到小的顺序为 电子激发进入
电子激发进入 能级参与形成化学键,请写出该激发态原子的价电子轨道表示式:
能级参与形成化学键,请写出该激发态原子的价电子轨道表示式:(4)与Ni同周期的铜、锌两种元素位于元素周期表的
 、第二电离能
、第二电离能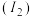 数据如表所示:
数据如表所示:电离能 |  |  |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
 小于锌,
小于锌, 却大于锌的主要原因是
却大于锌的主要原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】第23号元素钒在地壳中的含量大约为0.009%,在过渡元素中仅次于Fe、Ti、Mn、Zn,排第五位。我国四川攀枝花地区蕴藏着极其丰富的钒钛磁铁矿。
(1)钒在周期表中的位置为__________ ,电子占据的最高能层的轨道形状为__________ 。
(2)在地壳中含量最高的五种过渡金属元素Fe、Ti、Mn、Zn、V中,基态原子核外单电子数最多的是__________ 。
(3)过渡金属可形成许多羰基配合物,即CO作为配体形成的配合物。
①CO的等电子体有N2、CN-、__________ (任写一个)等。
②CO作配体时,配位原子是C而不是O,其原因是__________ 。
(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如[Fe(CO)5]、[Mn(CO)5]-等都满足这个规则。
①下列钒配合物中,钒原子满足18电子规则的是__________ 。
A.[V(H2O)6]2+ B.[V(CN)6]4- C.[V(CO)6]- D.[V(O2)4]3-
②化合物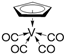 的熔点为138 ℃,其晶体类型为
的熔点为138 ℃,其晶体类型为__________ ;已知该化合物满足18电子规则,其配体“ ”中的大π键可表示为
”中的大π键可表示为__________ 。
(5)VCl2(熔点1027 ℃)和VBr2(熔点827 ℃)均为六方晶胞,结构如图所示。
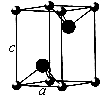
①VCl2和VBr2两者熔点差异的原因是__________ 。
②设晶体中阴、阳离子半径分别为r-和r+,该晶体的空间利用率为__________ (用含a、c、r+和r-的式子表示)。
(1)钒在周期表中的位置为
(2)在地壳中含量最高的五种过渡金属元素Fe、Ti、Mn、Zn、V中,基态原子核外单电子数最多的是
(3)过渡金属可形成许多羰基配合物,即CO作为配体形成的配合物。
①CO的等电子体有N2、CN-、
②CO作配体时,配位原子是C而不是O,其原因是
(4)过渡金属配合物常满足“18电子规则”,即中心原子的价电子数加上配体提供的电子数之和等于18,如[Fe(CO)5]、[Mn(CO)5]-等都满足这个规则。
①下列钒配合物中,钒原子满足18电子规则的是
A.[V(H2O)6]2+ B.[V(CN)6]4- C.[V(CO)6]- D.[V(O2)4]3-
②化合物
 的熔点为138 ℃,其晶体类型为
的熔点为138 ℃,其晶体类型为 ”中的大π键可表示为
”中的大π键可表示为(5)VCl2(熔点1027 ℃)和VBr2(熔点827 ℃)均为六方晶胞,结构如图所示。

①VCl2和VBr2两者熔点差异的原因是
②设晶体中阴、阳离子半径分别为r-和r+,该晶体的空间利用率为
您最近一年使用:0次
【推荐1】过渡金属及其化合物在生产生活中有着广泛应用。锰钢异常坚硬,且具抗冲击性能,是制造枪栓、保险库、挖掘机械和铁路设施的理想材料;锰也是人体的重要微量元素。请根据所学知识,回答下列问题:
(1)铬、锰、铁称为黑色金属,位于同一周期的相邻位置。锰的原子序数是______ ; 基态离子的价层电子排布图为
基态离子的价层电子排布图为______ 。
(2)下列状态的铁中,电离最外层的一个电子所需能量最大的是______(填编号)。
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与 形成黄色的配合物。锰试剂的结构如图所示,
形成黄色的配合物。锰试剂的结构如图所示,
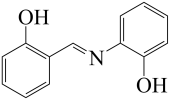
其分子中可能与 形成配位键的原子有
形成配位键的原子有______ ;锰试剂______ (填“能”或“不能”)形成分子内氢键。
(4)锰试剂分子中除氢以外的元素,第一电离能从小到大的顺序为______ (用元素符号表示)。
(5) 规则指的是配合物中心原子价电子数和配体提供的电子数之和为18.符合
规则指的是配合物中心原子价电子数和配体提供的电子数之和为18.符合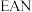 规则的配合物分子结构和化学性质都较稳定。已知
规则的配合物分子结构和化学性质都较稳定。已知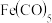 和
和 均符合
均符合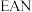 规则,性质稳定,而
规则,性质稳定,而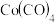 则容易在化学反应中表现氧化性。
则容易在化学反应中表现氧化性。
①x=______ 。
②从结构角度解释Co(CO)4容易在化学反应中表现氧化性的原因______ 。
(1)铬、锰、铁称为黑色金属,位于同一周期的相邻位置。锰的原子序数是
 基态离子的价层电子排布图为
基态离子的价层电子排布图为(2)下列状态的铁中,电离最外层的一个电子所需能量最大的是______(填编号)。
A.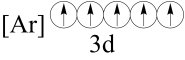 | B.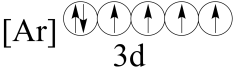 |
C.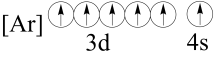 | D. |
 形成黄色的配合物。锰试剂的结构如图所示,
形成黄色的配合物。锰试剂的结构如图所示,
其分子中可能与
 形成配位键的原子有
形成配位键的原子有(4)锰试剂分子中除氢以外的元素,第一电离能从小到大的顺序为
(5)
 规则指的是配合物中心原子价电子数和配体提供的电子数之和为18.符合
规则指的是配合物中心原子价电子数和配体提供的电子数之和为18.符合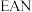 规则的配合物分子结构和化学性质都较稳定。已知
规则的配合物分子结构和化学性质都较稳定。已知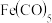 和
和 均符合
均符合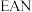 规则,性质稳定,而
规则,性质稳定,而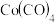 则容易在化学反应中表现氧化性。
则容易在化学反应中表现氧化性。①x=
②从结构角度解释Co(CO)4容易在化学反应中表现氧化性的原因
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】过渡金属不但能够与非金属元素形成化合物,还能与其他金属元素形成金属互化物。回答下列问题:
(1)Mn在元素周期表中的位置___________ ,属于___________ 区的元素,基态锰原子的价电子轨道表示式为___________ 。
(2)二茂铁化学式为 ,由
,由 与两个
与两个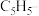 构成(如图),熔点为172℃。
构成(如图),熔点为172℃。___________ 。
②大 键通常用符号
键通常用符号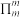 表示(m代表参与形大
表示(m代表参与形大 键的原子数,n代表大
键的原子数,n代表大 键的电子数),则
键的电子数),则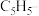 中的大
中的大 键表示为
键表示为___________ 。
③ 与两个
与两个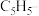 离子形成配位键后,使
离子形成配位键后,使 的3d、4s、4p能级中共具有18电子的稳定结构。则
的3d、4s、4p能级中共具有18电子的稳定结构。则 与两个
与两个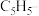 离子形成配位键的数目为
离子形成配位键的数目为___________ 。
(3)锰和镓形成的金属互化物立方晶胞如图所示。
___________ (填标号)。
A.面心B.体心C.顶点D.棱心
②晶胞中,相邻Mn原子构成的正四面体空隙完全由镍原子填充,可用于制备碳基金属催化剂。1号Mn原子坐标参数为 ,则填充在1、2、3、4号Mn构成的四面体空隙中心的镍原子的坐标参数为
,则填充在1、2、3、4号Mn构成的四面体空隙中心的镍原子的坐标参数为___________ ;晶胞参数为a nm,则填充镍后的晶胞的密度
___________  (用含
(用含 、a的代数式表示)。
、a的代数式表示)。
(1)Mn在元素周期表中的位置
(2)二茂铁化学式为
 ,由
,由 与两个
与两个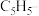 构成(如图),熔点为172℃。
构成(如图),熔点为172℃。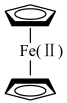
②大
 键通常用符号
键通常用符号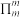 表示(m代表参与形大
表示(m代表参与形大 键的原子数,n代表大
键的原子数,n代表大 键的电子数),则
键的电子数),则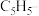 中的大
中的大 键表示为
键表示为③
 与两个
与两个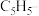 离子形成配位键后,使
离子形成配位键后,使 的3d、4s、4p能级中共具有18电子的稳定结构。则
的3d、4s、4p能级中共具有18电子的稳定结构。则 与两个
与两个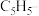 离子形成配位键的数目为
离子形成配位键的数目为(3)锰和镓形成的金属互化物立方晶胞如图所示。
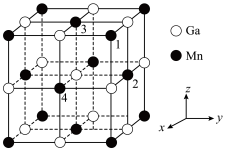
A.面心B.体心C.顶点D.棱心
②晶胞中,相邻Mn原子构成的正四面体空隙完全由镍原子填充,可用于制备碳基金属催化剂。1号Mn原子坐标参数为
 ,则填充在1、2、3、4号Mn构成的四面体空隙中心的镍原子的坐标参数为
,则填充在1、2、3、4号Mn构成的四面体空隙中心的镍原子的坐标参数为
 (用含
(用含 、a的代数式表示)。
、a的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】第四周期元素在生产生活中具有重要的作用。请回答下列问题:
(1)基态Sc原子的价电子排布图为___________ 。
(2)Zn2+和CN-、K+可组成化合物K2Zn(CN)4,其中存在的化学键类型有____________ ;Zn(CN) 中的配体为
中的配体为_______ ,配位原子为_____ ,与该配离子中配体等电子体的分子为___ 。
(3)与Br同主族的短周期元素有F、Cl,这三种元素的简单氢化物HF、HCl、HBr的沸点从高到低的顺序为___________ ,理由为______ 。
(4)Fe-Cr-Al合金可作为汽车尾气催化剂的载体,汽车尾气催化剂可将NO2还原为无毒害的气体,防止HNO3型酸雨的形成,NO2的空间构型为_____ 。HNO3的酸性强于HNO2的原因为___________ 。
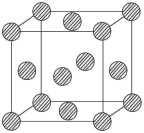
(5)金属铜采用面心立方堆积方式,其晶胞结构如图所示。已知该晶胞的密度为ρg. cm-3,晶胞参数为anm,阿伏加 德罗常数为NA,则铜原子的相对原子质量的表达式为_______ (用含有ρ、a、NA的表达式表示)。
(1)基态Sc原子的价电子排布图为
(2)Zn2+和CN-、K+可组成化合物K2Zn(CN)4,其中存在的化学键类型有
 中的配体为
中的配体为(3)与Br同主族的短周期元素有F、Cl,这三种元素的简单氢化物HF、HCl、HBr的沸点从高到低的顺序为
(4)Fe-Cr-Al合金可作为汽车尾气催化剂的载体,汽车尾气催化剂可将NO2还原为无毒害的气体,防止HNO3型酸雨的形成,NO2的空间构型为
(5)金属铜采用面心立方堆积方式,其晶胞结构如图所示。已知该晶胞的密度为ρg. cm-3,晶胞参数为anm,阿伏加 德罗常数为NA,则铜原子的相对原子质量的表达式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】元素周期表中的VA、ⅥA、ⅦA族非金属元素的单质及其化合物用途非常广泛。回答下列问题:
I.(1)基态锑(Sb)原子价电子排布式为____ 。[H2F]+[SbF6]-(氟酸锑)是一种超强酸,存在[H2F]+,该离子的VSEPR模型为______
II.已知: 含氧酸酸性强弱与非羟基氧原子数有关,几种含氧酸的分子式如下表:
回答下列问题:
(2)H3PO2酸性比H3PO3弱的原因为___________________________________ , H3PO2和过量的NaOH溶液反应的化学方程式是:_____________________ ,
(3)H3PO3和H3AsO3分子式相似,但它们的酸性差别很大,H3PO3是二元中强酸,H3AsO3既有弱酸性又有弱碱性。由此可推出它们的结构简式分别为__________________ ,______________________ 。
(4)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序_____ (填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性,则H3BO3的电离方程式为_____________________ 。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在_______ (填序号):
A.离子键 B.σ键 C.π键 D.配位键 E.范德华力
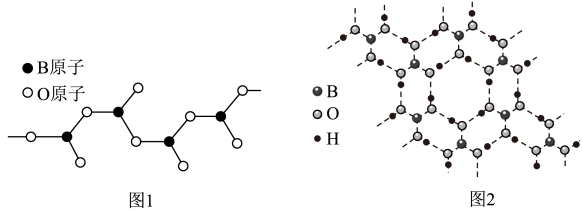
(5)图1表示多硼酸根离子的一种无限长的链式结构,其化学式可表示为___________ 。
(6)硼酸晶体是片层结构,其中一层的结构如图2所示。硼酸在冷水中溶解度很小,但在热水中较大,原因是_________________________________ 。
I.(1)基态锑(Sb)原子价电子排布式为
II.已知: 含氧酸酸性强弱与非羟基氧原子数有关,几种含氧酸的分子式如下表:
| 酸的名称 | 次磷酸 | 亚磷酸 | 硼酸 | 亚砷酸 |
| 分子式 | H3PO2 | H3PO3 | H3BO3 | H3AsO3 |
| 类别 | 一元中强酸 | 二元中强酸 | 一元弱酸 | 三元弱酸 |
回答下列问题:
(2)H3PO2酸性比H3PO3弱的原因为
(3)H3PO3和H3AsO3分子式相似,但它们的酸性差别很大,H3PO3是二元中强酸,H3AsO3既有弱酸性又有弱碱性。由此可推出它们的结构简式分别为
(4)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性,则H3BO3的电离方程式为
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在
A.离子键 B.σ键 C.π键 D.配位键 E.范德华力
(5)图1表示多硼酸根离子的一种无限长的链式结构,其化学式可表示为
(6)硼酸晶体是片层结构,其中一层的结构如图2所示。硼酸在冷水中溶解度很小,但在热水中较大,原因是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】短周期的5种非金属元素,其中A、B、C的特征电子排布可表示为:A:asa,B:bsbbpb,C:csccp2c;D与B同主族,E在C的下一周期,且是同周期元素中电负性最大的元素。
回答下列问题:
(1)由A、B、C、E四种元素中的两种元素可形成多种分子,下列分子:①BC2②BA4③A2C2④BE4,其中属于极性分子的是_____ (填序号),由极性键构成的非极性分子是______ 。
(2)C的氢化物比下一周期同族元素的氢化物沸点还要高,其原因是___________________________________ 。
(3)B、C两元素都能和A元素组成两种常见的溶剂,BE4在前者中的溶解性________ (填“大于”或“小于”)在后者中的溶解性,原因是___________________________________ 。
(4)BA4、BE4和DE4的沸点从高到低的顺序为__________________ (填化学式)。
(5)A、C、E三种元素可形成多种含氧酸,如AEC、AEC2、AEC3、AEC4等,以上列举的四种酸其酸性由强到弱的顺序为_______________________________________ (填化学式)。
回答下列问题:
(1)由A、B、C、E四种元素中的两种元素可形成多种分子,下列分子:①BC2②BA4③A2C2④BE4,其中属于极性分子的是
(2)C的氢化物比下一周期同族元素的氢化物沸点还要高,其原因是
(3)B、C两元素都能和A元素组成两种常见的溶剂,BE4在前者中的溶解性
(4)BA4、BE4和DE4的沸点从高到低的顺序为
(5)A、C、E三种元素可形成多种含氧酸,如AEC、AEC2、AEC3、AEC4等,以上列举的四种酸其酸性由强到弱的顺序为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】铜是人类最早使用的金属之一,用黄铜矿(主要成分为CuFeS2)生产粗铜的反应原理如下:
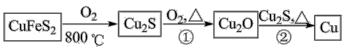
回答下列问题:
(1)第三周期主族元素中电负性比S小的元素有______ 种,H2S的沸点比H2O的______ (填“高”或“低”),原因是______ 。
(2)Cu2O和Cu2S均为______ 晶体,Cu2O的熔点为1235℃,Cu2S的熔点为1130℃,Cu2O熔点较高的原因是______ 。
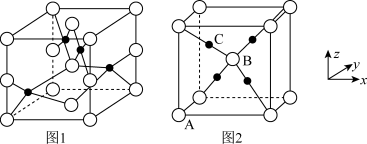
(3)铜的两种氧化物的晶胞如图1、图2所示,图1表示______ (填化学式),图2中,A原子坐标参数为(0,0,0),B原子为( ,
, ,
, ),则C原子的坐标参数为
),则C原子的坐标参数为______ 。
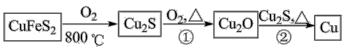
回答下列问题:
(1)第三周期主族元素中电负性比S小的元素有
(2)Cu2O和Cu2S均为
(3)铜的两种氧化物的晶胞如图1、图2所示,图1表示
 ,
, ,
, ),则C原子的坐标参数为
),则C原子的坐标参数为
您最近一年使用:0次



