已知: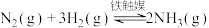
 ,选择500℃左右是因为催化剂(铁触媒)在此温度下活性最佳。最近我国研制出一种新型合成氨催化剂,其最佳活化温度为350℃左右。则使用该新型催化剂合成氨时,下列说法错误的是
,选择500℃左右是因为催化剂(铁触媒)在此温度下活性最佳。最近我国研制出一种新型合成氨催化剂,其最佳活化温度为350℃左右。则使用该新型催化剂合成氨时,下列说法错误的是
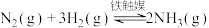
 ,选择500℃左右是因为催化剂(铁触媒)在此温度下活性最佳。最近我国研制出一种新型合成氨催化剂,其最佳活化温度为350℃左右。则使用该新型催化剂合成氨时,下列说法错误的是
,选择500℃左右是因为催化剂(铁触媒)在此温度下活性最佳。最近我国研制出一种新型合成氨催化剂,其最佳活化温度为350℃左右。则使用该新型催化剂合成氨时,下列说法错误的是| A.可提高反应物的平衡转化率 | B.可改变合成氨反应的焓变 |
| C.可减少合成氨的能耗 | D.可降低合成氨的反应温度 |
更新时间:2022/11/15 22:53:29
|
相似题推荐
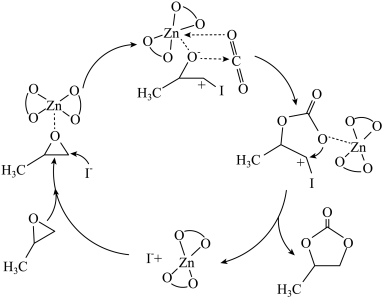
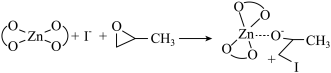
【推荐1】某种制备H2O2的反应机理如图。下列说法不正确的是
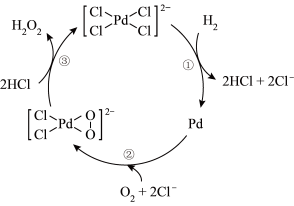

| A.总反应可表示为H2+O2=H2O2 |
B.该反应历程中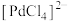 起到催化作用 起到催化作用 |
| C.HCl和Cl-可循环利用 |
| D.①、②、③均为氧化还原反应 |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
解题方法
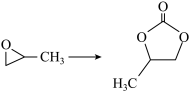
【推荐2】研究 与自由基Cl原子(Cl·表示)的反应有助于保护臭氧层。已知
与自由基Cl原子(Cl·表示)的反应有助于保护臭氧层。已知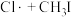 反应有4条反应路径(TS表示过渡态,IM表示中间物)如图所示。下列说法
反应有4条反应路径(TS表示过渡态,IM表示中间物)如图所示。下列说法不正确 的是
 与自由基Cl原子(Cl·表示)的反应有助于保护臭氧层。已知
与自由基Cl原子(Cl·表示)的反应有助于保护臭氧层。已知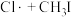 反应有4条反应路径(TS表示过渡态,IM表示中间物)如图所示。下列说法
反应有4条反应路径(TS表示过渡态,IM表示中间物)如图所示。下列说法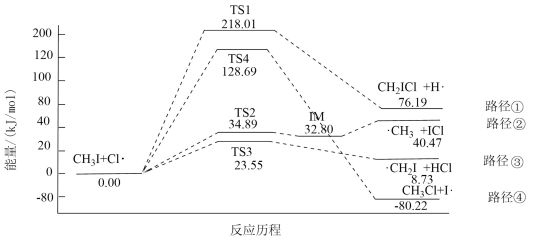
| A.升高温度有利于提高路径①产物的选择性 |
B.路径②中 与Cl·反应生成 与Cl·反应生成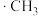 与ICl的过程不是一个基元反应 与ICl的过程不是一个基元反应 |
| C.反应较短时间时,路径④产物的选择性大于路径③ |
| D.四个反应路径都涉及极性键的断裂与生成 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】1,3-丁二烯与HBr发生加成反应分两步:第一步H+进攻1,3-丁二烯生成碳正离子(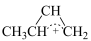 );第二步Br-进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。下列说法
);第二步Br-进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。下列说法不正确 的是
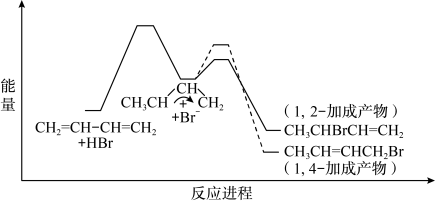
CH2=CHCH=CH2(g)+HBr(g)→CH3-CHBr -CH=CH2(g) ΔH1
CH2=CHCH=CH2(g)+HBr(g)→CH3-CH=CH-CH2Br(g) ΔH2
已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。
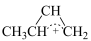 );第二步Br-进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。下列说法
);第二步Br-进攻碳正离子完成1,2-加成或1,4-加成。反应进程中的能量变化如下图所示。下列说法
CH2=CHCH=CH2(g)+HBr(g)→CH3-CHBr -CH=CH2(g) ΔH1
CH2=CHCH=CH2(g)+HBr(g)→CH3-CH=CH-CH2Br(g) ΔH2
已知在0℃和40℃时,1,2-加成产物与1,4-加成产物的比例分别为70:30和15:85。
| A.ΔH1>ΔH2 |
| B.1,4-加成产物比1,2-加成产物稳定 |
| C.与0℃相比,40℃时反应速率快且1,3-丁二烯的平衡转化率增大 |
| D.无论哪种加成方式,第一步反应速率均小于第二步反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
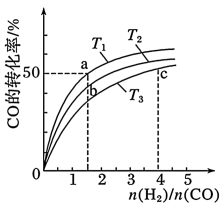
【推荐2】工业上以CO和H2为原料合成甲醇的反应: ,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
 ,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇,如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
| A.H2转化率:c>a>b |
| B.上述三种温度之间关系为T1>T2>T3 |
C.a点状态下再通入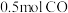 和 和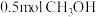 平衡向正方向移动 平衡向正方向移动 |
D.c点状态下再通入 和 和 ,新平衡中 ,新平衡中 的体积分数增大 的体积分数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知合成氨反应:N2(g)+3H2(g) 2NH3(g) ∆H<0,工业上选择的适宜条件为500 ℃、铁作催化剂、20 Mpa~50 Mpa下列叙述中正确的是
2NH3(g) ∆H<0,工业上选择的适宜条件为500 ℃、铁作催化剂、20 Mpa~50 Mpa下列叙述中正确的是
 2NH3(g) ∆H<0,工业上选择的适宜条件为500 ℃、铁作催化剂、20 Mpa~50 Mpa下列叙述中正确的是
2NH3(g) ∆H<0,工业上选择的适宜条件为500 ℃、铁作催化剂、20 Mpa~50 Mpa下列叙述中正确的是| A.工业合成氨的反应是∆H<0、∆S<0的反应,在任何温度下都可自发进行 |
| B.将氨从混合气中分离,可加快反应速率,且有利于平衡向合成氨的方向移动 |
| C.升高温度可以加快反应速率,所以工业生产中尽可能提高温度 |
| D.合成氨反应选择在400~500 ℃进行的重要原因是催化剂在500 ℃左右时的活性最大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】利用图中装置进行实验,能达到实验目的的是
| A | B |
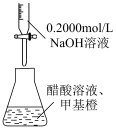 | 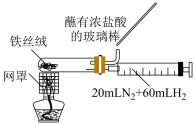 |
| 装置测定醋酸浓度 | 合成氨并检验氨的生成 |
| C | D |
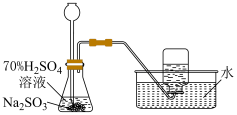 | 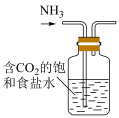 |
制备 | 模拟侯氏制碱法制备 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 +O=C=O
+O=C=O 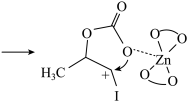
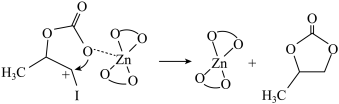 +I
+I 发生反应:
发生反应: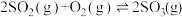 ,温度分别为
,温度分别为 和
和 时,
时, 的体积分数随时间的变化如图所示,平衡时体系的压强分别为
的体积分数随时间的变化如图所示,平衡时体系的压强分别为 、
、 。下列说法正确的是
。下列说法正确的是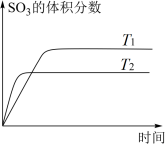

 、
、 在实际生产中可循环使用,所以总体来说合成氨的产率很高
在实际生产中可循环使用,所以总体来说合成氨的产率很高 只占15%,故合成氨厂的产率都很低
只占15%,故合成氨厂的产率都很低

