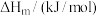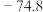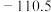回答下列问题:
(1)25℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如表:
则该温度下,
_______  ;
;
_______ (用 和
和 表示)。
表示)。
(2)25℃时,在体积为 的恒容密闭容器中通入
的恒容密闭容器中通入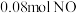 和
和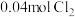 发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强
发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强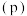 随时间
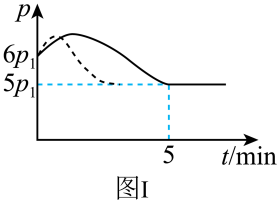
随时间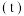 的变化如图Ⅰ实线所示,则
的变化如图Ⅰ实线所示,则
_______ (填“>”“<”或“=”)0;若其他条件相同,仅改变某一条件,测得其压强随时间的变化如图Ⅰ虚线所示,则改变的条件是_______ ;在 时,再充入
时,再充入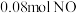 和
和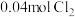 ,则混合气体的平均相对分子质量将
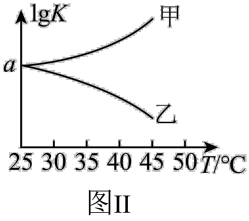
,则混合气体的平均相对分子质量将_______ (填“增大”、“减小”或“不变”)。图Ⅱ是甲、乙两同学描绘上述反应③的平衡常数的对数值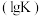 与温度的变化关系图,其中正确的曲线是
与温度的变化关系图,其中正确的曲线是_______ (填“甲”或“乙”),a值为_______ 。25℃时测得反应③在某时刻, 、
、 、
、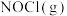 的浓度分别为0.7、0.1、0.3,则此时
的浓度分别为0.7、0.1、0.3,则此时
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)在300℃、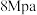 下,将
下,将 和
和 按物质的量之比
按物质的量之比 通入一密闭容器中发生
通入一密闭容器中发生 中反应,达到平衡时,测得
中反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)25℃时,制备亚硝酰氯所涉及的热化学方程式和平衡常数如表:
| 热化学方程式 | 平衡常数 | |
| ① | 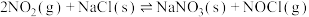  |  |
| ② | 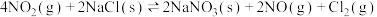 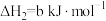 |  |
| ③ |   |  |

 ;
;
 和
和 表示)。
表示)。(2)25℃时,在体积为
 的恒容密闭容器中通入
的恒容密闭容器中通入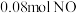 和
和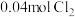 发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强
发生上述反应③,若反应开始与结束时温度相同,数字压强仪显示反应过程中压强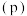 随时间
随时间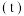 的变化如图Ⅰ实线所示,则
的变化如图Ⅰ实线所示,则
 时,再充入
时,再充入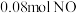 和
和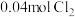 ,则混合气体的平均相对分子质量将
,则混合气体的平均相对分子质量将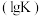 与温度的变化关系图,其中正确的曲线是
与温度的变化关系图,其中正确的曲线是 、
、 、
、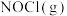 的浓度分别为0.7、0.1、0.3,则此时
的浓度分别为0.7、0.1、0.3,则此时
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。

(3)在300℃、
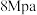 下,将
下,将 和
和 按物质的量之比
按物质的量之比 通入一密闭容器中发生
通入一密闭容器中发生 中反应,达到平衡时,测得
中反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
18-19高二上·福建·期中 查看更多[9]
【全国百强校】福建省师范大学附属中学2018-2019学年高二(理)上学期期中考试化学试题【全国百强校】福建省师范大学附属中学2018-2019学年高二(实验班)上学期期中考试化学试题河北省石家庄市第二中学2019-2020学年高一下学期期末考试化学试题安徽省皖北名校2020-2021学年高二上学期第一次联考化学试题江西省赣州市南康中学2020-2021学年高二上学期第二次大考化学试题河北省邯郸市联盟校2020-2021学年高二上学期期中考试化学试题陕西省汉中市洋县中学2022-2023学年高二上学期期中考试化学试题内蒙古赤峰市第四中学分校2021-2022学年高二上学期9月月考化学试题安徽省滁州市定远县育才学校2021-2022学年高二(实验班)下学期开学摸底考试化学试题
更新时间:2022-11-10 15:45:46
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】肼( )有较强的还原性,与
)有较强的还原性,与 等可组成火箭推进剂。
等可组成火箭推进剂。
(1)已知:Ⅰ.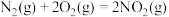

Ⅱ.
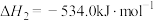
Ⅲ.

火箭发射时 与
与 反应生成
反应生成 和
和 。该反应的热化学方程式是
。该反应的热化学方程式是___________ 。
(2)肼的传统生产工艺为Raschig法,两步反应分别在不同容器的水溶液环境中进行:
i.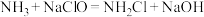 (快)
(快)
ii.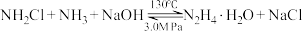 (慢)
(慢)
已知电负性N>Cl。下列说法正确的是___________ (填序号)。
a.反应i中NaClO做氧化剂
b.适当提高反应i温度,可显著提高相同时间内 的产量
的产量
c.采用3.0MPa压强可以增大 的溶解度,提高反应ii中
的溶解度,提高反应ii中 的利用率
的利用率
(3)采用Raschig法制得肼后,可采用分步蒸馏的方法将其从反应混合液中分离出来。
①水合肼( ,常温为液态)中
,常温为液态)中 与
与 间存在氢键,用“X-H…Y”表示
间存在氢键,用“X-H…Y”表示 与
与 间存在的氢键:
间存在的氢键:___________ 。
②蒸馏过程中首先馏出的物质是___________ (填序号)。
a. b.
b. c.NaCl
c.NaCl
(4)产品中肼含量的测定方法如下。
取0.50g产品加20mL水稀释,滴入2滴淀粉溶液,用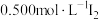 溶液滴定3次,平均每次消耗
溶液滴定3次,平均每次消耗 溶液20.00mL。已知:
溶液20.00mL。已知: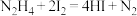
①样品中肼(以 计)的质量分数为
计)的质量分数为___________ 。
②若滴定过程中操作过于缓慢,则测定结果___________ (填“偏大”“偏小”或“不受影响”)。
(5)肼除做火箭推进剂外还可用于燃料电池中。某种碱性肼-空气燃料电池(电解质为KOH溶液)具有高效、无污染的特点,装置如右图所示。___________ 。
②电池工作一段时间后正极区KOH溶液pH基本保持不变,结合电极反应式解释原因___________ 。
 )有较强的还原性,与
)有较强的还原性,与 等可组成火箭推进剂。
等可组成火箭推进剂。(1)已知:Ⅰ.
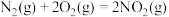

Ⅱ.

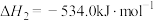
Ⅲ.


火箭发射时
 与
与 反应生成
反应生成 和
和 。该反应的热化学方程式是
。该反应的热化学方程式是(2)肼的传统生产工艺为Raschig法,两步反应分别在不同容器的水溶液环境中进行:
i.
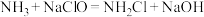 (快)
(快)ii.
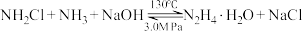 (慢)
(慢)已知电负性N>Cl。下列说法正确的是
a.反应i中NaClO做氧化剂
b.适当提高反应i温度,可显著提高相同时间内
 的产量
的产量c.采用3.0MPa压强可以增大
 的溶解度,提高反应ii中
的溶解度,提高反应ii中 的利用率
的利用率(3)采用Raschig法制得肼后,可采用分步蒸馏的方法将其从反应混合液中分离出来。
①水合肼(
 ,常温为液态)中
,常温为液态)中 与
与 间存在氢键,用“X-H…Y”表示
间存在氢键,用“X-H…Y”表示 与
与 间存在的氢键:
间存在的氢键:②蒸馏过程中首先馏出的物质是
a.
 b.
b. c.NaCl
c.NaCl(4)产品中肼含量的测定方法如下。
取0.50g产品加20mL水稀释,滴入2滴淀粉溶液,用
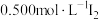 溶液滴定3次,平均每次消耗
溶液滴定3次,平均每次消耗 溶液20.00mL。已知:
溶液20.00mL。已知: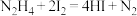
①样品中肼(以
 计)的质量分数为
计)的质量分数为②若滴定过程中操作过于缓慢,则测定结果
(5)肼除做火箭推进剂外还可用于燃料电池中。某种碱性肼-空气燃料电池(电解质为KOH溶液)具有高效、无污染的特点,装置如右图所示。
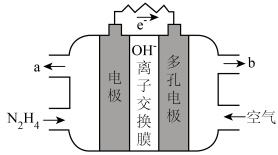
②电池工作一段时间后正极区KOH溶液pH基本保持不变,结合电极反应式解释原因
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】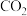 和
和 是两种重要的温室气体,通过
是两种重要的温室气体,通过 和
和 反应制造更高价值化学品是目前的研究目标。
反应制造更高价值化学品是目前的研究目标。
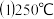 时,以镍合金为催化剂,向
时,以镍合金为催化剂,向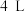 容器中通入
容器中通入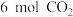 、
、 ,发生如下反应:
,发生如下反应: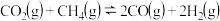 。平衡体系中各组分体积分数如下表:
。平衡体系中各组分体积分数如下表:
 此温度下该反应的平衡常数
此温度下该反应的平衡常数
__________
 已知:
已知: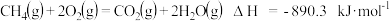
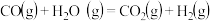
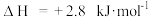
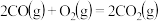
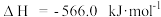
反应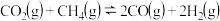 的
的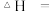
_____________ 
 以二氧化钛表面覆盖
以二氧化钛表面覆盖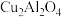 为催化剂,可以将
为催化剂,可以将 和
和 直接转化成乙酸。
直接转化成乙酸。
 在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。
在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。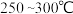 时,温度升高而乙酸的生成速率降低的原因是
时,温度升高而乙酸的生成速率降低的原因是___________ 。

 为了提高该反应中
为了提高该反应中 的转化率,可以采取的措施是
的转化率,可以采取的措施是_________ 。
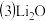 、
、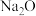 、MgO均能吸收
、MgO均能吸收 ;
;
 如果寻找吸收
如果寻找吸收 的其他物质,下列建议不合理的是
的其他物质,下列建议不合理的是______
 可在具有强氧化性的物质中寻找
可在具有强氧化性的物质中寻找
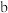 可在碱性氧化物中寻找
可在碱性氧化物中寻找
 可在ⅠA、ⅡA族元素形成的氧化物中寻找
可在ⅠA、ⅡA族元素形成的氧化物中寻找
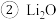 吸收
吸收 后,产物用于合成
后,产物用于合成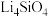 ,
,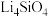 用于吸收、释放
用于吸收、释放 ,原理是:在
,原理是:在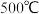 ,
, 与
与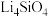 接触后生成
接触后生成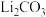 ;平衡后加热至
;平衡后加热至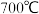 ,反应逆向进行,放出
,反应逆向进行,放出 ,
,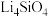 再生,说明该原理的化学方程式是
再生,说明该原理的化学方程式是_____________ 。
 高温电解技术能高效实现下列反应:
高温电解技术能高效实现下列反应: ,其可将释放的
,其可将释放的 转化为具有工业利用价值的产品。工作原理示意图如下:
转化为具有工业利用价值的产品。工作原理示意图如下:
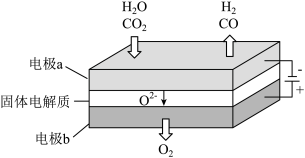
 在电极a放电的电极反应式是
在电极a放电的电极反应式是____________ 。
 和
和 是两种重要的温室气体,通过
是两种重要的温室气体,通过 和
和 反应制造更高价值化学品是目前的研究目标。
反应制造更高价值化学品是目前的研究目标。 时,以镍合金为催化剂,向
时,以镍合金为催化剂,向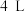 容器中通入
容器中通入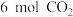 、
、 ,发生如下反应:
,发生如下反应: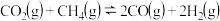 。平衡体系中各组分体积分数如下表:
。平衡体系中各组分体积分数如下表:| 物质 |  |  | CO |  |
| 体积分数 | 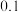 | 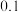 | 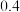 | 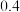 |
 此温度下该反应的平衡常数
此温度下该反应的平衡常数
 已知:
已知: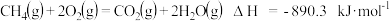
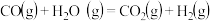
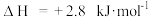
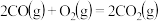
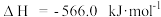
反应
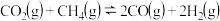 的
的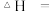

 以二氧化钛表面覆盖
以二氧化钛表面覆盖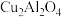 为催化剂,可以将
为催化剂,可以将 和
和 直接转化成乙酸。
直接转化成乙酸。 在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。
在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。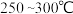 时,温度升高而乙酸的生成速率降低的原因是
时,温度升高而乙酸的生成速率降低的原因是
 为了提高该反应中
为了提高该反应中 的转化率,可以采取的措施是
的转化率,可以采取的措施是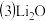 、
、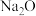 、MgO均能吸收
、MgO均能吸收 ;
; 如果寻找吸收
如果寻找吸收 的其他物质,下列建议不合理的是
的其他物质,下列建议不合理的是 可在具有强氧化性的物质中寻找
可在具有强氧化性的物质中寻找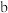 可在碱性氧化物中寻找
可在碱性氧化物中寻找 可在ⅠA、ⅡA族元素形成的氧化物中寻找
可在ⅠA、ⅡA族元素形成的氧化物中寻找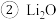 吸收
吸收 后,产物用于合成
后,产物用于合成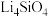 ,
,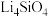 用于吸收、释放
用于吸收、释放 ,原理是:在
,原理是:在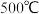 ,
, 与
与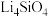 接触后生成
接触后生成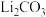 ;平衡后加热至
;平衡后加热至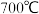 ,反应逆向进行,放出
,反应逆向进行,放出 ,
,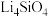 再生,说明该原理的化学方程式是
再生,说明该原理的化学方程式是 高温电解技术能高效实现下列反应:
高温电解技术能高效实现下列反应: ,其可将释放的
,其可将释放的 转化为具有工业利用价值的产品。工作原理示意图如下:
转化为具有工业利用价值的产品。工作原理示意图如下:
 在电极a放电的电极反应式是
在电极a放电的电极反应式是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】(1)环境污染已成人类社会面临的重大威胁。下列名词与环境污染无关的是________ (填:序号)。
①赤潮 ②温室效应 ③酸雨 ④光化学烟雾 ⑤水力发电 ⑥臭氧层空洞 ⑦潮汐 ⑧农药化肥的不当使用 ⑨地方性大脖子病 ⑩工业“三废”和生活污水的任意排放
(2)火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(NO2),已知热化学方程式:
N2(g)+2O2(g)==2NO2(g) △H=+67.7kJ/mol; N2H4(g)+O2(g)==N2(g)+2H2O(g) △H=-534kJ/mol。请写出气态肼与NO2气体反应生成氮气和水蒸气的热化学方程式___________________________ 。该反应应用于火箭推进,除能释放大量热和快速产生大量气体外,还有一个很突出的优点是:________________________________________________ 。
(3)乙烯(C2H4)结构简式为CH2=CH2,且知:C-H键、C=C键、O=O键、C=O键、O-H键的键能分别是:413kJ/mol、615kJ/mol、496kJ/mol、745kJ/mol、463kJ/mol,则表达乙烯(C2H4)气体“燃烧热”的热化学方程式:C2H4(g) +3O2(g) =2CO2(g) +2H2O(l)中,△H=-______ kJ/mol。
如果有2.4NA个电子发生转移,所放出的热量值是____________ kJ。
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成N3-。两步反应的能量变化如图:

①第一步是______ 反应(选填“放热”或“吸热”),判断依据是____________________ 。
①赤潮 ②温室效应 ③酸雨 ④光化学烟雾 ⑤水力发电 ⑥臭氧层空洞 ⑦潮汐 ⑧农药化肥的不当使用 ⑨地方性大脖子病 ⑩工业“三废”和生活污水的任意排放
(2)火箭推进器中装有强还原剂肼(N2H4)和强氧化剂(NO2),已知热化学方程式:
N2(g)+2O2(g)==2NO2(g) △H=+67.7kJ/mol; N2H4(g)+O2(g)==N2(g)+2H2O(g) △H=-534kJ/mol。请写出气态肼与NO2气体反应生成氮气和水蒸气的热化学方程式
(3)乙烯(C2H4)结构简式为CH2=CH2,且知:C-H键、C=C键、O=O键、C=O键、O-H键的键能分别是:413kJ/mol、615kJ/mol、496kJ/mol、745kJ/mol、463kJ/mol,则表达乙烯(C2H4)气体“燃烧热”的热化学方程式:C2H4(g) +3O2(g) =2CO2(g) +2H2O(l)中,△H=-
如果有2.4NA个电子发生转移,所放出的热量值是
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成N3-。两步反应的能量变化如图:

①第一步是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】二氧化碳的捕捉和利用是我国能源领域的一个重要战略方向。
(1)CO2的电子式是_____________ ,所含化学键的类型是______________ 。
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
①写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式___________________ 。
②一定条件下,上述合成二甲醚的的反应达到平衡状态后,若改变反应的某个条件,下列变化能说明平衡一定向正反应方向移动的是(只有一个选项符合题意)_________ (填字母代号)。
a.逆反应速率先增大后减小
b.H2的转化率增大
c.CO2的体积百分含量减小
d.容器中c(H2)/c(CO2)的值减小
③在某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如右图所示。T1温度下,将6 molCO2和12 molH2充入2 L的密闭容器中,5 min后反应达到平衡状态,则0~5 min内的平均反应速率v(CH3OCH3)=___________ ;KA、KB、KC三者之间的大小关系为__________________ 。

(3)CO2溶于水形成H2CO3。已知常温下H2CO3的电离平衡常数K1=4.4×10-7,K2=4.7×10-11,NH3·H2O的电离平衡常数K=1.75×10-5。常温下,用氨水吸收CO2可得到NH4HCO3溶液,NH4HCO3溶液显________ ;(填“酸性”、“中性”或“碱性”);请计算反应NH4++HCO3-+H2O NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=_________ 。
(1)CO2的电子式是
(2)工业上用CO2和H2反应合成二甲醚。已知:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-1
CH3OH(g)+H2O(g) △H1=-49.1 kJ·mol-12CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-24.5 kJ·mol-1①写出CO2(g)和H2(g)转化为CH3OCH3(g)和H2O(g)的热化学方程式
②一定条件下,上述合成二甲醚的的反应达到平衡状态后,若改变反应的某个条件,下列变化能说明平衡一定向正反应方向移动的是(只有一个选项符合题意)
a.逆反应速率先增大后减小
b.H2的转化率增大
c.CO2的体积百分含量减小
d.容器中c(H2)/c(CO2)的值减小
③在某压强下,合成二甲醚的反应在不同温度、不同投料比时,CO2的平衡转化率如右图所示。T1温度下,将6 molCO2和12 molH2充入2 L的密闭容器中,5 min后反应达到平衡状态,则0~5 min内的平均反应速率v(CH3OCH3)=

(3)CO2溶于水形成H2CO3。已知常温下H2CO3的电离平衡常数K1=4.4×10-7,K2=4.7×10-11,NH3·H2O的电离平衡常数K=1.75×10-5。常温下,用氨水吸收CO2可得到NH4HCO3溶液,NH4HCO3溶液显
 NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】甲烷干重整反应可以强化碳酸钙分解.
I.碳酸钙分解: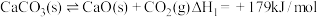
Ⅱ.甲烷干重整: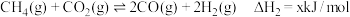
(1)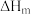 是指由稳定单质生成
是指由稳定单质生成 化合物的焓变,依据下表数据计算
化合物的焓变,依据下表数据计算
___________ .
(2)甲烷干重整反应机理可能如下,其中*代表活性中心,补全反应机理;
I.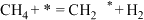 Ⅱ.
Ⅱ.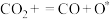
Ⅲ.___________ IV. V.
V.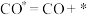
(3)在某温度下,压强恒定为P,向一密闭容器中投入等物质的量 和
和 ;
;
①下列能说明反应达到平衡状态的是___________ (填字母);
a. b.
b. 和
和 的体积比保持不变
的体积比保持不变
c.每生成 消耗
消耗 d.气体的体积保持不变
d.气体的体积保持不变
②反应达到平衡时, 的转化率为
的转化率为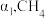 的转化率为
的转化率为 ,则反应I的平衡常数
,则反应I的平衡常数
___________ ;(用含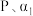 和
和 的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
(4)在该耦合反应体系中,碳酸钙分解转化率与反应速率常数的关系如下: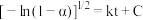 (其中k为速率常数,C为常数)分别在
(其中k为速率常数,C为常数)分别在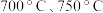 得到的
得到的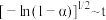 的曲线如图所示:
的曲线如图所示: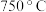 的曲线是曲线
的曲线是曲线___________ ,用碰撞理论解释原因___________ ;
(5)在某温度下,催化剂活性良好,加入一定量的 ,通入
,通入 ,和
,和 的流速为
的流速为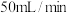 ,发生上述反应.甲烷转化率、出口
,发生上述反应.甲烷转化率、出口 的百分含量随时间的变化关系如图,结合图像解释
的百分含量随时间的变化关系如图,结合图像解释 时刻后,甲烷转化率降低的原因是
时刻后,甲烷转化率降低的原因是___________ 。
I.碳酸钙分解:
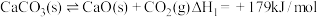
Ⅱ.甲烷干重整:
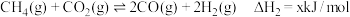
(1)
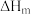 是指由稳定单质生成
是指由稳定单质生成 化合物的焓变,依据下表数据计算
化合物的焓变,依据下表数据计算
|
|
|
| |
|
|
|
| 0 |
(2)甲烷干重整反应机理可能如下,其中*代表活性中心,补全反应机理;
I.
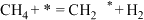 Ⅱ.
Ⅱ.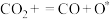
Ⅲ.
 V.
V.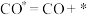
(3)在某温度下,压强恒定为P,向一密闭容器中投入等物质的量
 和
和 ;
;①下列能说明反应达到平衡状态的是
a.
 b.
b. 和
和 的体积比保持不变
的体积比保持不变c.每生成
 消耗
消耗 d.气体的体积保持不变
d.气体的体积保持不变②反应达到平衡时,
 的转化率为
的转化率为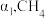 的转化率为
的转化率为 ,则反应I的平衡常数
,则反应I的平衡常数
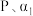 和
和 的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
的式子表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)(4)在该耦合反应体系中,碳酸钙分解转化率与反应速率常数的关系如下:
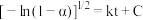 (其中k为速率常数,C为常数)分别在
(其中k为速率常数,C为常数)分别在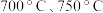 得到的
得到的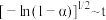 的曲线如图所示:
的曲线如图所示: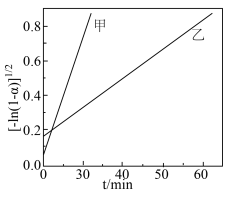
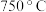 的曲线是曲线
的曲线是曲线(5)在某温度下,催化剂活性良好,加入一定量的
 ,通入
,通入 ,和
,和 的流速为
的流速为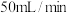 ,发生上述反应.甲烷转化率、出口
,发生上述反应.甲烷转化率、出口 的百分含量随时间的变化关系如图,结合图像解释
的百分含量随时间的变化关系如图,结合图像解释 时刻后,甲烷转化率降低的原因是
时刻后,甲烷转化率降低的原因是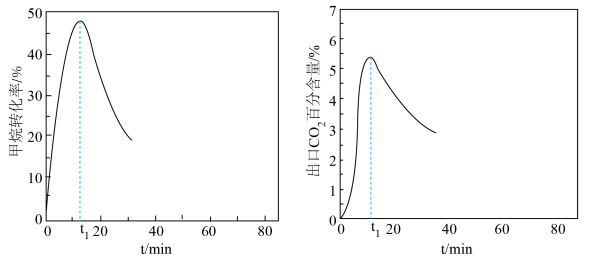
您最近一年使用:0次
【推荐3】I.中国科学家首次实现了二氧化碳到淀粉的全合成,相关成果由国际知名学术期刊《科学》在线发表。CO2的捕集、利用与封存是科学家研究的重要课题,利用CH4与CO2制备“合成气”CO、H2,合成气可直接制备甲醇,反应原理为:CO(g)+2H2(g) CH3OH(g) ΔH=-99 kJ·mol-1。
CH3OH(g) ΔH=-99 kJ·mol-1。
(1)若要该反应自发进行,___________ (填“高温”、“低温”或“任何温度”)更有利。
(2)在恒温、恒容的密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是___________。
(3)把CO2 转化为HCOOH 是降碳并生产化工原料的常用方法,有关反应如下:
①CO(g)+H2O(g) HCOOH(g) ΔH1=-72.6 kJ·mol-1
HCOOH(g) ΔH1=-72.6 kJ·mol-1
②2CO(g)+O2(g) 2CO2(g) ΔH2=-566 kJ·mol-1
2CO2(g) ΔH2=-566 kJ·mol-1
③O2(g)+2H2(g) 2H2O(g) ΔH3=-483.6 kJ·mol-1
2H2O(g) ΔH3=-483.6 kJ·mol-1
则CO2(g)与 H2(g)合成 HCOOH(g)反应的热化学方程式:___________ 。
(4)还可利用电化学方法可以将CO2有效地转化为HCOO-,后续经酸化转化为HCOOH,原理示意图如图所示,下列说法错误的是___________。
Ⅱ.我国学者结合实验与计算机模拟结果,研究了NO-CO的反应历程。在催化剂作用下, 此反应为2CO(g)+2NO(g) 2CO2(g)+N2(g) ΔH<0可有效降低汽车尾气污染物排放。
2CO2(g)+N2(g) ΔH<0可有效降低汽车尾气污染物排放。
(5)探究温度、压强(2MPa,5MPa)对反应的影响,如图所示,表示2MPa 的是___________。
(6)一定温度下,向容积1L的恒容密闭容器按体积比3:2的比例充入CO和NO,当反应达到平衡时NO的体积分数为 ,此温度下该反应的平衡常数K=
,此温度下该反应的平衡常数K=___________ =___________ 。(第一空写表达式,第二空保留三位有效数字)
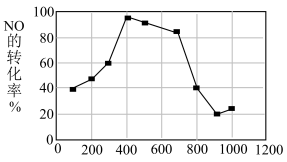
(7)使用相同催化剂,测得相同时间内 NO 的转化率随温度的变化曲线如图,解释 NO 的转化率在 100~900℃范围内随温度升高先上升后下降,且下降由缓到急的主要原因是___________ ;___________ 。
 CH3OH(g) ΔH=-99 kJ·mol-1。
CH3OH(g) ΔH=-99 kJ·mol-1。(1)若要该反应自发进行,
(2)在恒温、恒容的密闭容器中,对于合成气合成甲醇的反应,下列说法中能说明该反应达到化学平衡状态的是___________。
| A.混合气体中碳元素的质量分数不再改变 | B.混合气体的密度不再变化 |
| C.CO的百分含量不再变化 | D.2v(H2)正=v(CO)逆 |
(3)把CO2 转化为HCOOH 是降碳并生产化工原料的常用方法,有关反应如下:
①CO(g)+H2O(g)
 HCOOH(g) ΔH1=-72.6 kJ·mol-1
HCOOH(g) ΔH1=-72.6 kJ·mol-1②2CO(g)+O2(g)
 2CO2(g) ΔH2=-566 kJ·mol-1
2CO2(g) ΔH2=-566 kJ·mol-1③O2(g)+2H2(g)
 2H2O(g) ΔH3=-483.6 kJ·mol-1
2H2O(g) ΔH3=-483.6 kJ·mol-1则CO2(g)与 H2(g)合成 HCOOH(g)反应的热化学方程式:
(4)还可利用电化学方法可以将CO2有效地转化为HCOO-,后续经酸化转化为HCOOH,原理示意图如图所示,下列说法错误的是___________。

A.电解池的阴极电极反应式为2CO2+2e-+H2O=HCOO-+HCO |
| B.b为电源正极 |
| C.电解一段时间后,阳极区的KHCO3 溶液浓度降低 |
| D.若以氢氧碱性燃料电池作直流电源,那么负极的电极反应式为H2-2e-+2OH-=2H2O |
Ⅱ.我国学者结合实验与计算机模拟结果,研究了NO-CO的反应历程。在催化剂作用下, 此反应为2CO(g)+2NO(g)
 2CO2(g)+N2(g) ΔH<0可有效降低汽车尾气污染物排放。
2CO2(g)+N2(g) ΔH<0可有效降低汽车尾气污染物排放。(5)探究温度、压强(2MPa,5MPa)对反应的影响,如图所示,表示2MPa 的是___________。

| A.a | B.b | C.c | D.d |
(6)一定温度下,向容积1L的恒容密闭容器按体积比3:2的比例充入CO和NO,当反应达到平衡时NO的体积分数为
 ,此温度下该反应的平衡常数K=
,此温度下该反应的平衡常数K=(7)使用相同催化剂,测得相同时间内 NO 的转化率随温度的变化曲线如图,解释 NO 的转化率在 100~900℃范围内随温度升高先上升后下降,且下降由缓到急的主要原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】掺杂硒的纳米氧化亚铜催化剂可用于工业合成甲醇,其反应为
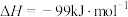 ,回答下列问题:
,回答下列问题:
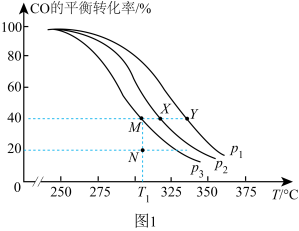
(1)按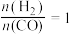 投料,将
投料,将 与CO充入一密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的变化关系如图1所示。
与CO充入一密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的变化关系如图1所示。
已知: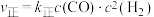 ,
,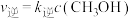 ,其中
,其中 、
、 为速率常数。
为速率常数。
①根据影响化学反应速率的因素,推测下列对速率常数的大小没有影响的是_______ (填标号)。
A.温度 B.活化能 C.反应物浓度 D.催化剂
②压强 、
、 、
、 由小到大的顺序是
由小到大的顺序是_______ 。
③ ℃、压强为
℃、压强为 时,若密闭容器体积为VL,向其中充入
时,若密闭容器体积为VL,向其中充入 和3molCO发生反应,5min后反应达到平衡,则0~5min内,
和3molCO发生反应,5min后反应达到平衡,则0~5min内,
_____  。若N点对应的压强为
。若N点对应的压强为 ,则反应处于该点时
,则反应处于该点时
_____ (填“>”“<”或“=”) 。X、Y、M三点对应的平衡常数从大到小的顺序是
。X、Y、M三点对应的平衡常数从大到小的顺序是_____ 。
(2)向10L恒容密闭容器中充入2molCO和 发生反应,若体系起始时和平衡时温度均为325℃,体系总压强
发生反应,若体系起始时和平衡时温度均为325℃,体系总压强 与时间
与时间 的关系如图2中曲线I所示,曲线II为只改变某一条件的变化曲线。
的关系如图2中曲线I所示,曲线II为只改变某一条件的变化曲线。
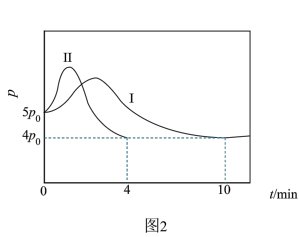
①曲线II所对应的反应改变的条件可能为_______ 。
②体系总压强先增大后减小的原因为_______ 。
③该条件下 的平衡转化率为
的平衡转化率为_______ %(结果保留1位小数)。

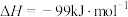 ,回答下列问题:
,回答下列问题:(1)按
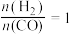 投料,将
投料,将 与CO充入一密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的变化关系如图1所示。
与CO充入一密闭容器中,在一定条件下发生反应,测得CO的平衡转化率与温度、压强的变化关系如图1所示。
已知:
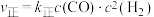 ,
,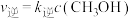 ,其中
,其中 、
、 为速率常数。
为速率常数。①根据影响化学反应速率的因素,推测下列对速率常数的大小没有影响的是
A.温度 B.活化能 C.反应物浓度 D.催化剂
②压强
 、
、 、
、 由小到大的顺序是
由小到大的顺序是③
 ℃、压强为
℃、压强为 时,若密闭容器体积为VL,向其中充入
时,若密闭容器体积为VL,向其中充入 和3molCO发生反应,5min后反应达到平衡,则0~5min内,
和3molCO发生反应,5min后反应达到平衡,则0~5min内,
 。若N点对应的压强为
。若N点对应的压强为 ,则反应处于该点时
,则反应处于该点时
 。X、Y、M三点对应的平衡常数从大到小的顺序是
。X、Y、M三点对应的平衡常数从大到小的顺序是(2)向10L恒容密闭容器中充入2molCO和
 发生反应,若体系起始时和平衡时温度均为325℃,体系总压强
发生反应,若体系起始时和平衡时温度均为325℃,体系总压强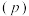 与时间
与时间 的关系如图2中曲线I所示,曲线II为只改变某一条件的变化曲线。
的关系如图2中曲线I所示,曲线II为只改变某一条件的变化曲线。
①曲线II所对应的反应改变的条件可能为
②体系总压强先增大后减小的原因为
③该条件下
 的平衡转化率为
的平衡转化率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】长征三号甲运载火箭(CZ—3A)与“嫦娥工程“太空摆渡车”“北斗卫星”“风云卫星”等中国航天大事件紧密相连。它是大型三级液体推进剂火箭,一子级和二子级均使用偏二甲肼(UDMH)-四氧化二氮(NTO)推进剂,反应产物绿色无污染。回答下列问题:
(1)已知(CH3)2NNH2(l)+4O2(g)= 2CO2(g)+4H2O(g)+N2(g) △H=a kJ/mol
N2(g)+O2(g)= 2NO(g) △H=b kJ/mol
2NO(g)+O2(g)= N2O4(l) △H=c kJ/mol
则UDMH-NTO推进剂反应的热化学方程式为________________________ 。
(2)偏二甲肼易溶于水,其一水合物的电离方式与一水合氨(Kb=1.7×10-5)相似但电离常数更小,偏二甲肼一水合物的电离方程式为___________________ ,向偏二甲肼溶液中加入等物质的量的醋酸(Ka=-1.7×10-5),充分反应后溶液呈______ (填“酸性”“碱性”或“中性”)。碱性偏二甲肼—空气燃料电池的电解质溶液是20~30%的KOH溶液,电池工作时正极的电极反应式为__________________________ 。
(3)N2O4是NO2的二聚产物,NO、NO2等氮氧化物是主要的大气污染物,氮氧化物与悬浮在大气中的微粒相互作用时,涉及如下反应:
(I)2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) △H1<0 K1
NaNO3(s)+ClNO(g) △H1<0 K1
(II)2NO(g)+Cl2(g) 2ClNO(g) △H2<0 K2
2ClNO(g) △H2<0 K2
则4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+C12(g)的平衡常数为
2NaNO3(s)+2NO(g)+C12(g)的平衡常数为_______ (用K1、K2表示);为研究不同条件对反应(Ⅱ)的影响,T℃时,向2L恒容密闭容器中加入0.2mol NO和0.2mol C12,5min时达到平衡,反应过程中容器内的压强减小了10%,则5min内反应的平均速率v(C1NO)=_____ mol/(L·min),NO的平衡转化率α1=_____ %;若其他条件保持不变,使反应(Ⅱ)在初始容积为2L的恒压密闭容器中进行,则NO的平衡转化率α2_______ α1(填“>”“<”或“=”)。
(1)已知(CH3)2NNH2(l)+4O2(g)= 2CO2(g)+4H2O(g)+N2(g) △H=a kJ/mol
N2(g)+O2(g)= 2NO(g) △H=b kJ/mol
2NO(g)+O2(g)= N2O4(l) △H=c kJ/mol
则UDMH-NTO推进剂反应的热化学方程式为
(2)偏二甲肼易溶于水,其一水合物的电离方式与一水合氨(Kb=1.7×10-5)相似但电离常数更小,偏二甲肼一水合物的电离方程式为
(3)N2O4是NO2的二聚产物,NO、NO2等氮氧化物是主要的大气污染物,氮氧化物与悬浮在大气中的微粒相互作用时,涉及如下反应:
(I)2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) △H1<0 K1
NaNO3(s)+ClNO(g) △H1<0 K1(II)2NO(g)+Cl2(g)
 2ClNO(g) △H2<0 K2
2ClNO(g) △H2<0 K2则4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+C12(g)的平衡常数为
2NaNO3(s)+2NO(g)+C12(g)的平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】研究反应机理以及化学平衡的原理,是揭示化学反应的规律和获得调控化学反应的理论依据。
I.一定条件下,在容积为5L的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达平衡后,降低温度,A的体积分数减小。
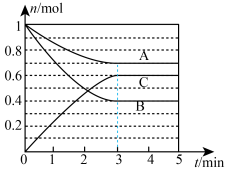
(1)该反应的化学方程式为___________ 。
(2)在一定温度下的容积不变的密闭容器中发生该反应。下列叙述中,不能说明反应达到化学平衡状态的是___________。
(3)该反应的反应速率v随时间t的关系如图所示。
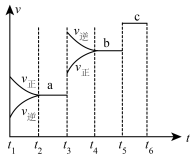
①根据上图判断,在t3时刻改变的外界条件是___________ 。
②根据上图判断a、b、c对应的平衡状态中,C的体积分数最大的是___________ 状态。
Ⅱ.在1L密闭容器中发生反应: ,其化学平衡常数K与温度T的关系如下表:
,其化学平衡常数K与温度T的关系如下表:
回答下列问题:
(4)该反应的平衡常数表达式为K=________ ;该反应的△H________ 0(填“>”或“<”)。
(5)下列措施既可以提高反应速率,又可以提高H2的平衡转化率的是___________。
(6)830℃时,将2molCO2和2molH2投入上述容器中开始反应,达到平衡时CO2的转化率为___________ 。
(7)800℃时,某时刻测得c(CO2)=0.5mol·L-1、c(H2)=1.5mol·L-1、c(CO)=0.5mol·L-1、c(H2O)=0.5mol·L-1,此时,v(正)___________ v(逆)(填“>”“<”或“=”)。
I.一定条件下,在容积为5L的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图所示。已知达平衡后,降低温度,A的体积分数减小。

(1)该反应的化学方程式为
(2)在一定温度下的容积不变的密闭容器中发生该反应。下列叙述中,不能说明反应达到化学平衡状态的是___________。
| A.A的消耗速率与C的生成速率比为1:2 |
| B.容器内压强不再变化 |
| C.混合气体平均摩尔质量不再改变 |
| D.混合气体密度不再改变 |
(3)该反应的反应速率v随时间t的关系如图所示。

①根据上图判断,在t3时刻改变的外界条件是
②根据上图判断a、b、c对应的平衡状态中,C的体积分数最大的是
Ⅱ.在1L密闭容器中发生反应:
 ,其化学平衡常数K与温度T的关系如下表:
,其化学平衡常数K与温度T的关系如下表:| T(℃) | 650 | 700 | 800 | 830 | 1000 |
| K | 0.5 | 0.6 | 0.9 | 1.0 | 1.7 |
(4)该反应的平衡常数表达式为K=
(5)下列措施既可以提高反应速率,又可以提高H2的平衡转化率的是___________。
| A.选择适当的催化剂 | B.增大压强 |
| C.及时分离出H2O(g) | D.升高温度 |
(6)830℃时,将2molCO2和2molH2投入上述容器中开始反应,达到平衡时CO2的转化率为
(7)800℃时,某时刻测得c(CO2)=0.5mol·L-1、c(H2)=1.5mol·L-1、c(CO)=0.5mol·L-1、c(H2O)=0.5mol·L-1,此时,v(正)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】CO、H2、CH3、OH均是清洁能源。
(1)已知部分化学键键能数据如下:
2CO(g) +O2(g)==2CO2(g) △H1
H2O(g)+CO(g)==H2(g) + CO2(g) △H2 = -41 kJ•mol-1
CH3OH(g)+ 3/2O2(g)==CO2(g)+2H2O(g) △H3 = -660kJ•mol-1
则△H1=_____ kJ•mol-1,反应CO(g)+2H2(g)⇌CH3OH(g)的△H=_____ kJ•mol-1。
(2)一定条件下,在容积为2 L的密闭容器Q中充人a mol CO与6 molH2合成甲醇:CO(g) +2H2(g)⇌CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。
①压强相同时,温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者之间的相对大小为t1___ t2(填“>”、“<”、“=”或“无法确定”)。
②X=___________ (用含a、b的式子表示),p1_____ p2(填“>”、“<”、“=”或“无法确定”)。
③若a =2,b=4,则压强为p1、温度为了T1时该反应的平衡常数K=______________ 。
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体,则反应开始时,v(CH3OH)正_____ v(CH3OH)逆(填“>”、“<”、“=”或“无法确定”)。
(3)甲醇燃料电池是一种具有高能量转化率的绿色电池,则用磷酸溶液作电解质时,负极的电极反应式为________________________ 。
(1)已知部分化学键键能数据如下:
| 化学键 | C O O | O=O | C=O | C-O |
| E/(kJ • mol-1) | 958.5 | 497 | 745 | 351 |
H2O(g)+CO(g)==H2(g) + CO2(g) △H2 = -41 kJ•mol-1
CH3OH(g)+ 3/2O2(g)==CO2(g)+2H2O(g) △H3 = -660kJ•mol-1
则△H1=
(2)一定条件下,在容积为2 L的密闭容器Q中充人a mol CO与6 molH2合成甲醇:CO(g) +2H2(g)⇌CH3OH(g)。测得平衡时混合气体中CH3OH的体积百分含量与温度、 压强之间的关系如图1所示,图2表示在一定温度下,H2的平衡转化率与反应开始时两种反应物的投料物质的量之比(用X表示)、压强之间的关系。

①压强相同时,温度为T1、T2时,反应达到平衡所需要的时间分别为t1、t2,则二者之间的相对大小为t1
②X=
③若a =2,b=4,则压强为p1、温度为了T1时该反应的平衡常数K=
④若在压强为P1、温度为T1时,向Q容器中同时加入等物质的量的CO、H2、CH3OH三种气体,则反应开始时,v(CH3OH)正
(3)甲醇燃料电池是一种具有高能量转化率的绿色电池,则用磷酸溶液作电解质时,负极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】将甲烷转化为既可作为液体燃料又可用作化工基本原料的甲醇,具有广泛的应用前景以及重要的经济价值和社会意义。甲烷部分氧化反应主要有气固相催化氧化、液相催化氧化等。回答下列问题:
(1)科研人员对O2直接将CH4氧化为甲醇的气固相催化体系进行了多年探索,在密闭容器中充入2molCH4和1molO2,在不同条件下发生反应:2CH4(g)+O2(g) 2CH3OH(g),平衡时甲醇的物质的量随温度、压强的变化如图所示,根据图象填空。
2CH3OH(g),平衡时甲醇的物质的量随温度、压强的变化如图所示,根据图象填空。
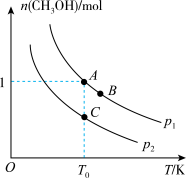
①p1_______ p2(选填“>”、“<”或“=”),该反应的△H_______ 0(选填“>”或“<”)。
②A、B、C点对应的化学反应速率由大到小的顺序为_______ 。[用v(A)、v(B)、v(C)表示]
③若A点,n(CH3OH)=1mol,总压强为2.5MPa,则T0时A点用分压强代替浓度表示的平衡常数Kp=_______ 。
(2)CH4在102%发烟硫酸溶剂中以配合物Pt(bpym)Cl2为催化剂的气液相催化体系,能达到较大的CH4转化率及选择性,原理为:CH4先转化为CH3OSO3H(CH4+H2SO4+SO3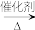 CH3OSO3H+H2SO4+SO2),SO2再与O2生成H2SO4,CH3OSO3H再水解生成甲醇,写出该水解反应的方程式:
CH3OSO3H+H2SO4+SO2),SO2再与O2生成H2SO4,CH3OSO3H再水解生成甲醇,写出该水解反应的方程式:_______ 。Pt(bpym)Cl2成本昂贵,HgSO4也可以作为该反应的催化剂,且催化活性及稳定性较好,HgSO4的突出缺点是_______ 。
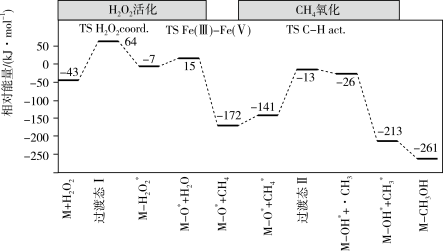
(3)Osadchi等合成了Fe/MIL-53催化剂,并用于H2O2催化氧化甲烷合成甲醇的研究(CH4+H2O2 CH3OH+H2O),反应历程如图所示,其中催化剂用M表示,•CH3为甲基自由基,结合在催化剂表面上的物质或基团用*标注。该历程中“H2O2活化”与“CH4氧化”较难发生的是
CH3OH+H2O),反应历程如图所示,其中催化剂用M表示,•CH3为甲基自由基,结合在催化剂表面上的物质或基团用*标注。该历程中“H2O2活化”与“CH4氧化”较难发生的是_______ ,试解释你的理由_______ 。
(1)科研人员对O2直接将CH4氧化为甲醇的气固相催化体系进行了多年探索,在密闭容器中充入2molCH4和1molO2,在不同条件下发生反应:2CH4(g)+O2(g)
 2CH3OH(g),平衡时甲醇的物质的量随温度、压强的变化如图所示,根据图象填空。
2CH3OH(g),平衡时甲醇的物质的量随温度、压强的变化如图所示,根据图象填空。
①p1
②A、B、C点对应的化学反应速率由大到小的顺序为
③若A点,n(CH3OH)=1mol,总压强为2.5MPa,则T0时A点用分压强代替浓度表示的平衡常数Kp=
(2)CH4在102%发烟硫酸溶剂中以配合物Pt(bpym)Cl2为催化剂的气液相催化体系,能达到较大的CH4转化率及选择性,原理为:CH4先转化为CH3OSO3H(CH4+H2SO4+SO3
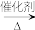 CH3OSO3H+H2SO4+SO2),SO2再与O2生成H2SO4,CH3OSO3H再水解生成甲醇,写出该水解反应的方程式:
CH3OSO3H+H2SO4+SO2),SO2再与O2生成H2SO4,CH3OSO3H再水解生成甲醇,写出该水解反应的方程式:(3)Osadchi等合成了Fe/MIL-53催化剂,并用于H2O2催化氧化甲烷合成甲醇的研究(CH4+H2O2
 CH3OH+H2O),反应历程如图所示,其中催化剂用M表示,•CH3为甲基自由基,结合在催化剂表面上的物质或基团用*标注。该历程中“H2O2活化”与“CH4氧化”较难发生的是
CH3OH+H2O),反应历程如图所示,其中催化剂用M表示,•CH3为甲基自由基,结合在催化剂表面上的物质或基团用*标注。该历程中“H2O2活化”与“CH4氧化”较难发生的是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】近年全国各地雾霾严重,为有效控制雾霾,各地积极采取措施改善大气质量。研究并有效控制空气中氮氧化物、碳氧化物等污染物是一项重要而艰巨的工作。
Ⅰ.氮氧化物的研究
(1)一定条件下,将2mol NO与2mol O2置于恒容密闭容器中发生反应:2NO(g)+O2(g) 2NO2(g),下列状态能说明该反应达到化学平衡的是
2NO2(g),下列状态能说明该反应达到化学平衡的是
(2)已知反应。 2NO(g) N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图所示。根据图像可以判断曲线R1、R2对应的下列反应条件中不同的是
N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图所示。根据图像可以判断曲线R1、R2对应的下列反应条件中不同的是_______ (填字母序号)。

A. 压强 B.温度 C.催化剂
根据图中的能量变化数据。计算反应2NO(g) N2(g)+O2(g)的ΔH=
N2(g)+O2(g)的ΔH=_______

Ⅱ.碳氧化物研究
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:
CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:

请回答:
①T1_______ T2(填“>”或“<”或“=”),理由是_______ 。已知T2℃时,第20min时容器内压强不再改变,此时H2的转化率为_______ ,该温度下的化学平衡常数为_______ 。
②若将1mol CO和2mol H2通入原体积为1L的恒压密闭容器(图3乙)中,在T2℃下达到平衡,此时反应的平衡常数为_______ ;若再向容器中通入l mol CH3OH(g),重新达到平衡后,CH3OH(g)在体系中的百分含量_______ (填“变大”或“变小”或“不变”)。
(4)一定条件下也可用NaOH溶液与CO反应生成甲酸钠,进一步反应生成甲酸来消除CO污染。常温下将a mol的CO通入2 L bmol/L NaOH溶液中,恰好完全反应生成甲酸钠和含少量甲酸的混合溶液(假设溶液体积不变),测得溶液中c(Na+)=c(HCOO-),则该混合溶液中甲酸的电离平衡常数Ka=_______ (用含a和b的代数式表示)。
Ⅰ.氮氧化物的研究
(1)一定条件下,将2mol NO与2mol O2置于恒容密闭容器中发生反应:2NO(g)+O2(g)
 2NO2(g),下列状态能说明该反应达到化学平衡的是
2NO2(g),下列状态能说明该反应达到化学平衡的是| A.混合气体的密度保持不变 |
| B.NO的转化率保持不变 |
| C.NO和O2的物质的量之比保持不变 |
| D.O2的消耗速率和NO2的消耗速率相等 |
 N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图所示。根据图像可以判断曲线R1、R2对应的下列反应条件中不同的是
N2(g)+O2(g) ΔH<O,在不同条件时N2的体积分数随时间(t)的变化如图所示。根据图像可以判断曲线R1、R2对应的下列反应条件中不同的是
A. 压强 B.温度 C.催化剂
根据图中的能量变化数据。计算反应2NO(g)
 N2(g)+O2(g)的ΔH=
N2(g)+O2(g)的ΔH=
Ⅱ.碳氧化物研究
(3)CO和H2在一定条件下可以合成甲醇:CO(g)+2H2(g)
 CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:
CH3OH(g) ΔH<O ,现在体积为1L的恒容密闭容器(图甲)中通入1mol CO和2mol H2,测定不同时间、不同温度(T)下容器中CO的物质的量,如下表:| 0min | 10min | 20min | 30min | 40min | |
| T1 | 1mol | 0.8mol | 0.62mol | 0.4mol | 0.4mol |
| T2 | 1mol | 0.7mol | 0.5mol | a | a |

请回答:
①T1
②若将1mol CO和2mol H2通入原体积为1L的恒压密闭容器(图3乙)中,在T2℃下达到平衡,此时反应的平衡常数为
(4)一定条件下也可用NaOH溶液与CO反应生成甲酸钠,进一步反应生成甲酸来消除CO污染。常温下将a mol的CO通入2 L bmol/L NaOH溶液中,恰好完全反应生成甲酸钠和含少量甲酸的混合溶液(假设溶液体积不变),测得溶液中c(Na+)=c(HCOO-),则该混合溶液中甲酸的电离平衡常数Ka=
您最近一年使用:0次