I.有下列8种晶体,用序号回答下列问题:
A.水晶B.冰醋酸C.白磷D.固态氩E.氯化铵F.铝G.金刚石
(1)属于原子晶体的化合物是____ ,属于离子晶体的是____ ,不含化学键的分子晶体是____ 。
(2)由极性分子构成的晶体是____ ,含有共价键的离子晶体是____ 。
II.含有NaOH的Cu(OH)2悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米Cu2O。
(3)Cu+基态核外电子排布式为____ 。
(4)含有NaOH的Cu(OH)2悬浊液与乙醛反应的化学方程式为____ 。
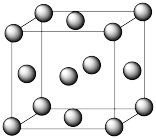
(5)Cu2O在稀硫酸中生成Cu和CuSO4。铜晶胞结构如图所示,铜晶体中每个铜原子周围距离最近的铜原子数目为_____ 。
III.臭氧(O3)在[Fe(H2O)6]2+催化下能将烟气中的SO2、NOx氧化为SO和NO,NOx也可在其他条件下被还原为N2。
(6)SO 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为_____ ;NO 的空间构型为
的空间构型为_____ (用文字描述)。
(7)与O3分子互为等电子体的一种阴离子为_____ (填化学式)。
(8)N2分子中σ键与π键的数目比n(σ)∶n(π)=_____ 。
A.水晶B.冰醋酸C.白磷D.固态氩E.氯化铵F.铝G.金刚石
(1)属于原子晶体的化合物是
(2)由极性分子构成的晶体是
II.含有NaOH的Cu(OH)2悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米Cu2O。
(3)Cu+基态核外电子排布式为
(4)含有NaOH的Cu(OH)2悬浊液与乙醛反应的化学方程式为
(5)Cu2O在稀硫酸中生成Cu和CuSO4。铜晶胞结构如图所示,铜晶体中每个铜原子周围距离最近的铜原子数目为

III.臭氧(O3)在[Fe(H2O)6]2+催化下能将烟气中的SO2、NOx氧化为SO和NO,NOx也可在其他条件下被还原为N2。
(6)SO
 中心原子轨道的杂化类型为
中心原子轨道的杂化类型为 的空间构型为
的空间构型为(7)与O3分子互为等电子体的一种阴离子为
(8)N2分子中σ键与π键的数目比n(σ)∶n(π)=
更新时间:2022-11-16 12:59:14
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】2019年诺贝尔化学奖由来自美、英、日的三人分获,以表彰他们在锂离子电池研究方面做出的贡献,他们最早发明用LiCoO2作离子电池的正极,用聚乙炔作负极。回答下列问题:
(1)基态钴原子的核外未成对电子数为___ ,第四电离能I4(Co)比I4(Fe)小是因为___ 。
(2)工业上曾用CuC2与水反应生成乙炔。CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为___ ;lmolO22+中含有的π键数目为___ 。
(3)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯( )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。
①LiBF4中阴离子的空间构型是___ ;与该阴离子互为等电子体的分子有___ (列一种)。
②碳酸亚乙酯分子中碳原子的杂化方式有___ 。
(4)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参数a=588pm。

①S2-的配位数为___ 。
②设NA为阿伏加 德罗常数的值,Li2S的晶胞密度为___ g•cm-3(列出计算式)。
(1)基态钴原子的核外未成对电子数为
(2)工业上曾用CuC2与水反应生成乙炔。CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为
(3)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯(
 )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。①LiBF4中阴离子的空间构型是
②碳酸亚乙酯分子中碳原子的杂化方式有
(4)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参数a=588pm。

①S2-的配位数为
②设NA为阿伏加 德罗常数的值,Li2S的晶胞密度为
您最近一年使用:0次
【推荐2】合成氨是人类科学技术上的一项重大突破,是化学和技术对社会发展与进步的巨大贡献之一。在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac + CO + NH3⇌Cu(NH3)3(CO)Ac。请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为________ 。
(2)写出基态Cu+的核外电子排布式_______ 。
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为______ 。
(4)写出与CO互为等电子体的阴离子______ 。(任写一个)
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],1mol尿素分子中,σ键的数目为______ 。
(6)已知铜的晶胞结构如图所示,则在铜的晶胞中所含铜原子数及配位数比为______ 。

(1)C、N、O的第一电离能由大到小的顺序为
(2)写出基态Cu+的核外电子排布式
(3)配合物Cu(NH3)3(CO)Ac中心原子的配位数为
(4)写出与CO互为等电子体的阴离子
(5)在一定条件下NH3与CO2能合成化肥尿素[CO(NH2)2],1mol尿素分子中,σ键的数目为
(6)已知铜的晶胞结构如图所示,则在铜的晶胞中所含铜原子数及配位数比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氮化硼( BN)是一种重要的功能陶瓷材料。以天然硼砂(主要成分Na2B4O7)为起始物,经过一系列反应可以得到BN和火箭高能燃料及有机合成催化剂BF3的过程如下:
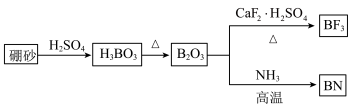
(1)写出由B203制备BF3的化学方程式 ,BF3中,B原子的杂化轨道类型为____________,BF3分子空间构型为____________。
(2)在硼、氧、氟、氮中第一电离能由大到小的顺序是(用元素符号表示)________________。
(3)已知:硼酸的电离方程式为H3B03 +H20 [B(OH)4] - +H+,试依据上述反应写出[ Al( OH)4] -的结构式____________,并推测1mol NH4BF4(氟硼酸铵)中含有____________个配位键。
[B(OH)4] - +H+,试依据上述反应写出[ Al( OH)4] -的结构式____________,并推测1mol NH4BF4(氟硼酸铵)中含有____________个配位键。
(4)由12个硼原子构成如图1的结构单元,硼晶体的熔点为1873℃,则硼晶体的1个结构单元中含有________________个B-B键。

(5)氮化硼(BN)晶体有多种相结构。六方相氮化硼(晶体结构如图2)是通常存在的稳定相可作高温润滑剂。立方相氮化硼(晶体结构如图3)是超硬材料,有优异的耐磨性。
①关于这两种晶体的说法,不正确的是____________(填字母)。
a.两种晶体均为分子晶体
b.两种晶体中的B-N键均为共价键
c.六方相氮化硼层间作用力小,所以质地软
d.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体内B-N键数与硼原子数之比为 __,其结构与石墨相似却不导电,原因是____________。
③立方相氮化硼晶体中,每个硼原子连接____________个六元环。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 。

(1)写出由B203制备BF3的化学方程式 ,BF3中,B原子的杂化轨道类型为____________,BF3分子空间构型为____________。
(2)在硼、氧、氟、氮中第一电离能由大到小的顺序是(用元素符号表示)________________。
(3)已知:硼酸的电离方程式为H3B03 +H20
 [B(OH)4] - +H+,试依据上述反应写出[ Al( OH)4] -的结构式____________,并推测1mol NH4BF4(氟硼酸铵)中含有____________个配位键。
[B(OH)4] - +H+,试依据上述反应写出[ Al( OH)4] -的结构式____________,并推测1mol NH4BF4(氟硼酸铵)中含有____________个配位键。(4)由12个硼原子构成如图1的结构单元,硼晶体的熔点为1873℃,则硼晶体的1个结构单元中含有________________个B-B键。

(5)氮化硼(BN)晶体有多种相结构。六方相氮化硼(晶体结构如图2)是通常存在的稳定相可作高温润滑剂。立方相氮化硼(晶体结构如图3)是超硬材料,有优异的耐磨性。
①关于这两种晶体的说法,不正确的是____________(填字母)。
a.两种晶体均为分子晶体
b.两种晶体中的B-N键均为共价键
c.六方相氮化硼层间作用力小,所以质地软
d.立方相氮化硼含有σ键和π键,所以硬度大
②六方相氮化硼晶体内B-N键数与硼原子数之比为 __,其结构与石墨相似却不导电,原因是____________。
③立方相氮化硼晶体中,每个硼原子连接____________个六元环。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是 。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】元素X是地壳中含量最多的元素;元素Y基态原子的3p轨道上有4个电子;元素Z位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。
(1)X基态原子的电子排布式为_______ 。
(2)X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是_______ 。
(3)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是_______ 。
(4)Y与X可形成YX 。
。
①YX 的立体构型为
的立体构型为_______ (用文字描述)。
②写出一种与YX 互为等电子体的分子的化学式
互为等电子体的分子的化学式_______ 。
(5)Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为_______ 。其晶胞边长为540.0 pm,密度为_______ g·cm-3(列式并计算),a位置Y与b位置Z之间的距离为_______ pm(列式表示)。

(6)Z的氯化物与氨水反应可形成配合物[Z(NH3)4]Cl2,2 mol 该配合物中含有σ键的数目为_______ 。
(1)X基态原子的电子排布式为
(2)X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是
(3)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是
(4)Y与X可形成YX
 。
。①YX
 的立体构型为
的立体构型为②写出一种与YX
 互为等电子体的分子的化学式
互为等电子体的分子的化学式(5)Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为

(6)Z的氯化物与氨水反应可形成配合物[Z(NH3)4]Cl2,2 mol 该配合物中含有σ键的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】形形色色的物质,构成了我们这个五彩缤纷的世界。学习物质结构和性质的知识,能使你想象的翅膀变得更加有力。
(1)BF3属于_______ 分子 填“极性”或“非极性)。
填“极性”或“非极性)。
(2)如图为硼酸晶体的片层结构,该晶体中存在的作用力有_______ 。
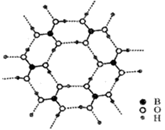
A.共价键 B.离子键 C.氢键 D.范德华力
(3)氮化硼和碳化硼均属于原子晶体,氮化硼的硬度高于碳化硼的原因为_______ ;B、C、N的电负性由大到小的顺序为_______ 。
(4)碳酸乙烯酯的结构简式为 ,其中碳原子杂化方式为
,其中碳原子杂化方式为_______ ,每个分子中含_______ 个σ键。
(5)CO2加氢得到CH3OH,CH3OH的沸点比CO2的高,原因是_______ 。
(6)下表为CO和N2的有关信息。
根据表中数据,说明CO比N2活泼的原因是_______ 。
(7)某离子晶体的晶胞结构如图所示。设该晶体的摩尔质量为Mg·mol-1,晶胞的密度为ρg·cm-3,阿伏加德罗常数为NA,则晶体中两个最近的X间的距离为_______ pm。

(1)BF3属于
 填“极性”或“非极性)。
填“极性”或“非极性)。(2)如图为硼酸晶体的片层结构,该晶体中存在的作用力有

A.共价键 B.离子键 C.氢键 D.范德华力
(3)氮化硼和碳化硼均属于原子晶体,氮化硼的硬度高于碳化硼的原因为
(4)碳酸乙烯酯的结构简式为
 ,其中碳原子杂化方式为
,其中碳原子杂化方式为(5)CO2加氢得到CH3OH,CH3OH的沸点比CO2的高,原因是
(6)下表为CO和N2的有关信息。
| 键的类型 | A-B(单键) | A=B(双键) | A≡B(三键) | |
| 键能kJ/mol | CO | 351 | 803 | 1071 |
| N2 | 159 | 418 | 946 | |
根据表中数据,说明CO比N2活泼的原因是
(7)某离子晶体的晶胞结构如图所示。设该晶体的摩尔质量为Mg·mol-1,晶胞的密度为ρg·cm-3,阿伏加德罗常数为NA,则晶体中两个最近的X间的距离为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】铜是人类最早使用的金属之一,其用黄铜矿(主要成分为CuFeS2)生产粗铜的反应原理如下:回答下列问题:

(1)Cu在周期表中的位置是___________ , 其晶体中原子堆积方式为__________ , 晶胞空间利用率为______ (用含π的式子表示)。
(2)反应①、②中都会生成气体SO2,S和O相比,第一电离能较小的是_____ ;SO2分子中心原子的杂化方式为_________ ,与之互为等电子体的分子有_____ (写一种)。
(3)已知Cu2O的熔点为1235°C, Cu2S 的熔点为1130°C, 请解释Cu2O熔点较高的原因是_____ 。
(4)工业上常用铜氨溶液制造人造丝,某学生做了如下实验: CuSO4溶液 蓝色沉淀
蓝色沉淀 深蓝色溶液,蓝色沉淀溶于氨水的离子方程式为
深蓝色溶液,蓝色沉淀溶于氨水的离子方程式为_____ 。
(5)Cu2O的晶胞结构如图所示,B代表的是_____ (选填Cu或O) ;若原子坐标参数A为(0,0,0), B为( ,
, ,
, ),则C原子的坐标参数为
),则C原子的坐标参数为_____ 。若该晶体的密度为dg/cm3,阿伏加德罗常数的值为NA,则该晶胞中Cu原子与O原子之间的距离为_____ pm。(用含d和NA的式子表示)。


(1)Cu在周期表中的位置是
(2)反应①、②中都会生成气体SO2,S和O相比,第一电离能较小的是
(3)已知Cu2O的熔点为1235°C, Cu2S 的熔点为1130°C, 请解释Cu2O熔点较高的原因是
(4)工业上常用铜氨溶液制造人造丝,某学生做了如下实验: CuSO4溶液
 蓝色沉淀
蓝色沉淀 深蓝色溶液,蓝色沉淀溶于氨水的离子方程式为
深蓝色溶液,蓝色沉淀溶于氨水的离子方程式为(5)Cu2O的晶胞结构如图所示,B代表的是
 ,
, ,
, ),则C原子的坐标参数为
),则C原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】现有几组物质的熔点(℃)数据:
据此回答下列问题:
(1)由表格可知,A组熔点普遍偏高,据此回答:
①A组属于_______ 晶体,其熔化时克服的粒子间的作用力是_______ ;
②硅的熔点低于二氧化硅,是由于_______ ;
③硬度比较:晶体硅_______ 晶体硼(“大于”或“小于”);
(2)B组晶体中存在的作用力是_______ ,其共同的物理性质是_______ (填序号)
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于_______ 。
(4)D组晶体可能具有的性质是_______ (填序号)。
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体中NaCl、KCl、RbCl的熔点由高到低的顺序为_______ ,MgO晶体的熔点高于三者,其原因解释为_______ 。
| A组 | B组 | C组 | D组 |
| 金刚石:3550 | Li:181 | HF:-83 | NaCl |
| 硅晶体:1410 | Na:98 | HCl:-115 | KCl |
| 硼晶体:2300 | K:64 | HBr:-89 | RbCl |
| 二氧化硅:1732 | Rb:39 | HI:-51 | Mg0:2800 |
(1)由表格可知,A组熔点普遍偏高,据此回答:
①A组属于
②硅的熔点低于二氧化硅,是由于
③硬度比较:晶体硅
(2)B组晶体中存在的作用力是
①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于
(4)D组晶体可能具有的性质是
①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电
(5)D组晶体中NaCl、KCl、RbCl的熔点由高到低的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】碳是形成单质和化合物种类最多的元素,其单质及化合物有独特的性质和用途。请回答下列问题。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图所示:
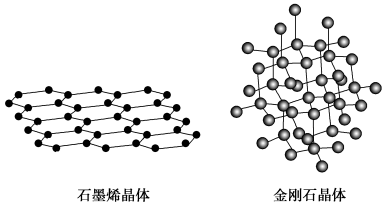
石墨烯能导电而金刚石不能导电的原因是________ 。
(2)碳的主要氧化物有CO和CO2
①CO能与金属Fe形成一种浅黄色液体Fe(CO)5,其熔点为-20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:该化合物的晶体中不涉及 的作用力有________ 。
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②CO2在一定条件下可以合成甲醇,反应方程式为: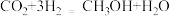 。该反应所涉及的4种物质,沸点从高到低的顺序为
。该反应所涉及的4种物质,沸点从高到低的顺序为________ 。
(3) 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为________ 。
(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图所示。
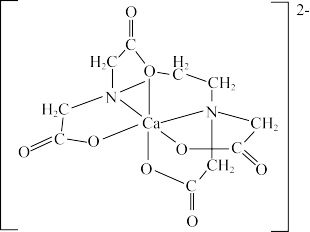
①钙离子的配位数是________ 。
②配体中碳原子的杂化方式有________ 。
(1)碳有多种单质,其中石墨烯与金刚石的晶体结构如图所示:

石墨烯能导电而金刚石不能导电的原因是
(2)碳的主要氧化物有CO和CO2
①CO能与金属Fe形成一种浅黄色液体Fe(CO)5,其熔点为-20℃,沸点为103℃,热稳定性较高,易溶于苯等有机溶剂,不溶于水。据此判断:该化合物的晶体中
A.离子键 B.极性键 C.非极性键 D.范德华力 E.配位键
②CO2在一定条件下可以合成甲醇,反应方程式为:
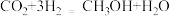 。该反应所涉及的4种物质,沸点从高到低的顺序为
。该反应所涉及的4种物质,沸点从高到低的顺序为(3)
 是重要的有机反应中间体,其空间构型为
是重要的有机反应中间体,其空间构型为(4)碳的有机物常作为金属有机化合物的配体,如EDTA(乙二胺四乙酸)。EDTA与Ca2+形成的配离子如图所示。

①钙离子的配位数是
②配体中碳原子的杂化方式有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)写出A、B、C、D、E 5种元素的元素符号
A是________ B是________ C是________ D是________ E是________
(2)D元素在周期表中的位置为_________________________ 。
(3)用电子排布式表示B元素原子的价电子构型_______________ 。
(4)元素的电负性的大小关系是B____ D,(填“>”、“<”或“﹦”),C与E的第一电离能的大小关系是C_____ E(填“>”、“<”或“﹦”)。
(5)A2D属于_____ (填“极性”或“非极性”)分子,其分子的空间构型为_________ 。
(6)D、E元素形成的化合物为________ 晶体,电子式为_______ 。
(1)写出A、B、C、D、E 5种元素的元素符号
A是
(2)D元素在周期表中的位置为
(3)用电子排布式表示B元素原子的价电子构型
(4)元素的电负性的大小关系是B
(5)A2D属于
(6)D、E元素形成的化合物为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铜元素及其化合物在生产实际中有许多重要用途。磷化铜(Cu3P2)常用于制造磷青铜(含少量锡、磷的铜合金)。请回答下列有关问题:
(1)现代化学中,常利用_______ 上的特征谱线来鉴定元素。
(2)铜晶体中铜原子的堆积方式如图所示,铜晶体中原子的堆积模型属于_____ 。

(3)基态磷原子中,电子占据的最高能层符号为______ ;该能层中具有的能量最高的电子所在能级有_____ 个伸展方向,原子轨道呈_____ 形。
(4)磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为____ ;P、S的第一电离能(I1)的大小为I1(P)______ I1(S)(填“>”“<”或“=”);PH3的沸点______ (填“高于”或“低于”)NH3的沸点,原因是______ 。
(5)磷青铜晶体的晶胞结构如图所示,该晶体中P原子位于由铜原子形成的______ 的空隙中。若晶体密度为agcm-3,则P与最近的Cu原子的核间距为______ nm(用含NA的代数式表示)。

(1)现代化学中,常利用
(2)铜晶体中铜原子的堆积方式如图所示,铜晶体中原子的堆积模型属于

(3)基态磷原子中,电子占据的最高能层符号为
(4)磷化铜与水反应产生有毒的磷化氢(PH3)气体,PH3分子的空间构型为
(5)磷青铜晶体的晶胞结构如图所示,该晶体中P原子位于由铜原子形成的

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)Fe3+的外围电子排布式为_____________ 。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于____ (填晶体类型)。
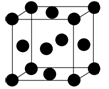
(3)Cu的晶胞如图所示,则晶体Cu的堆积方式为_________ 。
(4)若Cu单质的晶体密度为ρ g/cm3,Cu的相对原子质量为M g/mol,阿伏加德罗常数为NA mol-1,则Cu的原子半径为_________ cm。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有______ 个铜原子。
(1)Fe3+的外围电子排布式为
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于
(3)Cu的晶胞如图所示,则晶体Cu的堆积方式为

(4)若Cu单质的晶体密度为ρ g/cm3,Cu的相对原子质量为M g/mol,阿伏加德罗常数为NA mol-1,则Cu的原子半径为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】根据物质结构有关性质和特点,回答下列问题:
(1)Ti基态原子核外电子排布式为____________ ,碳原子的价电子 轨道表示式为________ 。
(2)钛存在两种同素异形体,α—Ti采纳六方最密堆积,β—Ti采纳体心立方堆积,由α—Ti转变为β—Ti晶体体积____________ (填“膨胀”或“收缩”)。
(3)写出一种与NH4+互为等电子体物质的化学式____________ 。
(4)SO2的空间构型为___________________ 。
(5)丙烯腈(CH2=CH—CN)分子中σ键和π键的个数比为____ ,分子中碳原子轨道杂化类型是______ 。
(6)FeCl3熔点282℃,而FeCl2熔点674℃,二者熔点差异的原因是______________ 。
(1)Ti基态原子核外电子排布式为
(2)钛存在两种同素异形体,α—Ti采纳六方最密堆积,β—Ti采纳体心立方堆积,由α—Ti转变为β—Ti晶体体积
(3)写出一种与NH4+互为等电子体物质的化学式
(4)SO2的空间构型为
(5)丙烯腈(CH2=CH—CN)分子中σ键和π键的个数比为
(6)FeCl3熔点282℃,而FeCl2熔点674℃,二者熔点差异的原因是
您最近一年使用:0次



