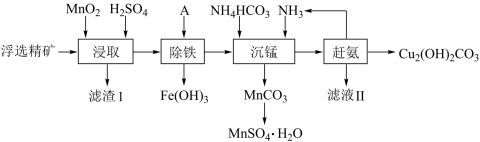
碱式碳酸铜在烟火、农药、颜料、杀菌剂等方面应用广泛。一种以辉铜矿( ,含有
,含有 和少量
和少量 等杂质)为原料制备碱式碳酸铜的流程如图所示:
等杂质)为原料制备碱式碳酸铜的流程如图所示:
已知:①有关金属离子形成氢氧化物沉淀的 范围如下:
范围如下:
② 常温稳定,在热水中会分解生成
常温稳定,在热水中会分解生成 ;
;
③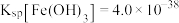 。
。
回答下列问题:
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有_______ 、_______ (任写两种)。
(2)滤渣Ⅰ经 提取后可获得一种淡黄色副产品,则滤渣Ⅰ中的主要成分除
提取后可获得一种淡黄色副产品,则滤渣Ⅰ中的主要成分除 外还有
外还有_______ (填化学式)。
(3)常温下“除铁”时加入的试剂A可用 ,调节
,调节 的范围为
的范围为_______ ,若加A后将溶液的 调为5,则溶液中
调为5,则溶液中 的浓度为
的浓度为_______  。
。
(4)写出“沉锰”(除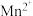 )过程中反应的离子方程式:
)过程中反应的离子方程式:_______ 。
(5)“赶氨”时,最适宜的操作方法是_______ 。
 ,含有
,含有 和少量
和少量 等杂质)为原料制备碱式碳酸铜的流程如图所示:
等杂质)为原料制备碱式碳酸铜的流程如图所示:
已知:①有关金属离子形成氢氧化物沉淀的
 范围如下:
范围如下:②
 常温稳定,在热水中会分解生成
常温稳定,在热水中会分解生成 ;
;③
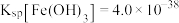 。
。| 金属离子 |  |  | 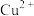 |  |
开始沉淀的 | 7.2 | 2.7 | 5.6 | 8.3 |
完全沉淀的 | 9.0 | 3.7 | 6.7 | 9.8 |
回答下列问题:
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有
(2)滤渣Ⅰ经
 提取后可获得一种淡黄色副产品,则滤渣Ⅰ中的主要成分除
提取后可获得一种淡黄色副产品,则滤渣Ⅰ中的主要成分除 外还有
外还有(3)常温下“除铁”时加入的试剂A可用
 ,调节
,调节 的范围为
的范围为 调为5,则溶液中
调为5,则溶液中 的浓度为
的浓度为 。
。(4)写出“沉锰”(除
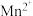 )过程中反应的离子方程式:
)过程中反应的离子方程式:(5)“赶氨”时,最适宜的操作方法是
更新时间:2022-12-11 23:18:03
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】生产生活中的化学电源、金属冶炼、环境污染等都与氧化还原反应息息相关,研究氧化还原反应,对人类进步和社会发展都具有极其重要的意义。
(1)已知下列反应在一定条件下可以发生:H2O2+2Fe2++2H+=2Fe3++2H2O;H2O2+2Fe3+= 2Fe2++2H+ +O2↑
①通过观察以上两个反应,对其中Fe2+的认识是__________________ 。
②I2和Fe2+一样也能与H2O2发生上述类似反应,类比上述反应,在下面空格上填入合适的化学方程式:H2O2+I2= 2HIO;___________ 。总的化学方程式为_____________________________ 。
(2)2017年4月1日,中共中央、国务院印发通知,决定设立河北雄安新区。据报道周边污水渗坑给雄安新区的水环境带来隐患,目前采用多种方法对污水进行处理,改善水资源状况。
①碱性环境下,Cl2可将水中残存的CN-转化为两种无毒的气体,则该反应生成两种无毒气体的物质的量之比为_________________ 。
②酸性环境下,向含重铬酸根(Cr2O72-)的废水中加入FeSO4溶液,然后调节溶液pH,使生成的Cr3+转化为Cr(OH)3,写出第一步反应对应的离子方程式________________________________ 。
(1)已知下列反应在一定条件下可以发生:H2O2+2Fe2++2H+=2Fe3++2H2O;H2O2+2Fe3+= 2Fe2++2H+ +O2↑
①通过观察以上两个反应,对其中Fe2+的认识是
②I2和Fe2+一样也能与H2O2发生上述类似反应,类比上述反应,在下面空格上填入合适的化学方程式:H2O2+I2= 2HIO;
(2)2017年4月1日,中共中央、国务院印发通知,决定设立河北雄安新区。据报道周边污水渗坑给雄安新区的水环境带来隐患,目前采用多种方法对污水进行处理,改善水资源状况。
①碱性环境下,Cl2可将水中残存的CN-转化为两种无毒的气体,则该反应生成两种无毒气体的物质的量之比为
②酸性环境下,向含重铬酸根(Cr2O72-)的废水中加入FeSO4溶液,然后调节溶液pH,使生成的Cr3+转化为Cr(OH)3,写出第一步反应对应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】有下列物质:①硫酸 ②盐酸 ③氯气 ④硫酸钡 ⑤酒精 ⑥铜 ⑦醋酸 ⑧氯化氢 ⑨蔗糖 ⑩氨气 ⑪CO2 ⑫NaHCO3 ⑬ NaOH。
(1)属于非电解质的为____ (填序号,下同),属于弱电解质的为___ ,能导电的是___ 。
(2)写出下列反应的离子方程式:
①NaHCO3溶于醋酸:______________________ 。
②过量CO2与NaOH溶液反应:______________ 。
③Cl2通入NaOH溶液中:___________________ 。
(1)属于非电解质的为
(2)写出下列反应的离子方程式:
①NaHCO3溶于醋酸:
②过量CO2与NaOH溶液反应:
③Cl2通入NaOH溶液中:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】运用分类方法,可以发现物质及其变化的规律,预测物质的性质及可能发生的变化。科学的分类能够反映事物的本质特征,有利于人们分门别类地进行深入研究。利用所学过的知识回答下列问题:
有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
(1)其中能导电的是_____ ;属于非电解质的是_____ 。
(2)等质量④和⑤中氢原子的数目之比为_____ ;若④和⑤中所含氢原子数相等,则④和⑤的质量之比为_____ 。
(3)写出⑥和⑩在水溶液中的离子方程式_____ 。
(4)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2混合气体和1mol空气,此时活塞的位置如图所示。
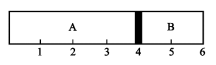
实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,(非气体体积忽略不计)最终活塞停留的位置在刻度_____ 处。
有以下物质①石墨;②钠;③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
(1)其中能导电的是
(2)等质量④和⑤中氢原子的数目之比为
(3)写出⑥和⑩在水溶液中的离子方程式
(4)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2混合气体和1mol空气,此时活塞的位置如图所示。

实验测得A室混合气体的质量为34g,若将A室H2、O2的混合气体点燃,恢复原温度后,(非气体体积忽略不计)最终活塞停留的位置在刻度
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】高锰酸钾可用于生活消毒,是中学化学常见的氧化剂。工业上,用软锰矿( 主要成分MnO2)制高锰酸钾的流程如下(部分条件和产物省略):

请回答下列问题:
(1)在“水浸”过程中,提高K2MnO4浸出率(浸出的K2MnO4质量与“熔块”质量之比)的措施有_______ ( 至少写出两点)。
(2)“熔融”过程中发生反应的化学方程式为___________ 。
(3)CO2 与K2MnO4反应的离子方程式为___________ 。
(4)“电解”过程中使用的是惰性电极,则:
①阳极反应的方程式为__________ 。
②阴极附近溶液的pH将__________ 。(填“增大”“减小” 或“ 不变”)。
(5)在上述过程中产生的Mn2+会对环境造成污染。工业上,通过调节pH使废水中的Mn2+形成Mn(OH)2 沉淀。当pH=10时,溶液中的c(Mn2+)=______ (已知:Ksp[Mn(OH)2]=2.0×10-13。相关数据均在常温下测定)。

请回答下列问题:
(1)在“水浸”过程中,提高K2MnO4浸出率(浸出的K2MnO4质量与“熔块”质量之比)的措施有
(2)“熔融”过程中发生反应的化学方程式为
(3)CO2 与K2MnO4反应的离子方程式为
(4)“电解”过程中使用的是惰性电极,则:
①阳极反应的方程式为
②阴极附近溶液的pH将
(5)在上述过程中产生的Mn2+会对环境造成污染。工业上,通过调节pH使废水中的Mn2+形成Mn(OH)2 沉淀。当pH=10时,溶液中的c(Mn2+)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)碳酸钠俗称纯碱,可作为碱使用的原因是__________________ (用离子方程式表示)。
(2)25℃时,pH均为11的 NaOH 溶液和Na2CO3溶液中,水电离的OH-浓度之比是_____
(3)在0.1 mol·L-1的Na2CO3溶液中,下列粒子浓度关系式正确的是________ 。
A.[CO32-]+[HCO3-]=0.1 mol·L-1
B.[CO32-]+[HCO3-]+[H2CO3]=0.1 mol·L-1
C.[OH-]=[H+]+[HCO3-]
D.[Na+]+[OH-]=[H+]+[HCO3-]
(4)常温下0.1 mol·L-1的Na2CO3溶液中,离子浓度由大到小的顺序是__________________________________ 。
(5)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中 =
=__________ 。(已知Ksp(BaCO3)=2.6×10−9,Ksp(BaSO4)=1.1×10−10,结果保留一位小数)
(2)25℃时,pH均为11的 NaOH 溶液和Na2CO3溶液中,水电离的OH-浓度之比是
(3)在0.1 mol·L-1的Na2CO3溶液中,下列粒子浓度关系式正确的是
A.[CO32-]+[HCO3-]=0.1 mol·L-1
B.[CO32-]+[HCO3-]+[H2CO3]=0.1 mol·L-1
C.[OH-]=[H+]+[HCO3-]
D.[Na+]+[OH-]=[H+]+[HCO3-]
(4)常温下0.1 mol·L-1的Na2CO3溶液中,离子浓度由大到小的顺序是
(5)向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时溶液中
 =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电子工业中,常用氯化铁溶液作为印刷电路铜板蚀刻液。请按要求回答下列问题:
(1)若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为:______________________________________ ,该过程中调节溶液的pH为5,则c(Fe3+)为:____________ mol·L-1。(已知:Ksp[Fe(OH)3]= 4.0×10-38)
(2)某探究小组设计如下线路处理废液和资源回收:
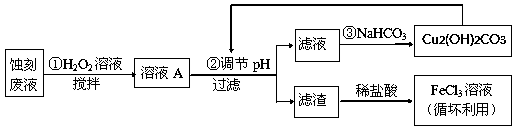
①用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有:_______________ 。
②FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是:_________________ 。
③步骤①中加入H2O2溶液的目的是:______________________________________ 。
④已知:生成氢氧化物沉淀的pH
根据表中数据推测调节pH的范围是:________________ 。
⑤写出步骤②中生成CO2的离子方程式:__________ (已知Cu2(OH)2CO3难溶于水)。
(1)若向氯化铁溶液中加入一定量的澄清石灰水,调节溶液pH,可得红褐色沉淀,该反应的离子方程式为:
(2)某探究小组设计如下线路处理废液和资源回收:

①用足量FeCl3溶液蚀刻铜板后的废液中含有的金属阳离子有:
②FeCl3蚀刻液中通常加入一定量的盐酸,其中加入盐酸的目的是:
③步骤①中加入H2O2溶液的目的是:
④已知:生成氢氧化物沉淀的pH
| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 4.7 | 7.0 | 1.9 |
| 沉淀完全时 | 6.7 | 9.0 | 3.2 |
⑤写出步骤②中生成CO2的离子方程式:
您最近一年使用:0次
【推荐1】碘是人类发现的第二个生命科学必需微量元素。回答下列问题:
(1)碘与氯是同族元素,它们位于元素周期表的第___ 族;HI的还原性比HCl___ (填“强”或“弱”)。
(2)自然界中的碘有的以NaIO3形态存在于硝石(NaNO3)中,向硝石母液中加入NaHSO3可以制得I2,请写出NaIO3溶液和NaHSO3溶液反应的离子方程式____ 。
(3)碘还以碘化物的形态存在于海水中,被海藻类植物吸收而富集,从海带中提取碘的过程如下:

步骤③的操作名称为__ ;步骤④发生反应的离子方程式为___ ;步骤⑤的实验操作为____ ;
(4)步骤③得到的滤液中c(I-)=0.004mol/L,取10mL滤液加入10mLPb(NO3)2溶液,若要生成PbI2沉淀,则所加Pb(NO3)2溶液的浓度应大于___ mol/L[已知Ksp(PbI2)=9.8×10-9]。
(1)碘与氯是同族元素,它们位于元素周期表的第
(2)自然界中的碘有的以NaIO3形态存在于硝石(NaNO3)中,向硝石母液中加入NaHSO3可以制得I2,请写出NaIO3溶液和NaHSO3溶液反应的离子方程式
(3)碘还以碘化物的形态存在于海水中,被海藻类植物吸收而富集,从海带中提取碘的过程如下:

步骤③的操作名称为
(4)步骤③得到的滤液中c(I-)=0.004mol/L,取10mL滤液加入10mLPb(NO3)2溶液,若要生成PbI2沉淀,则所加Pb(NO3)2溶液的浓度应大于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】以下为从铝土矿(Al2O3、Fe2O3、泥沙)提取铝的流程图(注:整个流程中,不考虑泥沙的溶解及有关反应;C可以用来治疗胃酸过多):

(1)A溶质的化学式___________ ;B的结构式____________ ,Y的名称_____________ 。
(2)写出①C与Ca(OH)2稀溶液反应的离子方程式:__________________________________ 。
②F→B的反应方程式:______________________________ 。
(3)操作(Ⅰ)、(Ⅱ)在工业生产中的意义________________________ 。

(1)A溶质的化学式
(2)写出①C与Ca(OH)2稀溶液反应的离子方程式:
②F→B的反应方程式:
(3)操作(Ⅰ)、(Ⅱ)在工业生产中的意义
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某校化学兴趣小组用如图所示过程除去硫酸铝中含有的Mg2+、K+杂质离子并尽可能减少硫酸铝的损失。
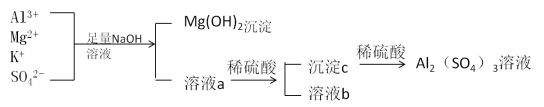
请回答下列问题:
(1)混合物中加入足量氢氧化钠溶液时,反应的离子方程式是________________ 、________________________________ 。
(2)能否用氨水代替氢氧化钠溶液____________ ,其原因是____________________________ 。
(3)溶液a中存在的离子有________________________ ,在溶液a中加入稀硫酸时需控制硫酸的量,其原因是__________________________________________ ,改进方法是__________________________________________________________ 。

请回答下列问题:
(1)混合物中加入足量氢氧化钠溶液时,反应的离子方程式是
(2)能否用氨水代替氢氧化钠溶液
(3)溶液a中存在的离子有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】碳酸钙常用作牙膏的摩擦剂。某同学设计了一种制备碳酸钙的方案,其流程图如下。(所用石灰石含有杂质SiO2)

回答下列问题:
(1)充分煅烧110吨石灰石得到固体66吨,则石灰石中碳酸钙的质量分数为______ %。
(2)假设第①步反应完全进行,则第②步反应过滤后得到的不溶液性滤渣的成分为___________ 。
(3)第③步反应一般不采用通入CO2的主要原因是_____________ ,相应的离子方程式为_______________ 。
(4)CaCO3是一种难溶液物质,25℃时其Ksp=2.8×10-9。现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2.0×10-4mol/L,则生成沉淀所需CaCl2溶液的物质的量浓度最小是________________ 。
(5)某生用石灰石为原料,设计了另一种制备碳酸钙的实验方案,其流程图如下:

与前一方案相比较,该方案的优点是_______________ 。

回答下列问题:
(1)充分煅烧110吨石灰石得到固体66吨,则石灰石中碳酸钙的质量分数为
(2)假设第①步反应完全进行,则第②步反应过滤后得到的不溶液性滤渣的成分为
(3)第③步反应一般不采用通入CO2的主要原因是
(4)CaCO3是一种难溶液物质,25℃时其Ksp=2.8×10-9。现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2.0×10-4mol/L,则生成沉淀所需CaCl2溶液的物质的量浓度最小是
(5)某生用石灰石为原料,设计了另一种制备碳酸钙的实验方案,其流程图如下:

与前一方案相比较,该方案的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是_________________ 。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是______________________ 。
“滤液”中的溶质主要是__________________ 。
(3)KIO3也可采用“电解法”制备,装置如图所示。

①写出电解时阴极的电极反应式________________________________ 。
②电解过程中通过阳离子交换膜的离子主要为_______________ 。
③与“电解法”相比,“KClO3氧化法”的主要不足之处有___________________________________________ (写出一点)。
(1)KIO3的化学名称是
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是
“滤液”中的溶质主要是
(3)KIO3也可采用“电解法”制备,装置如图所示。

①写出电解时阴极的电极反应式
②电解过程中通过阳离子交换膜的离子主要为
③与“电解法”相比,“KClO3氧化法”的主要不足之处有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】NH3和HNO3是重要的工业产品,下图为合成氨以及氨氧化制硝酸的流程。

(1)合成塔中发生反应的化学方程式是_______________________________
从氨分离器中又回到合成塔中的物质是_________________ 。
(2)氧化炉中发生反应的化学方程式是_________________________________________
(3)尾气中的少量NO、NO2可以用NH3来处理,在催化剂作用下生成无污染的气体,写出NO2和 NH3反应的化学方程式__________________________________________________
当有5.6L NO2被还原时,转移电子的物质的量为________________ mol.
(4)氧化炉中出来的气体,先降温再进入吸收塔,吸收塔中通入空气的作用是_________________ .若进入吸收塔的气体的体积分数为NO210.0%,NO 1.32% ,其余为N2、水蒸气等.当进入吸收塔中气体为10m3时,最少需要空气的体积为_____________ m3。

(1)合成塔中发生反应的化学方程式是
从氨分离器中又回到合成塔中的物质是
(2)氧化炉中发生反应的化学方程式是
(3)尾气中的少量NO、NO2可以用NH3来处理,在催化剂作用下生成无污染的气体,写出NO2和 NH3反应的化学方程式
当有5.6L NO2被还原时,转移电子的物质的量为
(4)氧化炉中出来的气体,先降温再进入吸收塔,吸收塔中通入空气的作用是
您最近一年使用:0次



