硼砂是含结晶水的四硼酸钠,请根据模型回答有关问题:
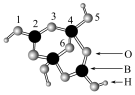
(1)硼砂中阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,则在Xm-中的2号硼原子的价层电子对数为_____ ;m=_____ (填数字)。
(2)硼可以与氮形成BN,其中B的化合价为_____ ,请解释原因:_____ 。
(3)BF3和过量NaF作用可生成NaBF4,BF 的空间结构为
的空间结构为_____ ;NaBF4的电子式为_____ 。

(1)硼砂中阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示,则在Xm-中的2号硼原子的价层电子对数为
(2)硼可以与氮形成BN,其中B的化合价为
(3)BF3和过量NaF作用可生成NaBF4,BF
 的空间结构为
的空间结构为
21-22高二下·全国·单元测试 查看更多[1]
(已下线)【知识图鉴】单元讲练测选择性必修2第二章01讲核心
更新时间:2022-12-15 21:48:16
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】用化学用语表示。
(1)氖气_____ ;
(2)碘酒中的溶剂_____ ;
(3)镁离子的结构示意图为_____ ;
(4)标出氢氧化铝中铝元素的化合价_____ 。
(1)氖气
(2)碘酒中的溶剂
(3)镁离子的结构示意图为
(4)标出氢氧化铝中铝元素的化合价
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】写出下列原子的电子式
O___________ 、Mg___________ 、C___________ 、N___________ 、Al___________ 、S___________ 。
O
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E、F代表6种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为________ ;
(2)B元素的-1价离子和C元素的+1价离子的电子层结构都与氩相同,则B的元素符号为_______ ,C的元素符号为________ ;
(3)D元素的+3价离子的3d能级为半充满,则D的元素符号为__ ,其基态原子的电子排布式为___ ;
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为________ ,其基态原子的电子排布式为________________________________ ;
(5)F元素的原子最外层电子排布式为nsnnpn,则n=________ ;原子中能量最高的是________ 能级。
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的-1价离子和C元素的+1价离子的电子层结构都与氩相同,则B的元素符号为
(3)D元素的+3价离子的3d能级为半充满,则D的元素符号为
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素符号为
(5)F元素的原子最外层电子排布式为nsnnpn,则n=
您最近一年使用:0次
【推荐2】元素周期表中锑元素的数据如图。

(1)根据锑的价层电子排布式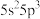 可知,锑在元素周期表中位于第
可知,锑在元素周期表中位于第_______ 周期第_______ 族。
(2)基态锑原子中有_______ 个未成对电子,这些未成对电子具有_______ (填“相同”或“不同”)的自旋状态。
(3)基态锑原子的5s轨道形状为_______ 形;该原子最外层电子占有_______ 个轨道。
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。
①下列推断正确的是_______ 。
a.电负性:Sb>Bi b.原子半径:Sb>Bi c.金属性:Sb>Bi d.氧化性: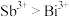
②第一电离能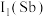
_______ (填“大于”或“小于”) 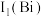 ,原因是
,原因是_______ 。

(1)根据锑的价层电子排布式
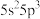 可知,锑在元素周期表中位于第
可知,锑在元素周期表中位于第(2)基态锑原子中有
(3)基态锑原子的5s轨道形状为
(4)Bi在元素周期表中与Sb相邻,位于Sb的正下方。
①下列推断正确的是
a.电负性:Sb>Bi b.原子半径:Sb>Bi c.金属性:Sb>Bi d.氧化性:
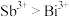
②第一电离能
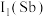
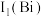 ,原因是
,原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】已知W、X、Y、Z、N是周期表中前四周期元素,它们的核电荷数依次增大。
回答下列问题:
(1)写出X的元素符号:X______ 。
(2)基态Y原子价电子的电子排布式:______ 。
(3)W、X、Z三种元素的电负性由大到小的顺序是______ (填元素符号)。
(4)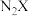 和
和 的熔点更高的是
的熔点更高的是______ (填化学式),原因是:______ 。
(5)根据价层电子对互斥理论, 的空间构型为
的空间构型为______ , 中心原子的杂化方式为
中心原子的杂化方式为______ , 和
和 中键角较小的是
中键角较小的是______ (用离子符号表示)。
元素 | 元素性质或原子结构或离子结构 |
W | 原子核内无中子 |
X | 基态原子核外s能级上的电子总数与p能级上的电子总数相等 |
Y | 元素的原子半径在同周期中最大 |
Z | 基态原子核外有9种不同空间运动状态的电子,且有两个未成对电子 |
N |
|
(1)写出X的元素符号:X
(2)基态Y原子价电子的电子排布式:
(3)W、X、Z三种元素的电负性由大到小的顺序是
(4)
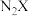 和
和 的熔点更高的是
的熔点更高的是(5)根据价层电子对互斥理论,
 的空间构型为
的空间构型为 中心原子的杂化方式为
中心原子的杂化方式为 和
和 中键角较小的是
中键角较小的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】按要求填空:
I.指出下列分子或离子的中心原子的杂化轨道类型及分子的空间结构
(1)SiF4:_______ 杂化,空间结构_______ ;
(2) :
:_______ 杂化,空间结构_______ ;
(3) :
:_______ 杂化,空间结构_______ ;
(4)CS2:_______ 杂化,空间结构_______ ;
II.
(5)O、S、Se为同主族元素, 和
和 的相对分子质量相等,常温下,
的相对分子质量相等,常温下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是_______ ;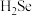 分子的中心原子杂化类型为
分子的中心原子杂化类型为_______ 杂化;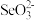 的空间构型为
的空间构型为_______ 。
I.指出下列分子或离子的中心原子的杂化轨道类型及分子的空间结构
(1)SiF4:
(2)
 :
:(3)
 :
:(4)CS2:
II.
(5)O、S、Se为同主族元素,
 和
和 的相对分子质量相等,常温下,
的相对分子质量相等,常温下, 呈液态,而
呈液态,而 呈气态,其主要原因是
呈气态,其主要原因是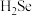 分子的中心原子杂化类型为
分子的中心原子杂化类型为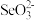 的空间构型为
的空间构型为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气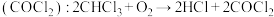 ,光气
,光气 分子的立体构型是
分子的立体构型是________ 形。
(2)某有机物的结构简式为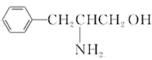 。该有机物分子是
。该有机物分子是____________ (填“极性”或“非极性”)分子,该有机物分子中采取 杂化的原子对应元素的电负性由大到小的顺序为
杂化的原子对应元素的电负性由大到小的顺序为____________ 。
(3)乙二胺 分子中氮原子杂化类型为
分子中氮原子杂化类型为_________________ 。
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸( )是一种弱酸,其分子结构可表示为
)是一种弱酸,其分子结构可表示为 ,肼
,肼 被亚硝酸氧化时便可得到氢叠氮酸
被亚硝酸氧化时便可得到氢叠氮酸 ,发生的反应为
,发生的反应为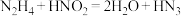 。
。 的酸性和醋酸相近,可微弱电离出
的酸性和醋酸相近,可微弱电离出 和
和 。
。
①叠氮酸根能与许多金属离子等形成配合物,如 ,根据价层电子对互斥理论判断
,根据价层电子对互斥理论判断 的空间构型为
的空间构型为________________ 。
②下列有关说法正确的是_____________ (填序号)。
A. 中含有5个
中含有5个 键
键
B. 中的三个氮原子均采用
中的三个氮原子均采用 杂化
杂化
C. 、
、 、
、 、
、 都是极性分子
都是极性分子
D.肼 的沸点高达
的沸点高达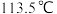 ,说明肼分子间可形成氢键
,说明肼分子间可形成氢键
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气
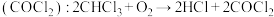 ,光气
,光气 分子的立体构型是
分子的立体构型是(2)某有机物的结构简式为
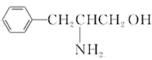 。该有机物分子是
。该有机物分子是 杂化的原子对应元素的电负性由大到小的顺序为
杂化的原子对应元素的电负性由大到小的顺序为(3)乙二胺
 分子中氮原子杂化类型为
分子中氮原子杂化类型为(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(
 )是一种弱酸,其分子结构可表示为
)是一种弱酸,其分子结构可表示为 ,肼
,肼 被亚硝酸氧化时便可得到氢叠氮酸
被亚硝酸氧化时便可得到氢叠氮酸 ,发生的反应为
,发生的反应为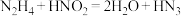 。
。 的酸性和醋酸相近,可微弱电离出
的酸性和醋酸相近,可微弱电离出 和
和 。
。①叠氮酸根能与许多金属离子等形成配合物,如
 ,根据价层电子对互斥理论判断
,根据价层电子对互斥理论判断 的空间构型为
的空间构型为②下列有关说法正确的是
A.
 中含有5个
中含有5个 键
键B.
 中的三个氮原子均采用
中的三个氮原子均采用 杂化
杂化C.
 、
、 、
、 、
、 都是极性分子
都是极性分子D.肼
 的沸点高达
的沸点高达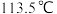 ,说明肼分子间可形成氢键
,说明肼分子间可形成氢键
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】小明同学上网查阅了如下资料:
中心原子杂化类型的判断方法:
(1)公式:n=(中心原子的价电子数+配位原子的成键电子数±电荷数)
说明:配位原子为氧原子或硫原子时,成键电子数看为0;当电荷数为正值时,公式中取“-”号,当电荷数为负值时,公式中取“+”号。
(2)根据n值判断杂化类型:
当n=2时为sp杂化;n=3时为sp2杂化;n=4时为sp3杂化。
请你运用该方法计算下列微粒的n值,并判断中心原子的杂化类型。
① NH3:n=___________ ,___________ 杂化;
② N:n=____________ ,___________ 杂化;
③ N:n=____________ ,____________ 杂化;
④ SO2:n=____________ ,____________ 杂化。
中心原子杂化类型的判断方法:
(1)公式:n=(中心原子的价电子数+配位原子的成键电子数±电荷数)
说明:配位原子为氧原子或硫原子时,成键电子数看为0;当电荷数为正值时,公式中取“-”号,当电荷数为负值时,公式中取“+”号。
(2)根据n值判断杂化类型:
当n=2时为sp杂化;n=3时为sp2杂化;n=4时为sp3杂化。
请你运用该方法计算下列微粒的n值,并判断中心原子的杂化类型。
① NH3:n=
② N:n=
③ N:n=
④ SO2:n=
您最近一年使用:0次

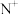 的M层全充满
的M层全充满

