下列事实,不能用勒夏特列原理解释的是
| A.工业上采用高压条件合成氨气 |
| B.实验室中常用排饱和食盐水的方法收集Cl2 |
| C.室温下,pH=1的醋酸溶液加水稀释100倍后pH<3 |
| D.往盛有30%H2O2的试管中加入少许MnO2粉末,迅速产生大量气泡 |
更新时间:2022-12-09 08:11:27
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】只用如图所示装置进行下列实验,能够得出相应实验结论的是
| 选项 | ① | ② | ③ | 实验结论 | 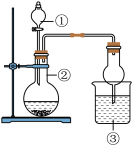 |
| A | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si | |
| B | 饱和食盐水 | 电石 | 高锰酸钾溶液 | 生成乙炔 | |
| C | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| D | 浓硫酸 | Na2SO3 | 溴水 | SO2具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列关于氯的说法正确的是 ( )
| A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂 |
| B.1735Cl、1737Cl为不同的核素,有不同的化学性质 |
| C.工业上用氯气和石灰乳为原料制造漂白粉 |
| D.实验室制备Cl2,可用排水集气法收集 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某温度下,反应N2(g)+3H2(g)⇌2NH3(g);△H<0,在密闭容器中达到平衡,平衡时改变外界条件,使反应再次平衡,新平衡时, 与原平衡相比变小了,则改变条件的可能有
与原平衡相比变小了,则改变条件的可能有
 与原平衡相比变小了,则改变条件的可能有
与原平衡相比变小了,则改变条件的可能有| A.保持容器的容积不变,升高了温度 |
| B.保持容器压强和温度不变,向容器内补充了Ar(g) |
| C.保持容器容积和温度不变,向容器内补充了N2 |
| D.保持容器容积和温度不变,液化分离走部分NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】纳米碗 是一种奇特的碗状共轭体系。高温条件下,
是一种奇特的碗状共轭体系。高温条件下, 可以由
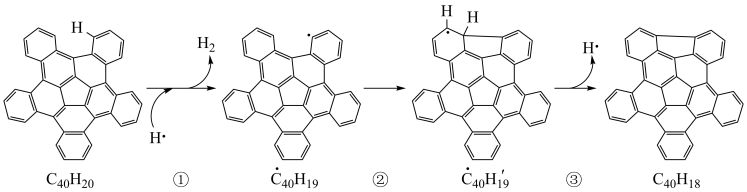
可以由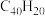 分子经过连续5步氢抽提和闭环脱氢反应生成,其中
分子经过连续5步氢抽提和闭环脱氢反应生成,其中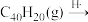
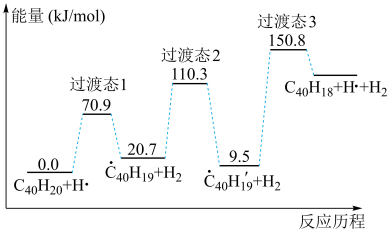
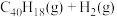 的反应机理和能量变化如图所示。已知
的反应机理和能量变化如图所示。已知 中的碳氢键和碳碳键的键能分别为
中的碳氢键和碳碳键的键能分别为 和
和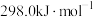 ,
, 键能为
键能为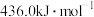 。下列说法正确的是
。下列说法正确的是
 是一种奇特的碗状共轭体系。高温条件下,
是一种奇特的碗状共轭体系。高温条件下, 可以由
可以由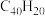 分子经过连续5步氢抽提和闭环脱氢反应生成,其中
分子经过连续5步氢抽提和闭环脱氢反应生成,其中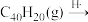
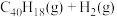 的反应机理和能量变化如图所示。已知
的反应机理和能量变化如图所示。已知 中的碳氢键和碳碳键的键能分别为
中的碳氢键和碳碳键的键能分别为 和
和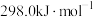 ,
, 键能为
键能为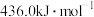 。下列说法正确的是
。下列说法正确的是

A.上述历程中涉及的中间体中的C原子的杂化方式均为 |
| B.图中基元反应均为吸热反应,步骤②为整个反应的决速步骤 |
C.反应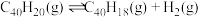 的 的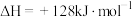 |
D.增大压强既能提高反应物的平衡转化率,又能增大生成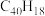 的反应速率 的反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】有两只密闭容器A和B,A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等物质的量SO3气体,并使A和B容积相等(如下图所示)。在保持400℃的条件下使之发生如下反应:2SO2+O2 2SO3。
2SO3。

则下列描述正确的是
 2SO3。
2SO3。
则下列描述正确的是
| A.达到平衡所需要的时间:A容器更短 |
| B.达到平衡时:B容器中SO3的转化率更大 |
| C.达到平衡时:A容器中SO2的物质的量更多 |
| D.达到平衡后,向两容器中分别通入等量的氦气,A容器中SO3的体积分数增大,B容器中SO3的体积分数不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列能用勒夏特列原理解释的是
| A.SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| B.铁在潮湿的空气中容易生锈 |
| C.红棕色NO2加压后颜色先变深后变浅 |
| D.H2、I2、HI平衡混和气加压后颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列事实不能用化学平衡移动原理解释的是
| A.高压比常压有利于合成NH3的反应 |
| B.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| C.Na2CO3在温水中去油污能力比在冷水中强 |
| D.常温时,AgCl在饱和氯化钠溶液中的溶解度小于在水中的溶解度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,相同体积的pH=2的醋酸和盐酸溶液分别采取下列措施,有关叙述正确的是
| A.加水稀释100倍后,两溶液的pH均为4 |
| B.使温度都升高20℃后,两溶液的pH均不变 |
| C.与足量的锌反应,盐酸的反应速率比醋酸大 |
| D.加足量的锌充分反应后,醋酸产生的氢气比盐酸多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,有100mLpH=2的两种一元酸x和y,稀释过程中pH与溶液体积的关系如下图所示,则:
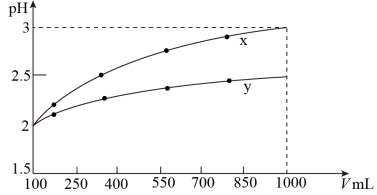

| A.x为弱酸,y为强酸 |
| B.随着稀释的进行,y的电离程度减小 |
| C.稀释前x、y的物质的量浓度相等 |
| D.稀释后的x、y分别分别与足量的锌反应,y放出的氢气多 |
您最近一年使用:0次

 的性质。下列说法正确的是
的性质。下列说法正确的是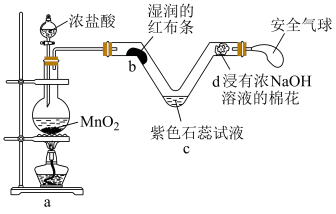
 处湿润的红布条褪色,说明
处湿润的红布条褪色,说明 处的紫色石蕊试液先变红,说明
处的紫色石蕊试液先变红,说明 气体
气体 处浓
处浓 溶液的作用是除去
溶液的作用是除去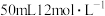 的盐酸与足量
的盐酸与足量 反应,产生
反应,产生
 HBr+HBrO,加入AgNO3溶液后,溶液颜色变浅
HBr+HBrO,加入AgNO3溶液后,溶液颜色变浅 的氨水,下列判断正确的是
的氨水,下列判断正确的是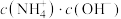 变大
变大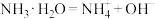
 溶液反应的离子方程式为
溶液反应的离子方程式为
 溶液恰好完全中和
溶液恰好完全中和

