已知化合物A与H2O在一定条件下反应生成化合物B与HCOO-,其反应历程如图所示,其中TS表示过渡态,I表示中间体。下列说法正确的是
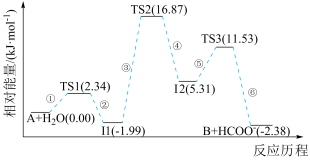

| A.该过程的总反应速率由⑥步骤决定 |
B.该历程中的最大能垒(活化能)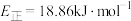 |
C.使用更高效的催化剂可降低该反应的 |
D.降低温度,有利于提高 的转化率 的转化率 |
22-23高二上·山东滨州·期中 查看更多[2]
更新时间:2022-12-17 13:23:40
|
相似题推荐
多选题
|
适中
(0.65)
【推荐1】2021年诺贝尔化学奖授予两位“不对称有机催化”领域的先驱,催化剂经常用在有机化学中,例如铁的配合物离子(用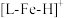 表示)催化甲酸分解的反应机理和相对能量的变化情况如图所示:
表示)催化甲酸分解的反应机理和相对能量的变化情况如图所示:

下列说法正确的是
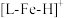 表示)催化甲酸分解的反应机理和相对能量的变化情况如图所示:
表示)催化甲酸分解的反应机理和相对能量的变化情况如图所示:
下列说法正确的是
| A.该过程的总反应为吸热反应 |
| B.该过程的总反应速率由Ⅱ→Ⅲ步骤决定 |
C.该过程中,溶液 值的大小会影响化学反应的快慢 值的大小会影响化学反应的快慢 |
D.在整个过程中,每生成标况下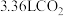 转移电子数为 转移电子数为 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】下列图示与对应的叙述相符的是
 |  |  |  |
| A.铁件镀银 | B.由褪色快慢研究反应物浓度对反应速率的影响 | C.稀硫酸与锌粒反应制氢气的能量变化 | D.蒸干硫酸铝溶液制无水硫酸铝固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
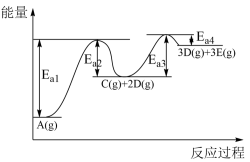
【推荐1】已知A转化为D和E分两步进:①A(g) C(g)+2D(g);②C(g)
C(g)+2D(g);②C(g) D(g)+3E(g),其反应过程能量变化如图所示,下列说法
D(g)+3E(g),其反应过程能量变化如图所示,下列说法错误 的是
 C(g)+2D(g);②C(g)
C(g)+2D(g);②C(g) D(g)+3E(g),其反应过程能量变化如图所示,下列说法
D(g)+3E(g),其反应过程能量变化如图所示,下列说法
A.反应②C(g) D(g)+3E(g)的∆H=Ea4-Ea3 D(g)+3E(g)的∆H=Ea4-Ea3 |
| B.A转化为D和E的速率是由反应①决定的 |
| C.1mol A(g)的能量低于1mol C(g)的能量 |
| D.反应过程中,C物质很难大量积累 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
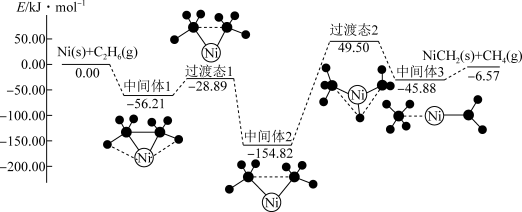
【推荐2】C2H6在Ni的活化下可放出CH4,其反应历程如下图所示:

下列关于活化历程的说法正确的是

下列关于活化历程的说法正确的是
| A.该转化过程ΔH>0 |
| B.在此反应过程中Ni的成键数目发生变化 |
| C.该反应过程中,最大能垒(活化能)为204.32kJ·mol-1 |
| D.整个过程中,Ni是该反应的催化剂 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】甲醇燃料是一种新的替代燃料,它和普通的汽油、柴油比较,优势十分明显。目前正在开发用甲烷和氧气合成甲醇:2CH4(g)+O2(g) 2CH3OH(g)。
2CH3OH(g)。
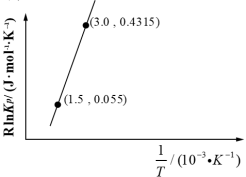
已知:RlnKp=- +C(R、C均为常数)。
+C(R、C均为常数)。
下列说法错误的是
 2CH3OH(g)。
2CH3OH(g)。
已知:RlnKp=-
 +C(R、C均为常数)。
+C(R、C均为常数)。下列说法错误的是
| A.恒压条件下,温度升高,Kp减小 |
| B.恒温条件下,压强增大,△H减小 |
| C.向恒压容器中加入2molCH4和1molO2,达到平衡,放出0.251kJ热量 |
| D.催化剂可以提高该反应的生产效率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】下列有关实验操作、现象和结论都正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 相同温度下,将两片质量和表面积相同的未经打磨的铝片分别投入足量等浓度的CuSO4溶液和CuCl2溶液中 | CuSO4溶液中无明显现象;CuCl2溶液中反应剧烈,铝片表面有红色物质生成 | Cl-能加速破坏铝片表面的氧化膜 |
| B | 用pH计测定Na2CO3溶液和CH3COONa溶液的pH | Na2CO3溶液的pH大于CH3 COONa | H2CO3酸性弱于CH3COOH |
| C | 分别向等体积的0.01mol L-1和0.1mol L-1和0.1mol L-1的KMnO4溶液中通入足量SO2,记录溶液褪色所需的时间 L-1的KMnO4溶液中通入足量SO2,记录溶液褪色所需的时间 | 0.1 mol L-1KMnO4溶液褪色所需时间更短 L-1KMnO4溶液褪色所需时间更短 | 其他条件相同时,增大反应物浓度,反应速率增大 |
| D | 向烧杯中加入一定量的Ca(OH)2和NH4Cl晶体的混合物,将烧杯放在有水的玻璃片上,用玻璃棒迅速搅拌 | 有刺激性气味气体生成,烧杯底部结冰,与玻璃片冻结在一起 | 吸热反应不一定需要加热才能进行 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】在恒容密闭容器中发生反应2SiHCl3(g)⇌SiH2Cl2(g)+SiCl4(g)。在323K和343K时SiHCl3的转化率随时间变化的结果如图所示。下列说法正确的是( )
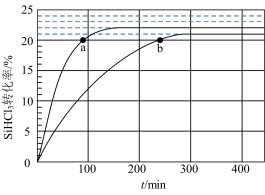

| A.323 K时,缩小容器体积可提高SiHCl3的转化率 |
| B.a、b点对应的反应速率大小关系:v(a)<v(b) |
| C.343 K时,上述反应的化学平衡常数约为0.02 |
| D.2SiHCl3(g)⇌SiH2Cl2(g)+SiCl4(g)的正反应为吸热反应 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】T ℃时,某1 L恒容密闭容器中存在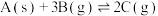 的反应,测得部分数据如表所示:
的反应,测得部分数据如表所示:
下列说法错误的是
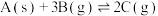 的反应,测得部分数据如表所示:
的反应,测得部分数据如表所示:| 物质 | A | B | C |
| 初始量/mol | 0.2 | 0.3 | 0 |
| 4 min末量/mol | 0.12 | b | c |
| 平衡量/mol | a | d | 0.18 |
A.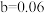 |
B.T ℃时,该反应的平衡常数为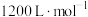 |
| C.若升高温度后C的平衡产率增大,则该反应是放热反应 |
| D.若向容器中再加入一定量A,平衡后C的体积分数增大 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
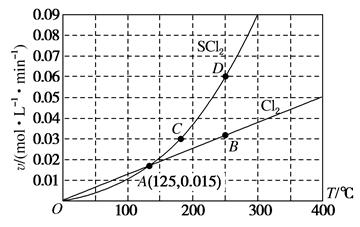
【推荐3】一定压强下,向10L密闭容器中充入1molS2Cl2和1molCl2,发生反应: S2Cl2(g)+Cl2(g) 2SCl2(g)。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图,以下说法错误的是
2SCl2(g)。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图,以下说法错误的是
 2SCl2(g)。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图,以下说法错误的是
2SCl2(g)。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图,以下说法错误的是
| A.正反应的活化能大于逆反应的活化能 |
| B.A、B、C、D四点对应状态下,达到平衡状态的为A点 |
| C.一定温度下,在密闭容器中达到平衡后缩小容器体积,重新达到平衡后,S2Cl2的平衡转化率不变 |
| D.达到平衡后再加热,平衡向逆反应方向移动 |
您最近一年使用:0次

 不能自发进行,则该反应的
不能自发进行,则该反应的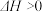
 、
、 、
、 的氧化性依次减弱
的氧化性依次减弱

