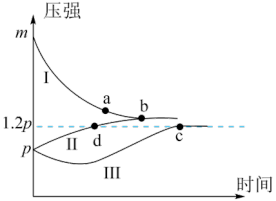
一定条件下,分别向体积为1L的密闭容器中充入气体,发生反应Z (g)  2X(g)+Y(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
2X(g)+Y(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
 2X(g)+Y(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
2X(g)+Y(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
| 实验 | 充入气体量 | 反应过程条件 |
| ① | 2mol X+1mol Y | 恒温 |
| ② | 1molZ | 恒温 |
| ③ | 1molZ | 绝热 |
| A.曲线Ⅰ对应实验①,且3m=p | B.Z的转化率:b<c |
C.气体的总物质的量: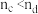 | D.b点平衡常数: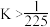 |
更新时间:2023-01-13 17:12:10
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】按体积比2:1向容器中充入NO和O2,发生反应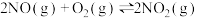 。测得温度、压强对NO平衡转化率的影响如下图所示。下列说法正确的是
。测得温度、压强对NO平衡转化率的影响如下图所示。下列说法正确的是
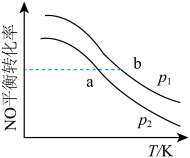
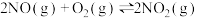 。测得温度、压强对NO平衡转化率的影响如下图所示。下列说法正确的是
。测得温度、压强对NO平衡转化率的影响如下图所示。下列说法正确的是
A.反应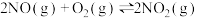 的 的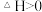 |
| B.该反应在任意条件下均能自反进行 |
C. |
D.平衡常数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图表示不同温度和压强对可逆反应: 2L(g) 2M(g)+N(g) △H>0 的影响,图中 y 轴表示的意义可能是
2M(g)+N(g) △H>0 的影响,图中 y 轴表示的意义可能是
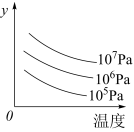
①一定条件下 L 的转化率 ②气体混合物中 M 的百分含量 ③气体混合物中L 的百分含量④混合气体的平均摩尔质量
 2M(g)+N(g) △H>0 的影响,图中 y 轴表示的意义可能是
2M(g)+N(g) △H>0 的影响,图中 y 轴表示的意义可能是
①一定条件下 L 的转化率 ②气体混合物中 M 的百分含量 ③气体混合物中L 的百分含量④混合气体的平均摩尔质量
| A.①② | B.①③ | C.②④ | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】CO可用于合成甲醇,其反应的化学方程式为CO(g)+2H2(g)⇌CH3OH(g)。在一容积可变的密闭容器中充有10molCO与20molH2,在催化剂作用下发生反应生成甲醇。CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示。下列说法正确的是


| A.合成甲醇的反应为吸热反应 |
| B.A、B、C三点的平衡常数为KA=KB>KC |
| C.压强为p1>p2 |
| D.若达平衡状态A时,容器的容积为10L,则在平衡状态B时容器的容积也为10L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】丙烯腈(C3H3N)是制备腈纶的单体。一种制备丙烯腈反应的热化学方程式为C3H6(g)+NH3(g)+ O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是
 O2(g)=C3H3N(g)+3H2O(g)
O2(g)=C3H3N(g)+3H2O(g)  H<0,下列说法正确的是
H<0,下列说法正确的是| A.该反应只有在低温下才能自发进行 |
B.该反应的平衡常数K= |
| C.该反应每消耗1molC3H6,转移电子的物质的量为6mol |
| D.其他条件相同,减压和升温均有利于提高丙烯腊的平衡产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】汽车尾气净化的主要原理为2NO(g)+2CO(g) N2(g)+2CO2(g),一定温度下,在三个容积均为2.0L的恒容密闭容器中起始物质的量与反应温度如表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示∶
N2(g)+2CO2(g),一定温度下,在三个容积均为2.0L的恒容密闭容器中起始物质的量与反应温度如表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示∶

下列说法正确的是
 N2(g)+2CO2(g),一定温度下,在三个容积均为2.0L的恒容密闭容器中起始物质的量与反应温度如表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示∶
N2(g)+2CO2(g),一定温度下,在三个容积均为2.0L的恒容密闭容器中起始物质的量与反应温度如表所示,反应过程中甲、丙容器中CO2的物质的量随时间变化关系如图所示∶| 容器 | 温度/℃ | 起始物质的量/mol | |
| NO(g) | CO(g) | ||
| 甲 | T1 | 0.20 | 0.20 |
| 乙 | T1 | 0.30 | 0.30 |
| 丙 | T2 | 0.20 | 0.20 |

下列说法正确的是
| A.该反应的正反应为吸热反应 |
| B.达到平衡时,乙中CO2的体积分数比甲中的小 |
| C.T1℃时,若起始时向甲中充入0.40molNO、0.40molCO、0.40molN2和0.40molCO2,则反应达到新平衡前v(正)>v(逆) |
| D.T2℃时,若起始时向丙中充入0.06molN2和0.12molCO2,则达平衡时N2的转化率<40% |
您最近一年使用:0次
【推荐3】在一定温度下,向1L的容器中充入Fe2O3(s)和CO(g)各1mol,发生反应:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g)。CO(g)随时间的变化如下表所示,下列说法错误的是
2Fe(s)+3CO2(g)。CO(g)随时间的变化如下表所示,下列说法错误的是
 2Fe(s)+3CO2(g)。CO(g)随时间的变化如下表所示,下列说法错误的是
2Fe(s)+3CO2(g)。CO(g)随时间的变化如下表所示,下列说法错误的是| 时间/s | 0 | 10 | 20 | 30 | 40 |
| CO物质的量/mol | 1 | 0.7 | 0.5 | 0.4 | 0.4 |
| A.前10s内用CO表示该反应速率为v(CO)=0.03mol·L-1·s-1 |
| B.该反应的化学平衡常数为3.375 |
| C.40s时,升高温度再次达到平衡时,n(CO)=0.5mol,则正反应为放热反应 |
| D.40s时,向该容器中充入1molCO,再次达到平衡后,CO的转化率减小 |
您最近一年使用:0次



