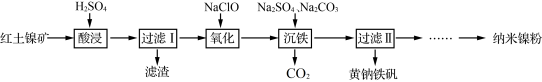
以红土镍矿(主要含有Fe2O3、FeO、NiO、SiO2等)为原料,获取净水剂黄钠铁矾[NaFe3(SO4)2(OH)6]和纳米镍粉的部分工艺流程如图:
已知:
①Fe3+在pH约为3.7时可完全转化为Fe(OH)3,Fe2+在pH约为9时可完全转化为Fe(OH)2;
②SiO2为不溶于水的酸性氧化物,常温下和硫酸不反应,但可以溶于强碱溶液。
下列说法不正确的是

已知:
①Fe3+在pH约为3.7时可完全转化为Fe(OH)3,Fe2+在pH约为9时可完全转化为Fe(OH)2;
②SiO2为不溶于水的酸性氧化物,常温下和硫酸不反应,但可以溶于强碱溶液。
下列说法不正确的是
| A.“滤渣”的主要成分是SiO2 |
| B.为提高“酸浸”速率,可将稀硫酸更换为浓硫酸 |
| C.“氧化”过程发生的离子方程式为:2H++2Fe2++ClO-=2Fe3++Cl-+H2O |
| D.“沉铁”过程中加入碳酸钠的作用是调节溶液的酸碱度,应将pH控制在3.7~9 |
更新时间:2023-01-14 18:25:40
|
相似题推荐
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】某反应的氧化剂与还原剂及部分产物如下所示: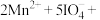 ∙∙∙∙∙∙
∙∙∙∙∙∙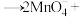 ∙∙∙∙∙∙已知该反应体系还包括
∙∙∙∙∙∙已知该反应体系还包括 、
、 与另一种含碘微粒。对于该氧化还原反应说法不正确的是
与另一种含碘微粒。对于该氧化还原反应说法不正确的是
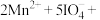 ∙∙∙∙∙∙
∙∙∙∙∙∙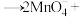 ∙∙∙∙∙∙已知该反应体系还包括
∙∙∙∙∙∙已知该反应体系还包括 、
、 与另一种含碘微粒。对于该氧化还原反应说法不正确的是
与另一种含碘微粒。对于该氧化还原反应说法不正确的是A. 是氧化剂, 是氧化剂, 是还原剂 是还原剂 | B.随着反应进行,溶液pH不断降低 |
C.体系中另一种含碘微粒为 | D.每有1个 参加反应,转移2个电子 参加反应,转移2个电子 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
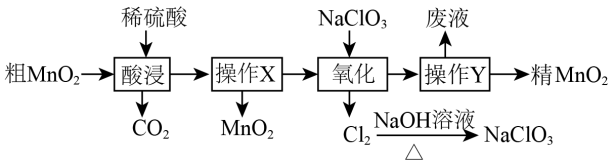
【推荐2】工业生产中高锰酸钾广泛用作氧化剂。以二氧化锰为原料制取高锰酸钾晶体的流程如下:
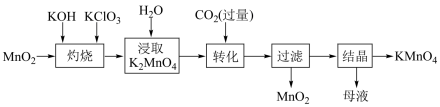
下列说法正确的是

下列说法正确的是
| A.“灼烧”时使用石英坩埚 |
| B.“转化”过程生成KMnO4和MnO2的物质的量之比为2:1 |
| C.母液中含有的溶质主要是KHCO3 |
| D.上述流程中可以循环利用的物质有3种 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐3】二氧化锰为黑色无定形粉末,难溶于水,常用于反应的氧化剂、除锈剂、催化剂。现以软锰矿(主要成分是 ,含少量
,含少量 和
和 )和闪锌矿(主要成分是ZnS,含少量FeS等)为原料制备
)和闪锌矿(主要成分是ZnS,含少量FeS等)为原料制备 和Zn,设计工艺流程如下:
和Zn,设计工艺流程如下:

已知:① 在酸性条件下比较稳定,pH高于5.5时易被
在酸性条件下比较稳定,pH高于5.5时易被 氧化。
氧化。
②室温下,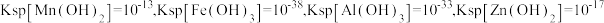 (当离子浓度≤10-5可认为沉淀完全)
(当离子浓度≤10-5可认为沉淀完全)
下列说法错误的是
 ,含少量
,含少量 和
和 )和闪锌矿(主要成分是ZnS,含少量FeS等)为原料制备
)和闪锌矿(主要成分是ZnS,含少量FeS等)为原料制备 和Zn,设计工艺流程如下:
和Zn,设计工艺流程如下:
已知:①
 在酸性条件下比较稳定,pH高于5.5时易被
在酸性条件下比较稳定,pH高于5.5时易被 氧化。
氧化。②室温下,
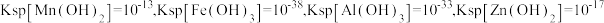 (当离子浓度≤10-5可认为沉淀完全)
(当离子浓度≤10-5可认为沉淀完全)下列说法错误的是
A.ZnS溶解离子方程式: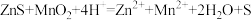 |
B.滤渣C主要成分: 和 和 |
C.若滤液B中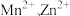 的浓度约为0.1mol/L,过程③调节pH的合理范围3≤pH<8 的浓度约为0.1mol/L,过程③调节pH的合理范围3≤pH<8 |
D.“电解”时,阳极产物制得 ,阴极制得Zn,余下电解质溶液经处理回“滤液B”中可循环利用 ,阴极制得Zn,余下电解质溶液经处理回“滤液B”中可循环利用 |
您最近一年使用:0次
【推荐1】国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)发电玻璃被誉为“挂在墙上的油田”。一种以镉废渣(含CdO及少量ZnO、CuO、MnO、FeO杂质)为原料制备镉的工艺流程如图:

已知:部分阳离子以氢氧化物形式沉淀时溶液的PH
下列说法错误的是

 |  |  | |
| 开始沉淀 | 2.7 | 6.3 | 3.8 |
| 完全沉淀 | 3.2 | 8.3 | 5.0 |
下列说法错误的是
A.调节 目的主要是除去Cu元素 目的主要是除去Cu元素 |
B.“滤渣2”主要成分为 |
C.“置换”后滤液溶质主要成分是 |
D.“熔炼”过程利用Cd与 的密度差异可以将二者分离 的密度差异可以将二者分离 |
您最近一年使用:0次
【推荐2】 (铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是
(铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备铋酸钠的流程如下。下列说法错误的是
等杂质)为原料制备铋酸钠的流程如下。下列说法错误的是
 (铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是
(铋酸钠,浅黄色不溶于冷水的固体)是分析化学常用试剂。工业上以辉铋矿粉(主要成分是 ,含少量
,含少量 、
、 、
、 等杂质)为原料制备铋酸钠的流程如下。下列说法错误的是
等杂质)为原料制备铋酸钠的流程如下。下列说法错误的是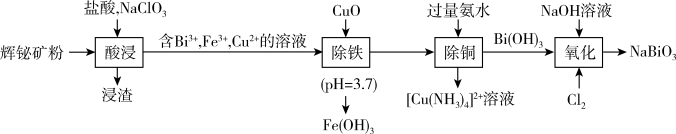
A.“酸浸”过程中,用硝酸代替“盐酸, ”更环保 ”更环保 |
B.“除铜”中涉及的离子方程式为: |
C.检验“酸浸”液中是否含有 ,可以选择“ ,可以选择“ 液”或“ 液”或“ 溶液和双氧水” 溶液和双氧水” |
D.“氧化”过程中,每消耗标准状况下5.6L ,生成70g ,生成70g |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐3】氧化铍(BeO)在航天航空等领域有着广泛的应用。一种以预处理后的硅铍矿(主要含BeO、Fe2O3、SiO2和FeO等)为原料提取BeO的流程如下图所示:

已知:Be(OH)2具有两性,在强碱性溶液中可转化为BeO 。下列说法错误的是
。下列说法错误的是

已知:Be(OH)2具有两性,在强碱性溶液中可转化为BeO
 。下列说法错误的是
。下列说法错误的是| A.“酸浸”步骤所得“滤渣①”的主要成分为Si |
| B.“滤液②”经处理后可获得副产品Na2SO4·10H2O |
C.“碱溶”时,主要反应为Be(OH)2+2OH-=BeO +2H2O +2H2O |
| D.“水解”时,适当增大溶液pH有利于提高BeO的提取率 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐1】已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在以下平衡: 。用该溶液做实验,溶液的颜色变化如图:
。用该溶液做实验,溶液的颜色变化如图:
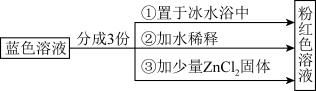
以下结论和解释正确的是( )
 。用该溶液做实验,溶液的颜色变化如图:
。用该溶液做实验,溶液的颜色变化如图:
以下结论和解释正确的是( )
| A.由实验①可推知正反应的△H>0 |
| B.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| C.由实验③可知配离子的稳定性:[ZnCl4]2->[CoCl4]2- |
| D.原蓝色溶液中加入少量NaCl固体,实验现象与实验③相同 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】下列实验现象与结论均正确,且具有因果关系的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向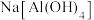 溶液中滴入 溶液中滴入 溶液 溶液 | 有白色沉淀产生 |  比 比 结合质子能力强 结合质子能力强 |
| B | 向 悬浊液中加入适量 悬浊液中加入适量 固体 固体 | 浊液变澄清 |  水解显酸性,溶解了 水解显酸性,溶解了 |
| C | 取两份新制氯水,分别滴加 溶液和淀粉 溶液和淀粉 溶液 溶液 | 前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| D | 压缩装有 气体的容器 气体的容器 | 气体颜色先变深后变浅 | 平衡向生成 的方向移动 的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
解题方法
【推荐1】铬和钒具有广泛用途。铬钒渣中铬和钒以低价态含氧酸盐形式存在,主要杂质为铁、铝、硅等的氧化物,从铬钒渣中分离提取铬和钒的一种流程如图所示。下列说法正确的是
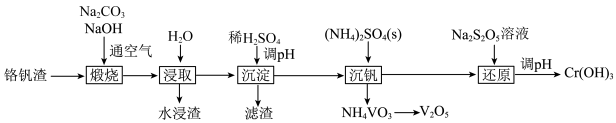
已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
② 。
。

已知:①“煅烧”时铬、铝和硅的氧化物均转化为可溶性钠盐:
②
 。
。A.“煅烧”后的含铬化合物是 |
B.“滤渣”中只含有 |
C.“沉钒”时 固体可增大 固体可增大 的浓度,有利于沉淀的生成 的浓度,有利于沉淀的生成 |
D.“还原”工序中氧化剂和还原剂的物质的量之比为 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】在微生物作用下 可以转化为
可以转化为 ,处理氨氮废水的工艺流程如下,
,处理氨氮废水的工艺流程如下,
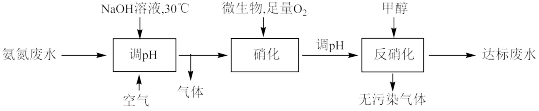
下列说法错误的是
 可以转化为
可以转化为 ,处理氨氮废水的工艺流程如下,
,处理氨氮废水的工艺流程如下,
下列说法错误的是
A.加入NaOH溶液调pH,可以实现部分 的回收 的回收 |
B.硝化过程的离子方程式为: |
| C.反硝化过程,需要继续加NaOH溶液调pH |
| D.理论上消耗1mol甲醇可以生成标准状况下35.84L气体 |
您最近一年使用:0次

 )>c(OH-)>c(H+)
)>c(OH-)>c(H+) 、Pb(OH)
、Pb(OH) 、OH-和H+
、OH-和H+