CrSi,Ge-GaAs、聚吡咯和碳化硅都是重要的半导体化合物。下列说法正确的是
| A.碳化硅属于分子晶体,其熔、沸点均大于金刚石 |
| B.Ge-GaAs中元素Ge、Ga、As的第一电离能从小到大的顺序为As<Ge<Ga |
C.聚吡咯的单体为吡咯(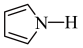 ),分子中σ键与π键的数目之比为5:2 ),分子中σ键与π键的数目之比为5:2 |
| D.基态铬与氮原子的未成对电子数之比为2:1 |
更新时间:2023-01-18 20:39:43
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】已知某元素+2价离子的核外电子排布式为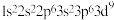 ,则该元素在元素周期表中的位置及所属分区是
,则该元素在元素周期表中的位置及所属分区是
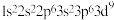 ,则该元素在元素周期表中的位置及所属分区是
,则该元素在元素周期表中的位置及所属分区是| A.第四周期Ⅷ族,p区 | B.第六周期ⅤB族,d区 |
C.第四周期ⅠB族, 区 区 | D.第四周期ⅤB族,f区 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法中正确的是
| A.价电子排布为3d104s1的元素位于第四周期第IA族,是s区元素 |
| B.SO2分子和O3分子的立体构型均为V形 |
| C.有机物CH2=CH―CH3分子中有1个π键、2个σ键 |
| D.由于氢键的存在,水分子的稳定性好,高温下也很难分解 |
您最近一年使用:0次
【推荐1】下列说法错误的是
A.CH4分子球棍模型: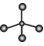 | B.基态Si原子价电子排布图: |
| C.第一电离能:N>O>C | D.石墨质软的原因是其层间作用力微弱 |
您最近一年使用:0次
【推荐2】下列说法正确的是
A.PH3的电子式为: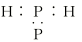 | B.CH4分子立体结构模型: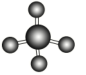 |
| C.晶体类型相同:SiO2和SO3 | D.第一电离能:S>P |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列说法中不正确的是
①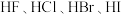 的熔、沸点依次升高
的熔、沸点依次升高
②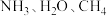 三种分子的键角依次减小
三种分子的键角依次减小
③正丁烷的沸点高于异丁烷
⑥ 和
和 的分子结构中,每个原子最外层都具有8电子稳定结构
的分子结构中,每个原子最外层都具有8电子稳定结构
①
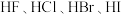 的熔、沸点依次升高
的熔、沸点依次升高②
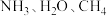 三种分子的键角依次减小
三种分子的键角依次减小③正丁烷的沸点高于异丁烷
④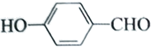 的沸点高于
的沸点高于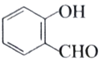 的主要原因是是因为其范德华力更大
的主要原因是是因为其范德华力更大
⑥
 和
和 的分子结构中,每个原子最外层都具有8电子稳定结构
的分子结构中,每个原子最外层都具有8电子稳定结构| A.②③④⑤⑥ | B.①②④⑤⑥ | C.①②③④⑥ | D.①②③④⑤ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列说法正确的是
| A.HX(X代表F、Cl、Br、I)中共价键的电子云是轴对称的 |
B. 中两个氢氧键(H—O)的键角大于 中两个氢氧键(H—O)的键角大于 的键角 的键角 |
C.3个B—F的键长相等,说明 分子中的四个原子在同一平面上 分子中的四个原子在同一平面上 |
D. 是非极性分子,C原子处于4个Cl原子所组成的正方形的中心 是非极性分子,C原子处于4个Cl原子所组成的正方形的中心 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列说法正确的是


| A.基态钙原子核外有2个未成对电子 |
| B.CaTiO3晶体中与每个Ti4+最邻近的O2−有12个(如图是其晶胞结构模型) |
| C.分子晶体中都存在共价键 |
| D.金属晶体的熔点都比分子晶体的熔点高 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】下列说法正确的是
| A.H2O2易分解是因为H2O2分子间作用力弱 |
| B.碘升华的过程中破坏的是共价键 |
| C.离子化合物中一定含有离子键,共价化合物中一定含有共价键 |
| D.SiO2属于原子晶体,熔化时破坏共价键和分子间作用力 |
您最近一年使用:0次

 分子通过氢键和分子间作用力有规则排列成分子晶体
分子通过氢键和分子间作用力有规则排列成分子晶体 和
和 晶体中,阴、阳离子数之比相等
晶体中,阴、阳离子数之比相等

