温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g) HCOOH(g)K=2。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g)K=2。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=_____ k正。温度为T2℃时,k正=1.9k逆,则T2℃时平衡压强____ (填“>”“<”或“=”)T1℃时平衡压强,理由是______ 。
 HCOOH(g)K=2。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g)K=2。实验测得:v正=k正c(CO2)•c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
2023高三·全国·专题练习 查看更多[1]
(已下线)专题18 速率方程及其应用-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)
更新时间:2023-02-01 19:33:18
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】可逆反应2Cl2(g)+2H2O(g) 4HCl(g)+O2(g)(△H>0),在一定条件下达到平衡后,分别采取下列措施(填“增大”、“减小”或“不变”):
4HCl(g)+O2(g)(△H>0),在一定条件下达到平衡后,分别采取下列措施(填“增大”、“减小”或“不变”):
(1)降低温度,Cl2的转化率_________ ;υ(逆)_________ ;
(2)保持容器体积不变,加入He,则HCl的物质的量_________ 。
(3)保持容器压强不变,加入He,则O2的物质的量_________ ;
 4HCl(g)+O2(g)(△H>0),在一定条件下达到平衡后,分别采取下列措施(填“增大”、“减小”或“不变”):
4HCl(g)+O2(g)(△H>0),在一定条件下达到平衡后,分别采取下列措施(填“增大”、“减小”或“不变”):(1)降低温度,Cl2的转化率
(2)保持容器体积不变,加入He,则HCl的物质的量
(3)保持容器压强不变,加入He,则O2的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 的制取及在烟气、废水处理方面的应用是当前科学研究的热点。
的制取及在烟气、废水处理方面的应用是当前科学研究的热点。
(1)工业上利用 、
、 联合去除废水中的次磷酸根(
联合去除废水中的次磷酸根(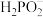 ),转化过程如图-1,过程(Ⅰ)的产物微粒有
),转化过程如图-1,过程(Ⅰ)的产物微粒有 、羟基自由基(·OH)和
、羟基自由基(·OH)和 。
。
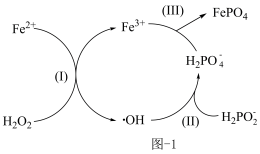
①羟基自由基(·OH)的电子式为___________ 。
②转化过程(Ⅰ)的离子反应方程式___________ 。
(2)① 在催化剂α-FeOOH的表面上会分解产生·OH,·OH可将烟气中的NO氧化而除去。当
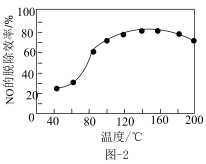
在催化剂α-FeOOH的表面上会分解产生·OH,·OH可将烟气中的NO氧化而除去。当 浓度一定时,NO的脱除效率与温度的关系如图-2。温度高于180℃,NO的脱除效率降低的可能原因是
浓度一定时,NO的脱除效率与温度的关系如图-2。温度高于180℃,NO的脱除效率降低的可能原因是___________ 。
② 可催化加快
可催化加快 氧化废水中氰根(
氧化废水中氰根( )的去除速率。其他条件相同时,总氰化物(
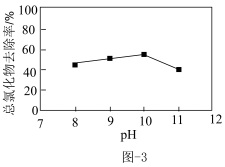
)的去除速率。其他条件相同时,总氰化物( 、HCN等)去除率随溶液初始pH变化如图-3。当溶液初始pH>10时,总氰化物去除率下降的原因可能是
、HCN等)去除率随溶液初始pH变化如图-3。当溶液初始pH>10时,总氰化物去除率下降的原因可能是___________ 。
(3)工业上用“乙基蒽醌法”和“氧阴极还原法”来制备过氧化氢。
①“乙基蒽醌法”反应过程如图-4,写出总反应的化学方程式___________ 。
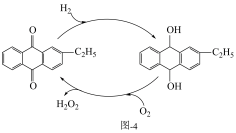
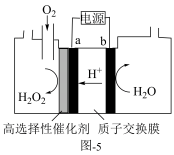
②“氧阴极还原法”的制备原理如图-5,a极的电极反应式为___________ 。
 的制取及在烟气、废水处理方面的应用是当前科学研究的热点。
的制取及在烟气、废水处理方面的应用是当前科学研究的热点。(1)工业上利用
 、
、 联合去除废水中的次磷酸根(
联合去除废水中的次磷酸根(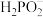 ),转化过程如图-1,过程(Ⅰ)的产物微粒有
),转化过程如图-1,过程(Ⅰ)的产物微粒有 、羟基自由基(·OH)和
、羟基自由基(·OH)和 。
。
①羟基自由基(·OH)的电子式为
②转化过程(Ⅰ)的离子反应方程式
(2)①
 在催化剂α-FeOOH的表面上会分解产生·OH,·OH可将烟气中的NO氧化而除去。当
在催化剂α-FeOOH的表面上会分解产生·OH,·OH可将烟气中的NO氧化而除去。当 浓度一定时,NO的脱除效率与温度的关系如图-2。温度高于180℃,NO的脱除效率降低的可能原因是
浓度一定时,NO的脱除效率与温度的关系如图-2。温度高于180℃,NO的脱除效率降低的可能原因是
②
 可催化加快
可催化加快 氧化废水中氰根(
氧化废水中氰根( )的去除速率。其他条件相同时,总氰化物(
)的去除速率。其他条件相同时,总氰化物( 、HCN等)去除率随溶液初始pH变化如图-3。当溶液初始pH>10时,总氰化物去除率下降的原因可能是
、HCN等)去除率随溶液初始pH变化如图-3。当溶液初始pH>10时,总氰化物去除率下降的原因可能是
(3)工业上用“乙基蒽醌法”和“氧阴极还原法”来制备过氧化氢。
①“乙基蒽醌法”反应过程如图-4,写出总反应的化学方程式

②“氧阴极还原法”的制备原理如图-5,a极的电极反应式为

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】 、CO、
、CO、 的过度排放会对环境和人体健康带来极大的危害,工业上可采取多种方法减少这些有害气体的排放。汽车尾气中的NO和CO在催化转化器中反应生成两种无毒无害的气体:
的过度排放会对环境和人体健康带来极大的危害,工业上可采取多种方法减少这些有害气体的排放。汽车尾气中的NO和CO在催化转化器中反应生成两种无毒无害的气体:
 ,可减少尾气中有害气体排放。
,可减少尾气中有害气体排放。
I.已知 是放热反应,将CO和NO按不同比例投入一密闭容器中,控制一定温度(
是放热反应,将CO和NO按不同比例投入一密闭容器中,控制一定温度( 或
或 ),发生反应达到平衡时,所得的混合气体中含
),发生反应达到平衡时,所得的混合气体中含 的体积分数随
的体积分数随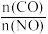 的变化曲线如图所示。
的变化曲线如图所示。

(1)图中a、b、c、d中对应NO转化率最大的是___________。
(2)
___________  (填“
(填“ ”或“
”或“ ”或“
”或“ ”)。
”)。
Ⅱ.已知 的
的 ,
, (
( 、
、 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。
(3)该可逆反应的平衡常数表达式为___________ 。
(4)若平衡后降低温度,则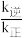
___________ (填“增大”、“不变”或“减小”)
(5)甲醇燃料可替代汽油、柴油,用于各种机动车。已知:在25℃和101kPa,1mol液态 完全燃烧生成
完全燃烧生成 和水蒸气时放出的热量为638kJ。1mol液态水转变成1mol气态水时吸收44kJ的热量。写出表示甲醇燃烧热的热化学反应方程式
和水蒸气时放出的热量为638kJ。1mol液态水转变成1mol气态水时吸收44kJ的热量。写出表示甲醇燃烧热的热化学反应方程式___________ 。
 、CO、
、CO、 的过度排放会对环境和人体健康带来极大的危害,工业上可采取多种方法减少这些有害气体的排放。汽车尾气中的NO和CO在催化转化器中反应生成两种无毒无害的气体:
的过度排放会对环境和人体健康带来极大的危害,工业上可采取多种方法减少这些有害气体的排放。汽车尾气中的NO和CO在催化转化器中反应生成两种无毒无害的气体:
 ,可减少尾气中有害气体排放。
,可减少尾气中有害气体排放。I.已知
 是放热反应,将CO和NO按不同比例投入一密闭容器中,控制一定温度(
是放热反应,将CO和NO按不同比例投入一密闭容器中,控制一定温度( 或
或 ),发生反应达到平衡时,所得的混合气体中含
),发生反应达到平衡时,所得的混合气体中含 的体积分数随
的体积分数随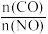 的变化曲线如图所示。
的变化曲线如图所示。
(1)图中a、b、c、d中对应NO转化率最大的是___________。
| A.a | B.b | C.c | D.d |
(2)

 (填“
(填“ ”或“
”或“ ”或“
”或“ ”)。
”)。Ⅱ.已知
 的
的 ,
, (
( 、
、 为速率常数,只与温度有关)。
为速率常数,只与温度有关)。(3)该可逆反应的平衡常数表达式为
(4)若平衡后降低温度,则
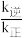
(5)甲醇燃料可替代汽油、柴油,用于各种机动车。已知:在25℃和101kPa,1mol液态
 完全燃烧生成
完全燃烧生成 和水蒸气时放出的热量为638kJ。1mol液态水转变成1mol气态水时吸收44kJ的热量。写出表示甲醇燃烧热的热化学反应方程式
和水蒸气时放出的热量为638kJ。1mol液态水转变成1mol气态水时吸收44kJ的热量。写出表示甲醇燃烧热的热化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在80℃时,将0.40 mol的N2O4气体充入1 L固定容积的密闭容器中发生反应:N2O4  2NO2(ΔH >0),每隔一段时间对容器内的物质进行测定,得到如下数据:
2NO2(ΔH >0),每隔一段时间对容器内的物质进行测定,得到如下数据:
(1)在20s — 40s之间,用N2O4表示的平均反应速率为_______________ 。
(2)在80℃时该反应的平衡常数K=________________ 。
(3)要增大该反应的平衡常数,可采取的措施有(填序号)_______________ 。
①增大N2O4的起始浓度 ②向混合气体中通入NO2
③使用高效催化剂 ④升高温度
(4)反应进行至100s后若降低温度,混合气体的颜色_________ (填“变浅”、“变深”或“不变”)。
(5)反应进行至100s后若向容器中再充入0.40 mol的N2O4气体,则达到新平衡后N2O4的转化率将________ (填“增大”、“减小”或“不变”)。
 2NO2(ΔH >0),每隔一段时间对容器内的物质进行测定,得到如下数据:
2NO2(ΔH >0),每隔一段时间对容器内的物质进行测定,得到如下数据:时间(s) | 0 | 4 | 8 | 12 | 16 | 20 |
n(N2O4)(mol) | 0.40 | a | 0.20 | c | d | e |
n(NO2)(mol) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(1)在20s — 40s之间,用N2O4表示的平均反应速率为
(2)在80℃时该反应的平衡常数K=
(3)要增大该反应的平衡常数,可采取的措施有(填序号)
①增大N2O4的起始浓度 ②向混合气体中通入NO2
③使用高效催化剂 ④升高温度
(4)反应进行至100s后若降低温度,混合气体的颜色
(5)反应进行至100s后若向容器中再充入0.40 mol的N2O4气体,则达到新平衡后N2O4的转化率将
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】对于反应2A(g) + B(g)  2C(g)在反应过程中C的质量分数WC随温度变化如图所示,试确定:
2C(g)在反应过程中C的质量分数WC随温度变化如图所示,试确定:

(1)T0对应的V正与V逆关系是V正___________ V逆(填“>”、“<”、“=”)。
(2)A、B两点正反应速率的大小关系VA___________ VB(填“>”、“<”、“=”)。
(3)温度T<T0时,Wc逐渐增大的原因是____________________ ;
(4)500℃条件下,该反应 K ="2.33" ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正)____________ v(逆)(填“>”“<”或“=”)
 2C(g)在反应过程中C的质量分数WC随温度变化如图所示,试确定:
2C(g)在反应过程中C的质量分数WC随温度变化如图所示,试确定:
(1)T0对应的V正与V逆关系是V正
(2)A、B两点正反应速率的大小关系VA
(3)温度T<T0时,Wc逐渐增大的原因是
(4)500℃条件下,该反应 K ="2.33" ,测得某时刻,A(g)、B(g)、C(g)的浓度均为0.5mol/L,则此时v(正)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g) +2H2(g) CH3OH(g) 。
CH3OH(g) 。

(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=________ mol•L-1•1min-1。
(2)乙图表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。反应的焓变是__________ (填“△H<0”或“△H>0”)反应,写出该反应的热化学方程式:__________ ;
(3)该反应平衡常数K的表达式为____ ,温度升高,平衡常数K________ (填“增大”、“不变”或“减小”)。
(4)下列措施能加快反应速率的是__________ 。
A 升高温度 B 增大容器的容积 C 再充入0.1molCO D 及时分离出CH3OH
(5)下列能说明反应达到平衡状态的是__________ 。
A 体系压强保持不变 B 混合气体总质量保持不变
C H2和CO的浓度相等 D 每消耗1 mol CO的同时生成1 mol CH3OH
 CH3OH(g) 。
CH3OH(g) 。
(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用CO浓度变化表示平均反应速率v(CO)=
(2)乙图表示该反应进行过程中能量的变化。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。反应的焓变是
(3)该反应平衡常数K的表达式为
(4)下列措施能加快反应速率的是
A 升高温度 B 增大容器的容积 C 再充入0.1molCO D 及时分离出CH3OH
(5)下列能说明反应达到平衡状态的是
A 体系压强保持不变 B 混合气体总质量保持不变
C H2和CO的浓度相等 D 每消耗1 mol CO的同时生成1 mol CH3OH
您最近一年使用:0次



