碳酸镁晶须是一种新型吸波隐形材料中的增强剂。某实验室以 含少量杂质
含少量杂质 、
、 为原料制备碳酸镁晶须
为原料制备碳酸镁晶须 的工艺流程如下:
的工艺流程如下:

已知: 、
、 、
、 生成氢氧化物沉淀时的pH
生成氢氧化物沉淀时的pH
注: 沉淀呈絮状,不易从溶液中除去。
沉淀呈絮状,不易从溶液中除去。
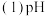 调节的范围
调节的范围___________________ ,滤渣的主要成分__________________  填化学式
填化学式 。
。
 操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法
操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法__________ 。
 水浸后溶液中
水浸后溶液中 、
、 含量的测定
含量的测定
 取水浸后溶液
取水浸后溶液 ,测得
,测得 的浓度为
的浓度为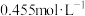 ,向其中缓缓通入氯气使
,向其中缓缓通入氯气使 恰好完全转化为
恰好完全转化为 ,测得此时溶液中
,测得此时溶液中 的浓度为
的浓度为 溶液体积变化忽略不计
溶液体积变化忽略不计 。
。
 另取水浸后溶液
另取水浸后溶液 ,向其中加入过量的
,向其中加入过量的 溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为
溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为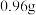 。
。
试通过计算确定水浸后溶液中 、
、 的物质的量浓度
的物质的量浓度 写出计算过程
写出计算过程 。
。________
 含少量杂质
含少量杂质 、
、 为原料制备碳酸镁晶须
为原料制备碳酸镁晶须 的工艺流程如下:
的工艺流程如下: 
已知:
 、
、 、
、 生成氢氧化物沉淀时的pH
生成氢氧化物沉淀时的pH| 物质 | 开始沉淀 | 沉淀完全 |
 |  | 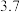 |
 | 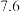 |  |
 |  | 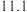 |
 沉淀呈絮状,不易从溶液中除去。
沉淀呈絮状,不易从溶液中除去。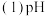 调节的范围
调节的范围 填化学式
填化学式 。
。 操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法
操作X包括过滤、洗涤、烘干,证明碳酸镁晶须已经洗涤干净的方法 水浸后溶液中
水浸后溶液中 、
、 含量的测定
含量的测定 取水浸后溶液
取水浸后溶液 ,测得
,测得 的浓度为
的浓度为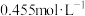 ,向其中缓缓通入氯气使
,向其中缓缓通入氯气使 恰好完全转化为
恰好完全转化为 ,测得此时溶液中
,测得此时溶液中 的浓度为
的浓度为 溶液体积变化忽略不计
溶液体积变化忽略不计 。
。 另取水浸后溶液
另取水浸后溶液 ,向其中加入过量的
,向其中加入过量的 溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为
溶液,充分反应后过滤、洗涤、灼烧,冷却后,称得固体粉末的质量为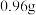 。
。 试通过计算确定水浸后溶液中
 、
、 的物质的量浓度
的物质的量浓度 写出计算过程
写出计算过程 。
。
更新时间:2019-12-26 15:41:37
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】Ⅱ以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)为原料,制备粗铅,实现铅的再生利用。其工作流程如下图所示:
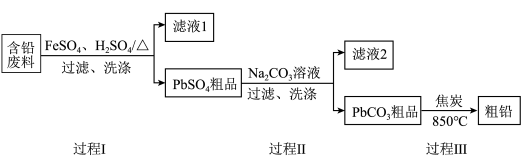
已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-l4。
(1)过程I中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是___________ 。
(2)过程I中,Fe2+催化过程可表示为:
i:2Fe2++PbO2+4H++ =2Fe3++PbSO4+2H2O
=2Fe3++PbSO4+2H2O
ii:……
①写出ii的离子方程式:___________ 。
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.___________ 。
(3)过程Ⅱ的目的是脱硫。若滤液2中c( )=1.6mol/L,c(
)=1.6mol/L,c( )=0.lmol/L,则PbCO3中
)=0.lmol/L,则PbCO3中___________ (填“是”或“否”)混有PbSO4。
(4)钠离子交换膜固相电解法是从含铅废料中提取铅的一种新工艺,其装置如图所示。将含铅废料投入阴极室,含铅废料中的PbSO4与NaOH溶液发生反应:PbSO4+3OH-=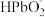 +
+ +H2O。
+H2O。
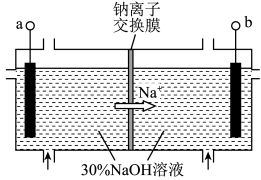
①a与外接电源的___________ 极相连。
②电解过程中,PbO2、PbO、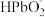 在阴极放电,其中PbO2放电生成Pb单质的电极反应式为
在阴极放电,其中PbO2放电生成Pb单质的电极反应式为___________ 。

已知:Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=3.3×10-l4。
(1)过程I中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是
(2)过程I中,Fe2+催化过程可表示为:
i:2Fe2++PbO2+4H++
 =2Fe3++PbSO4+2H2O
=2Fe3++PbSO4+2H2Oii:……
①写出ii的离子方程式:
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.
(3)过程Ⅱ的目的是脱硫。若滤液2中c(
 )=1.6mol/L,c(
)=1.6mol/L,c( )=0.lmol/L,则PbCO3中
)=0.lmol/L,则PbCO3中(4)钠离子交换膜固相电解法是从含铅废料中提取铅的一种新工艺,其装置如图所示。将含铅废料投入阴极室,含铅废料中的PbSO4与NaOH溶液发生反应:PbSO4+3OH-=
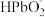 +
+ +H2O。
+H2O。
①a与外接电源的
②电解过程中,PbO2、PbO、
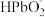 在阴极放电,其中PbO2放电生成Pb单质的电极反应式为
在阴极放电,其中PbO2放电生成Pb单质的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】氧化镁是优质的耐高温材料。某兴趣小组利用菱镁矿(主要成分为MgCO3,还含有少量SiO2、Al2O3等杂质)设计制备氧化镁的流程如图:

(1)步骤(Ⅰ)中分离操作的名称是_______ 。
(2)步骤(I)分离出的滤渣中主要含有_______ ,它属于_______ (填“酸性”或“碱性”)氧化物。
(3)写出步骤(II)生成Mg(OH)2的离子方程式:_______ 。

(1)步骤(Ⅰ)中分离操作的名称是
(2)步骤(I)分离出的滤渣中主要含有
(3)写出步骤(II)生成Mg(OH)2的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】钛(Ti)被称为继铁、铝之后的第三金属,钛白(TiO2)是目前最好的白色颜料。制备TiO2和Ti的原料是钛铁矿,我国的钛铁储量居世界首位。用含Fe2O3的钛铁矿(主要成分为FeTiO3)制备TiO2流程如下:
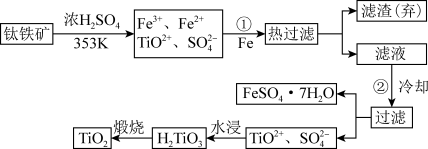
已知反应TiO2++2H2O H2TiO3+2H+ ΔH<0
H2TiO3+2H+ ΔH<0
(1)步骤①加Fe的目的是___________________________________ (用离子方程式表达);步骤②冷却的目的是_________________________________________________________ 。
(2)上述制备TiO2的过程中,可以利用的副产物是__________________ ;考虑成本和废物综合利用因素,废液中应加入______ 处理;在“水浸”步骤中加入大量的水即可获得H2TiO3沉淀,请用相关化学原理解释___________________________________________________ 。
(3)由金红石(TiO2)制取单质钛(Ti),涉及到的步骤为
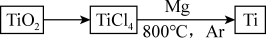
反应TiCl4+2Mg===2MgCl2+Ti在Ar气氛中进行的理由是___________________________ 。

已知反应TiO2++2H2O
 H2TiO3+2H+ ΔH<0
H2TiO3+2H+ ΔH<0(1)步骤①加Fe的目的是
(2)上述制备TiO2的过程中,可以利用的副产物是
(3)由金红石(TiO2)制取单质钛(Ti),涉及到的步骤为
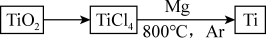
反应TiCl4+2Mg===2MgCl2+Ti在Ar气氛中进行的理由是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验室把学生做完实验后的废液(含氯化钠、氯化铁、氯化铜等)进行集中处理,过程如下:
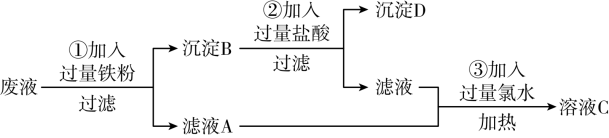
(1)沉淀D的化学式为_________________ 。
(2)反应③中Cl2属于_______________ (填“氧化剂”或“还原剂”)。
(3)写出①反应中的离子方程式________________________ ,___________________________ 。
(4)溶液C中的溶质是_______________ (提示:加热后,溶液中没有了HCl和Cl2),若要进一步进行分离,方法是____________________ 。
(5)萃取实验所用到的玻璃仪器:_______________ 、____________________ 。

(1)沉淀D的化学式为
(2)反应③中Cl2属于
(3)写出①反应中的离子方程式
(4)溶液C中的溶质是
(5)萃取实验所用到的玻璃仪器:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】工业上用含有 和
和 的废水回收铬.其工艺流程如图:
的废水回收铬.其工艺流程如图:
已知: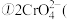 黄色
黄色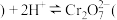 橙色
橙色 ;
;
 常温下,
常温下, ,
,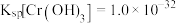 ;
;
 当离子浓度小于
当离子浓度小于
 时,认为沉淀完全.
时,认为沉淀完全.
 酸化后的溶液A显
酸化后的溶液A显 ______ 色.
 下列选项中,能说明反应
下列选项中,能说明反应 黄色
黄色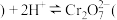 橙色
橙色 达到平衡状态的是
达到平衡状态的是 ______  填选项字母
填选项字母 ;
;
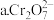 和
和 的浓度相同
的浓度相同 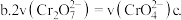 溶液的颜色不变
溶液的颜色不变 溶液的pH不变
溶液的pH不变
 为防止
为防止 溶液变质,在保存时需加入的试剂为
溶液变质,在保存时需加入的试剂为 ______  填试剂名称
填试剂名称 .
.
 过滤操作中需要用到的玻璃仪器有
过滤操作中需要用到的玻璃仪器有 ______ .
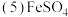 溶液与溶液A发生反应的离子方程式为
溶液与溶液A发生反应的离子方程式为 ______ .
 沉淀C的化学式为
沉淀C的化学式为 ______ ,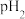 的范围为
的范围为 ______ .
 和
和 的废水回收铬.其工艺流程如图:
的废水回收铬.其工艺流程如图: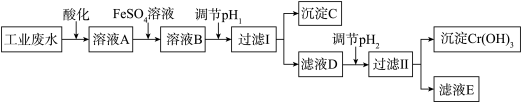
已知:
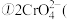 黄色
黄色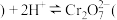 橙色
橙色 ;
;  常温下,
常温下, ,
,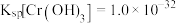 ;
;  当离子浓度小于
当离子浓度小于
 时,认为沉淀完全.
时,认为沉淀完全.  酸化后的溶液A显
酸化后的溶液A显  下列选项中,能说明反应
下列选项中,能说明反应 黄色
黄色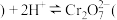 橙色
橙色 达到平衡状态的是
达到平衡状态的是  填选项字母
填选项字母 ;
; 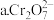 和
和 的浓度相同
的浓度相同 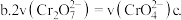 溶液的颜色不变
溶液的颜色不变 溶液的pH不变
溶液的pH不变  为防止
为防止 溶液变质,在保存时需加入的试剂为
溶液变质,在保存时需加入的试剂为  填试剂名称
填试剂名称 .
. 过滤操作中需要用到的玻璃仪器有
过滤操作中需要用到的玻璃仪器有 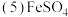 溶液与溶液A发生反应的离子方程式为
溶液与溶液A发生反应的离子方程式为  沉淀C的化学式为
沉淀C的化学式为 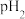 的范围为
的范围为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】高铁酸钾(K2FeO4)具有强氧化性,可作为水处理剂和高容量电池材料。工业上生产高铁酸钾的工艺流程如下:
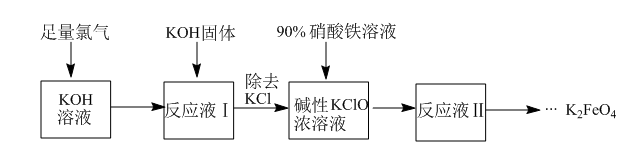
已知K2FeO4具有下列性质:①可溶于水,微溶于KOH溶液,难溶于异丙醇;②在0℃-5℃,强碱性溶液中比较稳定;③在Fe3+和Fe(OH)3催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。请完成下列填空:
请补充完整由“反应液Ⅱ”得到K2FeO4晶体的实验步骤。(可选用的试剂:NaOH溶液、KOH溶液、蒸馏水和异丙醇)
① 向反应液Ⅱ中加入饱和___________ ,在冰水浴中静置结晶后过滤,得K2FeO4粗产品;
② 将K2FeO4粗产品溶解在___________ 中,再次在冰水浴中静置结晶后过滤,得到较纯净的K2FeO4;
③ 将K2FeO4晶体再用少量___________ 洗涤,低温真空干燥,得到高铁酸钾成品。

已知K2FeO4具有下列性质:①可溶于水,微溶于KOH溶液,难溶于异丙醇;②在0℃-5℃,强碱性溶液中比较稳定;③在Fe3+和Fe(OH)3催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2。请完成下列填空:
请补充完整由“反应液Ⅱ”得到K2FeO4晶体的实验步骤。(可选用的试剂:NaOH溶液、KOH溶液、蒸馏水和异丙醇)
① 向反应液Ⅱ中加入饱和
② 将K2FeO4粗产品溶解在
③ 将K2FeO4晶体再用少量
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验题
化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙,氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生.
I.摩擦剂中氢氧化铝的定性检验:取适量牙膏样品,加水充足搅拌,过滤.
(1)往滤渣中加入过量NaOH溶液,过滤. 氢氧化铝与NaOH溶液反应的离子方程式是_______ .
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸.这一过程发生反应的化学方程式依次为:__________________________________ ,__________________________________ .
Ⅱ.牙膏样品中碳酸钙的定量测定:利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
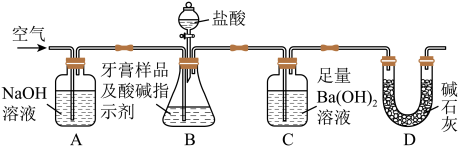
依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气.其作用除了可搅拌B,C中的反应物外,还有:_________ .
(4)C中反应生成BaCO3的离子方程式是___________________________________ .
(5)下列各项措施中,不能提高测定准确度的是( ) (填标号).
A.在加入盐酸之前,应排净装置内的CO2气体
B.滴加盐酸不宜过快
C.在A~B之间增添盛有浓硫酸的洗气装置
D.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g.则样品中碳酸钙的质量分数为________ .
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是_________________ .
(8)装置中U形管D中的碱石灰的作用是_____________________________ .
化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙,氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生.
I.摩擦剂中氢氧化铝的定性检验:取适量牙膏样品,加水充足搅拌,过滤.
(1)往滤渣中加入过量NaOH溶液,过滤. 氢氧化铝与NaOH溶液反应的离子方程式是
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸.这一过程发生反应的化学方程式依次为:
Ⅱ.牙膏样品中碳酸钙的定量测定:利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.

依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气.其作用除了可搅拌B,C中的反应物外,还有:
(4)C中反应生成BaCO3的离子方程式是
(5)下列各项措施中,不能提高测定准确度的是
A.在加入盐酸之前,应排净装置内的CO2气体
B.滴加盐酸不宜过快
C.在A~B之间增添盛有浓硫酸的洗气装置
D.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g.则样品中碳酸钙的质量分数为
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是
(8)装置中U形管D中的碱石灰的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】青蒿素是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为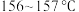 ,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为
,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为 。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法.乙醚浸取法的主要工艺为
。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法.乙醚浸取法的主要工艺为

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是_______________ 。
(2)操作I需要的玻璃仪器主要有:烧杯、玻璃棒、_______________ ,操作Ⅱ的名称是_______________ 。
(3)操作III的主要过程可能是_______________ (填字母)。
A.加水溶解,蒸发浓缩、冷却结晶 B.加 的乙醇,浓缩、结晶、过滤
的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将 青蒿素样品放在硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
青蒿素样品放在硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。

①装置E中盛放的物质是_______________ (填字母,下同),装置F中盛放的物质是_______________ 。
a.浓硫酸 b.无水硫酸铜 c.无水 d.碱石灰
d.碱石灰
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是_______________ 。
③用合理改进后的装置进行实验,称得:
则测得青蒿素的最简式是_______________ 。
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有 、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_______________(填字母)具有相同的性质。
、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_______________(填字母)具有相同的性质。
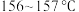 ,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为
,热稳定性差,青蒿素是高效的抗疟药。已知:乙醚沸点为 。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法.乙醚浸取法的主要工艺为
。从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法.乙醚浸取法的主要工艺为
请回答下列问题:
(1)对青蒿进行干燥破碎的目的是
(2)操作I需要的玻璃仪器主要有:烧杯、玻璃棒、
(3)操作III的主要过程可能是
A.加水溶解,蒸发浓缩、冷却结晶 B.加
 的乙醇,浓缩、结晶、过滤
的乙醇,浓缩、结晶、过滤C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将
 青蒿素样品放在硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
青蒿素样品放在硬质玻璃管中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
①装置E中盛放的物质是
a.浓硫酸 b.无水硫酸铜 c.无水
 d.碱石灰
d.碱石灰②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是
③用合理改进后的装置进行实验,称得:
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有
 、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_______________(填字母)具有相同的性质。
、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_______________(填字母)具有相同的性质。| A.乙醇 | B.乙酸 | C.乙酸乙酯 | D.葡萄糖 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO。已知:氯气和碱反应在室温下生成氯化物和次氯酸盐,温度升高时主要产物是氯化物和氯酸盐,氯气和碱的反应释放热量。
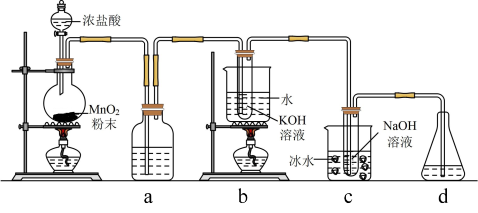
回答下列问题:
(1)盛放浓盐酸的仪器名称是_________ ,a中的试剂为_________ 。
(2)b中化学反应的离子方程式是_________ ,c采用冰水浴冷却的目的是_________ 。
(3)d的作用是_________ ,下列可选用的最佳试剂为_________ (填标号)。
A.KI溶液 B.饱和食盐水 C.Ca(OH)2溶液 D.浓H2SO4
(4)反应结束后,取出b中试管,经冷却结晶、_________ 、_________ 、干燥,得到KClO3晶体。(填写操作名称)
(5)称取上述制备出的KClO3粗产品3.0g并加入适量MnO2再称量后加热至质量不再改变(假设杂质受热不分解),测得固体总质量减轻0.96g,则制备的粗产品中氯酸钾纯度为_________ 。(保留到小数点后1位)
(6)反应结束后,c试管中溶液具有消毒、漂白作用,向c中通入或加入下列物质,能使其消毒、漂白效果明显增强的有_________。

回答下列问题:
(1)盛放浓盐酸的仪器名称是
(2)b中化学反应的离子方程式是
(3)d的作用是
A.KI溶液 B.饱和食盐水 C.Ca(OH)2溶液 D.浓H2SO4
(4)反应结束后,取出b中试管,经冷却结晶、
(5)称取上述制备出的KClO3粗产品3.0g并加入适量MnO2再称量后加热至质量不再改变(假设杂质受热不分解),测得固体总质量减轻0.96g,则制备的粗产品中氯酸钾纯度为
(6)反应结束后,c试管中溶液具有消毒、漂白作用,向c中通入或加入下列物质,能使其消毒、漂白效果明显增强的有_________。
| A.NH3 | B.CO2 | C.饱和食盐水 | D.NaOH溶液 |
您最近一年使用:0次



