碳元素在自然界中分布很广,是存在形式最复杂的元素。实验室可用邻二氮菲(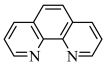 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
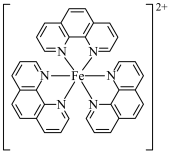
回答下列问题:
(1)基态 原子的价电子占据的能量最高的能级是
原子的价电子占据的能量最高的能级是_______ ,基态 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有_______ 种, 的价电子轨道表达式为
的价电子轨道表达式为_______ 。
(2)红色配离子的中心原子的配位数为_______ ;
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为_______ 、_______ ;
(4)红色配合物中H、C、N、Fe四种元素的电负性从大到小的顺序为_______ ;
(5)红色配离子中不存在的作用力有_______ ;
A. 键 B.
键 B. 键 C.离子键 D氢键 E.配位键
键 C.离子键 D氢键 E.配位键
(6)临床建议服用维生素 促进“亚铁”的吸收,避免生成
促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是_______ ;
(7)汽车安全气囊产生气体的功臣是叠氮化钠 ,
, 的空间构型为
的空间构型为_______ 。
 )与
)与 形成的红色配合物(如下图)测定铁的含量。
形成的红色配合物(如下图)测定铁的含量。
回答下列问题:
(1)基态
 原子的价电子占据的能量最高的能级是
原子的价电子占据的能量最高的能级是 原子核外电子的空间运动状态有
原子核外电子的空间运动状态有 的价电子轨道表达式为
的价电子轨道表达式为(2)红色配离子的中心原子的配位数为
(3)邻二氮菲分子中C、N两种元素原子的杂化方式分别为
(4)红色配合物中H、C、N、Fe四种元素的电负性从大到小的顺序为
(5)红色配离子中不存在的作用力有
A.
 键 B.
键 B. 键 C.离子键 D氢键 E.配位键
键 C.离子键 D氢键 E.配位键(6)临床建议服用维生素
 促进“亚铁”的吸收,避免生成
促进“亚铁”的吸收,避免生成 ,从结构角度来看,
,从结构角度来看, 易被氧化成
易被氧化成 的原因是
的原因是(7)汽车安全气囊产生气体的功臣是叠氮化钠
 ,
, 的空间构型为
的空间构型为
更新时间:2023-04-01 09:04:21
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】W、R、X,Y、Z是原子序数依次增大的前四周期元素,其元素性质或原子结构如下表所示:
回答下列问题:
(1)W的基态原子有_______ 种不同运动状态的电子,Z的价层电子排布图为_______ 。
(2)W、R、X的简单氢化物分子中,键角由大到小的顺序是_______ (用对应的分子式表示),原因是_______ 。
(3)已知:羧酸的酸性可用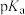 (
( )的大小来衡量,
)的大小来衡量,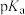 越小,酸性越强。
越小,酸性越强。
由表可见,酸性:三氯乙酸_______ 三氟乙酸(填“大于”“小于”或“等于”),从键的极性角度解释原因:_______ 。
| 元素 | 元素性质或原子结构 |
| W | 基态原子L能层所有能级上电子数相同 |
| R | 第二周期元素基态原子中未成对电子数最多 |
| X | 基态原子核外s能级上电子总数与p能级上电子总数相等,且第一电离能低于同周期相邻元素 |
| Y | 最外层电子数是次外层电子数的一半 |
| Z | 最外层只有1个电子,其他内层各能级所有轨道里的电子均成对 |
(1)W的基态原子有
(2)W、R、X的简单氢化物分子中,键角由大到小的顺序是
(3)已知:羧酸的酸性可用
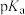 (
( )的大小来衡量,
)的大小来衡量,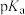 越小,酸性越强。
越小,酸性越强。| 羧酸 | 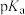 |
三氯乙酸(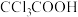 ) ) | 0.65 |
三氟乙酸( ) ) | 0.23 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为____ nm(填标号)。
A 404.4 B 553.5 C 589.2 D 670.8 E 766.5
(2)基态K原子中,核外电子占据最高能层的符号是____ ,占据该能层电子的电子云轮廓图形状为____ 。
(3)X射线衍射测定等发现,I3AsF6中存在I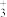 离子。I
离子。I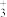 离子的几何构型为
离子的几何构型为____ ,中心原子的杂化形式为____ 。
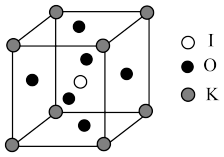
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为____ nm;与K紧邻的O个数为____ 。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于____ 位置,O处于____ 位置。
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为
A 404.4 B 553.5 C 589.2 D 670.8 E 766.5
(2)基态K原子中,核外电子占据最高能层的符号是
(3)X射线衍射测定等发现,I3AsF6中存在I
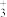 离子。I
离子。I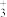 离子的几何构型为
离子的几何构型为
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有六种元素,其中A、B、C、D为短周期主族元素E、F为第四周期元素,它们的原子序数依次增大。
某同学根据上述信息,完成下列各题。
(1)画出A基态原子的核外电子轨道表示式:______ 。
(2)B基态原子的核外电子轨道表示式为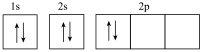 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了______ 。
(3)D基态原子中能量最高的电子,其电子云在空间有______ 个伸展方向,呈形______ 形。
(4)写出C原子的电子排布式:______ ;写出E原子的简化电子排布式:______ 。
(5)写出F元素原子的价层电子排布式:______ 。
| A元素原子的核外p电子数比s电子数少3 |
| B元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| C元素基态原子p轨道有3个未成对电子 |
| D原子核外所有p轨道全充满或半充满 |
| E在该周期中未成对电子数最多 |
F能形成红色(或砖红色)的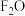 和黑色的FO两种氧化物 和黑色的FO两种氧化物 |
(1)画出A基态原子的核外电子轨道表示式:
(2)B基态原子的核外电子轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(3)D基态原子中能量最高的电子,其电子云在空间有
(4)写出C原子的电子排布式:
(5)写出F元素原子的价层电子排布式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E代表原子序数依次增大的前四周期元素,其中A和C为同一主族,C常用于制作半导体器件和集成电路,B的简单氢化物的水溶液呈碱性,E元素的正三价离子的3d亚层为半充满,D被称为“未来金属”,其重量轻、强度高、耐腐蚀,其在周期表中位于第4周期、第ⅣB族。
(1)A、B、C三种元素的第一电离能由小到大的顺序为______________________ ,电负性由小到大的顺序为____________________ 。
(2)B的简单氢化物易液化的原因是_______________ ;BH4+中B原子的杂化方式为___________ ,空间构型为__________________ 。
(3)E元素基态原子的电子排布式为____________________________________ 。
(4)B和C形成的化合物常用作高温耐火材料,化学性质稳定,据此推测它应属于__________________ 晶体。
(5)D有多种氧化物,其中一种氧化物的晶胞结构如图1所示,则该晶体中D的配位数为__________________ ;图2为E的一种面心立方晶胞结构,若晶胞的边长为acm,NA表示阿伏伽德罗常数的值,则E的密度为__________________ g·cm-3(用含a和NA的代数式表示)。

(1)A、B、C三种元素的第一电离能由小到大的顺序为
(2)B的简单氢化物易液化的原因是
(3)E元素基态原子的电子排布式为
(4)B和C形成的化合物常用作高温耐火材料,化学性质稳定,据此推测它应属于
(5)D有多种氧化物,其中一种氧化物的晶胞结构如图1所示,则该晶体中D的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)镍铬钢抗腐蚀性能强, 基态的核外电子排布式为
基态的核外电子排布式为_______ ,铬元素在周期表中_______ 区;根据价层电子对互斥理论,预测 的空间构型为
的空间构型为_______ 形。
(2) 与
与 甲基咪
甲基咪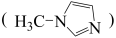 反应可以得到
反应可以得到 ,其结构如图所示:
,其结构如图所示:
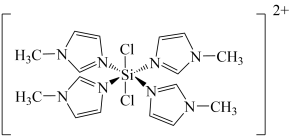
 甲基咪唑分子中碳原子的杂化轨道类型为
甲基咪唑分子中碳原子的杂化轨道类型为_______ ,H、C、N的电负性由大到小的顺序为_______ ,1个 中含有
中含有_______ 个 键。
键。
(3) 晶胞结构如图所示:
晶胞结构如图所示:

①位于大立方体体心“▽”代表_______ (填离子符号);
② 做面心立方最密堆积形成正四面体和正八面体两种空隙,正四面体空隙数和
做面心立方最密堆积形成正四面体和正八面体两种空隙,正四面体空隙数和 数之比为
数之比为_______ ,其中_______ %正八面体空隙被 填充;
填充;
③晶胞边长为x nm,则相距最近的两个 之间距离为
之间距离为_______ nm;设 的相对分子质量为M,阿伏加德罗常数的值为
的相对分子质量为M,阿伏加德罗常数的值为 ,则该晶体密度的计算表达式为
,则该晶体密度的计算表达式为_______  。
。
(1)镍铬钢抗腐蚀性能强,
 基态的核外电子排布式为
基态的核外电子排布式为 的空间构型为
的空间构型为(2)
 与
与 甲基咪
甲基咪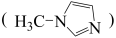 反应可以得到
反应可以得到 ,其结构如图所示:
,其结构如图所示:
 甲基咪唑分子中碳原子的杂化轨道类型为
甲基咪唑分子中碳原子的杂化轨道类型为 中含有
中含有 键。
键。(3)
 晶胞结构如图所示:
晶胞结构如图所示:
①位于大立方体体心“▽”代表
②
 做面心立方最密堆积形成正四面体和正八面体两种空隙,正四面体空隙数和
做面心立方最密堆积形成正四面体和正八面体两种空隙,正四面体空隙数和 数之比为
数之比为 填充;
填充;③晶胞边长为x nm,则相距最近的两个
 之间距离为
之间距离为 的相对分子质量为M,阿伏加德罗常数的值为
的相对分子质量为M,阿伏加德罗常数的值为 ,则该晶体密度的计算表达式为
,则该晶体密度的计算表达式为 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】阅读资料,获取信息,回答问题。
(A) A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C的原子序数为24;D2+的电子排布式和Ar相同。
(B)两元素电负性差值大于1. 7,原子间一般形成离子键;小于1. 7,原子间一般形成共价键。
(C)下列是周期表中部分元素的电负性x和第一电离能I1 (KJ·mol-1):

(1).A原子的轨道表示式为_______ ,B原子的价电子排布式为________ ,C原子的电
子排布式为___________ ,D在周期表中的位置为________ 周期________ 族。
(2).电负性最小的元素位于______ 族,第一电离能最大的元素是(填元素符号)______ ;
锂元素的电负性取值范围为____ <x(Li)<_____ ;A12S3属______ 化合物
(3)标出化合物OF2、 LiAlH4中各元素的化合价(写在元素符号上)____ 、____ 。
(A) A、 B、C、D为四种元素,A原子的1S轨道为半充满;在元素周期表中,B的电负性最大;C的原子序数为24;D2+的电子排布式和Ar相同。
(B)两元素电负性差值大于1. 7,原子间一般形成离子键;小于1. 7,原子间一般形成共价键。
(C)下列是周期表中部分元素的电负性x和第一电离能I1 (KJ·mol-1):

(1).A原子的轨道表示式为
子排布式为
(2).电负性最小的元素位于
锂元素的电负性取值范围为
(3)标出化合物OF2、 LiAlH4中各元素的化合价(写在元素符号上)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】研究氮及其化合物的性质在社会发展过程中具有极为重要的意义。
(1)N的核外电子排布图为__ ;C、N、O元素的第一电离能由大到小的顺序为___ (用元素符号表示),O的第二电离能大于N的第二电离能的原因是O的核电荷数较大,且__ 。
(2)影响NH3、NH4Cl的熔点的作用力分别是___ 、__ ;N 的空间构型为
的空间构型为__ 。
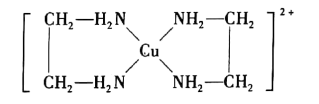
(3)一个乙二胺(H2N—CH2—CH2—NH2)分子中共有___ 个σ键,其中N原子的杂化方式为__ ,它能与Cu2+形成如图所示的配离子,请用箭头在图中标出配位键:___ 。
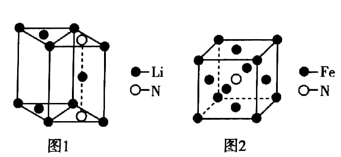
(4)金属氮化物在工业上有着很重要的应用,如氮化锂是一种新型无机贮氢材料,其晶胞结构如图1所示,该晶体的化学式为___ ;又如氮化铁的晶胞结构如图2所示,若氮化铁晶体的密度为dg•cm-3,阿伏加德罗常数的值为NA,则该氮化铁的晶胞边长为__ pm(用含d、NA的代数式表示)。
(1)N的核外电子排布图为
(2)影响NH3、NH4Cl的熔点的作用力分别是
 的空间构型为
的空间构型为(3)一个乙二胺(H2N—CH2—CH2—NH2)分子中共有

(4)金属氮化物在工业上有着很重要的应用,如氮化锂是一种新型无机贮氢材料,其晶胞结构如图1所示,该晶体的化学式为

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】元素X的基态原子中的电子共有7个能级,且最外层电子数为1,X原子的内层轨道全部排满电子,Y原子是最轻的原子,人们曾预言它可能是所有元素之母。
(1)X基态原子的电子排布式为___ 。
(2)C、H、O、N四种原子的电负性由大到小的顺序为___ 。
(3)Y负离子基态电子排布式为___ 。
(4)下列变化:H-(g)=H(g)+e-吸收的能量为73kJ/mol,H(g)=H+(g)+e-吸收的能量为1311kJ/mol,则氢负离子的第一电离能为__ 。
(5)水溶液中有H3O+、H5O 、H9O
、H9O 等微粒的形式。H3O+中,中心原子的杂化类型是
等微粒的形式。H3O+中,中心原子的杂化类型是__ ,请画出H5O 的结构式:
的结构式:__ 。
(1)X基态原子的电子排布式为
(2)C、H、O、N四种原子的电负性由大到小的顺序为
(3)Y负离子基态电子排布式为
(4)下列变化:H-(g)=H(g)+e-吸收的能量为73kJ/mol,H(g)=H+(g)+e-吸收的能量为1311kJ/mol,则氢负离子的第一电离能为
(5)水溶液中有H3O+、H5O
 、H9O
、H9O 等微粒的形式。H3O+中,中心原子的杂化类型是
等微粒的形式。H3O+中,中心原子的杂化类型是 的结构式:
的结构式:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】硼是新型无机材料中的明星元素。

(1)磷化硼是一种耐磨涂料,可由三溴化硼和三溴化磷高温下在氢气中反应合成,其化学方程式为______ ,图为磷化硼晶体结构中最小的重复单元,磷化硼的晶体类型是 ______ ,一个晶胞中含 ______ 个P原子,每个B或P均形成4个共价键,其中有一个配位键,提供空轨道的是 ______ 原子。
(2)氮化硼是一种重要的功能陶瓷材料,其结构与磷化硼相似,B和N相比,电负性较大的是______ (填元素符号),其基态原子的电子排布式为 ______ ,氮化硼中B元素的化合价为 ______ 。
(3)环硼氮烷与苯是等电子体,其一氯代物有两种结构、二氯代物有四种结构,写出环硼氮烷分子结构式______ 。
(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料。在BF3分子中,F-B-F的键角是______ 度,B原子采用 ______ 杂化; BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为 ______ 。

(1)磷化硼是一种耐磨涂料,可由三溴化硼和三溴化磷高温下在氢气中反应合成,其化学方程式为
(2)氮化硼是一种重要的功能陶瓷材料,其结构与磷化硼相似,B和N相比,电负性较大的是
(3)环硼氮烷与苯是等电子体,其一氯代物有两种结构、二氯代物有四种结构,写出环硼氮烷分子结构式
(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料。在BF3分子中,F-B-F的键角是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产生活中有着广泛的成用。
(1)基态Co3+原子的价电子排布式为_______ ,Co3+核外3d能级上有_______ 对成对电子。
(2)Co3+的一种配离子[Co(N3(NH3)5]2+产中,Co3+的配位数是_______ ,离子中所含δ键的数目为_______ ,配位体N3+中心原子杂化类型为_______ 。
(3)Co2+在水溶液中以[Co(H20)6]2+存在。向含Co2+的溶液中加入过量水可生成更稳定的[Co(NH3)6]2+,其原因是_______ 。
(4)某蓝色晶体中,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的某恰当位置上。据此可知该晶体的化学式为_______ ,立方体中Fe2+间连接起来形成的空间构型是_______ 。
(5)NiO的晶体结构如图中所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为_______ 。
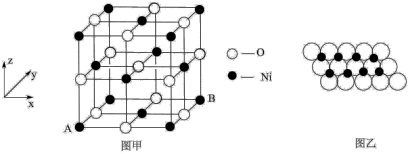
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+产填充其中(如图乙),已知O2-的半径为apm,每平方米面积上分散的该晶体的质量为_______ g(用含a、NA的代数式表示)。
(1)基态Co3+原子的价电子排布式为
(2)Co3+的一种配离子[Co(N3(NH3)5]2+产中,Co3+的配位数是
(3)Co2+在水溶液中以[Co(H20)6]2+存在。向含Co2+的溶液中加入过量水可生成更稳定的[Co(NH3)6]2+,其原因是
(4)某蓝色晶体中,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的某恰当位置上。据此可知该晶体的化学式为
(5)NiO的晶体结构如图中所示,其中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为

(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+产填充其中(如图乙),已知O2-的半径为apm,每平方米面积上分散的该晶体的质量为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D、E、F为原子序数依次增大的前四周期元素,A元素原子最外层电子数是其内层电子数的2.5倍,B元素是地壳中含量最高的元素,C元素的最高化合价和最低化合价的代数和等于0,D元素的单质可用于自来水消毒杀菌,E元素位于周期表的ⅥB族,F的基态原子中有4个未成对电子。
(1)A元素单质的结构式为___________ ;B元素原子中的未成对电子数为_______________________ 。
(2)在A的氢化物A2H4分子中,A原子轨道的杂化类型是______ ;A与B形成的AB2-的空间构型为___________________________ 。
(3)A、B、C三种元素的第一电离能从大到小的顺序为_______________________ (用元素符号表示)。
(4)基态F3+的核外电子排布式是_____________________ ;F3+与SCN-络合得到多种配合物,其中配位数为5的配合物的化学式为__________________ ;化合物FD3是棕色固体、易潮解,100℃左右时升华,FD3的晶体类型是__________________________ 。
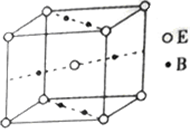
(5)元素B与E形成的一种化合物广泛应用于录音磁带上,其晶胞如图所示。该化合物的化学式为__________________________ 。
(1)A元素单质的结构式为
(2)在A的氢化物A2H4分子中,A原子轨道的杂化类型是
(3)A、B、C三种元素的第一电离能从大到小的顺序为
(4)基态F3+的核外电子排布式是
(5)元素B与E形成的一种化合物广泛应用于录音磁带上,其晶胞如图所示。该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】按要求填空
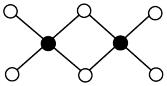
(1)在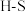 和H-Cl两种共价键中,键的极性较强的是
和H-Cl两种共价键中,键的极性较强的是___________ ,键长较长的是___________ 。
(2)氯化铝通常以双聚物存在,其结构如图所示。 该分子中含
该分子中含___________ 个配位键,该分子___________ (填“是”或“不是”)平面型分子。
(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色[Cu(NH3)4]SO4•H2O沉淀。
①写出上述实验前两步反应的离子方程式___________ ,___________ 。
②与NH3分子互为等电子体的一种阳离子是___________ 。
③在晶体[Cu(NH3)4]SO4•H2O中,中心原子是sp3杂化的原子有___________ (写元素符号),配离子(内界)中存在的化学键有___________ 。
a、离子键b、共价键c、配位键d、氢键e、范德华力
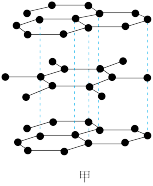
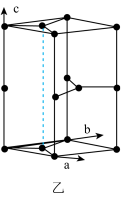
(4)图甲所示石墨晶体按ABAB方式堆积而成,图乙为石墨的六方晶胞。每个晶胞中的碳原子个数为___________ 。

(1)在
 和H-Cl两种共价键中,键的极性较强的是
和H-Cl两种共价键中,键的极性较强的是(2)氯化铝通常以双聚物存在,其结构如图所示。
 该分子中含
该分子中含(3)向硫酸铜溶液中滴加氨水会生成蓝色沉淀,再滴加氨水到沉淀刚好全部溶解可得到深蓝色溶液,继续向其中加入极性较小的乙醇可以生成深蓝色[Cu(NH3)4]SO4•H2O沉淀。
①写出上述实验前两步反应的离子方程式
②与NH3分子互为等电子体的一种阳离子是
③在晶体[Cu(NH3)4]SO4•H2O中,中心原子是sp3杂化的原子有
a、离子键b、共价键c、配位键d、氢键e、范德华力
(4)图甲所示石墨晶体按ABAB方式堆积而成,图乙为石墨的六方晶胞。每个晶胞中的碳原子个数为


您最近一年使用:0次



