用CO2和天然气可以制备CO和H2:CO2(g)+CH4(g)  2CO(g)+2H2(g)。密闭容器中浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下反应,测得CH4的平衡转化率[α(CH4)]与温度及压强的关系如图所示,则压强p1
2CO(g)+2H2(g)。密闭容器中浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下反应,测得CH4的平衡转化率[α(CH4)]与温度及压强的关系如图所示,则压强p1___________ p2(填“>”或“<”)。若p2=3 MPa,则T ℃时该反应的平衡常数Kp=___________ (MPa)2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
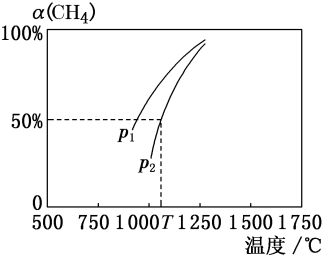
 2CO(g)+2H2(g)。密闭容器中浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下反应,测得CH4的平衡转化率[α(CH4)]与温度及压强的关系如图所示,则压强p1
2CO(g)+2H2(g)。密闭容器中浓度均为0.1 mol·L-1的CH4与CO2,在一定条件下反应,测得CH4的平衡转化率[α(CH4)]与温度及压强的关系如图所示,则压强p1
2023高三·全国·专题练习 查看更多[1]
(已下线)03 常考题空3 分压平衡常数(Kp)计算 (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
更新时间:2023-05-06 21:53:37
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】低碳经济是以低能耗、低污染、低排放为基础的经济模式。请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)现用300mL 0.5mol•L﹣1的NaOH溶液吸收2.24L(标准状况下)CO2,完全吸收反应后,所得溶液中离子浓度由大到小的顺序为:_______ 。
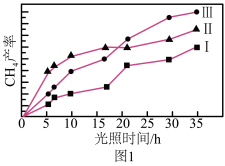
(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,紫外线照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图1所示。在0~15h内,对反应催化效果最好的催化剂是_______ 。(填序号)
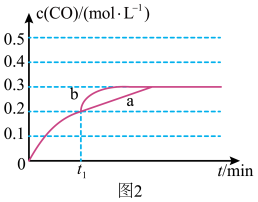
(3)一定温度下,在3L容积可变的密闭容器中发生反应H2(g)+CO2(g)⇌H2O(g)+CO(g)△H=+41.2kJ•mol﹣1,已知c(CO)随反应时间t的变化曲线a如图2所示,在t1时刻改变一个条件,曲线a变为b,则改变的条件是_______ 。
(4)如图3是利用甲烷燃料电池给C电极上镀金属铜,则乙池中选择的电解质溶液为_______ ,A电极的电极反应式为_______ ,若C电极增重0.96g,则B电极上消耗O2的物质的质量为_______ 。

(1)现用300mL 0.5mol•L﹣1的NaOH溶液吸收2.24L(标准状况下)CO2,完全吸收反应后,所得溶液中离子浓度由大到小的顺序为:
(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2,紫外线照射时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图1所示。在0~15h内,对反应催化效果最好的催化剂是

(3)一定温度下,在3L容积可变的密闭容器中发生反应H2(g)+CO2(g)⇌H2O(g)+CO(g)△H=+41.2kJ•mol﹣1,已知c(CO)随反应时间t的变化曲线a如图2所示,在t1时刻改变一个条件,曲线a变为b,则改变的条件是

(4)如图3是利用甲烷燃料电池给C电极上镀金属铜,则乙池中选择的电解质溶液为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】向1L的密闭容器中加入1molX、0.3molZ和0.5molY三种气体。一定条件下发生反应,各物质的浓度随时间的变化如图甲所示。图乙为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件,且没有使用催化剂。
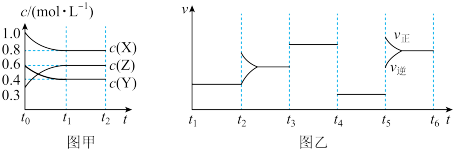
(1)请写出该反应的化学方程式___________ 。
(2)图乙中处于平衡的时间段是___________
(3)t3、t4、t5时刻改变的条件分别是___________ 、___________ 、___________ ,该反应
___________ 0(填“<”或“>”)。
(4)已知反应 ,改变下列条件,平衡如何移动(填“正向”“逆向”或“不”)。
,改变下列条件,平衡如何移动(填“正向”“逆向”或“不”)。
①增加反应物的浓度,平衡___________ 移动;
②增大压强,平衡___________ 移动;
③降低温度,平衡___________ 移动。

(1)请写出该反应的化学方程式
(2)图乙中处于平衡的时间段是___________
| A.t1-t2 | B.t2-t3 | C.t3-t5 | D.t5-t6 |
(3)t3、t4、t5时刻改变的条件分别是

(4)已知反应
 ,改变下列条件,平衡如何移动(填“正向”“逆向”或“不”)。
,改变下列条件,平衡如何移动(填“正向”“逆向”或“不”)。①增加反应物的浓度,平衡
②增大压强,平衡
③降低温度,平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某实验室模拟反应 ,在密闭容器中加入足量的C和一定量的
,在密闭容器中加入足量的C和一定量的 气体,维持温度为
气体,维持温度为 ,如图为不同压强下该反应经过相同时间
,如图为不同压强下该反应经过相同时间 的转化率随着压强变化的示意图。请从动力学角度分析,
的转化率随着压强变化的示意图。请从动力学角度分析,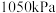 前,反应中
前,反应中 的转化率随着压强增大而增大的原因为
的转化率随着压强增大而增大的原因为_______ ;在 时,
时, 的体积分数为
的体积分数为_______ 。

 ,在密闭容器中加入足量的C和一定量的
,在密闭容器中加入足量的C和一定量的 气体,维持温度为
气体,维持温度为 ,如图为不同压强下该反应经过相同时间
,如图为不同压强下该反应经过相同时间 的转化率随着压强变化的示意图。请从动力学角度分析,
的转化率随着压强变化的示意图。请从动力学角度分析,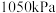 前,反应中
前,反应中 的转化率随着压强增大而增大的原因为
的转化率随着压强增大而增大的原因为 时,
时, 的体积分数为
的体积分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)将0.050mol SO2(g)和0.030mol O2(g)充入一个2L的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g) 2SO3(g)+Q。写出该反应的逆反应化学平衡常数表达式
2SO3(g)+Q。写出该反应的逆反应化学平衡常数表达式_______ ;经2分钟反应达到平衡,测得n(SO3)=0.040mol,则这个时间段O2的平均反应速率为_______ 。
(2)在容积不变时,下列措施中有利于提高SO2平衡转化率的有_______ (选填编号)。
a. 移出氧气 b. 降低温度 c. 减小压强 d. 再充入0.050mol SO2(g)和0.030mol O2(g)
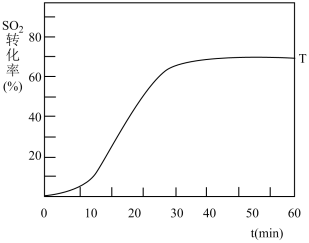
(3)在起始温度T1(673K)时SO2的转化率随反应时间(t)的变化如图。请在图中画出其他条件不变情况下,起始温度为T2(723K)时SO2的转化率随反应时间变化的示意图_______ 。
常温下,向1L pH=10的NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离产生的OH-离子浓度(c)的关系如图所示。
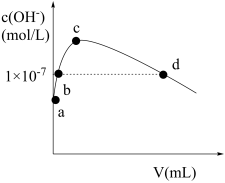
(4)c点溶液中离子浓度由大至小的关系是:_______ 。a点溶液中由水电离产生的c(H+)=_______ 。b点溶液中c(H+)_______ 1×10-7mol/L(填写“等于”、“大于”或“小于”)。
(5)写出c点到d点化学反应方程式_______ 。
(1)将0.050mol SO2(g)和0.030mol O2(g)充入一个2L的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)
 2SO3(g)+Q。写出该反应的逆反应化学平衡常数表达式
2SO3(g)+Q。写出该反应的逆反应化学平衡常数表达式(2)在容积不变时,下列措施中有利于提高SO2平衡转化率的有
a. 移出氧气 b. 降低温度 c. 减小压强 d. 再充入0.050mol SO2(g)和0.030mol O2(g)
(3)在起始温度T1(673K)时SO2的转化率随反应时间(t)的变化如图。请在图中画出其他条件不变情况下,起始温度为T2(723K)时SO2的转化率随反应时间变化的示意图

常温下,向1L pH=10的NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离产生的OH-离子浓度(c)的关系如图所示。

(4)c点溶液中离子浓度由大至小的关系是:
(5)写出c点到d点化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】CO、CO2是含碳元素的常见气体,也是参与碳循环的重要物质。
(1)利用煤化工中产生的CO和H2可制取甲醇,反应为CO(g)+2H2(g) CH3OH(g)。实验室中,在1L恒容的密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的物质的量(单位:mol)如下表所示:
CH3OH(g)。实验室中,在1L恒容的密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的物质的量(单位:mol)如下表所示:
①300℃和500℃对应的平衡常数大小关系为K300℃_________ K500℃(填“>”、“=”或“<”)。
②在一定条件下,下列描述中能说明上述反应已达平衡的是_______ (填标号)。
A.容器内气体的平均摩尔质量保持不变
B.2v(H2)正=v(CH3OH)逆
C.容器中气体的压强保持不变
D.单位时间内生成nmolCO的同时生成2nmolH2
③300℃时,前10min内,该反应的平均反应速率为v(H2)=_________ mol/(L·min)。
④下列措施能够增大此反应中CO的转化率的是_________ (填标号)。
A.充入CO气体B.升高温度
C.使用优质催化剂D.往容器中再充入1molCO和2molH2
⑤500℃时,保持反应体系的温度不变,60min时再向容器中充入CH3OH气体和H2各0.4mol,反应将向____________________ (填“正反应方向”、“逆反应方向”或“不”)进行。再次达到平衡时的平衡常数为____________ L2/mol2。
(2)二氧化碳催化加氢也可合成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H。在密闭容器中投入1molCO2和2.75molH2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如下图所示.
CH3OH(g)+H2O(g)△H。在密闭容器中投入1molCO2和2.75molH2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如下图所示.
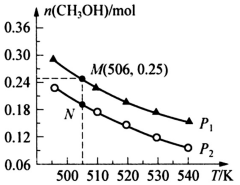
①二氧化碳合成甲醇正反应的△H______ 0(填“>”、“<”或“=”,下同)。
②M、N两点时化学反应速率:v(N)______ v(M)。
(3)一定条件下,向容积不变的某密闭容器中加入amolCO2和bmolH2发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是
CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是_________ 。
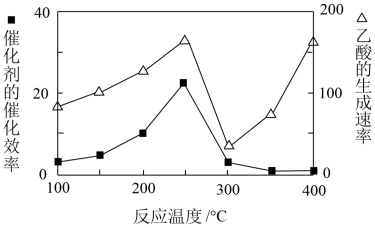
(4)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示。当乙酸的生成速率主要取决于温度时,其影响范围是_______________________ 。
(1)利用煤化工中产生的CO和H2可制取甲醇,反应为CO(g)+2H2(g)
 CH3OH(g)。实验室中,在1L恒容的密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的物质的量(单位:mol)如下表所示:
CH3OH(g)。实验室中,在1L恒容的密闭容器中进行模拟合成实验。将1molCO和2molH2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的物质的量(单位:mol)如下表所示:| 10min | 20min | 30min | 40min | 50min | 60min | |
| 300℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
| 500℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
①300℃和500℃对应的平衡常数大小关系为K300℃
②在一定条件下,下列描述中能说明上述反应已达平衡的是
A.容器内气体的平均摩尔质量保持不变
B.2v(H2)正=v(CH3OH)逆
C.容器中气体的压强保持不变
D.单位时间内生成nmolCO的同时生成2nmolH2
③300℃时,前10min内,该反应的平均反应速率为v(H2)=
④下列措施能够增大此反应中CO的转化率的是
A.充入CO气体B.升高温度
C.使用优质催化剂D.往容器中再充入1molCO和2molH2
⑤500℃时,保持反应体系的温度不变,60min时再向容器中充入CH3OH气体和H2各0.4mol,反应将向
(2)二氧化碳催化加氢也可合成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H。在密闭容器中投入1molCO2和2.75molH2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如下图所示.
CH3OH(g)+H2O(g)△H。在密闭容器中投入1molCO2和2.75molH2,在不同条件下发生反应,实验测得平衡时甲醇的物质的量随温度、压强的变化如下图所示.
①二氧化碳合成甲醇正反应的△H
②M、N两点时化学反应速率:v(N)
(3)一定条件下,向容积不变的某密闭容器中加入amolCO2和bmolH2发生反应:
CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是
CH3OH(g)+H2O(g),欲使整个反应过程中CO2的体积分数为恒定值,则a与b的大小关系式是(4)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系如图所示。当乙酸的生成速率主要取决于温度时,其影响范围是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】容积均为1 L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器。相同温度下,分别充入0.2 mol的NO2,发生反应: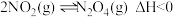 ,甲中NO2的相关量随时间变化如下图所示。
,甲中NO2的相关量随时间变化如下图所示。

(1)0~3 s内,甲容器中NO2的反应速率增大的原因是___________ 。
(2)甲达平衡时,温度若为 ,此温度下的平衡常数K=
,此温度下的平衡常数K=___________ 。
(3)平衡时,K甲___________ (填“>”“<”或“=”,下同)K乙,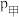
___________  。
。
(4)乙达平衡时再充入0.2 mol的NO2,重新达平衡后NO2的转化率___________ (填“增大”“减小”或“不变)
(5)甲达平衡时再充入0.1 mol的N2O4,重新达平衡后c(N2O4)___________ 0.18mol/L (填“>”“<”或“=”)
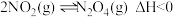 ,甲中NO2的相关量随时间变化如下图所示。
,甲中NO2的相关量随时间变化如下图所示。
(1)0~3 s内,甲容器中NO2的反应速率增大的原因是
(2)甲达平衡时,温度若为
 ,此温度下的平衡常数K=
,此温度下的平衡常数K=(3)平衡时,K甲
 。
。(4)乙达平衡时再充入0.2 mol的NO2,重新达平衡后NO2的转化率
(5)甲达平衡时再充入0.1 mol的N2O4,重新达平衡后c(N2O4)
您最近一年使用:0次



