根据下列图示得出的结论正确的是
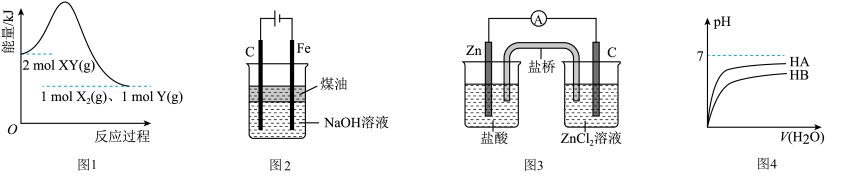

| A.由图1可判断该反应的反应物中化学键的总键能大于生成物中化学键的总键能 |
B.图2装置能制备 并能较长时间观察其颜色 并能较长时间观察其颜色 |
| C.图3装置中电流表指针发生明显偏转 |
D.由图4可证明图示条件下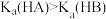 |
更新时间:2023-05-10 07:24:32
|
相似题推荐
【推荐1】甲烷与氯气在光照条件下取代反应的部分反应历程和能量变化如下:
第一步:Cl2(g)→2Cl(g) △H1= +242.7kJ/mol
第二步:CH4(g)+Cl(g)→CH3(g)+HCl(g) △H2= +7.5 kJ/mol
第三步:CH3(g)+Cl2(g)→CH3Cl(g)+Cl(g) △H3= -112.9 kJ/mol(其中CH3表示甲基,Cl表示氯原子)
下列说法不正确的是( )
第一步:Cl2(g)→2Cl(g) △H1= +242.7kJ/mol
第二步:CH4(g)+Cl(g)→CH3(g)+HCl(g) △H2= +7.5 kJ/mol
第三步:CH3(g)+Cl2(g)→CH3Cl(g)+Cl(g) △H3= -112.9 kJ/mol(其中CH3表示甲基,Cl表示氯原子)
下列说法不正确的是( )
| A.甲烷与氯气在光照下发生反应的过程中会生成少量的乙烷 |
| B.CH4(g)+Cl2(g)→CH3Cl(g)+HCl(g) △H= -105.4 kJ/mol |
| C.形成1mol CH3Cl(g)中C-Cl键放出的能量比拆开1mol Cl2(g)中Cl-Cl键吸收的能量多 |
| D.若是CH4与Br2发生取代反应,则第二步反应的△H<+7.5kJ/mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列图示与对应叙述相符的是
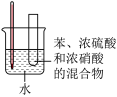 | 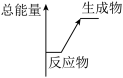 | 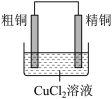 | 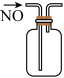 |
| A.硝基苯的制备 | B.盐酸与碳酸氢钠反应的能量变化 | C.粗铜的精炼 | D.一氧化氮气体的收集 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
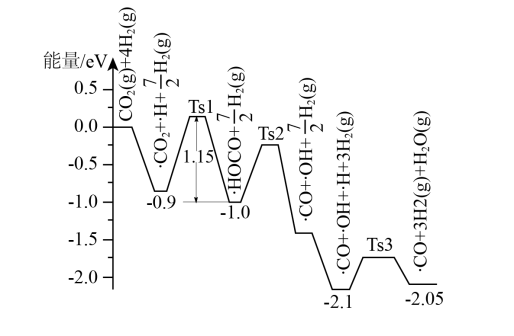
【推荐1】Shyam Kattle等结合实验与计算机模拟结果,研究了在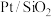 催化剂表面上
催化剂表面上 与
与 的反应历程,前三步历程如图所示,吸附在
的反应历程,前三步历程如图所示,吸附在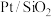 催化剂表面上的物种用“·”标注,
催化剂表面上的物种用“·”标注, 表示过渡态。下列有关说法错误的是
表示过渡态。下列有关说法错误的是
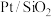 催化剂表面上
催化剂表面上 与
与 的反应历程,前三步历程如图所示,吸附在
的反应历程,前三步历程如图所示,吸附在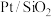 催化剂表面上的物种用“·”标注,
催化剂表面上的物种用“·”标注, 表示过渡态。下列有关说法错误的是
表示过渡态。下列有关说法错误的是
| A.物质被吸附在催化剂表面形成过渡态的过程是吸热的 |
B.形成过渡态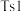 的活化能为 的活化能为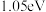 |
C.前三步总反应的 |
D.反应历程中能量变化最大的反应方程式为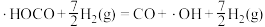 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知2mol氢气完全燃烧生成水蒸气时放出能量484kJ,且氧气中1molO=O键完全断裂时吸收热量496kJ,水蒸气中1molH-O键形成时放出能量463kJ,则氢气中1molH-H键断裂时吸收热量为( )
| A.920kJ | B.557kJ | C.436kJ | D.188kJ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】如图是草酸溶液中H2C2O4、HC2O4-、C2O42-三种微粒的分布分数(某微粒物质的量浓度与三种微粒物质的量浓度和的比值)与pH的关系,下列有关说法不正确的是

| A.pH=5 的溶液中c(C2O42-)>c(HC2O4-) |
| B.NaHC2O4溶液中:c(OH-)+c(C2O42-)=c(H+)+c(H2C2O4) |
| C.向NaHC2O4溶液中加强酸至pH与a点对应时,溶液中 2c(Na+)=c(HC2O4-)+ c(H2C2O4) |
| D.为使溶液中c(c(HC2O4-)尽可能多一些,溶液的pH最好控制在2.7左右 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】常温下,下列溶液的离子浓度关系正确的是
A. 的 的 溶液中, 溶液中,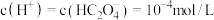 |
B.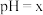 的 的 溶液100mL,稀释10倍后 溶液100mL,稀释10倍后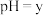 , ,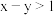 |
C. 的 的 溶液与 溶液与 的NaOH溶液以任意比混合,混合液中: 的NaOH溶液以任意比混合,混合液中: |
D.pH相同的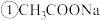 、 、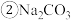 、 、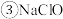 三种溶液中 三种溶液中 : :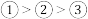 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】微生物脱盐电池既可以处理废水中CH3COOH和铵盐,同时实现海水的淡化,原理如下图所示,其中阳离子交换膜只允淡水许阳离子通过,阴离子交换膜只允许阴离子通过。下列说法正确的是
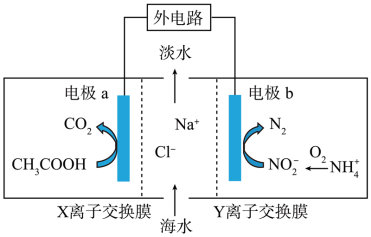

| A.电流从电极a流向电极b |
| B.电极a的电极反应式为CH3COOH-8e-+8OH-=2CO2↑+6H2O |
| C.每生成标准状况下2.24L N2,电路中转移0.6mol电子 |
| D.X离子交换膜为阳离子交换膜,Y离子交换膜为阴离子交换膜 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】某实验小组依据反应: 设计如图原电池,探究
设计如图原电池,探究 对
对 氧化性的影响。测得电压与pH的关系如图,下列有关叙述错误的是
氧化性的影响。测得电压与pH的关系如图,下列有关叙述错误的是
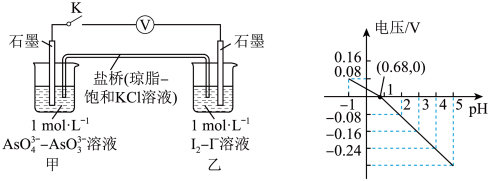
 设计如图原电池,探究
设计如图原电池,探究 对
对 氧化性的影响。测得电压与pH的关系如图,下列有关叙述错误的是
氧化性的影响。测得电压与pH的关系如图,下列有关叙述错误的是
A. 时,氧化性 时,氧化性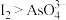 |
B.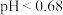 时盐桥中 时盐桥中 向右移 向右移 |
C.调节 可以改变反应的方向 可以改变反应的方向 |
D.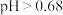 时,正极的电极反应为 时,正极的电极反应为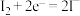 |
您最近一年使用:0次

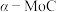 两种催化剂边界生成羟基作为温和还原剂,使乙炔选择性氢化,再以CO去除残留O。这一过程避免了经典路线中对
两种催化剂边界生成羟基作为温和还原剂,使乙炔选择性氢化,再以CO去除残留O。这一过程避免了经典路线中对
 的总反应为
的总反应为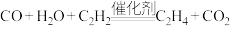





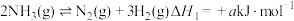
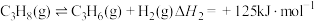
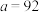
 分解率不变
分解率不变
 、
、 条件下,液态水的气化热为
条件下,液态水的气化热为 ,则
,则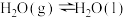 的
的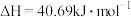
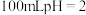 的新制氯水中:
的新制氯水中: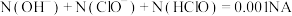



 (g)+3H2(g)→
(g)+3H2(g)→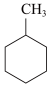 (g)的焓变为
(g)的焓变为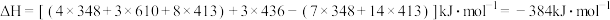
 的
的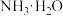 溶液中加入少量
溶液中加入少量 晶体,能使
晶体,能使 的电离度降低,溶液的pH减小
的电离度降低,溶液的pH减小



