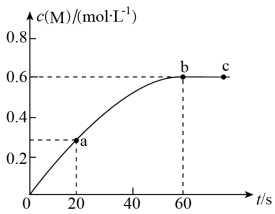
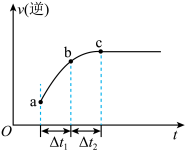
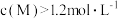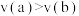向恒容密闭容器中通入SO2和NO2,在一定条件下使反应 达到平衡,逆反应速率随时间的变化如图所示。由图可得出的正确结论是
达到平衡,逆反应速率随时间的变化如图所示。由图可得出的正确结论是
 达到平衡,逆反应速率随时间的变化如图所示。由图可得出的正确结论是
达到平衡,逆反应速率随时间的变化如图所示。由图可得出的正确结论是
| A.从图像可知该反应一定为放热反应 |
| B.从a点到c点过程中反应物的浓度逐渐增大 |
| C.c点时,反应达到最大限度 |
D. 时, 时, 的浓度变化a~b段小于b~c段 的浓度变化a~b段小于b~c段 |
22-23高一下·广东佛山·期中 查看更多[2]
广东省顺德市李兆基中学2022-2023学年高一下学期4月期中考试化学试题(已下线)专题05 影响化学平衡的因素【考题猜想】(6大题型)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)
更新时间:2023-04-23 19:38:11
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】 的有效利用对发展碳循环经济产生了巨大的影响。其中利用
的有效利用对发展碳循环经济产生了巨大的影响。其中利用 和
和 ,在一定条件下合成乙醇的反应为
,在一定条件下合成乙醇的反应为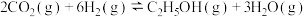
 。向2 L刚性不可变容器中充入1 mol
。向2 L刚性不可变容器中充入1 mol  和3 mol
和3 mol  ,单位时间内测得
,单位时间内测得 的转化率随温度变化关系如图所示。下列说法正确的是
的转化率随温度变化关系如图所示。下列说法正确的是

 的有效利用对发展碳循环经济产生了巨大的影响。其中利用
的有效利用对发展碳循环经济产生了巨大的影响。其中利用 和
和 ,在一定条件下合成乙醇的反应为
,在一定条件下合成乙醇的反应为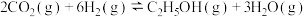
 。向2 L刚性不可变容器中充入1 mol
。向2 L刚性不可变容器中充入1 mol  和3 mol
和3 mol  ,单位时间内测得
,单位时间内测得 的转化率随温度变化关系如图所示。下列说法正确的是
的转化率随温度变化关系如图所示。下列说法正确的是
A.上述反应的 |
| B.混合气体的密度保持不变时,说明该反应达平衡状态 |
C.c点平衡后,向容器中再充入等量原反应气体,达新平衡时, 的转化率增大 的转化率增大 |
D.反应从开始到a点需时5 min,5 min内用 表示的反应速率为0.3 mol·L-1·min-1 表示的反应速率为0.3 mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知2HI(g)⇌H2(g) +I2(g), 443℃时IL密闭容器中充入1 mol HI,体系中c(HI)与反应时间t的关系如图所示。下列说法正确的是
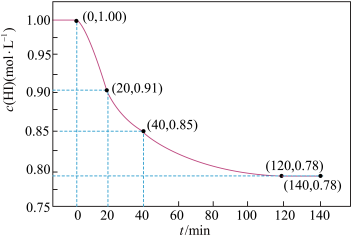

| A.0~20 min内,v(H2) = 0.0045mol·L-1·min-1 | B.升高温度,HI会完全分解 |
| C.40 min时,c(H2) = 0.075mol·L-1 | D.120 min反应达到最大限度,此时HI的转化率为78% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在一个密闭的容器中发生如下反应:2SO2(g)+O2(g) 2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度均为0.1 mol·L-1,当达到平衡时可能的数据是
2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度均为0.1 mol·L-1,当达到平衡时可能的数据是
 2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度均为0.1 mol·L-1,当达到平衡时可能的数据是
2SO3(g),反应过程中某一时刻SO2、O2、SO3的浓度均为0.1 mol·L-1,当达到平衡时可能的数据是| A.c(SO3)=0.15mol·L-1 | B.c(SO3)= c(SO2)=0.075 mol·L-1 |
| C.c(SO3)=0.2 mol·L-1 | D.c(O2)=0.05 mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已经建立化学平衡的某可逆反应,当条件改变时化学平衡向正反应方向移动,下列叙述正确的是①生成物的质量分数一定增加 ②生成物的产量一定增加 ③反应物的转化率一定增加 ④反应物的浓度一定减小 ⑤正反应速率一定比逆反应速率大
| A.①②③④⑤ | B.②④⑤ | C.②⑤ | D.⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】T℃下,向0.5L的恒容密闭容器中充入等物质的量的P和Q,发生反应2P(g)+2Q(g) R(g)+2S(g) △H>0,反应速率可表示为v(正)=k正c2(P)•c2(Q),v(逆)=k逆c(R)•c2(S),其中k正、k逆为速率常数。反应过程中S和P的物质的量浓度变化如图所示:
R(g)+2S(g) △H>0,反应速率可表示为v(正)=k正c2(P)•c2(Q),v(逆)=k逆c(R)•c2(S),其中k正、k逆为速率常数。反应过程中S和P的物质的量浓度变化如图所示:
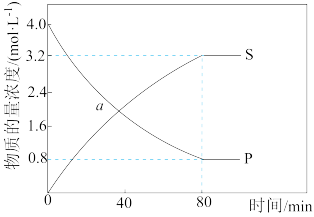
下列说法错误的是
 R(g)+2S(g) △H>0,反应速率可表示为v(正)=k正c2(P)•c2(Q),v(逆)=k逆c(R)•c2(S),其中k正、k逆为速率常数。反应过程中S和P的物质的量浓度变化如图所示:
R(g)+2S(g) △H>0,反应速率可表示为v(正)=k正c2(P)•c2(Q),v(逆)=k逆c(R)•c2(S),其中k正、k逆为速率常数。反应过程中S和P的物质的量浓度变化如图所示:
下列说法错误的是
| A.Q与S浓度相等时,v正>v逆 |
B.a点时, =160 =160 |
| C.容器中气体的平均相对分子质量不再变化时,可逆反应达到平衡状态 |
| D.反应到达平衡后,向容器中通过少量的氦气(不参与反应),R的浓度保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定条件下,可逆反应达到平衡时
| A.单位时间内反应物减少的分子数等于生成物增加的分子数 |
| B.反应物浓度等于生成物浓度 |
| C.反应物完全反应 |
| D.混合体系中各组成成分和含量保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】实验室中模拟合成氨反应: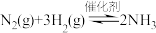 在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:
在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:
下列有关说法不正确的是
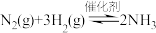 在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:
在恒容密闭容器中,初始投入量相等的条件下,得到三组实验数据如表所示:| 实验序号 | 温度( ) ) |  浓度( 浓度( ) ) | ||||||
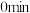 |  |  |  | 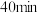 | 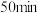 | 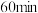 | ||
| 1 | 300 | 2.00 | 1.70 | 1.50 | 1.36 | 1.25 | 1.20 | 1.20 |
| 2 | 300 | 2.00 | 1.50 | 1.28 | 1.20 | 1.20 | 1.20 | 1.20 |
| 3 | 200 | 2.00 | 1.60 | 1.39 | 1.29 | 1.27 | 1.27 | 1.27 |
| A.当容器内的压强不再改变时,说明该可逆反应已达到化学平衡状态 |
B.实验2中,前 内以 内以 的浓度变化表示的化学反应速率为 的浓度变化表示的化学反应速率为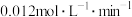 |
| C.比较实验1和2,说明实验2使用了更高效的催化剂 |
D.实验3中,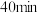 时向容器中充入一定量 时向容器中充入一定量 ,则正反应速率 ,则正反应速率 不变 不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列叙述与图中甲、乙、丙、丁相符合的是


A.图甲是锌粒与盐酸反应的反应速率随反应时间变化的曲线, 时刻溶液的温度最高 时刻溶液的温度最高 |
B.图乙是恒温密闭容器中发生 反应时 反应时 随反应时间变化的曲线, 随反应时间变化的曲线, 时刻改变的条件可能是缩小容器的体积 时刻改变的条件可能是缩小容器的体积 |
C.图丙表示反应 , , 起始时的物质的量相同,达到平衡时 起始时的物质的量相同,达到平衡时 的转化率大小为c<b<a 的转化率大小为c<b<a |
D.图丁表示恒容密闭容器中其他条件相同时改变温度,反应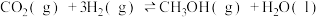 中, 中, 随时间变化的曲线,说明反应平衡常数KⅡ>KⅠ 随时间变化的曲线,说明反应平衡常数KⅡ>KⅠ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据实验目的,下列实验及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 比较 、 、 、 、 的氧化性 的氧化性 | 向含有等量KBr、KI混合溶液中依次加入少量新制氯水和 ,振荡、静置,溶液分层,下层呈紫红色 ,振荡、静置,溶液分层,下层呈紫红色 | 氧化性: |
| B | 探究温度对平衡移动的影响 | 将充有 的密闭烧瓶放入热水中,烧瓶内气体颜色加深 的密闭烧瓶放入热水中,烧瓶内气体颜色加深 |  为放热反应,升温平衡逆向移动 为放热反应,升温平衡逆向移动 |
| C | 检验酸性条件下淀粉的水解产物中是否含有葡萄糖 | 向水解液中加入新制 ,未出现砖红色沉淀 ,未出现砖红色沉淀 | 不含葡萄糖 |
| D | 在 溶液中通入 溶液中通入 气体 气体 | 有沉淀生成 | 酸性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】二甲醚催化制备乙醇主要涉及以下两个反应:
反应Ⅰ: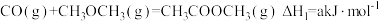
反应Ⅱ: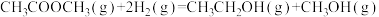
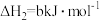
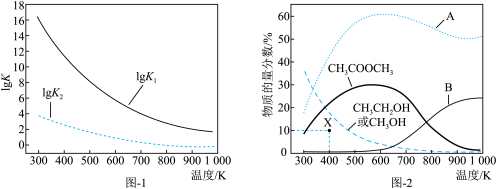
反应Ⅰ、Ⅱ的平衡常数的对数lgK1、lgK2与温度的关系如图1所示;固定CO、CH3OCH3、H2的原料比、体系压强不变的条件下,同时发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是
反应Ⅰ:
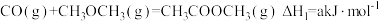
反应Ⅱ:
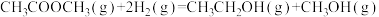
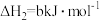
反应Ⅰ、Ⅱ的平衡常数的对数lgK1、lgK2与温度的关系如图1所示;固定CO、CH3OCH3、H2的原料比、体系压强不变的条件下,同时发生反应Ⅰ、Ⅱ,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是

| A.a>0 |
| B.600 K后升高温度,CH3COOCH3的物质的量分数降低原因是反应Ⅱ平衡右移 |
| C.测得X点CH3CH2OH的物质的量分数是10%,则X点反应Ⅱ有:v正>v逆 |
| D.曲线B表示H2的物质的量分数随温度的变化 |
您最近一年使用:0次

 和
和 ,发生反应:
,发生反应: 。反应过程中的部分数据如下表所示。下列说法正确的是
。反应过程中的部分数据如下表所示。下列说法正确的是

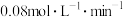
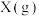 ,发生反应:
,发生反应: 。其中
。其中 的物质的量浓度随时间的变化曲线如图所示。下列说法正确的是
的物质的量浓度随时间的变化曲线如图所示。下列说法正确的是