部分元素在周期表的位置如图所示:
(1)G元素在周期表中的位置可表示为___________ ;
(2)BH2的电子式为___________ ;
(3)G与H元素最高价氧化物所对应的水化物,酸性较强的是___________ (填化学式);
(4)DF2属于___________ 晶体;
(5)CA4的分子空间构型为___________ ;
(6)物质EA4H存在的微粒间作用力有___________ ;
(7)AHF的电离方程式为___________ ;
(8)将A2F2的酸性溶液与M2G的水溶液混合可生成G的单质,发生反应的离子方程式为___________ 。

(1)G元素在周期表中的位置可表示为
(2)BH2的电子式为
(3)G与H元素最高价氧化物所对应的水化物,酸性较强的是
(4)DF2属于
(5)CA4的分子空间构型为
(6)物质EA4H存在的微粒间作用力有
(7)AHF的电离方程式为
(8)将A2F2的酸性溶液与M2G的水溶液混合可生成G的单质,发生反应的离子方程式为
更新时间:2023-04-26 08:26:06
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】已知25℃时部分弱电解质的电离平衡常数数据如表所示:
回答下列问题:
(1)写出H2CO3的第一级电离平衡常数表达式:Ka1=_______ 。
(2)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3溶液的pH由大到小的顺序为_______ (填字母)。
(3)常温下,0.1mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_______(填字母)。
(4)一定温度下,体积均为100mL、pH=2的CH3COOH溶液与一元酸HX的溶液,加水稀释过程中pH与溶液体积的关系如图所示,则HX的电离平衡常数_______ (填“大于”“小于”或“等于”,下同)CH3COOH的电离平衡常数。

(5)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=_______ mol·L-1(填精确值)。
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数/(mol·L-1) | 1.7×10-5 | 6.2×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
(1)写出H2CO3的第一级电离平衡常数表达式:Ka1=
(2)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3溶液的pH由大到小的顺序为
(3)常温下,0.1mol·L-1的CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_______(填字母)。
| A.c(H+) | B. | C.c(H+)c(OH-) | D. |

(5)25℃时,在CH3COOH与CH3COONa的混合溶液中,若测得pH=6,则溶液中c(CH3COO-)-c(Na+)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】Ⅰ.25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)写出碳酸的第一级电离方程式:________ 。
(2)物质的量浓度相同的三种溶液:a.CH3COONa b.NaHCO3 c.NaClO
三种溶液的pH由小到大排列的顺序是___ <___ < ___ (用编号填写)
(3)写出向NaClO溶液中通入少量CO2的化学方程式________ 。
Ⅱ.(4)碳酸钠溶液呈碱性的原因是:______ 。(写出离子方程式)。0.01mol/L Na2CO3溶液的pH____ 0.1mol/LNa2CO3溶液的pH。(填“>”或“<”或“==”)
(5)浓度均为0.1mol/L的①CH3COONa溶液②NH4Cl溶液③稀HCl④Na2SO4溶液按pH由大到小的排列顺序为____
(6)打开无水FeCl3的试剂瓶,常冒出许多“白烟”,发生反应的化学方程式为________
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11` | 3.0×10-8 |
(1)写出碳酸的第一级电离方程式:
(2)物质的量浓度相同的三种溶液:a.CH3COONa b.NaHCO3 c.NaClO
三种溶液的pH由小到大排列的顺序是
(3)写出向NaClO溶液中通入少量CO2的化学方程式
Ⅱ.(4)碳酸钠溶液呈碱性的原因是:
(5)浓度均为0.1mol/L的①CH3COONa溶液②NH4Cl溶液③稀HCl④Na2SO4溶液按pH由大到小的排列顺序为
(6)打开无水FeCl3的试剂瓶,常冒出许多“白烟”,发生反应的化学方程式为
您最近一年使用:0次
【推荐3】全球大气CO2浓度升高对人类生活产生了影响,CO2的捕集和资源化利用成为研究热点。
(1)CO2能引起海水酸化,原理为___ (用化学方程式表示),因此CO2过量排放对海洋生态系统会造成严重影响。
(2)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。下列物质中能作为捕碳剂的是___ 。
A.K2CO3 B.CaO C.NH3. D.NH4Cl
(3)CO2甲烷化是实现其资源化利用的有效方式之一。
I.热化学转化法:工业上常用CO2催化加氢合成CH4。
已知:①CO(g)+H2O(g) H2(g)+CO2(g) ΔH1=-41kJ·mol-1
H2(g)+CO2(g) ΔH1=-41kJ·mol-1
②C(s)+2H2(g) CH4(g) ΔH2=-73kJ·mol-1
CH4(g) ΔH2=-73kJ·mol-1
③2CO(g) C(s)+CO2(g) ΔH3=-171 kJ·mol-1
C(s)+CO2(g) ΔH3=-171 kJ·mol-1
反应CO2(g)+4H2(g) CH4(g)+2H2O(g)的ΔH=
CH4(g)+2H2O(g)的ΔH=___ kJ·mol-1
在该工业生产中,选用了高活性的Ni基催化剂,目的是:___ 。
II.电化学转化法:多晶Cu可高效催化CO2甲烷化,电解CO2制备CH4的原理示意图如图。
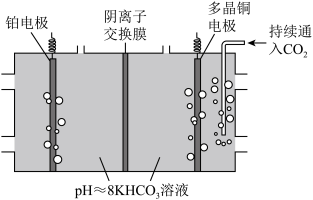
①多晶铜连接电源的___ 极。(填“正”或“负”)
②阳极氧化产物只有O2。电解时实际生成CH4的总最小于由O2理论计算所得CH4的量,结合电极反应式解释原因:___ 。
(1)CO2能引起海水酸化,原理为
(2)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。下列物质中能作为捕碳剂的是
A.K2CO3 B.CaO C.NH3. D.NH4Cl
(3)CO2甲烷化是实现其资源化利用的有效方式之一。
I.热化学转化法:工业上常用CO2催化加氢合成CH4。
已知:①CO(g)+H2O(g)
 H2(g)+CO2(g) ΔH1=-41kJ·mol-1
H2(g)+CO2(g) ΔH1=-41kJ·mol-1②C(s)+2H2(g)
 CH4(g) ΔH2=-73kJ·mol-1
CH4(g) ΔH2=-73kJ·mol-1③2CO(g)
 C(s)+CO2(g) ΔH3=-171 kJ·mol-1
C(s)+CO2(g) ΔH3=-171 kJ·mol-1反应CO2(g)+4H2(g)
 CH4(g)+2H2O(g)的ΔH=
CH4(g)+2H2O(g)的ΔH=在该工业生产中,选用了高活性的Ni基催化剂,目的是:
II.电化学转化法:多晶Cu可高效催化CO2甲烷化,电解CO2制备CH4的原理示意图如图。

①多晶铜连接电源的
②阳极氧化产物只有O2。电解时实际生成CH4的总最小于由O2理论计算所得CH4的量,结合电极反应式解释原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】A、B、C、D、E都是短周期元素,原子序数依次增大,A、B处于同周期,C、D、E同处另一周期,C、A可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙,B是最活泼的非金属元素,D是地壳中含量最高的金属元素,E的最高价氧化物对应的水化物是周期表中最强的含氧酸。
(1)元素B在周期表中的位置是_________ ,甲的电子式是_______ 。
(2)单质D与C的最高价氧化物对应水化物的水溶液反应的离子方程式是___________ 。
(3)单质E与C的最高价氧化物对应水化物的水溶液反应的化学方程式是________ 。
(4)物质乙与水反应的化学方程式____________ 。
(1)元素B在周期表中的位置是
(2)单质D与C的最高价氧化物对应水化物的水溶液反应的离子方程式是
(3)单质E与C的最高价氧化物对应水化物的水溶液反应的化学方程式是
(4)物质乙与水反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、M、N六种短周期主族元素,它们的核电荷数依次增大。A可与D、E形成10电子分子,其中B的最外层电子数等于次外层电子数,C原子最外层电子数是次外层电子数的2倍,M的L层电子数为K层和M层电子数之和,D和M同主族。回答下列问题:
(1)元素B的符号和名称分别是______ ,_____ ;在周期表中的位置是____________ 。
(2)元素C的原子结构示意图为______________________________ 。
(3)元素C与M可形成CM2,C与N可形成CN4,这两种化合物均可做溶剂,其电子式分别为:_________ 和_________ 。
(4)元素A与D、E形成10电子分子的结构式分别为:__________ 和__________ 。
(5)元素C和M相比,非金属性较强的是_________ (用元素符号表示)。
(6)元素D、M的氢化物的沸点高低顺序为:_________ (用化学式表示)。
(7)在一定条件下,A、D的单质和M的最高价氧化物对应水化物的溶液可构成原电池,该电池在放电过程中,电解质溶液的酸性将_________ (填“增大”“减小”或“不变”)。
(8)1 mol CA4与D2完全反应生成两种气体时放出热量802kJ,则该反应的热化学方程式为__________________________________________________________________ 。
(1)元素B的符号和名称分别是
(2)元素C的原子结构示意图为
(3)元素C与M可形成CM2,C与N可形成CN4,这两种化合物均可做溶剂,其电子式分别为:
(4)元素A与D、E形成10电子分子的结构式分别为:
(5)元素C和M相比,非金属性较强的是
(6)元素D、M的氢化物的沸点高低顺序为:
(7)在一定条件下,A、D的单质和M的最高价氧化物对应水化物的溶液可构成原电池,该电池在放电过程中,电解质溶液的酸性将
(8)1 mol CA4与D2完全反应生成两种气体时放出热量802kJ,则该反应的热化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】下面是元素周期表的草图,表中所列字母代号分别代表某一种元素,请回答:
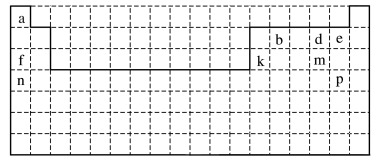
(1)表中最活泼的金属与最活泼的非金属形成的物质是__________________ (填化学式)。
(2)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:_____________________ ,
(3)e、f、k、m对应的单原子离子的半径由大到小的顺序为__________ (填离子符号)。
(4)d、m对应的离子还原性由强到弱顺序为_________________________ (填离子符号)。
(5)d、e、m的气态氢化物中,最不稳定的是________________________ (填分子式)。
(6)用电子式表示n与m形成的原子个数比2∶1的化合物的形成过程:________________ 。

(1)表中最活泼的金属与最活泼的非金属形成的物质是
(2)由a、d两种元素可形成两种化合物,写出其中一种化合物分解生成另一种化合物的化学方程式:
(3)e、f、k、m对应的单原子离子的半径由大到小的顺序为
(4)d、m对应的离子还原性由强到弱顺序为
(5)d、e、m的气态氢化物中,最不稳定的是
(6)用电子式表示n与m形成的原子个数比2∶1的化合物的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】下表是元素周期表中的一部分:
根据a~i在周期表中的位置,回答下列问题:
(1)a~i的单质中,化学性质最不活泼的是______ (填化学式,下同),氧化性最强的是_______ 。
(2)a与b形成的简单化合物的电子式是___________ 。
(3)最高价氧化物对应的水化物酸性最强的是___________ (填化学式);e、f的最高价氧化物对应的水化物之间反应的离子方程式为________________________ 。
(4)g的最高价氧化物对应水化物的浓溶液可与Cu在加热时反应,反应的化学方程式为___________________ ,该反应中氧化剂与还原剂的物质的量之比为_________ 。
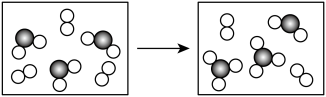
(5)如图表示由c、g元素组成的两种气体分子在一定 条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:_______________________ 。
I A | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 第1周期 | a | |||||||
| 第2周期 | b | c | d | |||||
| 第3周期 | e | f | g | h | i | |||
(1)a~i的单质中,化学性质最不活泼的是
(2)a与b形成的简单化合物的电子式是
(3)最高价氧化物对应的水化物酸性最强的是
(4)g的最高价氧化物对应水化物的浓溶液可与Cu在加热时反应,反应的化学方程式为
(5)如图表示由c、g元素组成的两种气体分子在一定 条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如图为元素周期表的一部分,图中所列字母分别代表一种化学元素。

(1)元素b、c、e形成的常见稳定单质中最易与H2化合的是___________ (填化学式)。
(2)元素d、c所形成的某化合物的摩尔质量为78g/mol,该化合物的化学式为___________ ,其中所含化学键的类型有___________ 。
(3)推测原子序数为35的元素在元素周期表中的位置是___________ 。
(4)依据元素周期律推测,元素f的单质及其化合物的性质正确的是___________(填字母)。
(5)含有非极性键的c的氢化物,其电子式为___________ 。(ab)2称为拟卤素,性质与卤素单质相似,常温下其与NaOH溶液反应的化学方程式为___________ 。

(1)元素b、c、e形成的常见稳定单质中最易与H2化合的是
(2)元素d、c所形成的某化合物的摩尔质量为78g/mol,该化合物的化学式为
(3)推测原子序数为35的元素在元素周期表中的位置是
(4)依据元素周期律推测,元素f的单质及其化合物的性质正确的是___________(填字母)。
| A.f的单质常温下呈气态 | B.f的单质具有强氧化性 |
| C.fc2属于酸性氧化物 | D.fc2既有氧化性又有还原性 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】有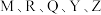 五种短周期主族元素,其中
五种短周期主族元素,其中 为短周期主族元素中原子半径最大的,
为短周期主族元素中原子半径最大的, 的最高正价与最低负价的代数和为
的最高正价与最低负价的代数和为 四种元素在元素周期表中的相对位置如图。回答下列问题:
四种元素在元素周期表中的相对位置如图。回答下列问题:
(1)R在元素周期表中的位置是_________ 。
(2)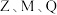 的简单离子的半径由大到小的顺序为
的简单离子的半径由大到小的顺序为_________ (用离子符号表示)。
(3)写出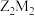 的电子式:
的电子式:_________ 。其所含的化学键类型为_________ 。
(4)下列事实能作为比较元素 与
与 的非金属性相对强弱依据的是_________(填标号)。
的非金属性相对强弱依据的是_________(填标号)。
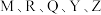 五种短周期主族元素,其中
五种短周期主族元素,其中 为短周期主族元素中原子半径最大的,
为短周期主族元素中原子半径最大的, 的最高正价与最低负价的代数和为
的最高正价与最低负价的代数和为 四种元素在元素周期表中的相对位置如图。回答下列问题:
四种元素在元素周期表中的相对位置如图。回答下列问题: | |||
 |  |  |
(2)
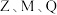 的简单离子的半径由大到小的顺序为
的简单离子的半径由大到小的顺序为(3)写出
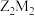 的电子式:
的电子式:(4)下列事实能作为比较元素
 与
与 的非金属性相对强弱依据的是_________(填标号)。
的非金属性相对强弱依据的是_________(填标号)。A.常温下 的单质呈固态, 的单质呈固态, 的单质呈气态 的单质呈气态 | B.最简单氢化物的稳定性: |
C. 与 与 形成的化合物中 形成的化合物中 呈正价 呈正价 | D.酸性: |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】根据表格完成下列问题:
(1)上述涉及原子中最活泼非金属原子核外电子排布式是____ ;某阴离子的轨道表示式为 ,该阴离子核外电子占有的轨道总数是
,该阴离子核外电子占有的轨道总数是___ 个,有____ 种能量不同的电子,有____ 种不同运动状态的电子。
(2)物质①的电子式:____ ,⑦的结构式:____ 。
(3)④的熔沸点相较①、②、③低许多,说明其为___ 晶体;熔化时___ 破坏。
(4)不能用于比较Na与Al金属性相对强弱的事实是____ 。
(5)⑧比⑦熔点高出很多,其理由是:____ ;①和②都属于离子晶体,但①比②的熔点高,请解释原因___ 。
| 编号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 物质 | Na2O | NaCl | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 熔点℃ | 920 | 801 | 1291 | 160 | -107 | 2072 | -57 | 1723 |
(1)上述涉及原子中最活泼非金属原子核外电子排布式是
 ,该阴离子核外电子占有的轨道总数是
,该阴离子核外电子占有的轨道总数是(2)物质①的电子式:
(3)④的熔沸点相较①、②、③低许多,说明其为
(4)不能用于比较Na与Al金属性相对强弱的事实是
| A.最高价氧化物对应水化物的碱性 | B.Na最外层1个电子而Al最外层3个电子 |
| C.单质与H2O反应的难易程度 | D.比较同浓度NaCl和AlCl3的pH值 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】秦始皇帝陵博物院首次在兵马俑的彩绘中发现了古人人工合成的“中国蓝”颜料。人们对这些颜料的研究发现,其成分主要是钡和铜的硅酸盐(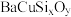 )。回答下列问题:
)。回答下列问题:
(1)基态Si原子的价电子排布式为___________ ,最高能级的电子云轮廓___________ 形。
(2)“中国紫”中存在 四面体结构,其中Si原子采取的杂化类型为
四面体结构,其中Si原子采取的杂化类型为___________ ;与 不同,
不同, 的立体构型为
的立体构型为___________ 。
(3)Si和C同主族,但 与
与 的熔沸点差异很大,这是因为
的熔沸点差异很大,这是因为 是
是___________ 晶体,而 是
是___________ 晶体。
(4) 的熔沸点
的熔沸点_____ 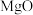 的熔沸点(填“
的熔沸点(填“ ”、“
”、“ ”、“
”、“ ”),原因是
”),原因是___________ 。
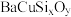 )。回答下列问题:
)。回答下列问题:(1)基态Si原子的价电子排布式为
(2)“中国紫”中存在
 四面体结构,其中Si原子采取的杂化类型为
四面体结构,其中Si原子采取的杂化类型为 不同,
不同, 的立体构型为
的立体构型为(3)Si和C同主族,但
 与
与 的熔沸点差异很大,这是因为
的熔沸点差异很大,这是因为 是
是 是
是(4)
 的熔沸点
的熔沸点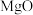 的熔沸点(填“
的熔沸点(填“ ”、“
”、“ ”、“
”、“ ”),原因是
”),原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】CrSi、GeGaAs、ZnGeAs2、聚吡咯、碳化硅和氧化亚铜都是重要的半导体化合物。请回答下列问题:
(1)基态铬原子的核外电子排布式为_______ ,其中未成对电子数为_______ 。
(2)GeGaAs中元素Ge、Ga、As的第一电离能从大到小的顺序为_______ 。ZnGeAs2中Zn、Ge、As的电负性从大到小的顺序为_______ 。
(3)聚吡咯的单体为吡咯( —H),该分子中氮原子的杂化轨道类型为
—H),该分子中氮原子的杂化轨道类型为_______ ;分子中σ键与π键的数目之比为_______ 。
(4)碳化硅、晶体硅及金刚石的熔点如下表:
分析熔点变化规律及其差异的原因:________ 。
(5)氧化亚铜的熔点为1 235 ℃,其固态时的单晶胞如图所示。

氧化亚铜属于_______ 晶体。
(1)基态铬原子的核外电子排布式为
(2)GeGaAs中元素Ge、Ga、As的第一电离能从大到小的顺序为
(3)聚吡咯的单体为吡咯(
 —H),该分子中氮原子的杂化轨道类型为
—H),该分子中氮原子的杂化轨道类型为(4)碳化硅、晶体硅及金刚石的熔点如下表:
| 物质 | 碳化硅 | 晶体硅 | 金刚石 |
| 熔点/℃ | 2 973 | 1 410 | 3 550~4 000 |
(5)氧化亚铜的熔点为1 235 ℃,其固态时的单晶胞如图所示。

氧化亚铜属于
您最近一年使用:0次



