世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,亚氯酸钠在3类致癌物清单中,但其在工业上可用作漂白剂、脱色剂、清毒剂、拔染剂等, 的一种生产工艺如下:
的一种生产工艺如下:
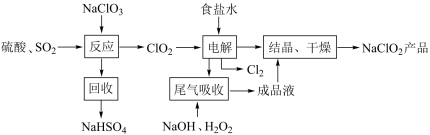
(1)写出“反应”步骤中生成 的化学反应方程式:
的化学反应方程式:_______ 。
(2)“电解所用食盐水由粗盐水精制而成,精制时为除去 ,加入的除杂试剂依次为
,加入的除杂试剂依次为_______ ,过滤后为得到纯净的 溶液还需加入
溶液还需加入_______ (以上填写相应物质的化学式)。设计除杂的实验方案时,除了要考虑所加试剂的种类,还要考虑_______ 。
(3)“电解”过程产生的 可用于工业制漂白液,写出工业制漂白液的化学方程式:
可用于工业制漂白液,写出工业制漂白液的化学方程式:_______ 。
(4)“尾气吸收”是吸收“电解”过程排出的少量 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为_______ ,该反应中氧化产物是_______ 。
(5)新冠流行期间,一种名叫“VB空气防护卡”成为了网红。商品介绍卡片中含有的主要活性成分—— 。在接触空气时可以释放安全可靠的低浓度
。在接触空气时可以释放安全可靠的低浓度 ,从而达到消除病毒、细菌活性的防护效果。有同学推测VB空气防护原理是因为。
,从而达到消除病毒、细菌活性的防护效果。有同学推测VB空气防护原理是因为。 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到
,同时得到 和钠的另一种正盐,试写出相应的化学反应方程式:
和钠的另一种正盐,试写出相应的化学反应方程式:_______ 。
 的一种生产工艺如下:
的一种生产工艺如下:
(1)写出“反应”步骤中生成
 的化学反应方程式:
的化学反应方程式:(2)“电解所用食盐水由粗盐水精制而成,精制时为除去
 ,加入的除杂试剂依次为
,加入的除杂试剂依次为 溶液还需加入
溶液还需加入(3)“电解”过程产生的
 可用于工业制漂白液,写出工业制漂白液的化学方程式:
可用于工业制漂白液,写出工业制漂白液的化学方程式:(4)“尾气吸收”是吸收“电解”过程排出的少量
 ,此吸收反应中,氧化剂与还原剂的物质的量之比为
,此吸收反应中,氧化剂与还原剂的物质的量之比为(5)新冠流行期间,一种名叫“VB空气防护卡”成为了网红。商品介绍卡片中含有的主要活性成分——
 。在接触空气时可以释放安全可靠的低浓度
。在接触空气时可以释放安全可靠的低浓度 ,从而达到消除病毒、细菌活性的防护效果。有同学推测VB空气防护原理是因为。
,从而达到消除病毒、细菌活性的防护效果。有同学推测VB空气防护原理是因为。 与空气中的
与空气中的 发生反应得到
发生反应得到 ,同时得到
,同时得到 和钠的另一种正盐,试写出相应的化学反应方程式:
和钠的另一种正盐,试写出相应的化学反应方程式:
更新时间:2023-05-24 00:07:40
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】某同学取海带灰加蒸馏水煮沸 ,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
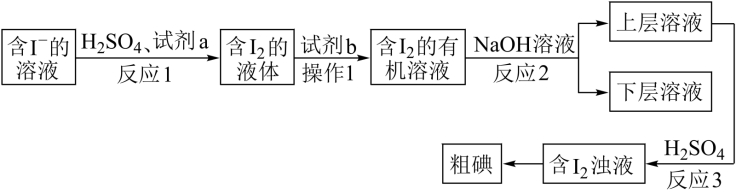
(1)反应1中硫酸的作用是提供酸性环境,则试剂a的作用是_______ 。
(2)试剂b应选择_______ (填标号)。
A.CCl4 B.酒精 C.醋酸
(3)操作1的名称是_______ 。实验室里进行操作1需要的玻璃仪器除烧杯外,还需要_______ ,有机层呈_______ 色
(4)反应2为3I2+6NaOH=5NaI+NaIO3+3H2O。此反应的氧化剂是_______ ,氧化产物是_______ 。
(5)反应3的离子方程式是_______ ,氧化产物和还原产物的物质的量之比_______
 ,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
,冷却,过滤,获得含I-的溶液,并设计如图所示实验方案,从中提取I2。
(1)反应1中硫酸的作用是提供酸性环境,则试剂a的作用是
(2)试剂b应选择
A.CCl4 B.酒精 C.醋酸
(3)操作1的名称是
(4)反应2为3I2+6NaOH=5NaI+NaIO3+3H2O。此反应的氧化剂是
(5)反应3的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】高铁酸钾(K2FeO4)是一种新型、高效、无毒的多功能水处理剂。查阅资料已知:K2FeO4为紫色固体,溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4
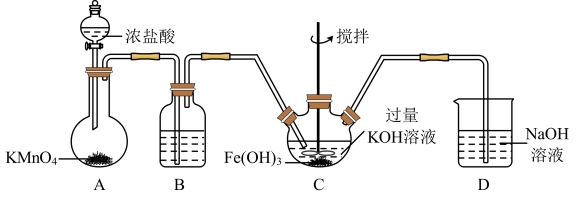
①在装置A中发生的化学反应中HCl显示出来的性质为___________ 。
②C为制备K2FeO4装置,写出次氯酸钾与氢氧化铁在碱性环境中反应的离子方程式:___________ 。
(2)探究K2FeO4的性质
取C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计如下方案:取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。由方案中溶液变红可知a中含有Fe3+,该离子的产生不能判断一定是由K2FeO4被Cl-还原而形成的,原因是___________ 。
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下: FeO
FeO +
+ H+=
H+= O2↑+
O2↑+ Fe3++
Fe3++ ___________
___________
①完成并配平上述离子方程式(方框内填化学计量数,横线上写物质)。___________
②现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为___________ 。(计算结果保留到0.1%)
(1)制备K2FeO4

①在装置A中发生的化学反应中HCl显示出来的性质为
②C为制备K2FeO4装置,写出次氯酸钾与氢氧化铁在碱性环境中反应的离子方程式:
(2)探究K2FeO4的性质
取C中浅紫红色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计如下方案:取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。由方案中溶液变红可知a中含有Fe3+,该离子的产生不能判断一定是由K2FeO4被Cl-还原而形成的,原因是
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:
 FeO
FeO +
+ H+=
H+= O2↑+
O2↑+ Fe3++
Fe3++ ___________
___________①完成并配平上述离子方程式(方框内填化学计量数,横线上写物质)。
②现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况)。则样品中高铁酸钾的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】以MnO2粉(含少量Fe3O4、CaO、MgO等杂质)和MnS(溶于酸,不溶于水)为原料制备MnSO4·H2O的过程如下:
(1)反应:将一定量MnO2粉和稀硫酸加入到如图所示实验装置的三颈烧瓶中,加热到90℃后开始加入MnS,并不断搅拌,充分反应。
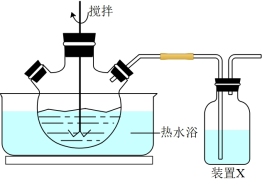
①三颈烧瓶中MnO2与MnS反应转化为Mn2+和S的离子方程式为_______ 。
②装置X中是NaOH溶液,作用是_______ 。
(2)除杂。查阅资料可知:
Ⅰ.常温下Ka(HF)=7.4×10-4。
Ⅱ.常温下Ksp(CaF2)=2.7×10−11,Ksp(MgF2)=6.5×10−9。
Ⅲ.有关氢氧化物开始沉淀和沉淀完全的pH如下表:
①将三颈烧瓶中的混合物过滤,加入MnF2将滤液中的Ca2+、Mg2+转化为沉淀除去。在Ca2+、Mg2+浓度相同的条件下,pH变化对钙镁去除率的影响如图所示。
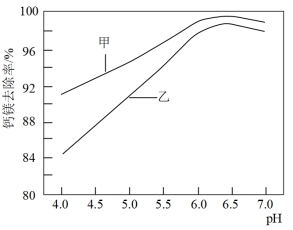
Mg2+去除率曲线为_______ (填写“甲”或“乙”)。随pH减小,钙镁去除率下降的原因是_______ 。
②以除去Ca2+、Mg2+所得的滤液为原料,制备MnSO4·H2O的实验方案:_______ ,控制温度在80~90℃之间蒸发结晶至有大量晶体出现,趁热过滤,用80~90℃的蒸馏水洗涤2~3次,干燥。(可选用的试剂:H2O2溶液、MnCO3固体、Na2CO3固体、蒸馏水等)。
(3)测定。准确称取0.3850 g MnSO4·H2O样品置于锥形瓶中,加入H3PO4和NH4NO3溶液,加热使Mn2+全部氧化成Mn3+,用0.1000 mol·L-1硫酸亚铁铵[Fe(NH4)2(SO4)2]标准溶液滴定至终点(滴定过程中Mn3+被还原为Mn2+),消耗标准溶液20.00 mL。计算MnSO4·H2O样品的纯度_______ (请写出计算过程)。
(1)反应:将一定量MnO2粉和稀硫酸加入到如图所示实验装置的三颈烧瓶中,加热到90℃后开始加入MnS,并不断搅拌,充分反应。

①三颈烧瓶中MnO2与MnS反应转化为Mn2+和S的离子方程式为
②装置X中是NaOH溶液,作用是
(2)除杂。查阅资料可知:
Ⅰ.常温下Ka(HF)=7.4×10-4。
Ⅱ.常温下Ksp(CaF2)=2.7×10−11,Ksp(MgF2)=6.5×10−9。
Ⅲ.有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 |
| 开始沉淀pH | 7.6 | 1.5 | 8.3 |
| 沉淀完全pH | 9.7 | 3.2 | 9.8 |

Mg2+去除率曲线为
②以除去Ca2+、Mg2+所得的滤液为原料,制备MnSO4·H2O的实验方案:
(3)测定。准确称取0.3850 g MnSO4·H2O样品置于锥形瓶中,加入H3PO4和NH4NO3溶液,加热使Mn2+全部氧化成Mn3+,用0.1000 mol·L-1硫酸亚铁铵[Fe(NH4)2(SO4)2]标准溶液滴定至终点(滴定过程中Mn3+被还原为Mn2+),消耗标准溶液20.00 mL。计算MnSO4·H2O样品的纯度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某化学兴趣小组用图甲装置制备了氯气,并进行了一系列实验。
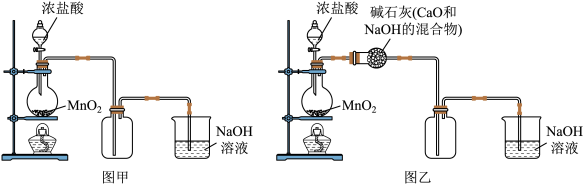
(1)实验室制备氯气的反应原理是___________ 。
(2)若有87gMnO2参加反应,则被氧化的氯化氢的物质的量为___________ ;而实际收集的氯气量总是比理论值小,试写出其可能的一种原因___________ 。
(3)乙同学认为图甲装置制备的氯气不纯净,其中混有HCl气体和水蒸气,对装置进行了如图乙改进。你认为合理吗?____ (合理则填入“合理”二字,如不合理则用文字说明理由)。
(4)将图甲装置合理改装后制取并收集一瓶氯气,将灼热的铁丝插到充满氯气的集气瓶中,看到铁丝在氯气中继续燃烧,在集气瓶内充满棕色的烟,烟的成分为_______ ,反应方程式为___________ 。

(1)实验室制备氯气的反应原理是
(2)若有87gMnO2参加反应,则被氧化的氯化氢的物质的量为
(3)乙同学认为图甲装置制备的氯气不纯净,其中混有HCl气体和水蒸气,对装置进行了如图乙改进。你认为合理吗?
(4)将图甲装置合理改装后制取并收集一瓶氯气,将灼热的铁丝插到充满氯气的集气瓶中,看到铁丝在氯气中继续燃烧,在集气瓶内充满棕色的烟,烟的成分为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】氯气、“84”消毒液、漂白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:
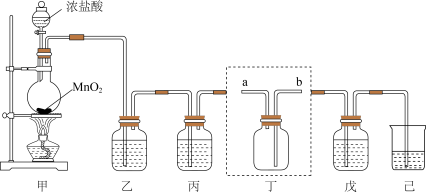
(1)盛装MnO2的仪器的名称为___________ ,装置甲中发生反应的化学方程式为___________ 。
(2)装置丁用来收集纯净且干燥的氯气,进气口为___________ (填a或b);装置丙盛装的试剂是___________ (填名称)。装置乙装的是饱和氯化钠溶液,能除去挥发出来的氯化氢外还能减少氯气的溶解度;请用文字和离子方程式解释还能减少氯气的溶解度的原因___________ 。
(3)将氯气通入装置己中制备“84”漂白液(NaClO),则装置己中发生反应的离子方程式为___________ 。
(4)装置戊中盛装石灰乳用来制备漂白粉[Ca(ClO)2],漂白粉长时间暴露在空气中容易发生变质的原因为___________ (结合化学方程式说明)。

(1)盛装MnO2的仪器的名称为
(2)装置丁用来收集纯净且干燥的氯气,进气口为
(3)将氯气通入装置己中制备“84”漂白液(NaClO),则装置己中发生反应的离子方程式为
(4)装置戊中盛装石灰乳用来制备漂白粉[Ca(ClO)2],漂白粉长时间暴露在空气中容易发生变质的原因为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】高铁酸钾K2FeO4是倍受关注的一类新型、高效、无毒的多功能水处理剂。实验室用如图所示装置先制备氯气,再制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备高效水处理剂K2FeO4。

(1)装置D的作用是_______ 。
(2)实验过程中,装置A观察到的实验现象是_______ 。
(3)装置C中发生的反应方程式为_______ 。
(4)若要制备K2FeO49.9 kg,计算所需Fe(NO3)3的质量______ (假设铁元素完全转化到产物中)

(1)装置D的作用是
(2)实验过程中,装置A观察到的实验现象是
(3)装置C中发生的反应方程式为
(4)若要制备K2FeO49.9 kg,计算所需Fe(NO3)3的质量
您最近一年使用:0次
【推荐1】为除去粗盐中的Ca2+、Mg2+、 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
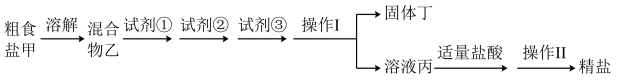
(1)操作Ⅰ需要用到的玻璃仪器有________ ,操作Ⅱ的名称是________ 。
(2)试剂①、②、③其实是三种物质:饱和Na2CO3溶液、BaCl2溶液、NaOH溶液,这三种物质的加入顺序可能有多种情况,下列选项中正确的是________ 。
A.饱和Na2CO3溶液、BaCl2溶液、NaOH溶液
B.BaCl2溶液、饱和Na2CO3溶液、NaOH溶液
C.NaOH溶液、BaCl2溶液、饱和Na2CO3溶液
D.饱和Na2CO3溶液、NaOH溶液、BaCl2溶液
(3)固体丁是混合物,除含有泥沙、CaCO3、BaSO4外,还含有________ (填化学式)。
(4)在混合物乙中分别加入试剂①、②、③的过程中,判断滴加BaCl2溶液已过量的方法是:加入BaCl2溶液后,静置,在上层清液中,________________ 。
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
(1)操作Ⅰ需要用到的玻璃仪器有
(2)试剂①、②、③其实是三种物质:饱和Na2CO3溶液、BaCl2溶液、NaOH溶液,这三种物质的加入顺序可能有多种情况,下列选项中正确的是
A.饱和Na2CO3溶液、BaCl2溶液、NaOH溶液
B.BaCl2溶液、饱和Na2CO3溶液、NaOH溶液
C.NaOH溶液、BaCl2溶液、饱和Na2CO3溶液
D.饱和Na2CO3溶液、NaOH溶液、BaCl2溶液
(3)固体丁是混合物,除含有泥沙、CaCO3、BaSO4外,还含有
(4)在混合物乙中分别加入试剂①、②、③的过程中,判断滴加BaCl2溶液已过量的方法是:加入BaCl2溶液后,静置,在上层清液中,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】海水的综合利用可以制备金属镁,其流程如图所示:
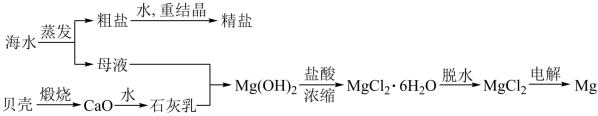
(1)写出下列变化的化学方程式,如该变化是离子反应,则写离子方程式:煅烧贝壳:__________________________________________ ; 与盐酸:
与盐酸:__________________________________ 。
(2)电解熔融 的反应方程式是
的反应方程式是_______________________________________ 。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发3个步骤的操作中都要用到玻璃棒,分别说明在这3种情况下使用玻璃棒的目的。
①溶解时:__________________________________________ 。
②过滤时:__________________________________________ 。
③蒸发时:__________________________________________ 。
(4)若在空气中加热 ,生成的是
,生成的是 和
和 ,写出相应反应的化学方程式:
,写出相应反应的化学方程式:_________________________________________ 。

(1)写出下列变化的化学方程式,如该变化是离子反应,则写离子方程式:煅烧贝壳:
 与盐酸:
与盐酸:(2)电解熔融
 的反应方程式是
的反应方程式是(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发3个步骤的操作中都要用到玻璃棒,分别说明在这3种情况下使用玻璃棒的目的。
①溶解时:
②过滤时:
③蒸发时:
(4)若在空气中加热
 ,生成的是
,生成的是 和
和 ,写出相应反应的化学方程式:
,写出相应反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】氢氧化铝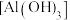 是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠
是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠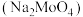 具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂
具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂 主要成分
主要成分 、
、 、
、 等
等 中回收
中回收 和
和 ,其工艺流程如图:
,其工艺流程如图:
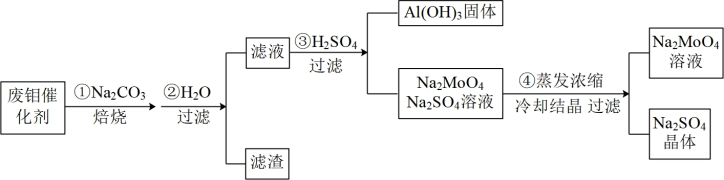
回答下列问题:
(1)已知 、
、 与
与 相似,均能在高温下跟
相似,均能在高温下跟 发生类似的反应,试写出①焙烧时
发生类似的反应,试写出①焙烧时 跟
跟 反应的化学方程式:
反应的化学方程式:___________ 。
(2)检验②操作后所得的滤渣中含有 的方法是:
的方法是:___________
(3)第③步操作中加入 需要适量,可以通过测定溶液
需要适量,可以通过测定溶液___________ 来控制 的用量。该步操作中制备
的用量。该步操作中制备 的离子方程式为
的离子方程式为___________
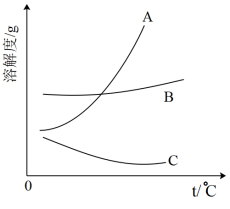
(4)从题目信息可知,下图曲线___________  填序号
填序号 为
为 的溶解度曲线。
的溶解度曲线。
(5)利用铝热反应可以回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得 。写出
。写出 发生铝热反应的化学方程式:
发生铝热反应的化学方程式:___________
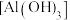 是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠
是重要的化工原料,也是用量最大和应用最广的无机阻燃添加剂,钼酸钠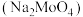 具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂
具有广泛的用途,可作新型阻燃剂、水处理剂和无公害型冷却水系统的金属抑制剂等。现从某废钼催化剂 主要成分
主要成分 、
、 、
、 等
等 中回收
中回收 和
和 ,其工艺流程如图:
,其工艺流程如图:
回答下列问题:
(1)已知
 、
、 与
与 相似,均能在高温下跟
相似,均能在高温下跟 发生类似的反应,试写出①焙烧时
发生类似的反应,试写出①焙烧时 跟
跟 反应的化学方程式:
反应的化学方程式:(2)检验②操作后所得的滤渣中含有
 的方法是:
的方法是:(3)第③步操作中加入
 需要适量,可以通过测定溶液
需要适量,可以通过测定溶液 的用量。该步操作中制备
的用量。该步操作中制备 的离子方程式为
的离子方程式为(4)从题目信息可知,下图曲线
 填序号
填序号 为
为 的溶解度曲线。
的溶解度曲线。
(5)利用铝热反应可以回收金属钼。将所得钼酸钠溶液用酸处理得到沉淀,再加热可得
 。写出
。写出 发生铝热反应的化学方程式:
发生铝热反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备KClO3和NaClO,并探究其氧化还原性质。
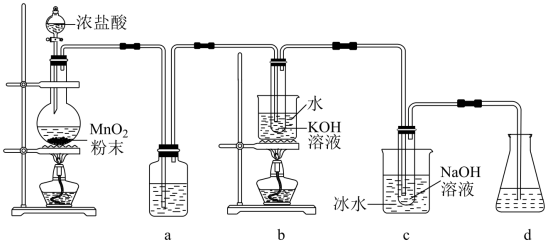
回答下列问题:
(1)盛放MnO2粉末的仪器名称是_______ ,a中的试剂为_______ 。
(2)b中反应的化学方程式为_______ 。
(3)c中反应的离子方程式是_______ ,采用冰水浴冷却的目的是_______ 。
(4)d中可选用试剂_______ (填标号)。

回答下列问题:
(1)盛放MnO2粉末的仪器名称是
(2)b中反应的化学方程式为
(3)c中反应的离子方程式是
(4)d中可选用试剂_______ (填标号)。
| A.Na2S溶液 | B.NaCl 溶液 | C.NaOH溶液 | D.H2SO4溶液 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】磁性纳米四氧化三铁在催化剂、DNA检测、疾病的诊断和治疗等领域应用广泛,其制备方法有多种,“共沉淀法”制备纳米 的流程如下:
的流程如下: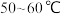 之间,生成
之间,生成 的离子方程式是
的离子方程式是___________ ,采用的加热方式为___________ 。
(2)操作Ⅲ分离 的方法为过滤,所需的玻璃仪器为
的方法为过滤,所需的玻璃仪器为___________ 。
(3)某同学依据上述“共沉淀法”的思路在实验室模拟制备纳米 为得到较纯净的纳米
为得到较纯净的纳米 ,
, 与
与 的个数之比最好为
的个数之比最好为___________ 。但实际操作时,却很难控制这一比例,原因是___________ 。
(4)经过多次实验发现,当混合溶液中 时,容易得到理想的纳米
时,容易得到理想的纳米 。烘干后再洗涤,检验纳米
。烘干后再洗涤,检验纳米 是否洗涤干净的实验方法是
是否洗涤干净的实验方法是_________ 。
(5)以太阳能为热源分解 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。
的过程如图所示。_________ 。
A.过程Ⅰ中 为氧化剂
为氧化剂
B.过程Ⅱ中 为氧化产物
为氧化产物
C.铁氧化合物循环制 具有节约能源、产物易分离等优点
具有节约能源、产物易分离等优点
②请写出反应Ⅱ对应的化学方程式_________ 。
 的流程如下:
的流程如下: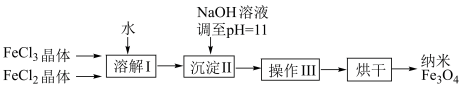
 之间,生成
之间,生成 的离子方程式是
的离子方程式是(2)操作Ⅲ分离
 的方法为过滤,所需的玻璃仪器为
的方法为过滤,所需的玻璃仪器为(3)某同学依据上述“共沉淀法”的思路在实验室模拟制备纳米
 为得到较纯净的纳米
为得到较纯净的纳米 ,
, 与
与 的个数之比最好为
的个数之比最好为(4)经过多次实验发现,当混合溶液中
 时,容易得到理想的纳米
时,容易得到理想的纳米 。烘干后再洗涤,检验纳米
。烘干后再洗涤,检验纳米 是否洗涤干净的实验方法是
是否洗涤干净的实验方法是(5)以太阳能为热源分解
 ,铁氧化合物循环分解水制
,铁氧化合物循环分解水制 的过程如图所示。
的过程如图所示。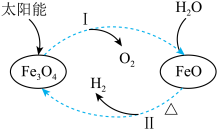
A.过程Ⅰ中
 为氧化剂
为氧化剂B.过程Ⅱ中
 为氧化产物
为氧化产物C.铁氧化合物循环制
 具有节约能源、产物易分离等优点
具有节约能源、产物易分离等优点②请写出反应Ⅱ对应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】安徽繁昌矿产资源十分丰富,其中峨山镇的随山主产辉铜矿。辉铜矿石主要含有硫化亚铜(Cu2S)、脉石(SiO2)和少量的银。孙村富铁矿业开发集团采用现代湿法炼铜工艺,用酸浸法从矿石中提取铜,其主要工艺流程图如下:

(1)矿泥的主要成分是_______ 。
(2)反应1中发生的离子方程式是_______ 。
(3)第一次萃取实验结束时,发现水层1的颜色仍然较蓝,接下来的操作是_______
(4)反萃取剂的作用是_______ 。
(5)反应2是用惰性电极电解水层2,写出阳极发生的反应方程式_______
(6)传统的湿法炼铜工艺是:粉碎矿石,先高温灼烧,加酸溶解产物,然后加入铁屑进一步得到铜。请评价两种工艺的优缺点_______

(1)矿泥的主要成分是
(2)反应1中发生的离子方程式是
(3)第一次萃取实验结束时,发现水层1的颜色仍然较蓝,接下来的操作是
(4)反萃取剂的作用是
(5)反应2是用惰性电极电解水层2,写出阳极发生的反应方程式
(6)传统的湿法炼铜工艺是:粉碎矿石,先高温灼烧,加酸溶解产物,然后加入铁屑进一步得到铜。请评价两种工艺的优缺点
您最近一年使用:0次



