芯片作为科技产业,以及信息化、数字化的基础,自诞生以来,就一直倍受关注, 也一直蓬勃发展。芯片制造会经过六个最为关键的步骤:沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。
(1)“沉积”是将导体、绝缘体或半导体材料薄膜沉积到纯硅晶圆上。GaN、GaAs是制造芯片的新型半导体材料。
①镓为第四周期元素,基态Ga原子的核外电子排布为:_______ ;
②GaN、GaP、 GaAs的结构类似于金刚石,熔点如表所示:试分析三者熔点变化的原因_______ 。
③将Mn掺杂到GaAs的晶体中替换部分Ga得到稀磁性半导体材料,晶体结构如下甲图。
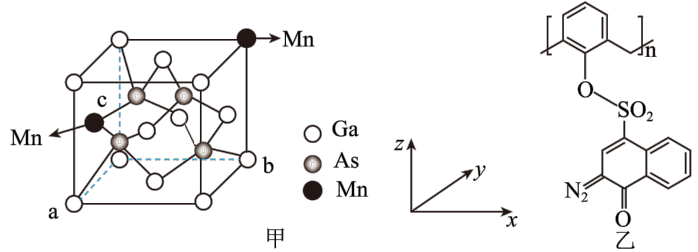
图中a、b的坐标为(0、0、0),(1、1、0),则c点Mn的原子坐标为_______ , 掺杂Mn之后,晶体中Mn、Ga、As的原子个数比为_______ 。
(2)“光刻胶涂覆”中用到一种701紫外正型光刻胶,结构如上图乙所示,其S的杂化方式为_______ 。
(3)“光刻”时,紫外负型光刻胶常含有-N3(叠氮基), 在紫外光下形成的阴离子 的等电子体有
的等电子体有______ (填化学式,任写一种),其空间构型为_______ 。
(4)“刻蚀”过程可能用到刻蚀剂HF, NH4BF4及清洗剂CH3CH(OH)CH3,三种物质中除H外的各元素的电负性由大到小的顺序为_______ , HF分子的极性_______ (填“大于”等于”或“小于”)HCl,1mol氟硼酸铵NH4BF4中含有_______ mol 配位键。
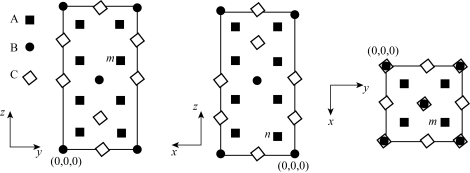
(5)一种Ag2HgI4固体导电材料为四方晶系,其晶胞参数为apm、apm 和2a pm,晶胞沿x、y、z的方向投影(如图所示),A、B、C表示三种不同原子的投影。其中代表Hg原子是_______ “A”、“B”、“C”)。设NA为阿伏加德罗常数的值,Ag2HgI4的摩尔质量为Mg·mol-1,该晶体的密_______ g·cm-3(用代数式表示)。
(1)“沉积”是将导体、绝缘体或半导体材料薄膜沉积到纯硅晶圆上。GaN、GaAs是制造芯片的新型半导体材料。
①镓为第四周期元素,基态Ga原子的核外电子排布为:
②GaN、GaP、 GaAs的结构类似于金刚石,熔点如表所示:试分析三者熔点变化的原因
| 物质 | GaN | GaP | GaAs |
| 熔点/°C | 1700 | 1480 | 1238 |

图中a、b的坐标为(0、0、0),(1、1、0),则c点Mn的原子坐标为
(2)“光刻胶涂覆”中用到一种701紫外正型光刻胶,结构如上图乙所示,其S的杂化方式为
(3)“光刻”时,紫外负型光刻胶常含有-N3(叠氮基), 在紫外光下形成的阴离子
 的等电子体有
的等电子体有(4)“刻蚀”过程可能用到刻蚀剂HF, NH4BF4及清洗剂CH3CH(OH)CH3,三种物质中除H外的各元素的电负性由大到小的顺序为
(5)一种Ag2HgI4固体导电材料为四方晶系,其晶胞参数为apm、apm 和2a pm,晶胞沿x、y、z的方向投影(如图所示),A、B、C表示三种不同原子的投影。其中代表Hg原子是

更新时间:2023-05-30 10:09:49
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】钛是一种稀有金属,具有密度小、强度高、耐腐蚀等特点,钛和钛的化合物在航天、化工、建筑、日常生活中都有着广泛的用途。已知:阿伏加德罗常数的值为 。
。
(1)基态钛原子价电子排布式为___________ ;与钛同周期的元素中,基态原子的未成对电子数与钛相同的还有___________ 种。
(2)钛的一种常见化合物是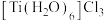 。
。 该物质中含有σ键的数目为
该物质中含有σ键的数目为___________ ,配体 的VSEPR模型名称是
的VSEPR模型名称是___________ ,其沸点高于 ,原因是
,原因是___________ 。
(3)常温下, 是易溶于
是易溶于 、易挥发的无色液体。
、易挥发的无色液体。 挥发过程中破坏的作用力类型是
挥发过程中破坏的作用力类型是___________ 。
(4) 的结构如图所示,
的结构如图所示, (IV)的配位数为
(IV)的配位数为___________ 。分子或离子中的大π键可用符号 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中大π键的可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中大π键的可表示为 ),则配体
),则配体 中含有的大π键应表示为
中含有的大π键应表示为___________ 。

(5)氮化钛( )晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体具有
)晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体具有 型结构,则该晶体中阳离子的配位数为
型结构,则该晶体中阳离子的配位数为___________ ;已知该晶体的晶胞参数为 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为___________  。
。
 。
。(1)基态钛原子价电子排布式为
(2)钛的一种常见化合物是
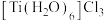 。
。 该物质中含有σ键的数目为
该物质中含有σ键的数目为 的VSEPR模型名称是
的VSEPR模型名称是 ,原因是
,原因是(3)常温下,
 是易溶于
是易溶于 、易挥发的无色液体。
、易挥发的无色液体。 挥发过程中破坏的作用力类型是
挥发过程中破坏的作用力类型是(4)
 的结构如图所示,
的结构如图所示, (IV)的配位数为
(IV)的配位数为 表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中大π键的可表示为
表示,其中m代表参与形成的大π键原子数,n代表参与形成的大π键电子数(如苯分子中大π键的可表示为 ),则配体
),则配体 中含有的大π键应表示为
中含有的大π键应表示为
(5)氮化钛(
 )晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体具有
)晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体具有 型结构,则该晶体中阳离子的配位数为
型结构,则该晶体中阳离子的配位数为 ,其晶体密度的计算表达式为
,其晶体密度的计算表达式为 。
。
您最近一年使用:0次
【推荐2】Ⅰ.氟在已知元素中电负性最大、非金属性最强,其单质在1886年才被首次分离出来。
(1)基态F原子的核外电子排布式为___________ 。
(2)氟氧化物O2F2、OF2的结构已经确定。
①依据数据推测O—O键的稳定性:O2F2___________ H2O2(填“>”或“<”)。
②OF2中F-O-F的键角小于H2O中H-O-H的键角,解释原因:___________ 。
(3)HF是一种有特殊性质的氢化物。
①已知:氢键(X—H···Y)中三原子在一条直线上时,作用力最强。测定结果表明,(HF)n固体中HF分子排列成锯齿形。画出含2个HF的重复单元结构:___________ 。
②HF中加入BF3可以解离出H2F+和具有正四面体形结构的阴离子,写出该过程的离子方程式:___________ 。
Ⅱ.金属冶炼过程中一种用有机化合物从水溶液中提取 的流程如下:
的流程如下: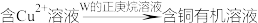
(4)有机化合物W的结构简式为:___________ 种,N、O杂化轨道类型分别为___________ 、___________ 。
(5)W可与 形成化合物Q,其结构如下所示:
形成化合物Q,其结构如下所示: 的价电子排布式为
的价电子排布式为___________ 。
②氢键对Q在水中溶解性的影响是___________ (填“增大”或“减小”)。
(1)基态F原子的核外电子排布式为
(2)氟氧化物O2F2、OF2的结构已经确定。
| O2F2 | H2O2 | |
| O—O键长/pm | 121 | 148 |
②OF2中F-O-F的键角小于H2O中H-O-H的键角,解释原因:
(3)HF是一种有特殊性质的氢化物。
①已知:氢键(X—H···Y)中三原子在一条直线上时,作用力最强。测定结果表明,(HF)n固体中HF分子排列成锯齿形。画出含2个HF的重复单元结构:
②HF中加入BF3可以解离出H2F+和具有正四面体形结构的阴离子,写出该过程的离子方程式:
Ⅱ.金属冶炼过程中一种用有机化合物从水溶液中提取
 的流程如下:
的流程如下: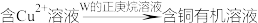
(4)有机化合物W的结构简式为:
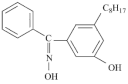
(5)W可与
 形成化合物Q,其结构如下所示:
形成化合物Q,其结构如下所示: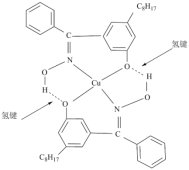
 的价电子排布式为
的价电子排布式为②氢键对Q在水中溶解性的影响是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。试回答下列问题:

(1)e原子的基态核外电子具有___________ 种不同的空间运动状态。
(2)第四周期基态o原子的价电子排布图为___________ 。
(3)p、q两元素的部分电离能数据列于下表:
比较两元素的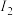 、
、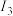 可知,气态
可知,气态 再失去一个电子比气态q2+再失去一个电子困难。对此,你的解释是
再失去一个电子比气态q2+再失去一个电子困难。对此,你的解释是___________ 。
(4)第3周期8种元素按单质熔点高低的顺序如图(Ⅰ)所示,其中电负性最大的是___________ (填Ⅰ图中的序号)。表中所列的某主族元素的电离能情况如图(Ⅱ)所示,则该元素是___________ (填元素名称)。

(5)a、d、l三种元素可形成一种离子化合物,其中的化学键类型除了离子键,还包括___________ ;与其中的阳离子互为等电子体的分子有___________ 。
(6)对于l元素的含氧酸来说,该元素的化合价越高,其含氧酸酸性越强的原因是__________________ 。

(1)e原子的基态核外电子具有
(2)第四周期基态o原子的价电子排布图为
(3)p、q两元素的部分电离能数据列于下表:
| 元素 | p | q | |
电离能/ | 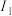 | 717 | 759 |
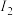 | 1509 | 1561 | |
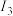 | 3248 | 2957 | |
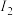 、
、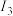 可知,气态
可知,气态 再失去一个电子比气态q2+再失去一个电子困难。对此,你的解释是
再失去一个电子比气态q2+再失去一个电子困难。对此,你的解释是(4)第3周期8种元素按单质熔点高低的顺序如图(Ⅰ)所示,其中电负性最大的是

(5)a、d、l三种元素可形成一种离子化合物,其中的化学键类型除了离子键,还包括
(6)对于l元素的含氧酸来说,该元素的化合价越高,其含氧酸酸性越强的原因是
您最近一年使用:0次
【推荐1】氢气的生产、存储是氢能应用的核心。目前较成熟的生产、存储路线之一为:利用CH3OH和H2O在某Cu/Zn-Al催化剂存在下生产H2,H2与Mg在一定条件下制得储氢物质X。
回答问题:。
(1)Al在周期表中的位置___________ 。基态Zn的价层电子排布式___________ 。
(2)水分了中氧原子的杂化轨道类型___________ 。
(3)键能是衡量共价键稳定性的参数之一、CH3OH键参数中有___________ 种键能数据。CH3OH可以与水以任意比例互溶的原因是__________ 。
(4)X的晶胞结构如图所示(晶胞参数:α =β =γ=90º,a=b=450.25 pm),密度为1.4 g·cm-3,X的储氢质量分数是___________ ,c= ___________ pm (列出计算式即可)。
(提示:晶胞结构,H-位于6个面上;Mg2+在立方体的中心和8个顶点)

回答问题:。
(1)Al在周期表中的位置
(2)水分了中氧原子的杂化轨道类型
(3)键能是衡量共价键稳定性的参数之一、CH3OH键参数中有
(4)X的晶胞结构如图所示(晶胞参数:α =β =γ=90º,a=b=450.25 pm),密度为1.4 g·cm-3,X的储氢质量分数是
(提示:晶胞结构,H-位于6个面上;Mg2+在立方体的中心和8个顶点)

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】G、M、R、X、Y、W、Q、T为原子序数依次增大的前四周期元素。G的一种简单粒子是一个质子,M基态原子L层中p轨道电子数是s轨道电子数的2倍,R原子K层的电子数与M层的电子数的乘积等于其L层的电子数,X和M是同主族元素,Y与X同周期且相邻,W是第一种过渡元素,Q位于第ⅠB族,T元素最高正价和最低负价的代数和为4.请回答下列问题:
(1)W的元素符号___________ ,Q在周期表中第___________ 列,T基态原子的简化电子排布式是___________ 。
(2)X与M形成的XM3分子的VSEPR模型是_______ ,GYM的电子式为________ 。
(3)R、T均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,中心原子杂化类型___________ (填“相同”或“不相同”)。
(4)已知高温下4QM→2Q2M+M2,从Q原子价层电子结构的角度分析,能生成Q2M的原因是___________ 。
(5)已知AlY3通常以二聚体(Al2Y6)形式存在,画出其二聚体的结构式___________ (标出配位键)。
(1)W的元素符号
(2)X与M形成的XM3分子的VSEPR模型是
(3)R、T均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,中心原子杂化类型
(4)已知高温下4QM→2Q2M+M2,从Q原子价层电子结构的角度分析,能生成Q2M的原因是
(5)已知AlY3通常以二聚体(Al2Y6)形式存在,画出其二聚体的结构式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】雷氏盐是一种铬的配合物(结构简式如图1),常用作分析试剂,制备反应为 (雷氏盐)
(雷氏盐) 。回答下列相关问题:
。回答下列相关问题:

(1) 的核外电子排布式为
的核外电子排布式为______ ;其基态原子核外电子的空间运动状态有______ 种;氟和氯处于同一主族, 的熔点为1100℃,
的熔点为1100℃, 的熔点为83℃,前者比后者高得多,是因为
的熔点为83℃,前者比后者高得多,是因为______ 。
(2)雷氏盐中与铬形成配位键的原子是______ ;中心原子的配位数为______ 。
(3) 中氮原子的杂化方式为
中氮原子的杂化方式为______ ,其立体构型的名称为______ 。
(4) 所含元素中电负性最小的是
所含元素中电负性最小的是______ (填元素符号,下同),它们的基态原子的第一电离能最大的是______ 。
(5)金属铬的晶胞结构如图2所示,设晶胞边长为 ,则铬的原子半径为
,则铬的原子半径为______  。
。
 (雷氏盐)
(雷氏盐) 。回答下列相关问题:
。回答下列相关问题:
(1)
 的核外电子排布式为
的核外电子排布式为 的熔点为1100℃,
的熔点为1100℃, 的熔点为83℃,前者比后者高得多,是因为
的熔点为83℃,前者比后者高得多,是因为(2)雷氏盐中与铬形成配位键的原子是
(3)
 中氮原子的杂化方式为
中氮原子的杂化方式为(4)
 所含元素中电负性最小的是
所含元素中电负性最小的是(5)金属铬的晶胞结构如图2所示,设晶胞边长为
 ,则铬的原子半径为
,则铬的原子半径为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某化学小组同学利用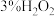 溶液制
溶液制 ,再用
,再用 氧化
氧化 ,并检验氧化产物。
,并检验氧化产物。
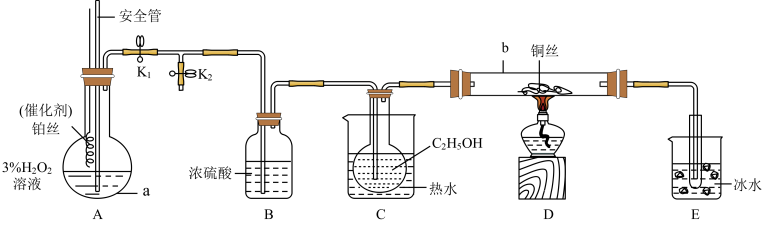
(1)仪器b中发生反应的化学方程式为_______ 。
(2)C和E两个水浴作用不相同,其中E中冰水的作用是_______ 。
(3)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
实验①~③中的结论不合理的是_______ (填序号),原因是_______ 。
(4)化合物的分子中采取 杂化方式成键的原子数目是
杂化方式成键的原子数目是_______ 个。
(5)氮化钛晶体的晶胞结构如图所示,则氮化钛晶体化学式为_______ ,该晶体结构中与N原子距离最近且相等的N原子有_______ 个;该晶胞的密度 ,则晶胞结构中两个氮原子之间的最近距离为
,则晶胞结构中两个氮原子之间的最近距离为_______ 。(NA为阿伏加德罗常数的数值,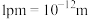 ,只列计算式)。
,只列计算式)。

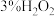 溶液制
溶液制 ,再用
,再用 氧化
氧化 ,并检验氧化产物。
,并检验氧化产物。
(1)仪器b中发生反应的化学方程式为
(2)C和E两个水浴作用不相同,其中E中冰水的作用是
(3)为检验上述实验收集到的产物,该小组同学进行了如下实验并得出相应结论。
| 实验序号 | 检验试剂和反应条件 | 现象 | 结论 |
| ① | 酸性 溶液 溶液 | 紫红色褪去 | 产物含有乙醛 |
| ② | 新制 加热 加热 | 生成砖红色沉淀 | 产物含有乙醛 |
| ③ | 微红色含酚酞的NaOH溶液 | 微红色褪去 | 产物可能含有乙酸 |
(4)化合物的分子中采取
 杂化方式成键的原子数目是
杂化方式成键的原子数目是
(5)氮化钛晶体的晶胞结构如图所示,则氮化钛晶体化学式为
 ,则晶胞结构中两个氮原子之间的最近距离为
,则晶胞结构中两个氮原子之间的最近距离为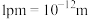 ,只列计算式)。
,只列计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】工业中可利用生产钛白的副产物 和硫铁矿
和硫铁矿 联合制备铁精粉(
联合制备铁精粉( )和硫酸,实现能源及资源的有效利用。
)和硫酸,实现能源及资源的有效利用。
(1) 结构示意图如图。
结构示意图如图。

①铁元素常见的化合价有+2和+3价, 比
比 稳定的因:
稳定的因:________ 。
②下列粒子的中心原子杂化方式与 中S的杂化方式相同的是:
中S的杂化方式相同的是:
A.HCN B. C.
C. D.
D.
③ 中Fe(Ⅱ)的配位数是
中Fe(Ⅱ)的配位数是_______ , 与
与 的作用力类型是
的作用力类型是_________ 。
(2) 晶体的晶胞形状为立方体,结构如图。
晶体的晶胞形状为立方体,结构如图。
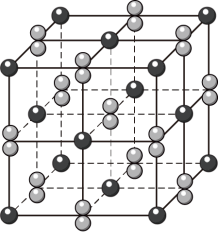
①距离 最近的阳离子有
最近的阳离子有___________ 个, 位于
位于 所形成的
所形成的___________ (填“正四面体”或“正八面体”)空隙。
② 晶体的晶胞参数为a nm,密度为
晶体的晶胞参数为a nm,密度为 ,
, 的摩尔质量为M
的摩尔质量为M  ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
___________ (用含a、ρ、M的代数式表示)。
(3) 加热脱水后生成
加热脱水后生成 ,再与
,再与 在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收
在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收 制得发烟硫酸(化学组成可表示为
制得发烟硫酸(化学组成可表示为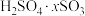 ),可生产
),可生产 质量分数为40%的发烟硫酸
质量分数为40%的发烟硫酸___________ 吨。
 和硫铁矿
和硫铁矿 联合制备铁精粉(
联合制备铁精粉( )和硫酸,实现能源及资源的有效利用。
)和硫酸,实现能源及资源的有效利用。(1)
 结构示意图如图。
结构示意图如图。
①铁元素常见的化合价有+2和+3价,
 比
比 稳定的因:
稳定的因:②下列粒子的中心原子杂化方式与
 中S的杂化方式相同的是:
中S的杂化方式相同的是:A.HCN B.
 C.
C. D.
D.
③
 中Fe(Ⅱ)的配位数是
中Fe(Ⅱ)的配位数是 与
与 的作用力类型是
的作用力类型是(2)
 晶体的晶胞形状为立方体,结构如图。
晶体的晶胞形状为立方体,结构如图。
①距离
 最近的阳离子有
最近的阳离子有 位于
位于 所形成的
所形成的②
 晶体的晶胞参数为a nm,密度为
晶体的晶胞参数为a nm,密度为 ,
, 的摩尔质量为M
的摩尔质量为M  ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
(3)
 加热脱水后生成
加热脱水后生成 ,再与
,再与 在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收
在氧气中掺烧可联合制备铁精粉和硫酸。硫酸工业中,用98%的浓硫酸a吨吸收 制得发烟硫酸(化学组成可表示为
制得发烟硫酸(化学组成可表示为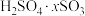 ),可生产
),可生产 质量分数为40%的发烟硫酸
质量分数为40%的发烟硫酸
您最近一年使用:0次
【推荐3】碱式磷酸钙[Ca10(PO4)6(OH)2],工业上叫羟基磷灰石或羟磷灰石,是人的牙齿中比较坚硬的物质,在水中有微弱的溶解,这是牙齿损坏的主要原因。氟磷酸钙也称氟磷灰石,它的化学式为Ca10(PO4)6F2,是牙表面牙釉的主要成分。
回答下列问题:
(1)基态钙原子的价层电子排布式为____________ 。基态磷原子的未成对电子数为______________ 。
(2)碱式磷酸钙中含氧酸根离子的中心原子杂化类型是______________________ ,含氧酸根离子的空间构型为______________ 。
(3)氢氟酸溶液中存在:2HF H2F2,H2F2为一元酸,则氢氟酸溶液中含氟阴离子是
H2F2,H2F2为一元酸,则氢氟酸溶液中含氟阴离子是______________ (填离子符号)。氢氟酸中存在H2F2的原因是______________________________________________ 。与H2F+互为等电子体的分子是________________ (写出一个即可)。
(4)O、F、P的电负性由小到大的顺序为______________ 。
(5)NH3和PH3的构型相似,NH3的键角略大于PH3,从原子结构角度解释其原因:________________ 。
(6)CaF2晶胞如图所示。位于体内的粒子的配位数为______________ 。

已知:氟化钙晶体密度为ρ g·cm-3,NA代表阿伏伽德罗常数的值。
氟化钙晶体中Ca2+和F-之间最近核间距(d)为______________ pm(只要求列出计算式即可)。
回答下列问题:
(1)基态钙原子的价层电子排布式为
(2)碱式磷酸钙中含氧酸根离子的中心原子杂化类型是
(3)氢氟酸溶液中存在:2HF
 H2F2,H2F2为一元酸,则氢氟酸溶液中含氟阴离子是
H2F2,H2F2为一元酸,则氢氟酸溶液中含氟阴离子是(4)O、F、P的电负性由小到大的顺序为
(5)NH3和PH3的构型相似,NH3的键角略大于PH3,从原子结构角度解释其原因:
(6)CaF2晶胞如图所示。位于体内的粒子的配位数为

已知:氟化钙晶体密度为ρ g·cm-3,NA代表阿伏伽德罗常数的值。
氟化钙晶体中Ca2+和F-之间最近核间距(d)为
您最近一年使用:0次



