将 转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人
转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 的浓度随时间变化如表所示。
的浓度随时间变化如表所示。
(1)从0min到6min,
___________  。
。
(2)能说明上述反应达到平衡状态的是___________(填标号)。
(3)上述反应10min时,混合气体中 的物质的量分数为
的物质的量分数为___________ %。(取整数)
(4)上述反应12min末时,混合气体中 和
和 的质量之比是
的质量之比是___________ 。
(5)第3min时的
___________ (填“>”、“<”、“=”或“无法比较”)第9min时的 。
。
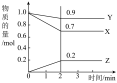
(6)在恒温条件下,若将一定量X和Y的混合气体通入容积为2L的恒容密闭容器中,发生反应 ,X和
,X和 两种物质的浓度随时间的变化情况如表所示。
两种物质的浓度随时间的变化情况如表所示。
①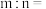
___________ 。
②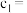
___________  。(保留两位有效数字)
。(保留两位有效数字)
③若反应在第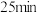 时改变某种条件,则
时改变某种条件,则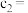
___________  。
。
 转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人
转化成有机物可有效实现碳循环。在体积为2L的恒温恒容密闭容器中,充人 和
和 ,一定条件下发生反应:
,一定条件下发生反应: ,测得
,测得 和
和 的浓度随时间变化如表所示。
的浓度随时间变化如表所示。时间 | 0 | 3 | 6 | 9 | 12 |
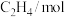 | 0 | 0.25 | 0.32 | 0.37 | 0.37 |
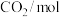 | 1 | 0.50 | 0.36 | 0.26 | 0.26 |

 。
。(2)能说明上述反应达到平衡状态的是___________(填标号)。
A.反应中 与 与 的物质的量浓度之比为 的物质的量浓度之比为 |
| B.混合气体的压强不随时间的变化而变化 |
C.单位时间内生成 ,同时生成 ,同时生成 |
| D.混合气体的平均相对分子质量不随时间的变化而变化 |
 的物质的量分数为
的物质的量分数为(4)上述反应12min末时,混合气体中
 和
和 的质量之比是
的质量之比是(5)第3min时的

 。
。(6)在恒温条件下,若将一定量X和Y的混合气体通入容积为2L的恒容密闭容器中,发生反应
 ,X和
,X和 两种物质的浓度随时间的变化情况如表所示。
两种物质的浓度随时间的变化情况如表所示。时间 | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 |
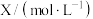 | 0.2 |  | 0.6 | 0.6 | 0.6 | 0.9 |  |  |
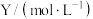 | 0.6 |  | 0.4 | 0.4 | 0.4 | 0.4 | 0.5 | 0.5 |
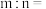
②
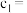
 。(保留两位有效数字)
。(保留两位有效数字)③若反应在第
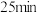 时改变某种条件,则
时改变某种条件,则
 。
。
更新时间:2023-05-30 14:47:47
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】CH3OH也可由CO2和H2合成。在体积为1L的密闭容器中,充入lmolCO2和3molH2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:___________ mol/(L·min)。
(2)10min时,CH3OH的物质的量为___________ mol,10min内,以H2表示的化学反应速率是___________ mol/(L·min)。
(3)到达平衡时,CO2的转化率为___________ 。
(4)3min时,v(正)___________ v(逆)(填“大于”、“等于”、“小于”),此时化学反应朝___________ 进行(填“正方向”或“逆方向”)。
 CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)浓度随时间变化如图所示:
(2)10min时,CH3OH的物质的量为
(3)到达平衡时,CO2的转化率为
(4)3min时,v(正)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】化学反应速率与生活、生产密切相关。
(1)为研究催化剂对H2O2分解反应速率的影响,某小组同学进行了如下实验:
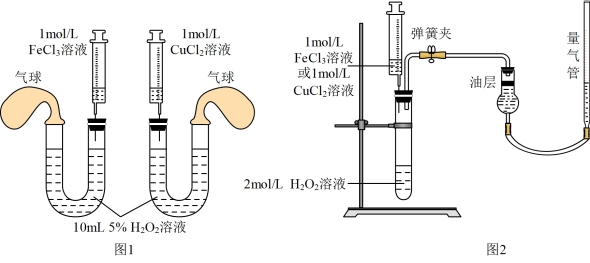
①定性研究:小组同学用图1装置进行实验,在注射器中分别加入相同体积的1mol/LFeCl3溶液和1mol/LCuCl2溶液,可通过观察___________ ,确定反应速率的大小。某同学提出用相同体积1mol/LCuSO4溶液代替1mol/LCuCl2溶液做实验,你认为是否合理及理由是___________ 。
②定量研究:为了更精确地研究催化剂对反应速率的影响,小组同学利用图2装置进行定量实验。向大试管中加入100mL2mol/L的H2O2溶液,向注射器中分别加入1mol/LCuCl2溶液和1mol/LFeCl3溶液,平行进行两次实验,测定的数据是___________ ,比较催化剂对反应速率的影响。若5min末得到标准状况下1.12L气体,忽略反应过程中溶液体积的变化,计算H2O2的分解反应速率为___________ 。
(2)一定条件下,在2L恒容容器中发生反应:2C(s)+2NO2(g) N2(g)+2CO2(g)。开始时加入2molNO2、3molC,在2min末测得N2的物质的量为0.4mol,2min~7min内N2和NO2的物质的量浓度的变化曲线如图所示。
N2(g)+2CO2(g)。开始时加入2molNO2、3molC,在2min末测得N2的物质的量为0.4mol,2min~7min内N2和NO2的物质的量浓度的变化曲线如图所示。
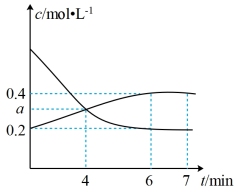
①在2min内,v(CO2)=___________ 。
②图3中,a=___________ (计算结果保留两位有效数字)。
③7min时,混合气体的平均相对分子质量为___________ (计算结果保留三位有效数字)。
(1)为研究催化剂对H2O2分解反应速率的影响,某小组同学进行了如下实验:

①定性研究:小组同学用图1装置进行实验,在注射器中分别加入相同体积的1mol/LFeCl3溶液和1mol/LCuCl2溶液,可通过观察
②定量研究:为了更精确地研究催化剂对反应速率的影响,小组同学利用图2装置进行定量实验。向大试管中加入100mL2mol/L的H2O2溶液,向注射器中分别加入1mol/LCuCl2溶液和1mol/LFeCl3溶液,平行进行两次实验,测定的数据是
(2)一定条件下,在2L恒容容器中发生反应:2C(s)+2NO2(g)
 N2(g)+2CO2(g)。开始时加入2molNO2、3molC,在2min末测得N2的物质的量为0.4mol,2min~7min内N2和NO2的物质的量浓度的变化曲线如图所示。
N2(g)+2CO2(g)。开始时加入2molNO2、3molC,在2min末测得N2的物质的量为0.4mol,2min~7min内N2和NO2的物质的量浓度的变化曲线如图所示。
①在2min内,v(CO2)=
②图3中,a=
③7min时,混合气体的平均相对分子质量为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】为倡导“节能减排”和“低碳经济”,降低大气中CO2含量及有效地开发利用CO2,工业上可用CO2来生产燃料甲醇。在体积为2L的密闭容器中,充入1molCO2、3molH2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
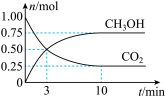
(1)写出该反应的化学平衡常数表达式:K=________ 。
(2)在3min末,反应速率v(正)________ v(逆)(选填>、<或=)。
(3)从反应开始到平衡,平均反应速率v(CO2)=_________ 。达到平衡时,H2的转化率为________ 。
(4)下列措施可以加快反应速率的是________ 。
(5)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为:甲:v(H2)=0.45mol•L-1•s-1;乙:v(CO2)=0.2mol•L-1•s-1;丙:v(CH3OH)=6mol•L-1•min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为________ 。
 CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
CH3OH(g)+H2O(g)。经测得CO2和CH3OH的物质的量随时间变化如图所示。
(1)写出该反应的化学平衡常数表达式:K=
(2)在3min末,反应速率v(正)
(3)从反应开始到平衡,平均反应速率v(CO2)=
(4)下列措施可以加快反应速率的是
| A.升高温度 | B.加入催化剂 | C.增大压强 | D.及时分离出CH3OH |
(5)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为:甲:v(H2)=0.45mol•L-1•s-1;乙:v(CO2)=0.2mol•L-1•s-1;丙:v(CH3OH)=6mol•L-1•min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g) 2NO(g) △H>0,已知该反应在T℃时,平衡常数K=9.0。请回答:
2NO(g) △H>0,已知该反应在T℃时,平衡常数K=9.0。请回答:
(1)该反应的平衡常数表达式为:K=_______ 。
(2)某温度下,向2L的密闭容器中充入N2和O2各1mol,5s后O2的物质的量为0.4mol,则0~5s内NO的反应速率_______ mol•L-1•min-1。
(3)下列为4种不同情况下测得的反应速率中,表明该反应进行最快的是_______ 。
(4)将N2、O2混合充入恒温恒容密闭容器中,下列变化趋势正确的是_______ (填字母序号)。
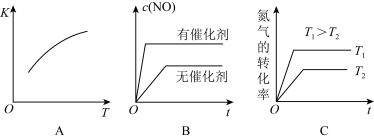
(5)T℃时,某时刻测得容器内N2、O2、NO的浓度分别为0.20mol/L,0.20mol/L和0.50mol/L,此时反应v正(N2)______ v逆(N2)(填“>”、“=”或“<”)原因为______ 。
 2NO(g) △H>0,已知该反应在T℃时,平衡常数K=9.0。请回答:
2NO(g) △H>0,已知该反应在T℃时,平衡常数K=9.0。请回答:(1)该反应的平衡常数表达式为:K=
(2)某温度下,向2L的密闭容器中充入N2和O2各1mol,5s后O2的物质的量为0.4mol,则0~5s内NO的反应速率
(3)下列为4种不同情况下测得的反应速率中,表明该反应进行最快的是
| A.v(N2)=0.4mol•L-1•min-1 | B.v(NO)=0.6mol•L-1•min-1 |
| C.v(O2)=0.3mol•L-1•s-1 | D.v(NO)=0.4mol•L-1•s-1 |
(4)将N2、O2混合充入恒温恒容密闭容器中,下列变化趋势正确的是

(5)T℃时,某时刻测得容器内N2、O2、NO的浓度分别为0.20mol/L,0.20mol/L和0.50mol/L,此时反应v正(N2)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
①反应速率最大的时间段是_______ min(填“0~1”“1~2”“2~3”“3~4”或“4~5”)。
②某学生为防止反应过快难以测量氢气体积,他事先在盐酸中加入一定量的下列溶液以减慢反应速率,你认为不可行的是_______ (填字母)。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(2)某温度下在4 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
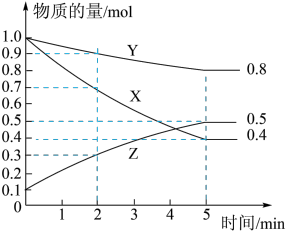
①该反应的化学方程式是_______ 。
②5 min内,X的转化率为_______ ;Z的平均反应速率v(Z)=_______ 。3min时的v正(X)与5min时的v逆(X)的大小关系为:v正(X)_______ v逆(X)(填“>”“<”或“=”)。
③上述反应在不同条件下进行,测得速率如下,该反应速率由快到慢的顺序为_______ 。
a.v(X)=0.2 mol·L-1·min-1 b.v(Y)=0.3 mol·L-1·min-1 c.v(Z)=0.005 mol·L-1·s-1
④下列条件的改变不能减慢上述反应速率的是_______ (填序号,下同)。
a.降低温度 b.分离产物 c.保持压强不变充入He d.保持容积不变充入He
⑤该反应达到平衡状态的标志是_______ (填字母)。
AY的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内混合气体的平均密度保持不变
E.生成1 mol Y的同时消耗2 mol Z
F.平均相对分子质量保持不变
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400 mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL(标准状况) | 100 | 240 | 464 | 576 | 620 |
②某学生为防止反应过快难以测量氢气体积,他事先在盐酸中加入一定量的下列溶液以减慢反应速率,你认为不可行的是
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(2)某温度下在4 L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②5 min内,X的转化率为
③上述反应在不同条件下进行,测得速率如下,该反应速率由快到慢的顺序为
a.v(X)=0.2 mol·L-1·min-1 b.v(Y)=0.3 mol·L-1·min-1 c.v(Z)=0.005 mol·L-1·s-1
④下列条件的改变不能减慢上述反应速率的是
a.降低温度 b.分离产物 c.保持压强不变充入He d.保持容积不变充入He
⑤该反应达到平衡状态的标志是
AY的体积分数在混合气体中保持不变
B.X、Y的反应速率比为3∶1
C.容器内气体压强保持不变
D.容器内混合气体的平均密度保持不变
E.生成1 mol Y的同时消耗2 mol Z
F.平均相对分子质量保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
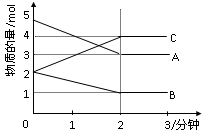
【推荐1】某可逆反应从0—2分钟进行过程中, 在不同反应时 间各物质的量的变化情况如下图所示。则该反应的的反应物是______ ,生成物是_______ ,化学方程式为_____________________________ ;反应开始至2分钟时,能否用C表示反应速率?若能,其反应速率为______________ ,若不能,则其原因为________________________________________________________ ;2分钟后A、B、C各物质的量不再随时间的变化而变化,说明在这个条件下,反应已达到了___________ 状态。

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】化学平衡状态的建立
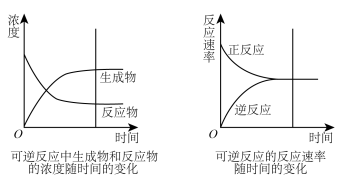
在反应物转化为生成物的一瞬间,___________ 开始进行。
反应开始时,反应物的浓度___________ ,正反应速率___________ ,由于生成物浓度很小,逆反应速率很小。
随着反应的进行,反应物浓度逐渐___________ ,正反应速率随着反应物浓度的___________ 逐渐___________ ;生成物浓度逐渐___________ ,逆反应速率随着生成物浓度的___________ 不断___________ 。当正反应速率与逆反应速率相等时,达到一种___________ 状态,反应物的浓度和生成物的浓度___________ ,正反应和逆反应都___________ 。

在反应物转化为生成物的一瞬间,
反应开始时,反应物的浓度
随着反应的进行,反应物浓度逐渐
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
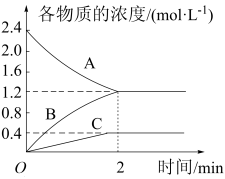
(1)该反应的化学方程式为__ 。
(2)从开始至2min,B的平均反应速率为__ 。
(3)下列叙述能说明该反应已达到化学平衡状态的是(填标号)__ 。
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗3nmolA,同时消耗nmol的B
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
(4)在某一时刻采取下列措施能使该反应速率减小的是___ 。
A.加催化剂
B.降低温度
C.体积不变,充入A
D.体积不变,从容器中分离出A
(5)改变影响平衡的一个条件,5分钟后又建立了新平衡,发现C占平衡混合气的体积分数为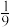 ,则反应物A的分解率为
,则反应物A的分解率为___ 。

(1)该反应的化学方程式为
(2)从开始至2min,B的平均反应速率为
(3)下列叙述能说明该反应已达到化学平衡状态的是(填标号)
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗3nmolA,同时消耗nmol的B
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
(4)在某一时刻采取下列措施能使该反应速率减小的是
A.加催化剂
B.降低温度
C.体积不变,充入A
D.体积不变,从容器中分离出A
(5)改变影响平衡的一个条件,5分钟后又建立了新平衡,发现C占平衡混合气的体积分数为
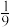 ,则反应物A的分解率为
,则反应物A的分解率为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】t℃时,在体积为2L的密闭容器中(容积不变)通入3mol和1molB,发生反应3A(g)+B(g)⇌xC(g);经过2min的时间该反应达到平衡状态(假设温度不变),剩余的B的物质的量为0.8mol并测得C的浓度为0.4 mol▪L-1
请回答下列问题:
(1)整个反应过程中,B的平均反应速率为______________
(2)x=_______ ,平衡常数K=_______ .
(3)如果向该平衡体系中通入少量氮气、增大反应体系的压强,那么化学平衡的移动方向是____________ .
(4)若温度不变,再向原平衡混合物的容器中充人amolC在t℃时达到新的平衡,此时B的物质的量为nmol,则C的物质的量为_____ (用含n的表达式表示),平衡常数K______ (填“增大”“减小”或不变”)
请回答下列问题:
(1)整个反应过程中,B的平均反应速率为
(2)x=
(3)如果向该平衡体系中通入少量氮气、增大反应体系的压强,那么化学平衡的移动方向是
(4)若温度不变,再向原平衡混合物的容器中充人amolC在t℃时达到新的平衡,此时B的物质的量为nmol,则C的物质的量为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、硫氧化物显得尤为重要。
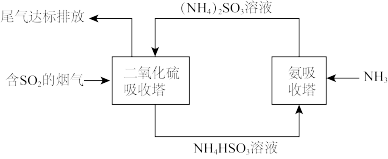
I.某企业利用下列流程综合处理工厂排放的含有 的烟气,以减少其对环境造成的污染。试回答下列问题:
的烟气,以减少其对环境造成的污染。试回答下列问题:
(1)二氧化硫吸收塔中发生反应的化学方程式为_______ 。
(2)氨吸收塔中发生反应的离子方程式为_______ 。
(3)一定条件下,通过下列反应可实现燃煤烟气中硫的回收: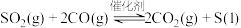 ,该反应的能量变化如图所示。
,该反应的能量变化如图所示。
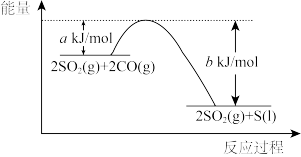
①该反应为_______ (填“放热”或“吸热”)反应。
②如果要提高该反应的反应速率,可以采取的措施是_______ (选填编号)
A.减压 B.增加 的浓度 C.升温 D.及时移出产物
的浓度 C.升温 D.及时移出产物
II.用活性炭还原法处理氮氧化物。有关反应为: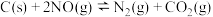 某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入
某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入 和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
(4)①表中b=_______ ,计算T1℃时 内,用
内,用 浓度增加来表示该反应的平均速率
浓度增加来表示该反应的平均速率_______ 。
②下列各项能判断该反应达到平衡状态的是_______ (填序号字母)。
A.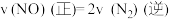 B.容器内
B.容器内 和
和 的体积比为
的体积比为
C.混合气体的平均相对分子质量保持不变 D.容器内压强保持不变

I.某企业利用下列流程综合处理工厂排放的含有
 的烟气,以减少其对环境造成的污染。试回答下列问题:
的烟气,以减少其对环境造成的污染。试回答下列问题:(1)二氧化硫吸收塔中发生反应的化学方程式为
(2)氨吸收塔中发生反应的离子方程式为
(3)一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
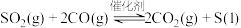 ,该反应的能量变化如图所示。
,该反应的能量变化如图所示。
①该反应为
②如果要提高该反应的反应速率,可以采取的措施是
A.减压 B.增加
 的浓度 C.升温 D.及时移出产物
的浓度 C.升温 D.及时移出产物II.用活性炭还原法处理氮氧化物。有关反应为:
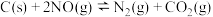 某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入
某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入 和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:| 时间/min | NO物质的量(mol) |  物质的量(mol) 物质的量(mol) |  物质的量(mol) 物质的量(mol) |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | a | a |
| 20 | b | 0.60 | 0.60 |
| 30 | b | 0.60 | 0.60 |
 内,用
内,用 浓度增加来表示该反应的平均速率
浓度增加来表示该反应的平均速率②下列各项能判断该反应达到平衡状态的是
A.
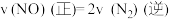 B.容器内
B.容器内 和
和 的体积比为
的体积比为
C.混合气体的平均相对分子质量保持不变 D.容器内压强保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:

(1)写出该反应的化学方程式__________ 。
(2)计算反应开始到10 s,用X表示的反应速率是__________ ,Y的转化率为______ 。
(3)下列叙述中能说明上述反应达到平衡状态的是____ 。
A.当X与Y的反应速率之比为1:1
B.在混合气体中X的质量百分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的的密度不随时间的变化而变化
E.X、Y、Z的浓度之比为1:1:2
(4)当反应达到平衡时,用Y表示的正反应速率v(正)与用Z表示的逆反应速率v(逆)的关系是_____________ 。
(5)为使该反应的反应速率增大,可采取的措施是______ .
a.恒容时充入Ne b.适当升高温度
c.缩小容器的体积 d.选择高效催化剂

(1)写出该反应的化学方程式
(2)计算反应开始到10 s,用X表示的反应速率是
(3)下列叙述中能说明上述反应达到平衡状态的是
A.当X与Y的反应速率之比为1:1
B.在混合气体中X的质量百分数保持不变
C.混合气体的平均摩尔质量不随时间的变化而变化
D.混合气体的的密度不随时间的变化而变化
E.X、Y、Z的浓度之比为1:1:2
(4)当反应达到平衡时,用Y表示的正反应速率v(正)与用Z表示的逆反应速率v(逆)的关系是
(5)为使该反应的反应速率增大,可采取的措施是
a.恒容时充入Ne b.适当升高温度
c.缩小容器的体积 d.选择高效催化剂
您最近一年使用:0次