碳酸二甲酯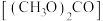 是一种绿色化工原料,用于汽车、医疗器械等领域。以甲醇为原料制备碳酸二甲酯的反应过程如下:
是一种绿色化工原料,用于汽车、医疗器械等领域。以甲醇为原料制备碳酸二甲酯的反应过程如下:
①
② 。下列说法错误的是
。下列说法错误的是
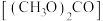 是一种绿色化工原料,用于汽车、医疗器械等领域。以甲醇为原料制备碳酸二甲酯的反应过程如下:
是一种绿色化工原料,用于汽车、医疗器械等领域。以甲醇为原料制备碳酸二甲酯的反应过程如下:①

②
 。下列说法错误的是
。下列说法错误的是A.电负性由大到小的顺序为: |
B.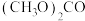 中 中 的杂化轨道类型为 的杂化轨道类型为 、 、 |
C.基态 的价电子排布式为 的价电子排布式为 |
| D.反应②中反应物与生成物所含π键数目相等 |
更新时间:2023-07-05 08:58:17
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】已知某元素的原子序数是30,下列关于该元素的说法正确的是
| A.基态原子的价电子排布式为4S2 | B.位于第四周期ⅡA族 |
| C.属于过渡金属元素 | D.最高化合价为+3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法不正确的是
| A.对于主族元素,中心原子的杂化轨道数等于价层电子对数 |
| B.sp3杂化轨道是由任意的1个s轨道和3个p轨道杂化形成的四个sp3杂化轨道 |
| C.核外电子数为偶数的基态原子,其原子轨道中可能含“未成对电子” |
| D.五种分子:①CO2②NO2③SO2④BF3⑤NH3,分子的VSEPR模型为平面三角形的是②③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
A.电负性: | B.离子半径: |
C.稳定性: | D.最高价氧化物对应水化物的酸性: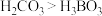 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】短周期主族元素X、Y、Z、W的原子序数依次增大。X的原子半径最小,Y是空气中含量最多的元素,基态时Z原子s能级和p能级的电子总数相等,W原子核外无未成对电子。下列说法正确的是
A.半径大小: |
B.电离能大小: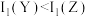 |
C.电负性大小: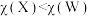 |
| D.由X、Y、Z三种元素组成的化合物一定是碱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】反应SiHCl3(g)+H2(g)=Si(s)+3HCl(g)可用于纯硅的制备,下列说法正确的是
| A.SiHCl3中Si原子的杂化方式为sp2杂化 |
| B.SiHCl3中Si元素的化合价为+2 |
| C.键长:Si-Si>C-C,故键能:Si-Si<C-C |
| D.HCl易溶于水是因为HCl和水分子之间能形成氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】设NA为阿伏加德罗常数的数值。下列有关叙述正确的是:
| A.标准状况下,22.4LCCl4中所含C-Cl键的数目为4NA |
B.7.8g 中所含的离子数目为0.3NA 中所含的离子数目为0.3NA |
C.向密闭容器中充入1mol HCl和1mol NH3,生成 的分子数为NA 的分子数为NA |
D.标准状况下,22.4L 和 和 的混合物中,所含碳碳双键的总数为NA 的混合物中,所含碳碳双键的总数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.常温下,18gD2O中含有中子的数目为9NA |
| B.4.48LCH4中含有C-H键数目为0.8NA |
| C.7.8gNa2O2与足量水反应转移电子数为0.2NA |
| D.1mol/L的MgCl2溶液中,含有Cl-的数目为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】有关原子杂化的说法正确的是( )
| A.凡是中心原子都是以sp3杂化轨道成键的分子,其空间结构都是正四面体 |
| B.苯分子中的碳原子以sp2杂化轨道形成π键、未杂化的2p轨道也形成σ键 |
| C.乙烯分子的碳原子以sp2杂化,其中,C—H之间是以sp2杂化轨道形成的σ键,C—C之间除了以sp2杂化轨道形成σ键外,未参加杂化的2p轨道也形成π键 |
| D.只要分子的中心原子的杂化类型相同,分子的键角就一定相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】布洛芬是一种用于小儿发热的经典解热镇痛药,异丁基苯是合成它的一种原料,二者的结构简式如图。下列说法正确的是

| A.异丁基苯属于芳香烃,与对二乙苯互为同分异构体 |
B.异丁基苯和布洛芬中碳原子均有 和 和 杂化 杂化 |
C.1mol布洛芬与足量的 溶液反应生成 溶液反应生成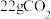 |
| D.两者均能发生加成、取代和消去反应 |
您最近一年使用:0次

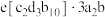 。下列说法正确的是
。下列说法正确的是





