利用废Pd催化剂(主要成分Pd、a-Al2O3和活性炭,含少量Fe、Cu等元素)回收海绵钯(Pd)和副产品的工艺流程如下:
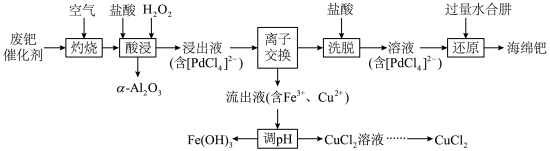
已知:①Pd在800℃转化为惰性PdO;②水合肼(N2H4·H2O)为二元弱碱;③阴、阳离子交换树脂工作原理: 、
、 。下列说法正确的是
。下列说法正确的是

已知:①Pd在800℃转化为惰性PdO;②水合肼(N2H4·H2O)为二元弱碱;③阴、阳离子交换树脂工作原理:
 、
、 。下列说法正确的是
。下列说法正确的是| A.“灼烧”和“酸浸”过程中温度均不宜过高 |
| B.“离子交换”和“洗脱”过程为提高效率,应尽量提高液体流速及溶液浓度 |
C.“还原”过程的离子反应: |
| D.“调pH”可选用氨水、CuO、Cu(OH)2等试剂 |
更新时间:2023-07-23 07:47:48
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】工业上制取硫酸铜采用途径Ⅱ而不采用途径I,这样做的优点是

①节省能源 ②不产生污染大气的SO2 ③提高了H2SO4的利用率 ④提高了Cu的利用率

①节省能源 ②不产生污染大气的SO2 ③提高了H2SO4的利用率 ④提高了Cu的利用率
| A.仅①② | B.仅②③④ | C.仅①②③ | D.全部 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知: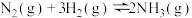 ,
, ,下列关于合成氨工业的说法
,下列关于合成氨工业的说法不正确 的是
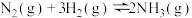 ,
, ,下列关于合成氨工业的说法
,下列关于合成氨工业的说法| A.温度选择400~500℃是为了提高氮气的转化率 |
| B.将原料气净化处理是为了防止其中混有的杂质使催化剂“中毒” |
| C.不选择过高压强的主要原因是压强越大,对材料的强度和设备的制造要求越高 |
| D.迅速冷却、液化氨气是为了使化学平衡向生成氨气的方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸是一种重要的化工产品,目前的重要生产方法是“接触法”,反应原理为:2SO2+O2 2SO3,已知该反应为放热反应。则下列说法正确的是
2SO3,已知该反应为放热反应。则下列说法正确的是
 2SO3,已知该反应为放热反应。则下列说法正确的是
2SO3,已知该反应为放热反应。则下列说法正确的是| A.只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B.达到平衡后,反应就停止了,故此时正、逆反应速率相等且均为零 |
| C.由反应可知,2mol SO2的能量大于2mol SO3的能量 |
| D.工业在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】磷酸二氢钙是一种常用的呈酸性的磷肥,下列说法不正确 的是
| A.磷酸二氢钙属于离子化合物 |
B.磷酸二氢钙溶液因 离子水解呈酸性 离子水解呈酸性 |
| C.Ca元素位于s区 |
| D.不能与草木灰混合施用 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验操作所得的现象及结论均正确的是
| 实验操作 | 现象及结论 | |
| A | 将AlCl3溶液加热蒸干 | 得到白色固体,成分为纯净的AlCl3 |
| B | 将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生,则Na2SO3已变质 |
| C | 常温下,向等体积、等浓度的NaCN和CH3COONa溶液中分别滴加2滴酚酞 | 均变红,NaCN溶液红色更深,则常温下电离平衡常数:Ka(CH3COOH)>Ka(HCN) |
| D | 向FeI2溶液中通入少量Cl2 | 溶液变黄,则Cl2的氧化性强于Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】海水开发利用的部分过程如图所示。下列说法正确的是( )


| A.过程①中,粗盐的提纯只涉及除杂、结晶等物理过程 |
| B.过程②中,工业上常用 NaOH 作为沉淀剂得到 Mg(OH)2 |
| C.过程③中,直接加热蒸干 MgCl2 溶液即可得到无水 MgCl2 |
| D.过程④中,可以选用 Na2SO3 饱和溶液来代替 SO2 水溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】我国古代科技十分发达,表中对古文献的解释不正确的是
| 序号 | 古文献 | 解释 |
| A | 曾青得铁则化为铜 | 可以用铁来冶炼铜 |
| B | 烧酒非古法也,自元时创始,其法用浓酒和糟入甑(指蒸锅),蒸令气上,用器承滴露 | 白酒(烧酒)的制造过程中采用了蒸馏的方法来分离和提纯 |
| C | 初,人不知盖泥法,元时南安有黄长者为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之 | 蔗糖的分离提纯采用了黄泥来吸附红糖中的色素 |
| D | 丹砂(HgS)烧之成水银,积变又成丹砂 | 加热时HgS熔融成液态,冷却时重新结晶为HgS晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】侯德榜制碱法的简单流程如下:

下列说法正确的是

下列说法正确的是
| A.X 为 CO2 |
B.NH3的电子式为 |
| C.煅烧炉中的反应属于氧化还原反应 |
| D.沉淀池中加入饱和食盐水后,先通入足量CO2再通入足量NH3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上可通过“酸性歧化法”和“电解法”制备 。“酸性歧化法”中,利用软锰矿(主要成分为
。“酸性歧化法”中,利用软锰矿(主要成分为 )先生成
)先生成 ,进而制备
,进而制备 的流程如下所示。
的流程如下所示。 。下列说法正确的是
。下列说法正确的是
 。“酸性歧化法”中,利用软锰矿(主要成分为
。“酸性歧化法”中,利用软锰矿(主要成分为 )先生成
)先生成 ,进而制备
,进而制备 的流程如下所示。
的流程如下所示。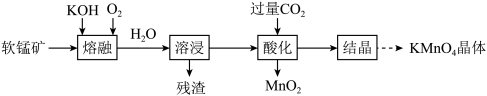
 。下列说法正确的是
。下列说法正确的是| A.为加快“熔融”反应速率,可将矿石粉碎,并用玻璃棒不断翻炒固体 |
B.“酸化”时若改用盐酸,则反应为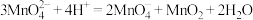 |
C.“结晶”获取 晶体时采用蒸发结晶 晶体时采用蒸发结晶 |
| D.该流程中涉及到的氧化还原反应至少有2个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一种制备 及纯度测定的实验步骤如下:
及纯度测定的实验步骤如下:
①分别称取 (稍过量)和
(稍过量)和 溶于适量水,当固体完全溶解后,水浴加热蒸发浓缩至表面出现晶体膜为止;
溶于适量水,当固体完全溶解后,水浴加热蒸发浓缩至表面出现晶体膜为止;
②自然冷却后,减压抽滤,便得到硫酸亚铁铵晶体;低温干燥、称重7.6g;
③准确称取wg产品溶于水,配制成100mL溶液;准确量取20.00mL所配制溶液于锥形瓶,加入适量稀硫酸,用标准 溶液滴定至终点,消耗滴定液VmL。
溶液滴定至终点,消耗滴定液VmL。
已知: 、
、 、
、 摩尔质量依次为
摩尔质量依次为 、
、 、
、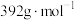 。产品收率指实际产量与理论产量之比。下列叙述错误的是
。产品收率指实际产量与理论产量之比。下列叙述错误的是
 及纯度测定的实验步骤如下:
及纯度测定的实验步骤如下:①分别称取
 (稍过量)和
(稍过量)和 溶于适量水,当固体完全溶解后,水浴加热蒸发浓缩至表面出现晶体膜为止;
溶于适量水,当固体完全溶解后,水浴加热蒸发浓缩至表面出现晶体膜为止;②自然冷却后,减压抽滤,便得到硫酸亚铁铵晶体;低温干燥、称重7.6g;
③准确称取wg产品溶于水,配制成100mL溶液;准确量取20.00mL所配制溶液于锥形瓶,加入适量稀硫酸,用标准
 溶液滴定至终点,消耗滴定液VmL。
溶液滴定至终点,消耗滴定液VmL。已知:
 、
、 、
、 摩尔质量依次为
摩尔质量依次为 、
、 、
、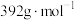 。产品收率指实际产量与理论产量之比。下列叙述错误的是
。产品收率指实际产量与理论产量之比。下列叙述错误的是| A.步骤①“出现晶体膜”表明已制成“热饱和溶液” |
| B.由步骤①、②可得到产品收率约为73.8% |
C.步骤③测得产品纯度为 |
D.若滴加 溶液前没有润洗酸式滴定管,测得结果偏高 溶液前没有润洗酸式滴定管,测得结果偏高 |
您最近一年使用:0次




