氯化铁(FeCl3)是一种棕色结晶,易升华,有强烈的吸水性。实验室制备无水氯化铁并探究氯化铁性质的相关实验如下。
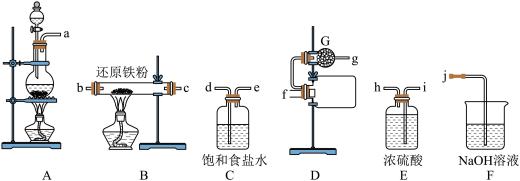
(1)装置A中发生反应的离子方程式是_______ 。
(2)实验装置接口的连接顺序是a→_______ →j, G中盛装的物质是_______ 。
(3)当观察到出现_______ 现象时,再点燃B处的酒精灯。
(4)若没有使用C装置,则可能导致的不良后果是_______ 。
Ⅱ.探究D中固态产物的相关性质
(5)取适量D中收集到的固态物质进行相关实验,完成下列实验,回答问题。

(1)装置A中发生反应的离子方程式是
(2)实验装置接口的连接顺序是a→
(3)当观察到出现
(4)若没有使用C装置,则可能导致的不良后果是
Ⅱ.探究D中固态产物的相关性质
(5)取适量D中收集到的固态物质进行相关实验,完成下列实验,回答问题。
| 序号 | 实验操作 | 实验现象 | 问题或结论 |
① | 取少量固态物质置于烧杯中,加入适量蒸馏水,搅拌,溶解 | 溶液浑浊,滴加某试剂,振荡,得到棕黄色澄清溶液 | 该试剂是 |
② | 取少量①中的澄清溶液于试管 中,滴加一滴 | 无明显现象 | 证明原固体中不含 FeCl2 |
③ | 将①中的澄清溶液滴入刚做完 银镜反应实验的试管中,振荡 | 管壁上的银镜溶解,溶液浑 浊 | 相关离子方程式是 |
更新时间:2023-06-27 18:20:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】为探究氯气的性质,某同学设计了如下所示的实验装置。
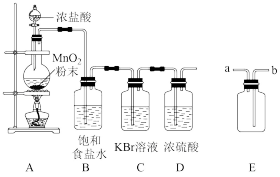
回答下列问题:
(1)装有浓盐酸的仪器名称为___________ 。
(2)写出装置A中发生反应的化学方程式:___________ 。
(3)装置B的作用是___________ 。
(4)装置C中的现象为___________ ,发生反应的离子方程式为___________ 。
(5)装置E用于收集Cl2,装置D应与E中的___________ (填“a”或“b”)端口连接。
(6)氯气通入饱和NaHCO3溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有___________ (填“盐酸”或“次氯酸”)。
(7)加热MnO2和4 mol/L稀盐酸混合物,无明显现象。可能是c(H+)或c(Cl-)较低,为探究c(H+)或c(Cl-)浓度变化对MnO2氧化盐酸的影响,设计实验进行探究:

将ⅰ、ⅱ作对比,得出的结论是___________ 。

回答下列问题:
(1)装有浓盐酸的仪器名称为
(2)写出装置A中发生反应的化学方程式:
(3)装置B的作用是
(4)装置C中的现象为
(5)装置E用于收集Cl2,装置D应与E中的
(6)氯气通入饱和NaHCO3溶液中能产生无色气体,已知酸性:盐酸>碳酸>次氯酸,该实验证明氯气与水反应的生成物中含有
(7)加热MnO2和4 mol/L稀盐酸混合物,无明显现象。可能是c(H+)或c(Cl-)较低,为探究c(H+)或c(Cl-)浓度变化对MnO2氧化盐酸的影响,设计实验进行探究:

将ⅰ、ⅱ作对比,得出的结论是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学兴趣小组为探究在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明氯气的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),请按要求回答问题:

(1)如图A装置中分液漏斗盛有浓盐酸,圆底烧瓶中的固体是二氧化锰。写出A中发生的化学反应方程式___________ 。
(2)①装置B中盛有无水硫酸铜,其中的现象是___________ 。
②装置C的作用是___________ ,③装置D、E出现不同的现象说明___________ 。
(3)装置F吸收反应生成的Cl2,装置G验证HCl挥发出来。乙同学认为此处有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入G中的气体只有一种,乙同学提出在F、G之间再增加一个装置。你认为该装管中应该盛放___________ (填写试剂或用品名称)。

(1)如图A装置中分液漏斗盛有浓盐酸,圆底烧瓶中的固体是二氧化锰。写出A中发生的化学反应方程式
(2)①装置B中盛有无水硫酸铜,其中的现象是
②装置C的作用是
(3)装置F吸收反应生成的Cl2,装置G验证HCl挥发出来。乙同学认为此处有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种,为了确保实验结论的可靠性,证明最终通入G中的气体只有一种,乙同学提出在F、G之间再增加一个装置。你认为该装管中应该盛放
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】化学实验室中常用下列装置利用二氧化锰和浓盐酸反应制取氯气,请回答下列问题
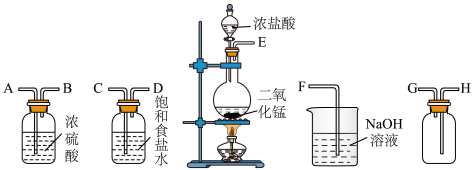
(1)连接上述仪器的正确顺序(填各接口处的字母):
___________ 接___________ ;___________ 接___________ ;___________ 接___________ ;___________ 接___________ 。
(2)装置中,盛放浓盐酸的仪器名称___________ ;NaOH溶液的作用是___________ 。
(3)该实验室制氯气的化学反应方程式___________ ,在该反应中浓盐酸体现的性质有___________ 。

(1)连接上述仪器的正确顺序(填各接口处的字母):
(2)装置中,盛放浓盐酸的仪器名称
(3)该实验室制氯气的化学反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】如图为制取无水氯化铁粉末的装置,已知氯化铁粉末很容易吸水生成含结晶水的化合物。
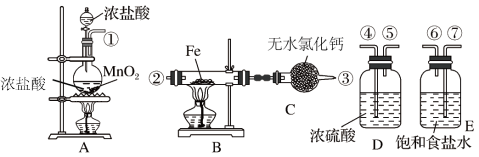
(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):
①接___________,___________接___________,___________接___________。___________
(2)烧瓶A发生反应的离子方程式为___________ 。
(3)容器D的作用是___________ ,容器E的作用是___________ 。
(4)A、B中的酒精灯应先点燃___________ 处(填“A”或“B”)的酒精灯。
(5)这套实验装置是否完整?___________ (填“是”或“否”);若不完整,还须补充什么装置?___________ (若第一问填“是”,则此问不需要作答)。

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序):
①接___________,___________接___________,___________接___________。
(2)烧瓶A发生反应的离子方程式为
(3)容器D的作用是
(4)A、B中的酒精灯应先点燃
(5)这套实验装置是否完整?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】用MnO2和浓盐酸制取纯净干燥的氯气,并让氯气与铜粉反应制取纯净的无水CuCl2,装置如图所示。请回答下列问题:
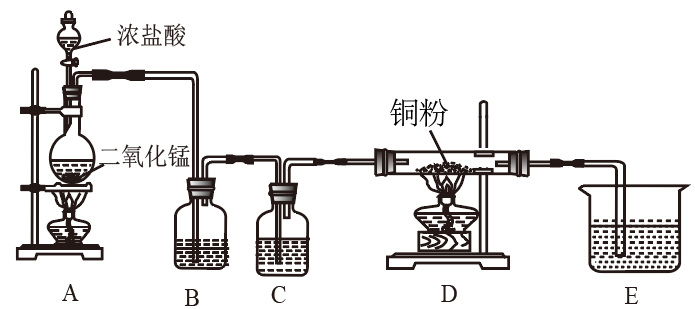
(1)写出制备氯气的化学方程式___________ 。
(2)B中选用的试剂是___________ ,其作用是___________ ;C中选用的试剂是___________ ,其作用是___________ 。
(3)装置E选用的试剂是___________ ,目的是___________ 。写出E中发生反应的化学方程式___________ 。
(4)但实验发现D中得到的无水CuCl2总是偏蓝色,请你提出改进方案___________ 。

(1)写出制备氯气的化学方程式
(2)B中选用的试剂是
(3)装置E选用的试剂是
(4)但实验发现D中得到的无水CuCl2总是偏蓝色,请你提出改进方案
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】如图所示,将仪器 A 中的浓盐酸滴加到盛有 MnO2的烧瓶中,加热后产生的气体依次通过装置 B 和 C,然后再将纯净干燥的气体通过加热的石英玻璃管 D(放置有铁粉)。请回答下列问题:
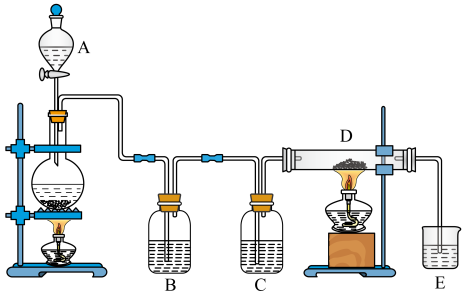
(1)仪器 A 的名称是_________ ,烧瓶中发生反应的化学方程式是___________ , 若制备 1 瓶体积为 100mL 的氯气(常温下,氯气的密度约为 2.90g/L),理论上需要 MnO2 ______ g(保留两位小数)。
(2)装置B、C中盛放的试剂名称分别为:________ 、_________ 。
(3)D中反应的化学方程式是_________ 。
(4)烧杯E中盛放的液体是_____ ,作用是______ ,反应的离子方程式是_____ 。

(1)仪器 A 的名称是
(2)装置B、C中盛放的试剂名称分别为:
(3)D中反应的化学方程式是
(4)烧杯E中盛放的液体是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】为了将混有硫酸钠、碳酸氢铵的氯化钠提纯,并制得纯净的氯化钠溶液,某学生设计如下实验:
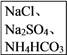
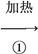
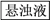

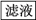
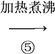
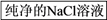
请回答下列问题:
(1)操作②________ (填“能”或“不能”)用硝酸钡溶液,说明理由:_______________ 。
(2)进行操作②后,判断SO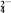 已除尽的方法是
已除尽的方法是____________________ 。
(3)操作③的目的是________ ;不先过滤就滴加碳酸钠溶液,其理由是_________ 。
(4)此设计方案是否严密?______ (填“是”或“否”),说明理由______ 。
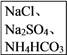
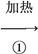
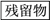
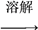
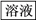
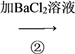
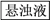

请回答下列问题:
(1)操作②
(2)进行操作②后,判断SO
 已除尽的方法是
已除尽的方法是(3)操作③的目的是
(4)此设计方案是否严密?
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】在 时,将氯气通入
时,将氯气通入 和炭粉的混合物中,反应生成四氯化钛和氯化铁,同时产生一种还原性气体。现制取并收集四氯化钛的装置如图1所示(部分夹持装置略)。
和炭粉的混合物中,反应生成四氯化钛和氯化铁,同时产生一种还原性气体。现制取并收集四氯化钛的装置如图1所示(部分夹持装置略)。

已知:① 高温时能与
高温时能与 反应,不与
反应,不与 反应;②
反应;② 与
与 的部分物理性质如下表。
的部分物理性质如下表。
(1)组装好仪器,添加试剂前,应该进行的操作是_________ 。
(2)用 与浓盐酸制备
与浓盐酸制备 ,反应的离子方程式为
,反应的离子方程式为_________ 。实验中需先后通入 两次,第二次通入
两次,第二次通入 时活塞
时活塞 、
、 的状态为
的状态为___________ ,作用是_________________ 。
(3) 时,瓷舟中发生反应的化学方程式为
时,瓷舟中发生反应的化学方程式为__________ 。
(4)控温箱的温度在 ,目的是
,目的是__________ 。
(5)装置单元X的作用是________ 。
(6)利用如图2所示装置测定所得 的纯度:取
的纯度:取 产品加入烧瓶,向安全漏斗中加入适量蒸馏水,待
产品加入烧瓶,向安全漏斗中加入适量蒸馏水,待 充分反应后,将烧瓶和安全漏斗中的液体一并转入锥形瓶中,滴入3滴
充分反应后,将烧瓶和安全漏斗中的液体一并转入锥形瓶中,滴入3滴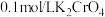 溶液作指示剂.用
溶液作指示剂.用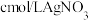 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗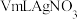 标准溶液。已知:
标准溶液。已知: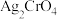 呈砖红色。
呈砖红色。
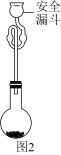
①安全漏斗在本实验中的作用除加水外,还有___________ .
②达到滴定终点时的现象为_________ 。
③产品中 的纯度为
的纯度为________ (用含w,c和V的代数式表示)。
 时,将氯气通入
时,将氯气通入 和炭粉的混合物中,反应生成四氯化钛和氯化铁,同时产生一种还原性气体。现制取并收集四氯化钛的装置如图1所示(部分夹持装置略)。
和炭粉的混合物中,反应生成四氯化钛和氯化铁,同时产生一种还原性气体。现制取并收集四氯化钛的装置如图1所示(部分夹持装置略)。
已知:①
 高温时能与
高温时能与 反应,不与
反应,不与 反应;②
反应;② 与
与 的部分物理性质如下表。
的部分物理性质如下表。熔点/ | 沸点/ | 水溶性 | |
|
| 136.4 | 极易水解生成白色沉淀 |
| 306 | 315 | 易水解生成红褐色沉淀 |
(2)用
 与浓盐酸制备
与浓盐酸制备 ,反应的离子方程式为
,反应的离子方程式为 两次,第二次通入
两次,第二次通入 时活塞
时活塞 、
、 的状态为
的状态为(3)
 时,瓷舟中发生反应的化学方程式为
时,瓷舟中发生反应的化学方程式为(4)控温箱的温度在
 ,目的是
,目的是(5)装置单元X的作用是
(6)利用如图2所示装置测定所得
 的纯度:取
的纯度:取 产品加入烧瓶,向安全漏斗中加入适量蒸馏水,待
产品加入烧瓶,向安全漏斗中加入适量蒸馏水,待 充分反应后,将烧瓶和安全漏斗中的液体一并转入锥形瓶中,滴入3滴
充分反应后,将烧瓶和安全漏斗中的液体一并转入锥形瓶中,滴入3滴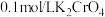 溶液作指示剂.用
溶液作指示剂.用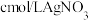 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗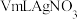 标准溶液。已知:
标准溶液。已知: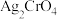 呈砖红色。
呈砖红色。
①安全漏斗在本实验中的作用除加水外,还有
②达到滴定终点时的现象为
③产品中
 的纯度为
的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验化学乙酰苯胺为无色晶体,有“退热冰”之称。其制备原理为:

已知:①苯胺易被氧化;
②苯胺、醋酸和乙酰苯胺的部分物理性质如下表:
制备乙酰苯胺的实验步骤如下:
步骤1:在下图1装置的圆底烧瓶中,加入6.0 mL苯胺、9.0 mL冰醋酸及0.2g锌粉。
步骤2:控制温度计示数约105 ℃,小火加热回流1 h。
步骤3:趁热将反应混合物倒入盛有100 mL冷水的烧杯中,抽滤,洗涤,得到粗产品。
步骤4:通过重结晶提纯粗产品后,获得无色片状晶体,干燥后得目标产品。
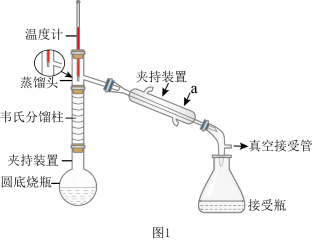

(1)仪器a的名称为_____________ 。
(2)步骤1中加入锌粉的作用是_____________ 。
(3)步骤2中控制温度计示数约105 ℃的原因是_____________ 。
(4)步骤3中,抽滤装置如图2所示,仪器c的名称是_____________ ,当过滤的溶液具有强酸性、强碱性或强氧化性时要用_____________ 代替布氏漏斗,停止抽滤时的操作为_____________ 。

已知:①苯胺易被氧化;
②苯胺、醋酸和乙酰苯胺的部分物理性质如下表:
| 试剂名称 | 熔点℃ | 沸点℃ | 溶解度(20 ℃) |
| 苯胺 | -6.2 | 184.4 | 稍溶于水(3.4g),与乙醇、乙醚、苯混溶 |
| 乙酸 | 16.7 | 118 | 易溶于水、乙醇、乙醚等 |
| 乙酰苯胺 | 114~116 | 280~290 | 0.46g |
步骤1:在下图1装置的圆底烧瓶中,加入6.0 mL苯胺、9.0 mL冰醋酸及0.2g锌粉。
步骤2:控制温度计示数约105 ℃,小火加热回流1 h。
步骤3:趁热将反应混合物倒入盛有100 mL冷水的烧杯中,抽滤,洗涤,得到粗产品。
步骤4:通过重结晶提纯粗产品后,获得无色片状晶体,干燥后得目标产品。


(1)仪器a的名称为
(2)步骤1中加入锌粉的作用是
(3)步骤2中控制温度计示数约105 ℃的原因是
(4)步骤3中,抽滤装置如图2所示,仪器c的名称是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】一种以黄铜矿和硫磺为原料制取铜和其他产物的新工艺,原料的综合利用率较高.其主要流程如下:
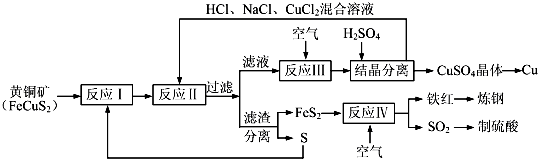
注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl-=2[CuCl2]-+S
请回答下列问题:
(1)反应Ⅰ的产物为____________ (填化学式).
(2)反应Ⅲ的离子方程式为____________ ;
(3)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其可能的原因是____________ ;
(4)反应Ⅳ在高温条件下进行,化学方程式是____________ ;
(5)某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000mol•L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL.已知:Cr2O72-+Fe2++H+→Cr3++Fe3++H2O(未配平)
①SO2通入Fe(SO4)3溶液中,发生反应的离子方程式为____________ ;
②反应Ⅳ所得气体中SO2的体积分数为____________ 。

注:反应Ⅱ的离子方程式为Cu2++CuS+4Cl-=2[CuCl2]-+S
请回答下列问题:
(1)反应Ⅰ的产物为
(2)反应Ⅲ的离子方程式为
(3)一定温度下,在反应Ⅲ所得的溶液中加入稀硫酸,可以析出硫酸铜晶体,其可能的原因是
(4)反应Ⅳ在高温条件下进行,化学方程式是
(5)某硫酸厂为测定反应Ⅳ所得气体中SO2的体积分数,取280mL(已折算成标准状况)气体样品与足量Fe2(SO4)3溶液完全反应后,用浓度为0.02000mol•L-1的K2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7溶液25.00mL.已知:Cr2O72-+Fe2++H+→Cr3++Fe3++H2O(未配平)
①SO2通入Fe(SO4)3溶液中,发生反应的离子方程式为
②反应Ⅳ所得气体中SO2的体积分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】铝及其化合物在医药、食品、污水处理等多个行业有重要作用。以高岭土(主要成分为Al2Si2Ox(OH)y,合有SiO2,Fe3O4、NiO等杂质)为原料,制备Al2O3的一种流程如下:
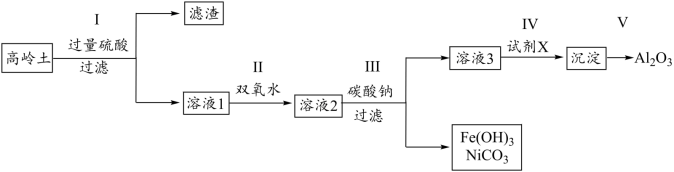
已知部分金属离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如表所示:
(1)Al2Si2Ox(OH)y中x、y的值可能是_______ (填字母)
A.7、2 B.5、4 C.6、3 D.3、8
(2)过程I中形成的滤渣主要成分为_______ (填化学式)。
(3)过程II中,加入双氧水的目的是_______ 。
(4)过程III中形成NiCO3的化学方程式_______ 。检验溶液3中铁元素是否沉淀完全的方法是_______ 。
(5)在过程IV中,试剂X应选用_______ (填字母,a.氨水,b.NaOH溶液,c.澄清石灰水),写出对应反应的离子方程式_______ 。

已知部分金属离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如表所示:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀时的pH | 3.7 | 2.3 | 7.6 | 5.9 |
| 完全沉淀时的pH | 5.2 | 3.2 | 9.7 | 8.9 |
(1)Al2Si2Ox(OH)y中x、y的值可能是
A.7、2 B.5、4 C.6、3 D.3、8
(2)过程I中形成的滤渣主要成分为
(3)过程II中,加入双氧水的目的是
(4)过程III中形成NiCO3的化学方程式
(5)在过程IV中,试剂X应选用
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上利用氧化铝基废催化剂(主要成分为Al2O3,少量Pd)回收Al2(SO4)3及Pd的流程如图:
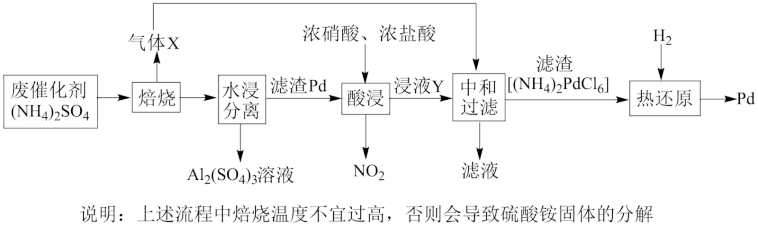
(1)焙烧时产生气体X的电子式为_______ 。
(2)水浸分离中,滤渣Pd的颗粒比较大,一般可以采用的分离方法是_______ (填字母)。
A.过滤 B.抽滤 C.渗析 D.倾析
(3)写出酸浸时发生反应的离子方程式_______ 。(已知氯钯酸为弱酸)
(4)某同学在实验室用如下图所示装置完成Pd的热还原实验,并计算滤渣中(NH4)2PdCl6的百分含量(滤渣中的杂质不参与热还原反应) 。
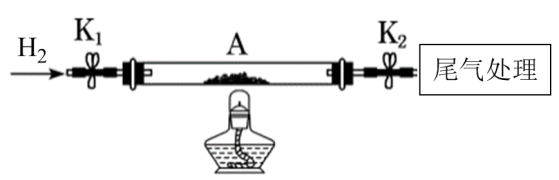
①写出热还原法过程中发生反应的化学方程式_______ 。
② i。将石英玻璃管中(带开关K1和K2)(设为装置A)称重,记为m1 g。将滤渣[(NH4)2PdCl6]装入石英玻璃管中,再次将装置A称重,记为m2 g。
ii.连接好装置后,按d→__ →__ →b→__ →__ →e(填标号)顺序进行实验。
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2 e.称量A f.冷却至室温 g.缓缓通入H2
iii.重复上述操作步骤,直至A恒重,记为m3 g。
③根据实验记录,计算滤渣中(NH4)2PdCl6的百分含量_______ [列式表示,其中(NH4)2PdCl6相对分子质量为355]。
④实验结束时,发现硬质试管右端有少量白色固体,可能是_______ (填化学式),这种情况导致实验结果_______ (填“偏高”、“偏低”、“无影响”)。

(1)焙烧时产生气体X的电子式为
(2)水浸分离中,滤渣Pd的颗粒比较大,一般可以采用的分离方法是
A.过滤 B.抽滤 C.渗析 D.倾析
(3)写出酸浸时发生反应的离子方程式
(4)某同学在实验室用如下图所示装置完成Pd的热还原实验,并计算滤渣中(NH4)2PdCl6的百分含量(滤渣中的杂质不参与热还原反应) 。

①写出热还原法过程中发生反应的化学方程式
② i。将石英玻璃管中(带开关K1和K2)(设为装置A)称重,记为m1 g。将滤渣[(NH4)2PdCl6]装入石英玻璃管中,再次将装置A称重,记为m2 g。
ii.连接好装置后,按d→
a.点燃酒精灯,加热 b.熄灭酒精灯 c.关闭K1和K2
d.打开K1和K2 e.称量A f.冷却至室温 g.缓缓通入H2
iii.重复上述操作步骤,直至A恒重,记为m3 g。
③根据实验记录,计算滤渣中(NH4)2PdCl6的百分含量
④实验结束时,发现硬质试管右端有少量白色固体,可能是
您最近一年使用:0次





